四黄定痛贴剂药效学研究
2017-09-03潘传波郭剑华马善治刘渝松刘才英叶承莉
潘传波,郭剑华,郭 亮,李 卿,马善治,刘渝松,漆 伟,刘才英,叶承莉,唐 彦
(1.重庆市中医骨科医院,重庆 400010;2.重庆市中药研究院,重庆 400020)
四黄定痛贴剂药效学研究
潘传波1,郭剑华1,郭 亮1,李 卿2,马善治1,刘渝松1,漆 伟1,刘才英1,叶承莉1,唐 彦1
(1.重庆市中医骨科医院,重庆 400010;2.重庆市中药研究院,重庆 400020)
目的:观察四黄定痛贴剂的药效学作用。方法:给大鼠涂抹四黄定痛贴剂(高、中、低3种剂量),以大鼠急性痛风性关节炎和急性血瘀为模型,观察其药理作用。结果:四黄定痛贴剂高剂量组对大鼠急性痛风性关节炎造模后2h和6h的步态评分明显降低、足肿胀周径有明显减小作用、肿胀率有明显抑制作用、明显降低大鼠急性痛风性关节炎关节腔的中性粒细胞、IL-1β、TNF-α和MPO的含量;组织病理学检查结果显示:模型组大鼠踝关节滑膜细胞增生,血管翳形成,周围结缔组织水肿、变性坏死伴急慢性炎细胞浸润。四黄定痛贴剂高、中剂量组对造模处踝关节组织病理变化有一定改善和修复趋势。四黄定痛贴剂高剂量组能明显降低大鼠的全血黏度(高切、低切)、高、中、低切还原黏度和红细胞刚性指数。结论:四黄定痛贴剂对急性炎症有明显的抗炎作用,同时还具有一定的活血化瘀作用。
四黄定痛贴剂;大鼠;药效学研究
四黄定痛贴剂源于治疗急性痛风性关节炎的经验方四黄定痛汤,通过优化处方和剂型改良为外用中药贴剂,功效散寒祛湿、通络止痛。本研究拟通过动物试验观察四黄定痛贴剂抗炎镇痛和活血化瘀的药效学作用,为临床用药提供参考依据。
1 实验材料
动物:SD大鼠,SPF级,全雄,180~220g,由重庆市中药研究院实验动物研究所提供,实验动物生产许可证号:SCXK(渝)2012-0006,动物合格证号0001954。SD大鼠,SPF级,雌雄兼用,200~260g,由重庆市中药研究院实验动物研究所提供,实验动物生产许可证号SCXK(渝)2012-0006,动物合格证号0002236。
试剂及耗材:0.9%氯化钠注射液,太极集团西南药业股份有限公司,批号16041016;戊巴比妥钠,SIGMA公司,批号908M031;盐酸肾上腺素注射液,重庆迪康长江制药有限公司,批号160801;大鼠白介素1β(IL-1β)、大鼠髓过氧化物酶(MPO)、大鼠肿瘤坏死因子α(TNF-α)酶联免疫分析试剂盒Shanghai jijin chemistry technology,批号E201609014A;HCT,济南希森美康医用电子有限公司,批号G5365。EDTA一次性真空采血管,河北鑫乐医疗器械科技股份有限公司生产,批号16109002;肝素钠一次性真空采血管,河北鑫乐医疗器械科技股份有限公司生产,批号16078802。
主要实验仪器与设备:UW-4200S电子天平,岛津国际贸易有限公司;Allegra X-12离心机,美国贝克曼库尔特有限公司;FASCO-3010B全自动血液流变快测仪,重庆大学维多生物工程研究所;XT-2000i全自动动物血液分析仪,日本希森美康株式会社;ST-360酶标仪,上海科华试验系统有限公司;PV-200足趾容积测量仪,成都泰盟科技有限公司;DNP-98021A电热恒温培养箱,上海三发科学仪器有限公司;RM2235轮转切片机,德国琜卡仪器有限公司;ASP300S高级智能脱水机,德国徕卡仪器有限公司;TK-218型恒温摊片烤片机,湖北泰维医疗科技有限责任公司;TB-718型生物组织自动包埋机,湖北泰维医疗科技有限责任公司;TR-180生物组织全自动染色机,湖北泰维医疗科技有限公司;Mias2000图象处理系统,四川大学图象处理国家研究所。
供试品与阳性对照药品:四黄定痛贴剂,由重庆市中药研究院药化研究所提供,1mL相当于4.4g药材,批号160601。双氯芬酸二乙胺乳胶剂(扶他林),北京诺华制药有限公司生产,批号VP0345。
2 实验方法与结果
2.1 对急性痛风性关节炎模型大鼠的影响
2.1.1 实验方法[1-5]
SD大鼠60只,全雄,待检疫及适应饲养期结束后,采用随机区组法(以体质量为主要关键字、随机数字为次要关键字)分为6组,每组10只,即溶媒对照组(纯化水)、模型组(纯化水)、四黄定痛贴剂高、中、低剂量组(生药76.0、38.0、19.0mg/cm2)和阳性对照组(双氯芬酸二乙胺乳胶剂0.5mg/cm2)。各组于给药前一天备皮,用6%的硫化钠脱毛剂将动物背部脊柱两侧毛发脱去,去毛范围约为40cm2(4cm×10cm)。将各样品均匀涂抹于整个脱毛区,在上面用二层灭菌纱布覆盖(溶媒对照品用灭菌纱布吸附后贴敷与脱毛区),再用胶布固定,6h后,去除覆盖物,用温水去除残留的各样品。给药体积为2.0mL/只,1日1次,连续9天。
第7天测定动物右侧踝关节周径和容积,然后给药后0.5h造模(正常组除外):模型组、阳性对照组、四黄定痛贴剂高、中、低剂量组,分别用5号注射针在大鼠右侧踝关节后侧插入至跟腱内侧,将0.2mL尿酸钠溶液注入到关节腔内,其中空白组将0.2mL生理盐水注入到关节腔内,测定造模后分别于药后2h、6h、12h、24h、48h测定右侧踝关节周径和容积,计算肿胀率、步态进行分级评分,评分标准见表4。造模48h后麻醉处死,随后消毒右侧踝关节部位,立即以锐利刀片切开关节囊,用1mL的无菌生理盐水冲洗大鼠关节腔,涂片并固定后镜下计数白细胞,并用酶联免疫法测定关节冲洗液中IL-1β、TNF-α、MPO的含量;最后取踝关节组织,10%甲醛溶液固定,HE染色。对关节滑膜组织进行组织形态检查,评分标准见表2。


表1 大鼠步态分级评分标准

表2 关节滑膜组织炎症程度分级标准
2.1.2 结果
对急性痛风性关节炎模型大鼠步态的影响。与溶媒对照组比较,模型组大鼠造模后2、6、12和24h的步态评分明显增加(P<0.01)。与模型组比较,四黄定痛贴剂生药76.0 mg/cm2组在造模后2h和6h的大鼠步态评分明显降低(P<0.05),提示四黄定痛贴剂对造模后的急性痛风性关节炎模型大鼠的步态有明显的改善作用。结果见表3。
表3 对急性痛风性关节炎模型大鼠步态的影响 (±s)

表3 对急性痛风性关节炎模型大鼠步态的影响 (±s)
注:与模型组比较,*P<0.05,**P<0.01。
组别 n 剂量(mg生药/cm2)造模后2h(mm)造模后6h(mm)造模后12h(mm)造模后24h(mm)造模后48h(mm)溶媒对照组 10 / 0.20±0.42**0.10±0.32**0.00±0.00**0.00±0.00**0.00±0.00模型组 10 / 2.70±0.48 2.40±0.70 1.50±0.71 1.30±0.67 0.70±0.82阳性对照组 10 0.5 1.60±0.52**1.20±0.92**0.50±0.53**0.50±0.71*0.10±0.32高剂量组 10 76.0 2.00±0.47*1.50±0.71*0.90±0.57 0.70±0.48 0.20±0.42中剂量组 10 38.0 2.30±0.67 1.80±0.79 1.30±0.82 1.00±0.82 0.50±0.97低剂量组 10 19.0 2.90±0.32 2.30±0.48 1.50±0.71 1.20±0.42 0.70±0.48
对急性痛风性关节炎模型大鼠足周径的影响。与溶媒对照组比较,模型组大鼠造模后2、6、12、24和48h的足周径明显增加(P<0.01)。与模型组比较,四黄定痛贴剂生药76.0 mg/cm2组在造模后2h和6h的大鼠足周径明显降低(P<0.05),提示四黄定痛贴剂对造模后的急性痛风性关节炎模型大鼠足肿胀有明显的改善作用。见表4。
表4 对急性痛风性关节炎模型大鼠足周径的影响 (±s)
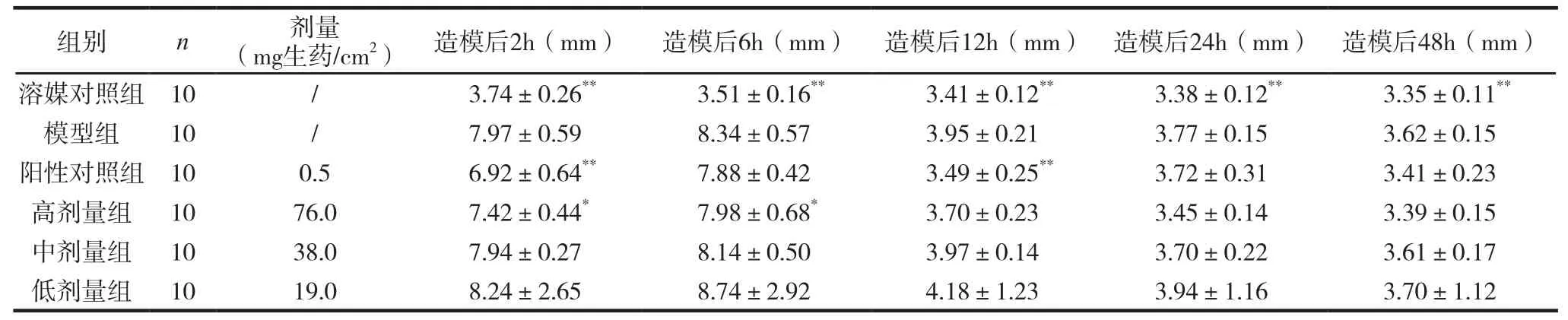
表4 对急性痛风性关节炎模型大鼠足周径的影响 (±s)
注:与模型组比较,*P<0.05,**P<0.01。
组别 n 剂量(mg生药/cm2) 造模后2h(mm) 造模后6h(mm) 造模后12h(mm) 造模后24h(mm) 造模后48h(mm)溶媒对照组 10 / 3.74±0.26**3.51±0.16**3.41±0.12**3.38±0.12**3.35±0.11**模型组 10 / 7.97±0.59 8.34±0.57 3.95±0.21 3.77±0.15 3.62±0.15阳性对照组 10 0.5 6.92±0.64**7.88±0.42 3.49±0.25**3.72±0.31 3.41±0.23高剂量组 10 76.0 7.42±0.44*7.98±0.68*3.70±0.23 3.45±0.14 3.39±0.15中剂量组 10 38.0 7.94±0.27 8.14±0.50 3.97±0.14 3.70±0.22 3.61±0.17低剂量组 10 19.0 8.24±2.65 8.74±2.92 4.18±1.23 3.94±1.16 3.70±1.12
对急性痛风性关节炎模型大鼠足肿胀的影响。与溶媒对照组比较,模型组大鼠造模后2、6、12、24和48h的足肿胀率明显增加(P<0.01)。与模型组比较,四黄定痛贴剂生药76.0 mg/cm2组在造模后2和6h的大鼠肿胀率明显降低(P<0.05),提示四黄定痛贴剂对造模后的急性痛风性关节炎模型大鼠足肿胀有明显的抑制作用。见表5。
表5 对急性痛风性关节炎模型大鼠足肿胀的影响 (±s)
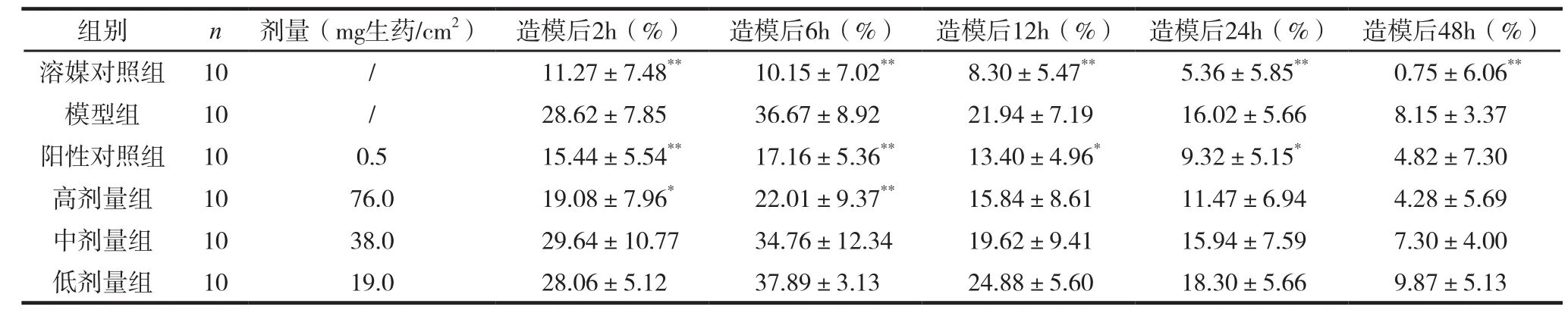
表5 对急性痛风性关节炎模型大鼠足肿胀的影响 (±s)
注:与模型组比较,*P<0.05,**P<0.01。
组别 n 剂量(mg生药/cm2) 造模后2h(%) 造模后6h(%) 造模后12h(%) 造模后24h(%) 造模后48h(%)溶媒对照组 10 / 11.27±7.48**10.15±7.02**8.30±5.47**5.36±5.85**0.75±6.06**模型组 10 / 28.62±7.85 36.67±8.92 21.94±7.19 16.02±5.66 8.15±3.37阳性对照组 10 0.5 15.44±5.54**17.16±5.36**13.40±4.96*9.32±5.15*4.82±7.30高剂量组 10 76.0 19.08±7.96*22.01±9.37**15.84±8.61 11.47±6.94 4.28±5.69中剂量组 10 38.0 29.64±10.77 34.76±12.34 19.62±9.41 15.94±7.59 7.30±4.00低剂量组 10 19.0 28.06±5.12 37.89±3.13 24.88±5.60 18.30±5.66 9.87±5.13
对急性痛风性关节炎模型大鼠关节腔中性粒细胞、IL-1β、TNF-α及MPO的影响。与溶媒对照组比较,模型组大鼠关节腔中性粒细胞、IL-1β、TNF-α、MPO含量明显升高(P<0.01)。与模型组比较,四黄定痛贴剂生药76.0mg/cm2组能明显降低大鼠急性痛风性关节炎关节腔的中性粒细胞、IL-1β、TNF-α、MPO的含量(P<0.05);四黄定痛贴剂38.0mg生药/cm2组亦能降低IL-1β、TNF-α的含量(P<0.05)。提示四黄定痛贴剂对造模后的急性痛风性关节炎模型大鼠踝关节腔中的炎性介质和过氧化物等有明显的抑制作用。见表6。
表6 对关节腔中性粒细胞、IL-1β、TNF-α及MPO的影响 (±s)

表6 对关节腔中性粒细胞、IL-1β、TNF-α及MPO的影响 (±s)
注:与模型组比较,*P<0.05,**P<0.01。
组别 n 剂量(mg生药/cm2) 中心粒细胞(个/ mm2) IL-1β(pg/mL) TNF-α(pg/mL) MPO(pg/mL)溶媒对照组 10 / 18.9±5.9**35.4±3.1**374.1±38.2**643.5±61.4**模型组 10 / 390.0±86.8 56.1±6.3 648.3±63.4 1057.3±112.8阳性对照组 10 0.5 285.5±47.4**36.7±4.8**431.6±17.7**799.5±47.0**高剂量组 10 76.0 296.7±47.3*39.7±5.4**515.0±22.8**882.5±62.8**中剂量组 10 38.0 320.7±79.0 43.6±5.2**570.4±33.7*945.6±53.7低剂量组 10 19.0 356.4±69.0 54.5±7.9 640.8±36.9 1180.2±49.9
对急性痛风性关节炎模型大鼠关节滑膜组织病理学的影响。与模型组比较,溶媒对照组与模型组踝关节病理表现有显著性差异,表明模型组踝关节组织有明显的病理变化发生,表现为造模处踝关节滑膜细胞增生,血管翳形成,周围结缔组织水肿、变性坏死伴急慢性炎细胞浸润。四黄定痛贴剂生药76.0、38.0、19.0mg/cm2组与模型组比较造模处踝关节组织病理表现未见显著性差异,但四黄定痛贴剂生药76.0、38.0mg/cm2组对造模处踝关节组织病理变化有一定改善和修复趋势。
2.2 对急性血瘀模型大鼠血液流变学指标的影响
2.2.1 实验方法[6-7]
SD大鼠60只,雌雄各30只,待检疫及适应饲养期结束后,随机分为6组,每组10只,即溶媒对照组(纯化水)、模型组(纯化水)、四黄定痛贴剂高、中、低剂量组(生药16.0、8.0、4.0mg/cm2)和阳性对照组(双氯芬酸二乙胺乳胶剂0.5mg/cm2)。各组于给药前一天备皮,用6%的硫化钠脱毛剂将动物背部脊柱两侧毛发脱去,去毛范围约为40cm2(4cm×10cm)。将各样品均匀涂抹于整个脱毛区,在上面用二层灭菌纱布覆盖(溶媒对照品用灭菌纱布吸附后贴敷与脱毛区),再用胶布固定,6h后,去除覆盖物,用温水去除残留的各样品。给药体积为2.0mL,1日1次,连续7天。
末次给药后1h,除溶媒对照组外,其余各组均按0.08mL/100g皮下注射0.1%的盐酸肾上腺素注射液,2h后将动物置于4℃冰水中浸泡5min,于首次注射后4h再次给予同等剂量相同途径的盐酸肾上腺素注射液,禁食不禁水18h。次日取血测定红细胞压积(HCT),再分别用1%肝素抗凝的试管采血,肝素抗凝血测定全血黏度,再将血离心,测定血浆黏度。
2.2.2 结果
与溶媒对照组比较,模型组大鼠全血黏度,血浆黏度,高、中、低切还原黏度和红细胞刚性指数均明显升高(P<0.01)。与模型组比较,四黄定痛贴剂生药76.0mg/cm2组能明显降低大鼠的全血黏度(高切、低切)、高、中、低切还原黏度和红细胞刚性指数(P<0.05);生药38.0mg/cm2组亦明显降低大鼠的高切还原黏度和低切还原黏度(P<0.01)。提示四黄定痛贴剂对大鼠急性血瘀模型有一定的活血化瘀作用。见表7。
表7 对急性血瘀模型大鼠血液流变学指标的影响 (±s)
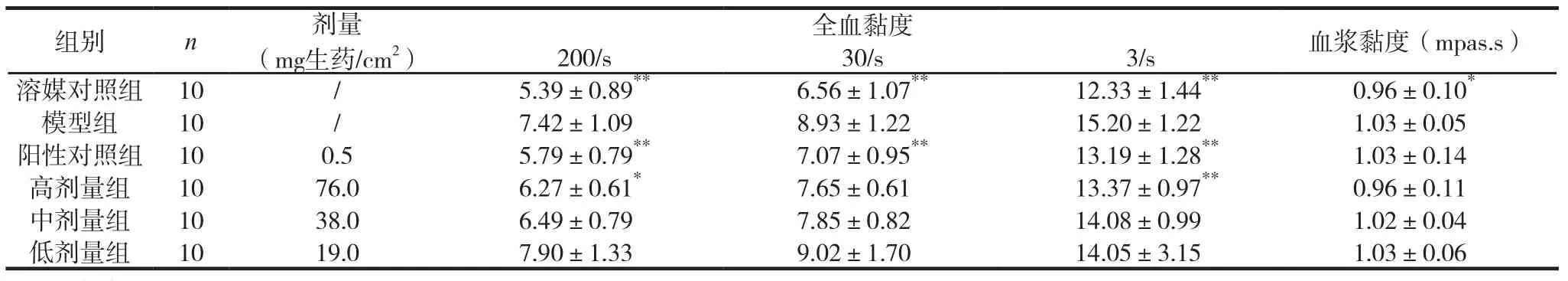
表7 对急性血瘀模型大鼠血液流变学指标的影响 (±s)
全血黏度 血浆黏度(mpas.s)200/s 30/s 3/s溶媒对照组 10 / 5.39±0.89**6.56±1.07**12.33±1.44**0.96±0.10*模型组 10 / 7.42±1.09 8.93±1.22 15.20±1.22 1.03±0.05阳性对照组 10 0.5 5.79±0.79**7.07±0.95**13.19±1.28**1.03±0.14高剂量组 10 76.0 6.27±0.61*7.65±0.61 13.37±0.97**0.96±0.11中剂量组 10 38.0 6.49±0.79 7.85±0.82 14.08±0.99 1.02±0.04低剂量组 10 19.0 7.90±1.33 9.02±1.70 14.05±3.15 1.03±0.06组别 n 剂量(mg生药/cm2)
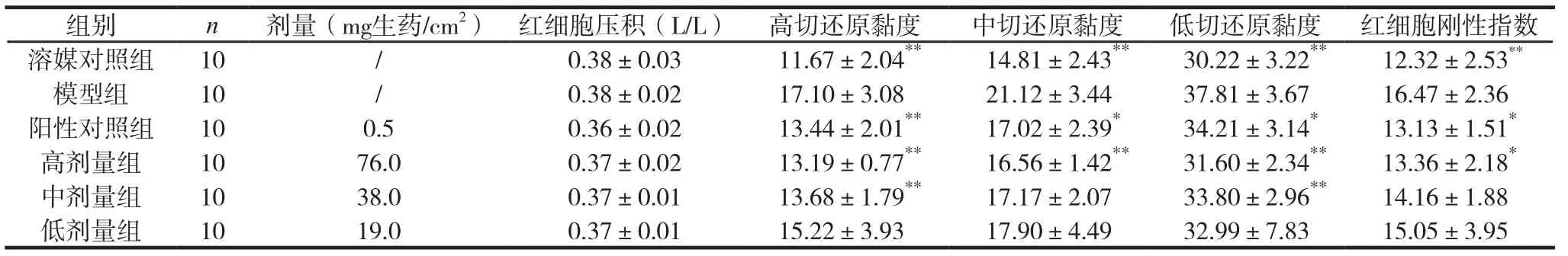
续表7
3 讨 论
痛风是由于嘌呤代谢紊乱和(或)尿酸排泄障碍所导致的一种异质性疾病,其临床特点是高尿酸血症、痛风性急性关节炎反复发作、痛风石沉积、特征性慢性关节炎和关节畸形,常累及肾引起慢性间质性肾炎和肾尿酸结石形成。
四黄定痛贴剂的功能主治为散寒祛湿、通络止痛,临床用于治疗急性痛风性关节炎。药效学主要有以下两个方面。
抗炎作用。四黄定痛贴剂生药76.0mg/cm2组对大鼠急性痛风性关节炎造模后2h和6h的步态评分明显降低,对大鼠急性痛风性关节炎造模后2h和6h足肿胀的周径和肿胀率有明显降低作用,明显降低大鼠急性痛风性关节炎关节腔的中性粒细胞、IL-1β、TNF-α和MPO的含量;生药38.0mg/cm2组能降低IL-1β、TNF-α的含量。组织病理学检查结果显示生药76.0、38.0mg/cm2组对造模处踝关节组织病理变化有一定改善和修复趋势。提示四黄定痛贴剂对尿酸钠致大鼠急性痛风性关节炎有明显抗炎作用。
活血化瘀作用。四黄定痛贴剂生药76.0mg/cm2组能明显降低大鼠的全血黏度(高切、低切)、高、中、低切还原黏度和红细胞刚性指数,生药38.0mg/cm2组亦明显降低大鼠的高切还原黏度和低切还原黏度。提示四黄定痛贴剂对大鼠急性血瘀模型有一定的活血化瘀作用。
研究结果表明,四黄定痛贴剂对急性炎症有明显的抗炎作用,同时还具有一定活血化瘀作用。
[1] 杨辉.急性痛风性关节炎的中医证治探讨及其外用巴布剂的研制[D].浙江中医药大学,2014,7:15-20.
[2] 梁莎,夏有兵,朱毅,等.急性痛风性关节炎大鼠局部造模方法的改良.中国现代医学杂志[J],2014,24(2):10-13.
[3] 黄凯裕,梁爽,王菊菊,等.电针结合二妙散对急性痛风性关节炎模型大鼠步态及关节影响[J].辽宁中医药大学学报,2015,17(8):134-136.
[4] 曹世霞,张三印,赵云龙,等.秦皮总香豆素对急性痛风性关节炎大鼠模型IL-1β、TNF-α的影响[J].中药药理与临床,2010;26(5):55-56.
[5] 刘蕊,孙琳,邢瑞,等.双醋瑞因对急性痛风性关节炎大鼠模型的防治作用[J].中华风湿病学杂志,2015,19(11):761-764.
[6] 李伟霞,黄美艳,唐于平,等.大鼠急性血瘀模型造模方法的研究与评价[J].中国药理学通报,2011,27:1761-1765.
[7] 李丽明,齐耀群,李阿荣,等.脉复生对急性血瘀模型大鼠血液流变学及凝血功能的影响[J].广州中医药大学学报,2016,33(3):353-357.
Objective:To observe pharmacodynamic effect of Sihuang Dingtong Patch. Method: Taking acute gouty arthritis and acute blood stasis of rats as the models, we smear Sihuang Dingtong Patch for rats and observe its pharmacological action. Result: The crude drug of 76.0mg /cm2 Sihuang Dingtong Patch decreased gait score significantly, reduced paw swelling perimeter significantly, had obvious inhibition on swelling rate and decreased the content of neutrophil, IL-1β, TNF-α and MPO in articular cavity of acute gouty arthritis rats at the time point of 2h and 6h after acute gouty arthritis rat models were established. Histopathology examination result showed that synovial cells hyperplasia, pannus formation, peripheral connective tissue edema, degeneration and necrosis companied with acute and chronic inflammatory cell infiltration in ankle joint of rats in model group. The crude drug of 76.0mg /cm2and 38.0mg / cm2Sihuang Dingtong Patch had certain improving and repairing development trend in histopathological changes of ankle joint at the site of model establishment. The crude drug of 76.0mg /cm2Sihuang Dingtong Patch could decrease whole blood viscosity, including whole high blood viscosity and whole low blood viscosity, high shear relative reduced viscosity, middle shear relative reduced viscosity, low shear relative reduced viscosity and erythrocyte rigidity index. Conculsion: Sihuang Dingtong Patch has obvious anti-inflammatory effect on acute inflammation as well as activating blood and resolving blood stasis effect.
Sihuang Dingtong Patch;Rat;Pharmacodynamic study
R285.9
B
1004-2814(2017)07-0744-04
2017-04-19
