国内外兽药管理比较研究
2017-09-03葛林刘晓飞王勤王忠田
葛林,刘晓飞,王勤, 王忠田
(1.对外经济贸易大学英语学院,北京 100029; 2.中国检验检疫科学研究院动物检疫研究所,北京 100029;3.中国兽医药品监察所,北京 100081)
国内外兽药管理比较研究
葛林1,刘晓飞2,王勤2, 王忠田3
(1.对外经济贸易大学英语学院,北京 100029; 2.中国检验检疫科学研究院动物检疫研究所,北京 100029;3.中国兽医药品监察所,北京 100081)
兽药在防治动物疫病、提高养殖效益、保障公共卫生安全中发挥着重要作用,随着公众对公共卫生安全、食品安全要求的逐步提高,我国兽药管理领域面临残留监控、产业监管、耐药性管控等多重挑战。本文简要发达国家兽药监管模式及法律基础,并结合我国兽药管理实际进行了比较研究,提出了进一步完善兽药管理体制的意见建议。
兽药;监管;建议
兽药是养殖业生产的重要投入品,也是动物疫病防控的重要物资。近年来,我国兽药产业呈蓬勃发展态势,但是也面临着多重挑战,既要满足养殖业生产发展需要,又要在保障公共卫生和食品安全中发挥保驾护航作用。如何在全球兽药行情不断变化、国际竞争日益激烈、社会各界对药物残留和细菌耐药性高度关注的今天,把握新形势、解决新问题,是我国兽药产业面临的一个重大课题。本文介绍了发达国家在兽药管理制度及体系建设方面的经验,简要比较了国内外兽药管理体制机制,以期为加快我国兽药管理科学化、制度化、规范化进程提供意见参考,收取长补短、促进发展之效。
1 发达国家兽药监管模式及法律基础
经过多年的发展,很多发达国家的兽药产业已经进入稳定发展时期。除2009年受全球金融危机影响出现负增长以外,全球兽药市场一直保持稳定增长。从国外兽药市场区域分布情况看,北美和西欧市场规模较大,分别占30%以上的市场份额,远东、拉丁美洲合计约占30%,亚洲市场(除中国外)规模则相对较小[1]。鉴于兽药产业的健康发展离不开健全的法制和规范的监管,现将美国、欧盟、加拿大、澳大利亚、日本、我国等国家和地区的兽药监管模式及制度基础简要概述见表1。
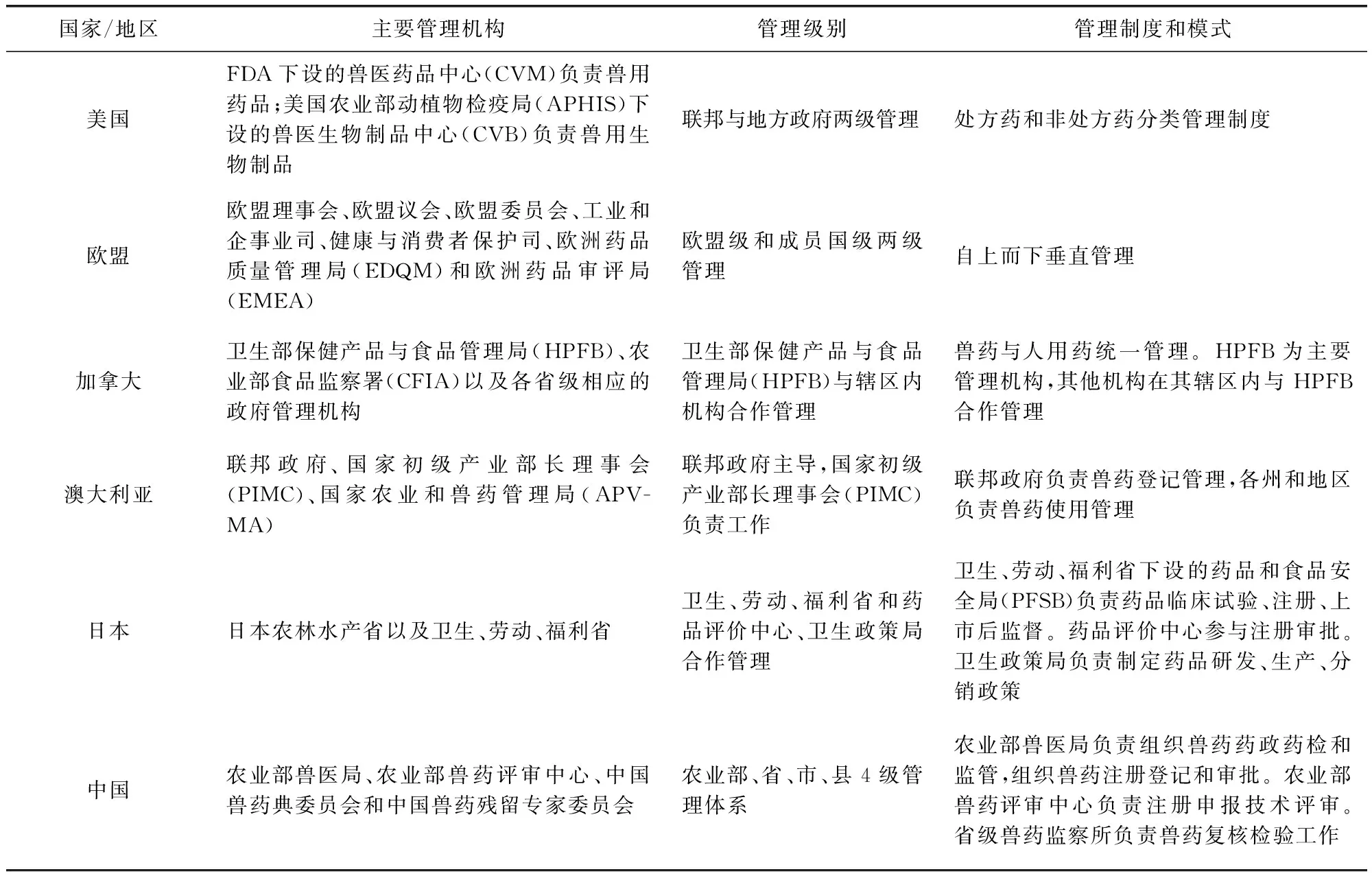
表1 有关国家兽药管理机构及管理模式一览表Tab 1 Veterinary medicine management structure&mode in relevent countries
1.1 美国 美国1968年颁布《兽药修正案》,开始了真正意义上的兽药法制化管理[2]。在兽药管理体制上,美国有联邦与地方两级管制机构,共同负责药物监督管理[3]。兽用药品由美国健康和人类服务部食品与药物管理局(FDA)下设的兽医药品中心(CVM)负责;美国兽用生物制品由美国农业部动植物检疫局(APHIS)下设的兽医生物制品中心(CVB)负责。
经过几十年的发展,美国形成了较完善的、与人用药同步的兽药管理法规体系,对兽药开发、生产等各阶段均有行业规范性标准加以控制,如良好实验室管理规范(GLP)、临床实验规范(GCP)、药品制造规范(GMP)。值得一提的是,美国首先提出的药品分类管理制度,即处方药(Rx)和非处方药(OTC)管理模式,已成为当今世界上广为采用且行之有效的药品管理模式[4]。1938年,美国颁布《食品、药品、化妆品法》,首次使用处方药与非处方药的法定用语;1951年国会通过《Durham-Humphrey修正案》,正式确立了处方药与非处方药的分类标准和OTC制度。随后日本、法国、德国等国先后借鉴美国经验,实行药品分类管理制度。自2000年起,我国正式在人用药品管理上实施该制度。
1.2 欧盟 欧洲是全球兽药产业的领导核心,兽药管理法治化程度较高,技术法规主要以条例、指令、决议等形式颁布实施,已经形成了一套相当完备、有机联系的法律体系。欧盟兽药管理机构组织模式是“直线职能制”,实行自上而下的垂直管理和欧盟级和成员国两级管理制度。成员国负责强化兽药管理机关独立性建设,切实保护消费者权益。欧盟理事会、欧盟议会、欧盟委员会负责统一管理法规和标准,协调制定行业发展大政方针;工业和企事业司、健康与消费者保护司协同运作,欧洲药品质量管理局(EDQM)和欧洲药品审评局(EMEA)负责药品的集中统一管理;国家兽药主管机关则负责处理具体事务[5]。
1.3 加拿大 在加拿大,兽药与人用药按照药品进行统一管理。联邦《食品药物法》和《食品药物规章》,有时统称为联邦《食品药物法案与规章》(FDAR),是加拿大管理食品、药物、化妆品、设备、管制药物和限制药物的两部主要法案,其规定条款具有强制性。参与兽药管理的机构主要包括卫生部保健产品与食品管理局(HPFB)、农业部食品监察署(CFIA)以及各省级相应的政府管理机构。这些机构各司其职,共同对兽药进行监督管理。其中,HPFB是主要的兽药管理机构,其下设的生物产品与食品监察处负责兽药企业和兽药生产的许可批准管理,其他机构在其辖区内协助 HPFB开展管理工作[6]。
1.4 澳大利亚 澳大利亚对兽药管理体系相对完整。联邦政府主导开发、管理、评价和改进兽药管理体系,国家初级产业部长理事会(PIMC)具体负责此项工作。国家农药和兽药管理局(APVMA)负责制定国家级的兽药登记计划。该计划对所有在澳大利亚使用的兽药生产和供应进行登记与管理。
1.5 日本 日本农林水产省以及卫生、劳动、福利省负责兽药和兽用器械管理。卫生、劳动、福利省下设的药品和食品安全局(PFSB)负责药品临床试验、注册、上市后监督,药品评价中心参与注册审批,卫生政策局负责制订药品研发、生产、分销政策。日本药品管理完全实行国际化标准,药典同欧盟药典、美国药典协调一致。自20世纪80年代开始,注重同欧美国家合作,药品管理系统与欧美药品管理系统密切合作,相互认可,并与欧美共同建立了协调组织——国际兽药注册协调会(VICH),负责协同药品管理政策制度。
1.6 中国 我国兽药行政管理体系由农业部、省、市、县4级构成。2004年7月,农业部正式成立了主管全国兽医兽药工作的行政管理机构--农业部兽医局,形成了以农业部兽医局为核心,由中国兽医药品监察所(农业部兽药评审中心)、中国兽药典委员会和中国兽药残留专家委员会组成的相对健全的兽药管理组织架构。
《兽药管理条例》明确规定,国务院兽医行政管理部门负责全国的兽药监督管理工作,兽用新生物制品和进口兽用生物制品必须到国务院畜牧兽医行政管理部门申报、批准,明确提出实施兽药分类管理的新制度。作为农业部内设机构,农业部兽医局负责组织兽药药政药检和兽医实验室监管,组织制订兽医、兽药标准并监督实施,统一组织兽药、兽医医疗器械及兽用生物制品的注册登记和进出口审批,并负责兽用生物制品和兽用药品的审批发证等[7]。经农业部授权,农业部兽药评审委员会对国内兽用新生物制品和新兽药的申报资料及进口兽用生物制品和兽用药品的注册申报资料进行审评;负责定期召开注册资料的初审和复审会,由委员会聘任的评审专家对申报资料进行评议[8]。农业部直属单位——中国兽医药品监察所(农业部兽药评审中心)负责对申报的兽用新生物制品、进口兽用生物制品注册技术评审和兽用新生物制品的复核检验工作[9]。省级兽药监察所负责兽药制品的复核检验工作。
1998年1月5日农业部发布的农业部令第34号《进口兽药管理办法》规定,国家对进口兽药实行注册管理制度,凡外国企业生产的兽药首次向中华人民共和国销售的,必须申请注册,取得《进口兽药登记许可证》;未经注册的兽药,不准在中华人民共和国境内销售、分装、使用和进行商业性宣传[10]。 2013年9月,农业部令第2号出台,正式实施兽用处方药和非处方药制度。随后,农业部发布了第1997号公告《兽用处方药品种目录》、第2069号《乡村兽医基本用药目录》,开始逐步深入推进兽药分类管理制度实施。
2 比较分析
美国、欧盟等发达国家的兽药管理法制化程度较高,药政、药监和药检三个体系并存,各司其职、彼此衔接、相互监督。药政体系负责制定兽药管理制度;药监体系负责兽药生产、经营和使用的监督和处罚;药检体系负责兽药产品质量检验,为行政执法部门提供技术支持[3]。美国和欧盟兽医生物制品注册管理起步较早,注册程序和技术要求相对全面合理,管理模式较为成熟。相对而言,我国兽药管理的法规体系还存在不够完善、效力不足等问题。
2004年新修订的《兽药管理条例》颁布实施以后,农业部发布了相关配套规章,为推动兽药产业发展奠定了法律基础。但是,由于《兽药管理条例》处罚条款效力有限,所以在实际工作中执法监督的有效性受到了明显影响。
相关配套规章不完善,如尚未制定完善的兽用处方药和非处方药分类管理办法、兽药储备制度、兽药非临床研究质量管理规范(兽药GLP)、兽药临床研究质量管理规范(兽药GCP)、兽药经营质量管理规范(兽药GSP)、兽药安全使用管理规范、兽药不良反应监测报告制度等[3]。
中国兽药监控网络、工作机制尚不健全。兽药质量相关监测设施设备落后、缺乏,监测经费不足,难以有效、深入开展兽药质量监控、兽药残留监测、病原微生物耐药性监测等工作。
3 加强我国兽药管理的对策与建议
加强兽药管理意义重大,任务艰巨,不可能一蹴而就。建议深入研究欧美兽药管理体制,立足国情研究借鉴发达国家的有益经验和做法,完善我国兽药管理体制。
3.1 进一步加强兽药法律体系建设 加快立法进程,修改完善《兽药管理条例》,并力争出台《兽药管理法》。进一步完善相关配套规章,解决GSP、GLP、GCP等规章制度操作性不强问题,以及兽用生物制品GCP制度落实难的问题。
3.2 创新兽药管理制度 研究建立兽药产品的相关质量认证和市场准入资格制度,确立兽药企业资格认证标准。加大知识产权保护力度,完善兽药产品批准文号管理制度,修订兽药注册办法,调整不同类别兽药注册要求,建立符合中兽药特点的注册制度,科学设定宠物用药质量标准与食品动物用药质量标准。
3.3 完善市场准入和退出机制 提高兽药生产经营技术门槛,遏制低水平重复建设势头;淘汰生产工艺落后、质量安全隐患大的兽药产品。改革完善强制免疫疫苗定点企业指定制度。完善新兽药安全评价标准,强化兽用抗菌药安全风险评估,加快淘汰高风险品种。建立兽药研发、生产和经营企业信用记录,实施基于企业信用评价的差别化监管制度。
3.4 加快国家、省、市级兽药残留监控网络建设 完善并深入实施国家残留监控计划,加大动物及动物产品兽药残留监控力度,加强动物源细菌耐药性监测。同时,引导广大养殖场(户)科学合理使用兽药,促进养殖主体改善养殖条件,减少兽药使用并严格遵守休药期规定。
3.5 大力实施兽用药品追溯监管制度 推进兽药产品追溯系统建设,完善全国性的兽药残留信息网络,逐步实现兽药生产、经营和使用环节全程可追溯监管,为有效控制兽药残留提供信息支撑[11]。
[1] 中商情报网. 2012年全球兽药行业发展概况. http://www.askci.com/news/201204/26/2615555227721.shtml
Askci Corporation. Overview of Global Veterinary Drug Industry in 2012. http://www.askci.com/news/201204/26/261555522-7721.shtml
[2] 周生俊. 初论兽医产业[J].中国动物检疫, 2001,18(7):9-10.
ZHOU S. Brief study of veterinary drug industry. [J]China Animal Inspection, 2001, 18(7): 9-10.
[3] 游锡火, 王倩倩, 张兴. 美国兽药管理及经验借鉴[J]. 世界农业, 2013 (6): 4-6.
You X H, Wang Q Q, Zhang X. Veterinary drug administration and experience in the United States.[J]. Globle Agriculture, 2013 (6): 4-6.
[4] 冯忠武. 加快兽药分类管理 确保兽药使用安全[J]. 中国兽药杂志, 2007, 41(11): 1-3.
Feng Zh W. Facilitating classification management of veterinary drugs-to ensure safe utilizatization of veterinary drugs.[J]. Chinese Journal of Veterianry Drug, 2007, 41(11): 1-3.
[5] Pastoret P P, Falize F. Licensing procedures for immunological veterinary medicinal products in the European Union[J]. Advances in Veterinary Medicine, 1999, 41(41):595-607.
[6] Health Products & Food Branch/ Branches & Agencies/ Health Canada About Veterinary Drugs Directorate [EB/OL]. (2006)
[7] 国务院. 《兽药管理条例》. 2004年4月9日发布.
State Council. Regulation on veterinary drugs. April 9, 2004.
[8] 农业部兽药审评委员会办公室. 《兽用生物制品评审工作管理办法》.
Department of Vveterinary Drug Review Committee of the Ministry of Agriculture. Management measures of veterinary biologicals review and approval.
[9] 农业部. 《兽药药政药检管理办法》. 1989年9月2日发布.
Ministry of Agriculture. Management measures of veterinary drug administration and Inspection. September 2, 1989.
[10]农业部. 《进口兽药管理办法》. 1998年1月5日发布.
Ministry of Agriculture. Management measures of imported veterinary drugs. January 5, 1998.
[11]董义春, 孙立新, 黄玲利, 等. 发达国家的兽药管理现状及对策[J]. 世界农业, 2008 (10): 27-30.
Dong Y Ch, Sun L X, Huang L L,etal. Currenct situation and countermeasure study of veterinary drug administration in developed countriesy.[J]Globle Agriculture, 2008(10): 27-30
(编辑:陈希)
中国兽药杂志
CHINESE JOURNAL OF VETERINARY DRUG
编辑委员会
顾 问: 于康震 陈焕春 夏咸柱 刘秀梵 张改平
主 任: 才学鹏
副主任: 李 明 徐肖君 程新元 杨劲松 冯忠泽 陈光华 李慧姣
委 员:(按姓氏笔画排序)
丁家波 才学鹏 万仁玲
王乐元 王永胜 王树双
冯忠泽 朱鸿飞 刘业兵
刘湘涛 李 明 李慧姣
杨汉春 杨劲松 步志高
沈志强 沈建忠 张存帅
张许科 张继喻 陈光华
陈瑞爱 赵彦岭 段文龙
班付国 袁宗辉 夏业才
顾进华 徐士新 徐肖君
殷 宏 高艳春 康 凯
董义春 蒋玉文 蒋桃珍
童光志 曾振灵 翟新验
发行范围 国内外公开发行
国内发行 北京报刊发行局
邮发代号 2-924
印 刷 北京科信印刷有限公司
广告许可证 京海工商广字第0030号
每期定价 12.00元
A Comparitive Study of Domestic and Overseas Veterinary Drug Administration
GE Lin1, LIU Xiao-fei2, WANG Qin2, WANG Zhong-tian3
(1.University of International Business and Economics, Beijing 100029, China; 2.Chineses Academy of Inspection and Quarantine, Beijing 100029, China; 3.China Institute of Veterinary Drug Control, Beijing 100081, China)
Veterinary drugs play a vital role in the prevention and control of animal diseases, improving the efficiency of animal breeding, and safeguard of public health. Nevertheless, more effective management of veterinary drugs is in great demand, especially in such areas as veterinary drug residue control and antimicrobial resistance control. This essay gives a brief introduction on veterinary drug management system in the developed countries. Some suggestions are made to strengthen the administration of veterinary drugs and promote the development of veterinary drug industry in China.
veterinary drugs; supervision; suggestions
10.11751/ISSN.1002-1280.2017.8.13
葛林, 副教授,从事兽药相关研究。E-mail: sunyan@agri.gov.cn
2017-06-09
A
1002-1280 (2017) 08-0073-05
S851.66
