临床微生物形态学及特殊耐药性检测室间质量评价体系的建立及应用
2017-08-17魏莲花邹凤梅刘刚杨永清王晚霞吴玲李军春王欣陈玉芊陈晓青李可可邵海鑫朱吉超
魏莲花,邹凤梅,刘刚,杨永清,王晚霞,吴玲,李军春,王欣,陈玉芊,陈晓青,李可可,邵海鑫,朱吉超
(1.甘肃省人民医院检验科,甘肃省临床检验中心,兰州 730000;2.甘肃中医药大学,兰州 730000;3.宁夏医科大学临床医学院,银川 750004)
·质量管理研究·
临床微生物形态学及特殊耐药性检测室间质量评价体系的建立及应用
魏莲花1,邹凤梅1,刘刚1,杨永清1,王晚霞1,吴玲1,李军春1,王欣1,陈玉芊1,陈晓青2,李可可2,邵海鑫2,朱吉超3
(1.甘肃省人民医院检验科,甘肃省临床检验中心,兰州 730000;2.甘肃中医药大学,兰州 730000;3.宁夏医科大学临床医学院,银川 750004)
目的 研究临床微生物形态学及特殊耐药性检测室间质量评价(external quality assessment, EQA)体系的建立、运行与实施,探讨该体系的临床应用价值。方法 每年2次定期在甘肃省对各参评实验室发放已知的临床微生物细(真)菌落、革兰染色、抗酸染色图片,以及美国临床和实验室标准化协会(Clinical and Laboratory Standards Institute, CLSI)标准更新的知识点(特殊耐药性检测)结果图片。要求各参评单位在规定时间内完成判读并上报结果。回报结果以完全符合、基本符合和不符合的形式进行总结、分析。结果 临床微生物形态学及特殊耐药性检测EQA体系运行2年,共进行24次,年度完全符合率逐年上升,2015年达到91.3%。结论 临床微生物形态学及CLSI标准知识点考核EQA体系可督导二级以上医院临床微生物检验人员掌握形态学识别技能及学习CLSI知识点,全面提高临床微生物人员专业技能。
微生物形态学;CLSI;特殊耐药;室间质量评价
近年来,随着自动化细菌鉴定及药敏分析仪、质谱技术等快速检测技术在临床微生物实验室的广泛应用,部分检验人员过分依赖自动化仪器的现象较为严重,以致自动化仪器鉴定错误时不能结合微生物形态学等传统手段加以综合分析。微生物形态学检测或传统鉴定方法应用已普遍成为当前国内临床微生物检验人员的薄弱环节。而细(真)菌菌落形态、镜下形态是准确鉴定细菌、真菌的重要手段之一。美国临床和实验室标准化协会(Clinical and Laboratory Standards Institute, CLSI)制定的药敏试验标准是我国微生物实验室遵循的指导性文件[1],加上CLSI每年有更新,其中也涉及特殊耐药性检测的方法。很多临床微生物检验人员对此主动学习不够,致使缺乏相关知识和基本检测技能。基于此,2014年,我们在全国率先开始探索临床微生物形态学、细菌特殊耐药检测室间质量评价(external quality assessment,EQA)体系,并在全省范围内应用。本研究通过对近2年EQA结果的分析,探讨其临床应用价值。
1 材料与方法
1.1 细(真)菌菌落图片及镜下形态图片制作 收集质控菌株、临床标本中分离的典型菌株。细菌按照标准划线方法接种于血平板上,35 ℃温育18 h;丝状真菌接种于沙氏平板,25 ℃温育48 h。用高像素相机拍摄菌落形态图片;根据考核要求,按照常规方法涂片、革兰染色、抗酸染色,油镜下拍摄镜下形态图片。部分图片见图1-4。
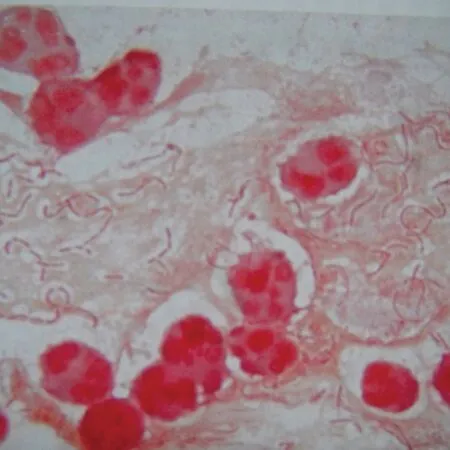
图1 黏液型铜绿假单胞菌革兰染色镜下形态(×1 000)

图2 “鬼影细胞”革兰染色镜下形态(×1 000)
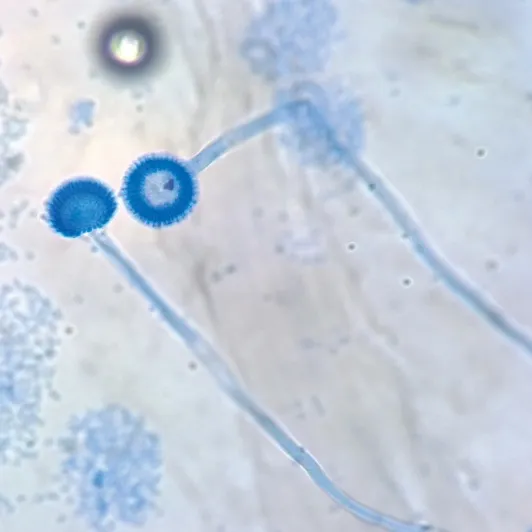
图3 曲霉乳酸酚棉蓝染色镜下形态(×1 000)
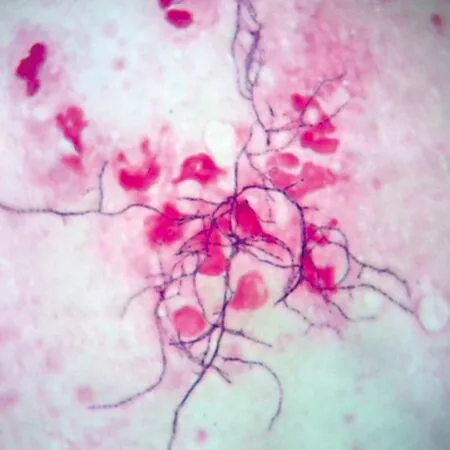
图4 诺卡菌革兰染色镜下形态(×1 000)
1.2 特殊耐药检测考核图片制作 根据CLSI[2]要求进行特殊耐药性检测(如:ESBLs检测、MRSA检测、耐青霉素的交叉耐药性检测和协同试验等)并拍照制成图片。
1.3 EQA方法 根据已知的细菌、真菌菌落形态及细菌特殊耐药现象检测进行定靶。甘肃省临床检验中心对全省130家二级以上医院检验科,2014和2015年每年统一发放2次,每次发放6张图片,共计24张图片,分别按照年份加序号编号:2014年为201401-201412,2015年为201501-201512,并同时对患者主要症状、体征或临床诊断等做简明阐述。要求参评单位在规定时间内回报结果,结果回报方式为选择题或自主回答2种方式,如判断特殊耐药试验的阴阳性,根据菌落形态或涂片染色镜检形态报告疑似菌名。检验中心收到回报结果后按照评价标准,将质评结果、正确结果、误差原因分析、有关新资料等信息及时反馈给参评实验室。
2 结果
2.1 回报率 2次EQA共24张图片,2014年参评单位119家,2次回报率均为68.07%(81/119);2015年参评单位103家,2次回报率分别为65.05%(67/103)和77.67%(80/103)。总回报率由2014年的68.07%提高到2015年的71.36%。
2.2 考核结果符合率
2.2.1 菌落及显微镜下形态学 2014年临床微生物菌落形态EQA考核内容为卫星试验和马尔尼菲蓝状菌,完全符合率分别为98.77%和61.73%;2015年的考核内容为变形杆菌的迁徙现象,完全符合率为91.04%。2014年镜下形态考核内容有铜绿假单胞菌“腊肠样”、抗酸染色阳性、淋球菌、“鬼影”细胞、丝状真菌及奴卡菌等图片,完全符合率分别为71.60%、97.53%、98.77%、66.67%、80.25%及98.77%。见表1。
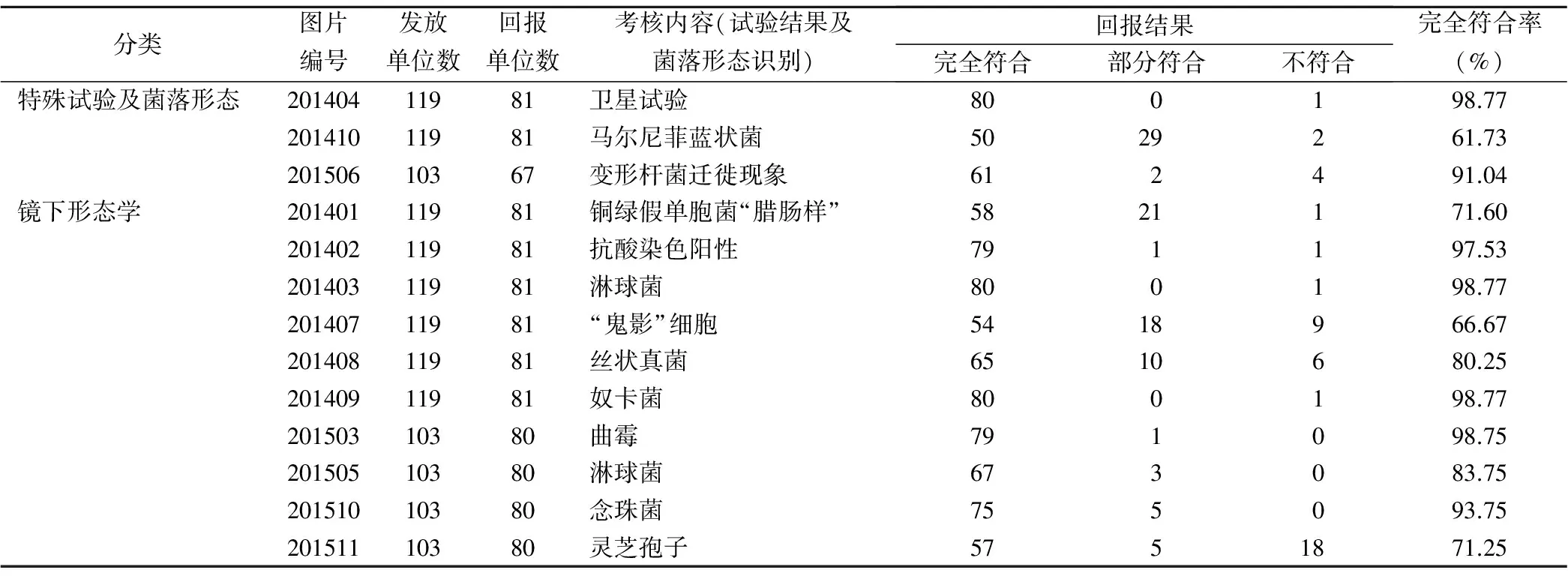
表1 2014至2015年临床微生物菌落及镜下菌体形态室间质评结果
2.2.2 细菌特殊耐药现象 2014年细菌特殊耐药现象考核内容有D-试验、ESBLs筛查试验、β-内酰胺酶试验及肺炎链球菌青霉素E-试验,完全符合率分别为96.30%、82.72%、92.59%及51.85%。2015年考核内容有替加环素E-试验、改良Hodge试验结果判断、MRSA筛选、Carba NP试验、D-试验、ESBLs筛查试验及耐青霉素肺炎链球菌(PRSP)筛查,完全符合率分别为75.00%、98.51%、71.25%、92.50%、100%、97.50%及47.50%。见表2。

表2 2014至2015年临床微生物特殊耐药检测方法图片室间质评结果回报
3 讨论
甘肃省临床检验中心自2014年开始在以往传统的EQA项目的基础上,结合省内临床技术人员的现状,对临床微生物室间质评的调查内容进行创新改革,增设细(真)菌形态学及特殊耐药现象判断的考核。通过将相关内容制作成图片,在省检验中心网站上统一发布,要求参评单位认真参照图片,按照要求回答考核点并及时回复结果。菌落质评图以细(真)菌常见典型菌落或特殊菌落为主;显微镜下形态以典型形态和特殊形态为主;细菌特殊耐药考核涉及多方面,包括E-试验判读、特殊耐药性检测(ESBLs、AmpC、Hodge试验、β-内酰胺酶检测及判断等。发放范围包括二级以上参评实验室,以自愿参加为原则,质评结果以“完全符合、部分符合及不符合”进行评价。每年固定进行2次,考核的内容逐渐扩大,但保证每年有CLSI的最新更新内容。
特殊试验及菌落形态考核,我们设计了3个图片:卫星试验是鉴定嗜血杆菌属中流感嗜血杆菌和副流感嗜血杆菌的关键试验,第一次调查时卫星试验图片参评实验室合格率较高,达98.77%,说明各单位对判该实试验的判断要领已基本掌握。马尔尼菲蓝状菌是引起艾滋病患者感染的真菌,为了让参评实验室认识该真菌在沙氏琼脂平板上培养2周左右呈玫瑰红色菌落[3],我们在2014年EQA活动中发放了1张该菌菌落形态图片,完全符合率仅为61.73%,这也从一个侧面反映出微生物实验室在日常工作中对该菌存在漏检或错误鉴定的问题。提示质评组织者今后还需反复发放该菌菌落图片,以强化检验人员真正认识该菌。变形杆菌迁徙现象较常见,第一次发放完全符合率达到91.04%,提示组织者对一些基本理论及基本现象可以通过这种形式督导检验人员学习掌握。
显微镜下形态学考核图片较多,包括黏液型铜绿假单胞菌“腊肠样”、抗酸染色阳性、淋球菌、“鬼影”细胞、丝状真菌、诺卡菌、曲霉、淋球菌、念珠菌、灵芝孢子等,其中,黏液型铜绿假单胞菌“腊肠样”镜下判断符合率仅为71.60%。说明有一部分检验人员对此形态学并不认识。
抗酸杆菌在革兰染色时不易着色,有经验者在显微镜下可观察到白色的条状影子,称之为“鬼影”细胞[4],提示操作者可再进行抗酸染色以验证,无经验者因不认识这种形态就容易漏检。“鬼影”细胞图片第一次调查完全符合率仅有66.67%,今后还将继续发放。患者口服灵芝孢子后留取痰液标本时易受此污染,不熟悉或不认识此形态者易将此判为寄生虫卵,第一次调查时完全符合率仅为72.50%。其他图片如抗酸染色、革兰阴性双球菌(疑似淋球菌)、丝状真菌、奴卡菌、曲霉、念珠菌等有比较好的符合率。
特殊耐药性检测考核中设计了11项考核点,围绕CLSI M100-S24、S25中规定的检测方法进行。CLSI规定当肺炎链球菌对青霉素抑菌环直径小于19 mm时,必须用E-test或其他方法检测该菌的最低抑菌浓度(MIC),以确认是否真正耐青霉素肺炎链球菌菌株。2014年第一次发放E-试验结果判读调查图片,要求准确判读E-试验结果,但由于很多实验室日常工作中对CLSI M100-S24、S25中涉及到的检测方法领会不深,甚至在工作中并未按照CLSI指南进行常规工作,因此,在结果判读上出现很多错误,完全符合率仅为51.85%;2015年,进行第二次调查,要求通过图片判断是否“PRSP”,结果完全符合率甚至比第一次还低,仅仅为47.50%。说明参评实验室对CLSI M100-S24、S25知识点的掌握还不够牢固。相反,在室间质评中也发现检验人员对CLSIM100-S24、S25上的一些简单知识点掌握较好,如金黄色葡萄球菌D-试验,第一次考核时完全符合率达到96.30%,第二次考核完全符合率为100%。
我们从2014年开始,通过设置一系列新的考核点,逐步建立、完善并实施微生物形态学EQA体系,对错误结果进行反馈分析并发放相关新资料,这种新形式的临床微生物EQA体系的建立及实施使我省大部分实验室开始重视形态学技能及CLSI知识点的学习。有的图片如D-试验,通过反复发放,完全符合率明显提高,说明临床微生物形态学及CLSI中规定的特殊耐药检测室间质量评价体系的建立及应用是提高细(真)菌检验及督促学习CLSI M100进而提高药敏试验水平的重要手段之一。另一方面,本研究中的部分结果,如淋球菌、马尔尼菲蓝状菌等仅根据染色形态难以准确鉴定到种,回报单位仅仅是报告疑似结果,不要求报告鉴定结果,这在一定程度上影响了回报结果的完全符合率,也是我们下一步需要着重解决的问题之一。
致谢:卫生部北京医院检验科微生物室陈东科老师提供部分图片,特此致谢!
[1]张雅薇,王辉. 2016年CLSI M100S(第26版)主要更新内容解读[J].中华检验医学杂志,2016,39(3):165-169.
[2]Clinical and Laboratory Standards Institute. M100S. Performance standards for antimicrobial susceptibility testing:twenty-sixth edition[S].Wayne,PA:CLSI,2016.
[3]陈东科, 孙长贵. 实用临床微生物学检验与图谱[M]. 北京:人民卫生出版社, 2011.
[4]Trifiro S, Bourgault AM, Lebel F,etal. Ghost mycobacteria on Gram stain[J]. J Clin Microbiol, 1990, 28(1):146-147.
(本文编辑:刘群)
Establishment and application of external quality assessment system for microbial morphology and detection of special drug-resistance in clinical laboratory
WEILian-hua1,ZOUFeng-mei1,LIUGang1,YANGYong-qing1,WANGWan-xia1,WULing1,LIJun-chun1,WANGXin1,CHENYu-qian1,CHENXiao-qing2,LIKe-ke2,SHAOHai-xing2,ZHUJi-chao3
( 1.DepartmentofClinicalLaboratory,GansuProvincialCenterforClinicalLaboratory,GansuProvincialHospital,Lanzhou730000,Gansu; 2.GansuUniversityofChineseMedicine,Lanzhou730000,Gansu; 3.SchoolofClinicalMedicine,NingxiaMedicalUniversity,Yinchuan750004,Ningxia,China)
Objective To investigate the establishment, operation and performance of external quality assessment(EQA) system for microbial morphology and detection of special drug-resistance in clinical laboratory, and explore the value of the developed system in clinical application. Methods The pictures of known bacteria and fungi colony, gram staining and acid-fast staining from clinical microbiology were distributed to the participating laboratories in Gansu province twice a year at regular intervals. The pictures of standard knowledge points from CLSI, such as special drug resistance were distributed simultaneously. All the participating laboratories were required to complete the interpretation for the pictures and report their results in a scheduled time. Then the results were summarized and analyzed as 3 modes: complete consistency, general consistency and non-consistency. Results During the 2 years when the EQA system for microbial morphology and detection of special drug-resistance were performed for 24 times, the rate of annual complete consistency increased year by year and reached to 91.3% in 2015. Conclusion The EQA system based on the examinations of microbial morphology and CLSI standard knowledge points for clinical laboratory may supervise the staff of clinical microbiology laboratories in the hospitals at second grade or above to master the skills of morphological identification and learn CLSI knowledge points, so their professional skills of clinical microbiology could be comprehensively improved.
microbial morphology; CLSI; special drug-resistance; external quality assessment
10.13602/j.cnki.jcls.2017.07.16
魏莲花,1965年生,女,主任技师,博士,从事临床微生物检验及临床微生物室间质量评价管理工作。
R446.5
A
2017-03-02)
