301例抗菌药物致药品不良反应/事件报告Δ
2017-08-12姚楠泓许伟帅余小红彭怀东钟询龙
姚楠泓,许伟帅,余小红,彭怀东,钟询龙#
(1.广东省中医院药剂科,广东 广州 510105; 2.佛山市南海区第三人民医院药剂科,广东 佛山 528244; 3.广州医科大学附属第二医院药学部,广东 广州 510260)
·药学监护·
301例抗菌药物致药品不良反应/事件报告Δ
姚楠泓1*,许伟帅1,余小红2,彭怀东3,钟询龙3#
(1.广东省中医院药剂科,广东 广州 510105; 2.佛山市南海区第三人民医院药剂科,广东 佛山 528244; 3.广州医科大学附属第二医院药学部,广东 广州 510260)
目的:探讨抗菌药物致药品不良反应(adverse drug reaction,ADR)/药品不良事件(adverse drug event,ADE)发生的一般特点及规律,为促进临床合理用药提供参考。方法:收集2006年1月1日—2014年4月30日上报至国家ADR监测中心的301例抗菌药物致ADR/ADE报告,根据患者的年龄、性别、原患疾病,给药途径、联合用药、ADR/ADE发生时间、涉及抗菌药物种类、累及器官和(或)系统及主要临床表现、严重的ADR/ADE涉及药品等进行回顾性分析。结果:301例抗菌药物致ADR/ADE报告中,女性患者略多于男性;>60岁患者数最多(122例,占40.53%);呼吸系统疾病患者数最多(139例,占46.18%);静脉滴注仍是引发ADR/ADE的主要给药方式; 联合用药引发的ADR/ADE较多。头孢菌素类抗菌药物引发的ADR/ADE例次数排序居首位,其次为氟喹诺酮类和青霉素类抗菌药物;引发ADR/ADE例次数排序居前3位的药品分别为头孢哌酮他唑巴坦、左氧氟沙星、环丙沙星。ADR/ADE以皮肤及其附件损害最为常见,其次为全身性损害、消化系统损害等。301例ADR/ADE报告中,严重的ADR/ADE共24例(占7.97%),头孢菌素类抗菌药物引发严重的ADR/ADE最多。结论:ADR/ADE的发生与诸多因素有关,临床应强医、药、患合作,同时积极发挥临床药师的作用,促进合理用药。
抗菌药物; 药品不良反应/事件; 回顾性分析; 合理用药
抗菌药物具有抗菌谱广、抗菌活性强等特点,被广泛应用于临床,挽救了无数患者生命,是临床上重要的治疗药物。近年来,随着抗菌药物的广泛应用,有关抗菌药物致药品不良反应(adverse drug reaction,ADR)/药品不良事件(adverse drug event,ADE)的报道也日渐增多[1-4]。ADR指质量合格的药品在正确的用法与用量下出现的与治疗目的无关的有害反应;ADE指药物治疗过程中出现的不良临床事件。本调查对收集的301例抗菌药物致ADR/ADE报告进行回顾性分析,旨在探讨抗菌药物致ADR/ADE的一般特点和规律,为临床合理用药提供参考。
1 资料与方法
1.1 资料来源
收集2006年1月1日—2014年4月30日某院上报国家ADR检测中心的抗菌药物致ADR/ADE报告,共301例。
1.2 方法
对患者的年龄、性别、原患疾病,给药途径、联合用药、ADR/ADE发生时间、涉及抗菌药物种类、累及器官和(或)系统及主要临床表现、严重的ADR/ADE涉及的药品等进行回顾性统计分析。参照《世界卫生组织不良反应术语集》对ADR/ADE累及器官和(或)系统进行分类。
2 结果
2.1 发生ADR/ADE患者的性别、年龄及原患疾病分布
301例发生ADR/ADE的患者中,男性149例(占49.50%),女性152例(占50.50%),男女比例约为1∶1.02;>60岁患者数最多,其次为40~≤60岁者;呼吸系统疾病患者数最多,见表1。
2.2 发生ADR/ADE的给药途径分布及联合用药情况
301例ADR/ADE中,静脉滴注给药引发278例,仍是引发ADR/ADE的主要给药方式;大多数ADR/ADE由联合用药引发(包括抗菌药物与抗菌药物、抗菌药物与其他种类药物的联合应用),见表2。
2.3 ADR/ADE发生时间分布
ADR/ADE最早发生在用药1 min后,最晚发生在用药15 d后,多发生在用药30 min内,见表3。
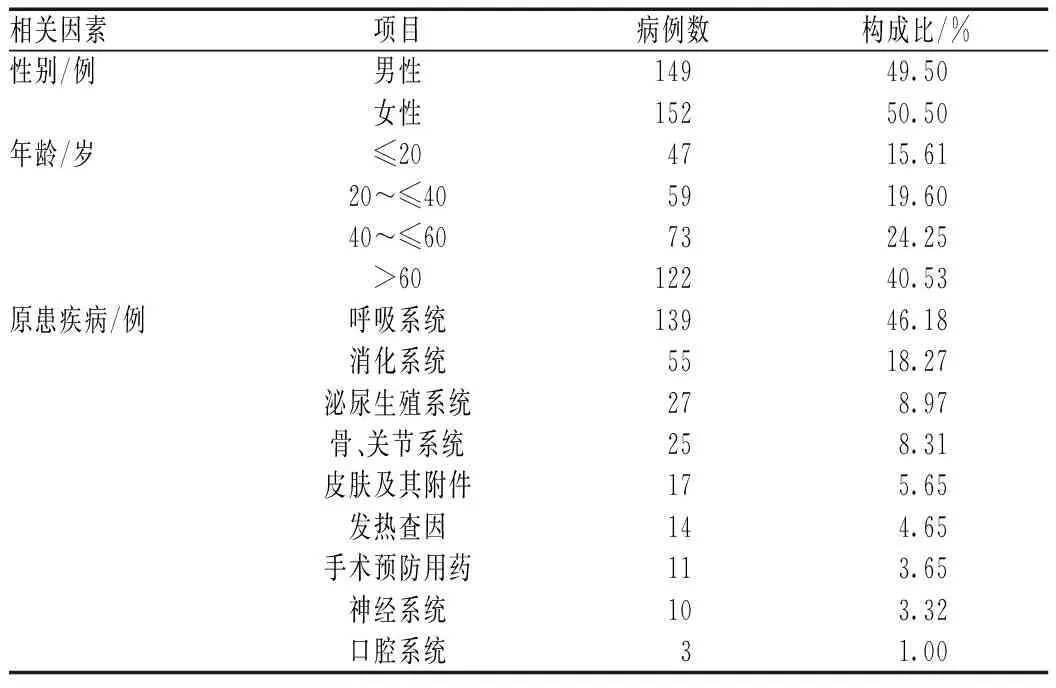
表1 发生ADR/ADE患者性别、年龄及原患疾病分布
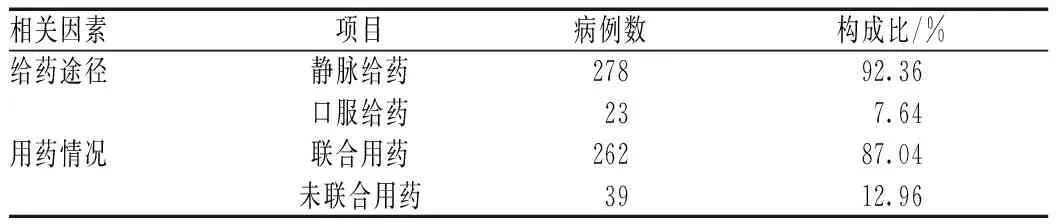
表2 发生ADR/ADE的给药途径分布及联合用药情况Tab 2 Distribution of routes of administration of ADR patients and the drug combination
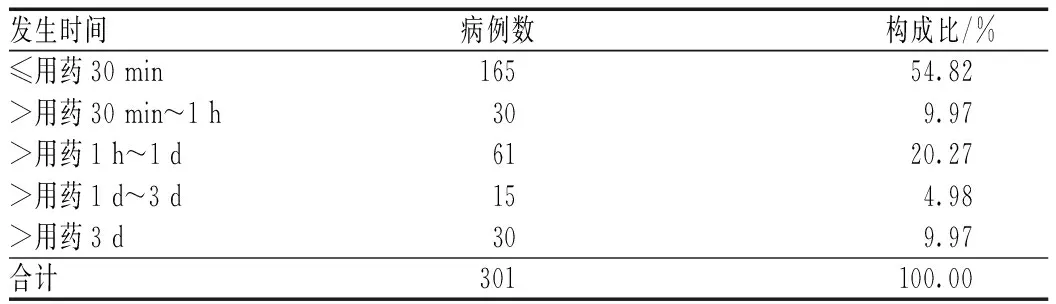
表3 ADR/ADE发生时间分布
2.4 ADR/ADE涉及抗菌药物种类分布
301例ADR/ADE共涉及抗菌药物10类54个品种,其中头孢菌素类抗菌药物引发的ADR/ADE例次数最多,其次为氟喹诺酮类和青霉素类抗菌药物;引发ADR/ADE例次数排序居前3位的药品分别为头孢哌酮他唑巴坦、左氧氟沙星、环丙沙星,见表4。

表4 ADR/ADE涉及抗菌药物种类分布
注:由于存在联合用药,故总例次数>301例
Note: due to the drug combination, therefore the total number of cases >301
2.5 ADR/ADE累及器官和(或)系统及主要临床表现
301例ADR/ADE中,皮肤及其附件损害最为常见(216例,占60.85%),其次分别为全身性损害(44例,占12.39%)、消化系统损害(23例,占6.48%)等,见表5。

表5 ADR/ADE累及器官和(或)系统及主要临床表现
注:同一ADR/ADE可能累及多个器官和(或)系统,故总例次数>301例
Note: several organs and (or) systems could be involved by one ADR/ADE, therefore the total number of cases >301
2.6 严重的ADR/ADE涉及药品分布
301例ADR/ADE中,严重的ADR/ADE共24例(占7.97%),其中新的、严重的ADR/ADE 5例,多由头孢菌素类、氟喹诺酮类及青霉素类等抗菌药物引起,见表6。
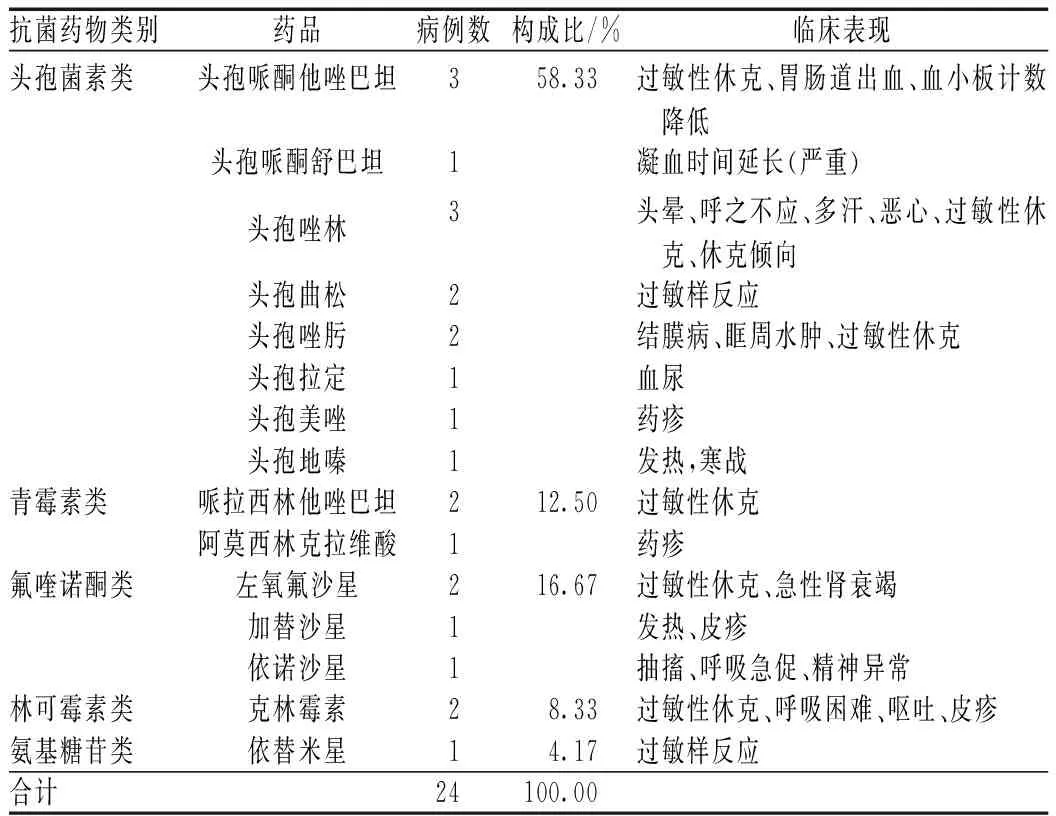
表6 严重的ADR/ADE涉及药品分布Tab 6 Distribution of severe ADR/ADE involved drugs and its constituent ratios
3 讨论
3.1 ADR/ADE与患者个体因素的关系
不同个体在性别、年龄、遗传、病理、生理、药物代谢酶及个人饮食生活习惯等方面存在差异,对药物的敏感性不同。老年患者易发生ADR/ADE,分析原因为:(1)老年患者肝、肾功能存在不同程度的衰退,机体对药物的代谢和排泄功能亦随之下降,发生ADR/ADE的风险增加;(2)老年患者多伴有多种慢性疾病,常需要联合、长期用药,药物相互作用也是发生ADR/ADE的诱因[5]。因此,老年患者在用药时应谨慎小心,用药过程中需加强监护和指导,并采取个体化的给药方案,以减少ADR/ADE的发生。
3.2 ADR/ADE与药物自身因素的关系
本调查中,头孢菌素类抗菌药物致ADR/ADE例次数最多,其原因为:(1)临床应用广泛。头孢菌素类抗菌药物具有抗菌谱广、抗菌作用强、对β-内酰胺酶的稳定性好、过敏反应少、毒性小等优点,是临床预防手术感染和治疗严重感染的首选药物。临床对抗菌药物进行分级管理后,非限制使用级头孢菌素类抗菌药物的用量大大增加,导致ADR/ADE发生率上升。ADR/ADE发生时间主要集中在用药30 min内,多为速发型过敏反应,主要包括严重的过敏性休克、过敏样反应等,因此,应加强患者用药后的监测,避免严重的ADR/ADE发生。同时,头孢菌素抗原决定簇的基本结构主要和其7位R1侧链的结构有关,青霉素与头孢菌素都含有β-内酰胺环,可以发生交叉过敏反应[6];头孢菌素7位侧链结构和青霉素6位侧链的结构越相似,交叉过敏反应越强。因此,10%~30%对青霉素过敏的患者仍对头孢菌素过敏,故在应用头孢菌素类抗菌药物前需进行皮肤敏感试验[7]。(2)在原料药(晶型、旋光异构体、稳定性)和制剂(有关物质、辅料、制备工艺)等方面存在差异。同一品种不同厂家的药品,其临床疗效和安全性可能存在差异。部分仿制药的组分含量及生物利用度低,杂质、中间体、副产物、降解产物、聚合物等相对较多,使药物疗效降低,甚至引发ADR/ADE。相关研究采用体内外模型评价仿制抗菌药物中微粒对危重症患者的影响,结果发现,仿制药的质量差别较大,很多仿制药含有大量微粒[8]。已有研究结果证实,静脉给药时,药物中的微粒会加重微循环功能受损。因此,高龄、危急重症、合并多种疾病、以及需联合用药的患者最好避免使用仿制药,以降低ADR/ADE的发生概率。
3.3 ADR/ADE与临床用药的关系
3.3.1 适应证:本调查中,上呼吸道感染和发热原因待查患者盲目使用抗菌药物是导致呼吸系统疾病患者ADR/ADE发生率较高的主要原因。上呼吸道感染大多为病毒感染,应用抗菌药物不仅不能达到治疗效果,反而会引起耐药性增加及菌群失调[9]。发热的原因较多,自身免疫性疾病如系统性红斑狼疮及亚急性甲状腺炎等均为引起发热的常见原因,应用抗菌药物治疗均不适宜。因此,用药前应结合患者症状和体征、辅助检查(血、尿、粪3大常规,血沉,C反应蛋白,降钙素原等)、病原学检查及药物敏感试验、抗菌药物治疗效果等进行综合评价。
3.3.2 用法与用量:给药剂量、给药频率以及用药疗程不合理常常是导致ADR/ADE发生的重要因素。老年高龄患者大多肾功能低下,大量或长期用药,血药浓度过高会导致ADR/ADE的发生。如某80岁患者(肌酐清除率<30 ml/min),给予头孢哌酮他唑巴坦2.0 g、1日3次、静脉滴注,连续使用7 d后出现严重凝血功能障碍,考虑为用药剂量偏大所致,该药说明书明确规定,严重肾功能不全者(肌酐清除率<30 ml/min),他唑巴坦的给药剂量不超过0.5 g,故应给予头孢哌酮他唑巴坦2.0 g、每12 h给药1次、静脉滴注。如某69岁患者,给予左氧氟沙星0.3 g、1日2次、静脉滴注,连续使用5 d后出现急性肾衰竭,氟喹诺酮类为浓度依赖性抗菌药物,有明显的抗菌后效应,故1日1次给药较为合理,相关文献报道,氟喹诺酮类日剂量>400 mg患者的ADR发生率明显高于日剂量≤400 mg的患者[10]。因此,抗菌药物的给药剂量、给药次数和疗程应严格遵循药品说明书,老年患者更应如此,应遵循药动学和药效学相结合的原则,及时调整给药剂量和用药时间,避免超剂量、超用法用药。本调查中,静脉滴注给药所致ADR/ADE病例数较多,可能与静脉滴注给药后,药物直接进入血液循环、起效快以及药物的pH、内毒素、杂质等因素有关,因此,临床用药时应注意选择合适的给药途径,严格规范静脉给药,遵循“能口服不肌内注射,能肌内注射不静脉滴注”的用药原则。
3.3.3 联合用药:抗菌药物通过抑制或诱导肝药酶CYP和P-糖蛋白(P-gp)对底物药物的代谢作用,导致与其联用的CYP450及P-gp底物药物产生代谢性药物相互作用。同时CYP450及P-gp抑制剂、诱导剂也可影响作为CYP450及P-gp底物的抗菌药物的体内过程,导致ADR/ADE或药源性疾病的发生[11]。老年患者常伴发多种疾病,如高血压病、糖尿病、冠心病、高脂血症等,需要联合使用多种药物,容易因代谢性药物相互作用引发ADR/ADE。本调查中,除头孢菌素类抗菌药物外,氟喹诺酮类所致ADR/ADE的病例数最多。氟喹诺酮类药物对CYP1A2有抑制作用,当与CYP1A2的底物药物联合应用时,可抑制CYP1A2底物药物(如氨茶碱、华法林、普萘洛尔等)的体内代谢过程,产生ADR/ADE。左氧氟沙星是P-gp的底物药物,与同是P-gp的底物药物(地高辛、洛伐他汀、多潘立酮、西米替丁)联合应用可产生竞争性抑制作用,与P-gp抑制药物(如胺碘酮、酮康唑、硝苯地平等)联合应用可降低其代谢,升高血药浓度,引发ADR/ADE。因此,临床应重视联合用药后的监测工作,尽量减少联合用药所致ADR/ADE。
3.3.4 皮肤敏感试验:目前,国外使用头孢菌素类抗菌药物无需进行皮肤敏感试验,国内对头孢菌素类抗菌药物尚无规范、统一的皮肤敏感试验标准,《中华人民共和国药典·临床用药须知》(2015年版)和《抗菌药物临床应用指导原则(2015年版)》中均未要求使用头孢菌素类抗菌药物前进行皮肤过敏试验[12]。但相关研究结果显示,皮肤敏感试验对于预防和减少国产头孢菌素类药物严重过敏事件的发生起着重要作用。除药物本身因素外,过敏反应的发生还与患者自身的过敏性体质密切关系,头孢菌素类药物(头孢美唑、头孢曲松除外)的皮肤敏感试验只限于过敏性体质的患者[13]。同时,在临床用药前,应仔细询问患者是否为过敏体质(如有无药物过敏史、食物过敏史以及过敏性疾病史等)。
3.4 ADR/ADE的预防策略
ADR/ADE的发生与多种因素相关,为避免或减少ADR/ADE,临床应用抗菌药物时应注意:(1)掌握老年患者药动学特征,把握个体化用药原则,严格遵循药品说明书的用法与用量;(2)肝、肾功能不全者应注意及时调整给药剂量,避免选用经肝或肾代谢和清除的药物;(3)严格掌握抗菌药物的适应证,熟悉抗菌谱、药理作用及其所致ADR的特点,合理选择药物,规范用法与用量;(4)用药前应仔细询问是否有药物过敏史,需皮肤敏感试验时应以该药原液作皮肤敏感试验;(5)加强用药监护,一旦发生严重过敏反应如过敏性休克或过敏样反应时应立即停药,并积极进行抢救和对症治疗;(6)注意药物代谢性相互作用的潜在风险,尽管许多药物的潜在相互作用还未见研究报道,然而临床实践证明,严重的药物相互作用常发生在联合用药的老年、危重患者。临床应加强对药物相互作用的预测,避免不必要的联合用药;(7)加强临床药理知识培训,提高其防范意识,发现问题及时报告和处理,确保患者用药安全。
总之,临床应严格遵守国家相关规定的要求,合理使用抗菌药物;加强ADR/ADE的监测、巡查、上报,并将ADR/ADE相关制度切实贯彻于整个医疗服务中,积极做好ADR/ADE的预防工作,及时应对和处理ADR突发事件或群体性ADE;积极发挥临床药师的作用,保证患者合理用药。
[1]梁江萍,方丽华,洪帆.抗菌药物不良反应调查分析[J].中华医院感染学杂志,2013,23(3):654-656.
[2]赵婷,赵鸿昆,李林春,等. 497例β-内酰胺类抗生素致不良反应分析[J].中国药房,2013,24(10): 929-931.
[3]刘晓,孔妍,崔一民,等.抗感染药物相关严重不良反应147例分析[J].中国临床药理学杂志,2017,33 (1): 70-73.
[4]欧燕,毛艳,周俊,等.万古霉素致严重不良反应1例[J].医药导报,2016,35(9):1020.
[5]易爱玲,胡芙蓉,叶芳,等.378例抗菌药物不良反应报告分析[J].医药导报,2012,31(5):682-685.
[6]胡昌勤,赵建西,金少鸿,等.头孢菌素和青霉素交叉过敏反应的结构基础探讨[J].中国抗生素杂志,1991,16(4):270-275.
[7]王德才,张继国.头孢菌素类抗生素致过敏性休克文献调查[J].药物不良反应杂志,2004,6(6):383-386.
[8]Kirkpatrick J,Rangoonwala R,Reshetnykovown M,et al.Non-Equiv-alence of Antibiotic Generic Drugs and Risk for Intensive Care Patients[J].Pharmaceutical Regulatory Affairs Open Access,2013,2: 109.doi:10.4172/2167-7689.1000109
[9]李连新,付燕霞.医院临床不合理使用抗菌药物分析及干预措施[J].中国药业,2012,21(1): 60-62.
[10] 李瑜.529例药品不良反应/事件表中的不合理用药现象分析[J].中国医药指南,2012,10(28):180-181.
[11] 胡晓波,谭蓉.影响CYP450和P-gp活性的抗菌药物联合用药探讨[J].抗感染药学,2012,9(4):257-260.
[12] 金海英,沈爱国,叶宗敏,等.20806例头孢类药物皮肤敏感试验影响因素的logistic回归分析[J].中国医院药学杂志,2017,37(3):278-282.
[13] 郑波.客观对待头孢菌素类抗生素的皮肤敏感试验[J].中华内科杂志,2014,53(6):435-436.
Reports on 301 Cases of Adverse Drug Reactions Induced by AntibioticsΔ
YAO Nanhong1, XU Weishuai1, YU Xiaohong2, PENG Huaidong3, ZHONG Xunlong3
(1.Dept.of Pharmacy, Guangdong Traditional Chinese Medicine Hospital, Guangdong Guangzhou 510105, China; 2.Dept.of Pharmacy, the Third People’s Hospital of Nanhai, Guangdong Foshan 528244, China; 3.Dept.of Pharmacy, the Second Affiliated Hospital of Guangzhou Medical University, Guangdong Guangzhou 510260, China)
OBJECTIVE: To probe into relevant factors and regularities of adverse drug reactions (ADR)/ adverse drug events (ADE) induced by general characteristics, so as to provide references for promoting clinical rational drug application. METHODS: 301 cases of ADR/ADE reports in National Center for ADR Monitoring from Jan. 1st 2006 to Apr. 30th 2014 were collected and retrospectively analyzed in terms of patients’ ages, genders, diseases, routes of administration, drug combinations, occurrence time, species of antibiotics, organs and (or) systems involved and their clinical features, severe ADR/ADE involved drugs, etc. RESULTS: Of 301 reports on ADR/ADE induced by antibiotics, the number of female was slightly more than male; mostly aged over 60 years(122 cases, accounted for 40.53%); mostly respiratory disease (139 cases, accounted for 46.18%); intravenous drip was the main route of administration inducing ADR/ADE; most ADR/ADE were induced by drug combination. Cephalosporins was the No.1 antibiotics inducing ADR/ADE, secondly were fluoroquinolones and penicillin; the top 3 drugs were respectively cefoperazone tazobactam, levofloxacin and ciprofloxacin. The main organs and (or) systems involved by ADR was skin and its accessories, secondly were systemic damage and digestive system damage. Of 301 reports of ADR/ADE, 24 cases (accounted for 7.97%) were severe ADR/ADE, mostly were induced by cephalosporins. CONCLUSIONS: The occurrence of ADR/ADE is related to many factors, doctor-medicine-patients cooperation should be reinforced to develop the function of clinical pharmacist, so as to promote rational drug application.
Antibacterial drugs; Adverse drug reactions/events; Retrospective analysis; Rational drug application
广东省医院药学研究基金(No.2016A30)
R969.3
A
1672-2124(2017)07-0975-04
2017-03-26)
*药师。研究方向:医院药学。E-mail:348100151@qq.com
#通信作者:主管药师。研究方向:临床药学。E-mail:zxl_hp200910@sina.com
DOI 10.14009/j.issn.1672-2124.2017.07.038
