氧化苦参碱对牙龈卟啉菌内毒素作用下人牙周膜细胞碱性磷酸酶活性的影响
2017-08-11汪义永
汪义永, 陈 凌, 魏 斌, 吴 贇
氧化苦参碱对牙龈卟啉菌内毒素作用下人牙周膜细胞碱性磷酸酶活性的影响
汪义永, 陈 凌, 魏 斌, 吴 贇
目的 研究氧化苦参碱对牙龈卟啉菌内毒素(Pg-LPS)作用下人牙周膜细胞(PDLC)碱性磷酸酶(ALP)的活性及其表达的影响。 方法 采用细胞培养技术分离PDLC,对照组为仅含1%胎牛血清的细胞培养液,实验组分别加入不同浓度的氧化苦参碱溶液和Pg-LPS。采用细胞培养技术和酶联免疫、实时荧光定量RT-PCR技术,观察Pg-LPS对PDLC的ALP活性及其表达的影响。 结果 在25 μg/mL的Pg-LPS作用下,PDLC的ALP活性及其表达明显减低,加入一定浓度的氧化苦参碱溶液后,PDLC的ALP活性及其表达有一定程度恢复。 结论 氧化苦参碱可以减轻Pg-LPS对PDLC的破坏,对Pg-LPS抑制PDLC的ALP活性及其表达的现象具有拮抗作用。
氧化苦参碱; 内毒素类; 牙龈/微生物学; 拟杆菌属; 牙周膜/细胞学; 碱性磷酸酶
研究表明,体外培养的人牙周膜细胞(periodontal ligament cell, PDLC)具有成骨细胞样特性,牙龈卟啉菌内毒素(porphyromonas gingivalis lipopolysaccharide, Pg-LPS)是破坏牙周支持组织的重要致病物质,可抑制PDLC的碱性磷酸酶(alkaline phosohatase, ALP)活性,对PDLC的分化产生严重影响,造成牙周膜的修复过程不能正常进行[1-2]。氧化苦参碱是从中药苦参中提取的有重要药理活性的成分,已有多类制剂被研发,并广泛应用于抗炎、抗病毒、抗肿瘤及免疫治疗等方面,具有良好的应用前景。现本课题组通过观察氧化苦参碱对Pg-LPS抑制PDLC的ALP活性及其表达的影响,研究其是否能够对抗Pg-LPS对牙周组织的破坏,为氧化苦参碱用于牙周病防治的可能性提供理论依据。
1 材料与方法
1.1 试剂 DMEM细胞培养液、新生牛血清及胰蛋白酶(美国Gibco公司);双抗(青霉素:100 U/mL;链霉素:100 μg/mL,美国Hyclone公司);PBS(杭州吉诺生物科技有限公司);Triton X-100(华美生物工程公司);ALP试剂盒(南京建成生物工程研究所);Pg-LPS(晶美生物工程公司);氧化苦参碱(陕西惠科生物工程)。
1.2 方法
1.2.1 PDLC分离培养 健康双尖牙4颗(无牙体牙髓及牙周病变),置于4 ℃的含双抗的平衡盐溶液中,在超净工作台内用PBS冲洗牙根表面血污,用功刮勺刮去牙根中1/3的牙周膜,再用0.2%的Ⅰ型胶原酶37 ℃水浴消化40 min,加入4 mL含20%新生牛血清的DMEM培养液(37 ℃、体积分数为0.045的CO2)进行培养。使用倒置显微镜观察细胞的生长及形态变化,当细胞铺满孔底的60%~80%,消化传代培养,免疫组织化学法鉴定组织来源,矿化诱导后茜素红染色观察矿化结节的形成情况,取4~6代细胞用于实验。
1.2.2 氧化苦参碱对Pg-LPS作用下PDLC的ALP活性的影响 将生长状况良好的第4代PDLC用胰酶-EDTA消化后计数,调整细胞浓度,接种于96孔培养板。接种细胞浓度为1×105mL-1,待细胞贴壁后在无菌超净工作台内弃去上清,PBS清洗3次,并分为5组,每组设6个复孔。A组为空白对照组,仅含1%新生牛血清的DMEM培养液;B组为25 μg/mL的Pg-LPS刺激组;C组为25 μg/mL的Pg-LPS+1 μg/mL氧化苦参碱;D组为25 μg/mL的Pg-LPS+10 μg/mL氧化苦参碱;E组为25 μg/mL的Pg-LPS+25 μg/mL氧化苦参碱。去除培养液,PBS洗3次,每孔加入0.1% Triton X-100 100 μL,4 ℃冰箱过夜。观察已无完整细胞结构后,吹打,按ALP试剂盒说明书操作,加入缓冲液50 μL,基质液50 μL,底物100 μL,37 ℃孵育30 min,酶联仪于520 nm下测吸光度值。
1.2.3 实时荧光定量RT-PCR检测ALP mRNA的表达水平
1.2.3.1 细胞RNA的提取 将生长状态良好的第4代PDLC传入25 cm2的培养瓶,按上述分组连续培养24 h,使用Trizol RNA提取液提取PDLC中的RNA。取适量的RNA分别进行定量与琼脂糖凝胶电泳,鉴定提取效果。
1.2.3.2 逆转录 样本cDNA合成,反应体系如下:逆转录Buffer 2 μL,上下游引物均为0.2 μL,dNTP 0.1 μL,逆转录酶0.5 μL,DEPC水5 μL,RNA模板2 μL,总体积10 μL。加入逆转录酶之前,先于70 ℃下干浴3 min,取出后立即冰水浴至管内外温度一致。加逆转录酶0.5 μL,37 ℃水浴60 min。取出后立即于95 ℃下干浴3 min,得到逆转录终溶液,即cDNA溶液,保存于-80 ℃待用。
1.2.3.3 荧光定量PCR检测
1.2.3.3.1 GAPDH阳性模板的标准梯度制备 阳性模板的浓度为1011mmol/L,反应前取3 μL,按10倍稀释(加水27 μL并充分混匀)为1010mmol/L,依次稀释至109,108,107,106,105及104mmol/L,备用。
1.2.3.3.2 采用TAKARA SYBR Green染料法对PCR反应进行荧光定量检测,反应体系共50 μL,其中:模板5 μL,上下游引物各0.8 μL, SYBR Green PCR Mix 25 μL, ddH2O 18.4 μL,进行PCR循环,反应条件为:95 ℃ 60 s→95 ℃ 15 s→60 ℃ 15 s,共40个循环。
GAPDH引物:
上游:5′-GCACCGTCAAGGCTGAGAAC-3′
下游:5′-TGGTGAAGACGCCAGTGGA-3′
ALP引物:
上游:5′-ACCATTCCCACGTCTTCACATTT-3′
下游:5′-AGACATTCTCTCGTTCACCGCC-3′
1.2.3.4 Real-Time PCR结果分析 使用荧光定量PCR分析软件,根据阳性内参模板GAPDH制作标准曲线,对ALP cDNA扩增后产物进行定量分析,作为mRNA表达水平的相对值。
2 结 果
2.1 体外培养PDLC培养矿化能力检测 培养6 d后组织块周围见细胞爬出,呈长梭形或星形(图1A)。培养时间增长,见矿化诱导液培养组的胞密度逐渐增大,出现不透光黑色结节并逐渐增大(图1B);茜素红染色后可见矿化诱导液实验组形成多处红染矿化结节,显示为钙盐沉积部位(图1C)。
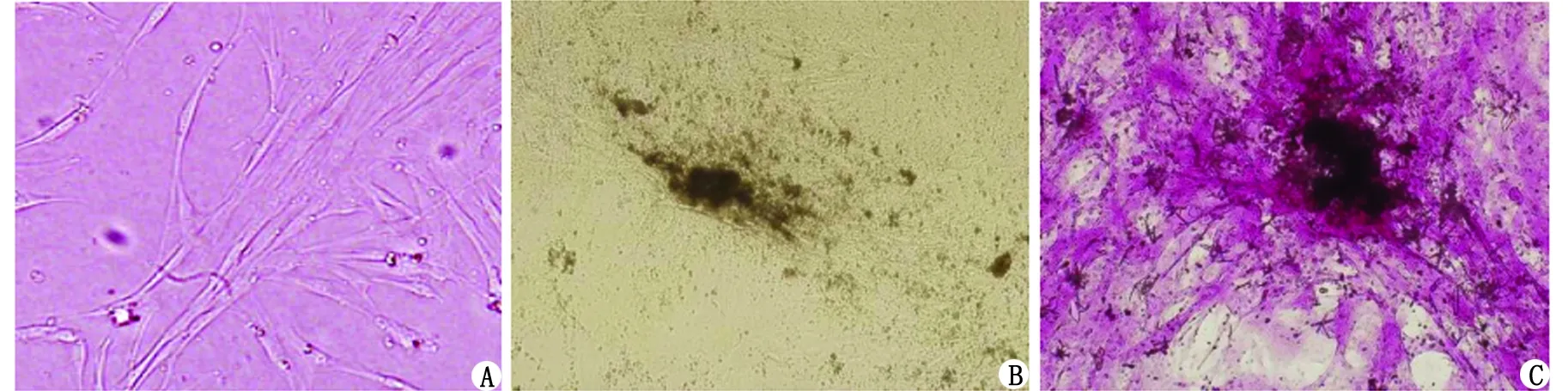
A:人牙周膜细胞;B:矿化诱导液培养;C:茜素红染色.图1 人牙周膜细胞及其培养矿化检测Fig 1 Human periodontal ligament cells mineralization
2.2 不同浓度氧化苦参碱对Pg-LPS作用下PDLC的ALP活性的影响 25 μg/mL的Pg-LPS能够有效降低PDLC的ALP活性,而加入不同浓度氧化苦参碱后,ALP的活性均有所提高(表1)。
2.3 PCR产物结果 25 μg/mL的Pg-LPS作用于PDLC后,其ALP mRNA的表达明显降低,与空白对照组比较,差别具有统计学意义(P<0.05)。加入Pg-LPS,并以1,10,25 μg/mL的氧化苦参碱作用,3组PDLC表达的ALP mRNA水平均有所增高,并在一定范围内随浓度的增高而增加,加入氧化苦参碱的3个实验组与仅加入25 μg/mL Pg-LPS的实验组间比较,差别均具有统计学意义(P<0.05,图2)。
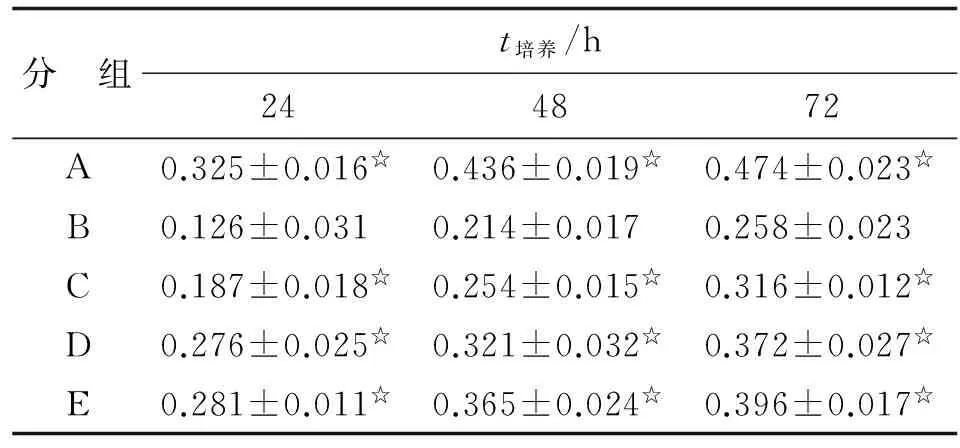
表1 不同时间点各组碱性磷酸酶活性
Pg-LPS:牙龈卟啉菌内毒素. A:空白对照组; B:Pg-LPS刺激组; C:Pg-LPS+1 μg/mL氧化苦参碱; D:Pg-LPS+10 μg/mL氧化苦参碱; E:Pg-LPS+25 μg/mL氧化苦参碱. 与B组比较,☆:P<0.05.
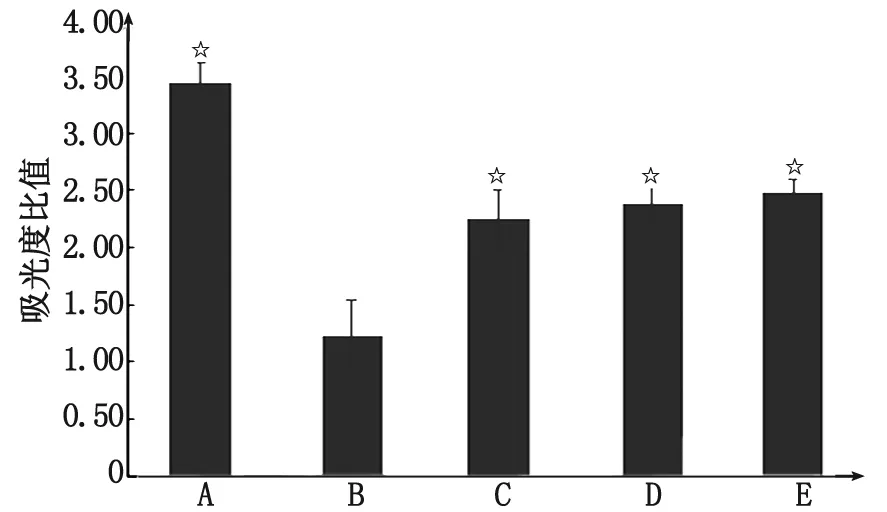
Pg-LPS:牙龈卟啉菌内毒素. A:空白对照组; B:Pg-LPS刺激组; C:Pg-LPS+1 μg/mL氧化苦参碱; D:Pg-LPS+10 μg/mL氧化苦参碱; E:Pg-LPS+25 μg/mL氧化苦参碱. 与B组比较,☆:P<0.05.图2 ALP mRNA与GAPDH吸光度比值Fig 2 The absorbance ratio of ALP mRNA and GAPDH
3 讨 论
研究发现,在骨组织的形成、改建和修复的过程中,ALP发挥了十分重要的调节作用。ALP的含量高低代表了组织细胞的分化以及形成骨组织的能力,ALP活性的高低表明骨组织的代谢和改建能力。体外培养的PDLC采用矿化诱导液培养可形成矿化结节,能够分泌高活性的ALP,表达成骨的相关蛋白和细胞因子,具有成骨细胞的特性。Pg是牙周病的主要致病菌之一,LPS是其主要致病成分,能够降低PDLC的生物活性,直接破坏PDLC的超微结构,可对PDLC产生不可逆的损伤[3]。近期研究表明,Pg-LPS会明显抑制PDLC的分化能力,导致其不能向成骨样细胞分化;还可抑制PDLC表达ALP的活性,这些不良影响将导致牙槽骨的代谢和更新减慢,造成牙周支持组织的破坏,牙周组织的更新和改建过程将无法正常进行[4-5]。研究如何通过药物拮抗Pg-LPS对PDLC的的破坏,保护PDLC免受Pg-LPS的损伤对牙周病的预防和治疗具有重要作用。
氧化苦参碱一直被认为具有抗炎作用,可抑制多种炎症介质的活性,并影响炎症过程的各个阶段。研究发现,苦参碱及氧化苦参碱等苦豆子生物碱可显著抑制白三烯的作用,并随剂量的增大而增强[6];还可以降低核因子-κB(nuclear factor κB,NF-κB)及丝裂原活化蛋白激酶相关的炎症反应,抑制肿瘤坏死因子-α(tumor necrosis factor-α, TNF-α)及白细胞介素-6(interleukin-6, IL-6)等炎症因子的产生[7]。而NF-κB是调控促炎因子产生、激发炎症反应的重要调控因子。在细胞水平,对于脂多糖刺激后的RAW264.7细胞,氧化苦参碱可抑制NF-κB活化,减少炎性黏附分子和细胞因子的分泌,剂量依赖性地降低炎症相关因子IL-11、C反应蛋白和TNF-α的表达[8]。说明氧化苦参碱可对抗炎症反应,对机体及细胞产生保护作用。
本研究结果显示,浓度为25 μg/mL的Pg-LPS作用于PDLC,其ALP的表达和活性明显降低,表明该浓度的Pg-LPS对PDLC造成了明显破坏;分别加入1,10及25 μg/mL的氧化苦参碱后,ALP的表达和活性均有所提高,并随氧化苦参碱浓度的升高而升高,表明氧化苦参碱对Pg-LPS抑制PDLC的ALP活性具有拮抗作用,在一定范围内,氧化苦参碱浓度越高,保护作用越好,且在ALP的mRNA表达和蛋白翻译阶段具有同等作用。文献报道,氧化苦参碱具有很强的药理活性,对血管内皮细胞、心肌细胞、肝脏细胞等都具有保护作用[9-11]。本研究发现,氧化苦参碱的抗炎及抑制炎症介质的特性可能同时在牙周发挥相同的作用,它能够对抗Pg-LPS对PDLC的破坏,促进PDLC的ALP活性,促进其成骨能力,而且这种作用在1~25 μg/mL呈浓度依赖关系,可能的途径是氧化苦参碱对Pg-LPS导致的炎症反应发挥相应的对抗作用,需进一步深入研究证实。本研究对氧化苦参碱在牙周组织中的作用进行探讨,为牙周病的治疗开辟新途径,提供新的思路。
[1] 申 涛, 常慧君, 简从相, 等. 改良法分离培养人牙周膜干细胞[J].华西口腔医学杂志, 2011,29(1):71-74.
[2] Li X, Zhou L, Takai H,etal. Aggregatibacter actinomycetemcomitans lipopolysaccharide regulates bone sialoprotein gene transcription[J].JCellBiochem, 2012,113(9):2822-2834.
[3] Smith Mac Donald E, Nowzari H,etal. Clinical and microbiological evaluation of a bioabsorbable and a nonresorbable barrier membrane in the treatment of periodontal intraosseous lesions[J].JPeriodontol, 1998,69(4):445-453.
[4] 张风秋. 牙周优势菌内毒素对人牙周膜细胞的生物学效应及mCD14表达的研究[D].西安:第四军医大学口腔医学院, 2002.
[5] 田亚光, 廖天安, 陈小滨, 等. 牙髓卟啉单胞菌超声提取物对成骨细胞周期和凋亡的影响[J].实用口腔医学杂志, 2015,31(2):188-191.
[6] 黄秀梅, 李 波. 氧化苦参碱对TNF-α、IL-6和IL-8的影响[J].中成药, 2003,25(11):903-906.
[7] Dong X Q, Du Q, Yu W H,etal. Anti-inflammatory effects of oxymatrine through inhibition of nuclear factor-kappa B and mitogen-activated protein kinase activation in lipopolysaccharide-induced BV2 microglia cells[J].IranJPharmRes, 2013,12(1):165-174.
[8] Yuan X, Sun Y, Miao N,etal. The synergistic anti-inflammatory effect of the combination of sodium ferulate and oxymatrine and its modulation on inflammation-associated mediators in RAW 264.7 cells[J].JEthnopharmacol, 2011,137(3):1477-1485.
[9] 韩延忠, 周永峰, 桑秀秀, 等. 氧化苦参碱对H2O2诱导L02细胞损伤的抑制作用及其机制的研究[J]. 中国中药杂志, 2016,41(7):1302-1307.
[10] 易 云, 吴 琴, 黄莉萍, 等. 氧化苦参碱对高糖毒性下血管内皮细胞的保护作用[J]. 中国药理学通报, 2015,31(4):499-503.
[11] 赵 阳. 氧化苦参碱对H9c2心肌细胞氧化应激损伤的保护作用及其机制[J]. 山东医药, 2015,55(37):29-31.
(编辑:何佳凤)
Effects of Oxymatrine on the Activity of Alkaline Phosphatase in Human Periodontal Ligament Cells Stimulated by Porphyromonas Gingivalis Lipopolysaccharide
WANG Yiyong, CHEN Ling, WEI Bin, WU Yun
Department of Stomatology, The First Affiliated Hospital of Fujian Medical University, Fuzhou 350005, China
Objective To study the effect of oxymatrine on the activity of alkaline phosphatase(ALP)and the expression of human periodontal ligament cells (PDLC) stimulated by Porphyromonas gingivalis lipopolysaccharide (Pg-LPS). Method The human PDLC were isolated by cell culture technique. The control group was treated with 1% fetal bovine serum. The experimental groups were treated with different concentrations of oxymatrine solution and Pg-LPS. The activity of ALP and its expression in human PDLC were observed by cell culture and enzyme-linked immunosorbent assay and real time PCR. Results The activity and expression of ALP in human PDLC were significantly decreased at 25 μg/mL Pg-LPS. After addition of oxymatrine solution at a certain concentration, the ALP activity and expression had a certain degree of recovery. Conclusion Oxymatrine can reduce the damage of Pg-LPS on human PDLC and raise the ALP activity and its expression.
oxymatrine; endotoxins; gingiva/microbiology; bacteroides; periodontal ligament/cytology; alkaline phosphatase
2017-02-17
福建省自然科学基金(2017J05124);中华口腔医学会口腔疾病与全身疾病关系研究项目(CSA-Y2015-09)
福建医科大学 附属第一医院口腔科,福州 350005
汪义永,男,主治医师
吴 贇. Email: wuyun488@aliyun.com
R322.41; R378.99; R392.11; R996
A
1672-4194(2017)03-0166-04
