子宫动脉栓塞与甲氨蝶呤治疗不同MRI分型的剖宫产术后疤痕妊娠的疗效评价
2017-08-11李奎颜国辉邹煜
李奎 颜国辉 邹煜
子宫动脉栓塞与甲氨蝶呤治疗不同MRI分型的剖宫产术后疤痕妊娠的疗效评价
李奎 颜国辉 邹煜
目的:探讨剖宫产后疤痕妊娠(CSP)的MRI影像学表现及分型对其治疗的指导意义,评价甲氨蝶呤(MTX)联合刮宫及子宫动脉化疗栓塞术(UACE)联合刮宫治疗不同类型CSP的适应证、有效性及安全性。方法:回顾性分析于我院治疗且影像资料完整的CSP患者187例,其中CSP 1型57例,CSP 2型130例,根据MRI分型及治疗方式的不同将患者分为4组:A1组(CSP 1型患者行MTX联合刮宫术者)45例,B1组(CSP 1型患者行UACE联合刮宫术)12例;A2组(CSP 2型患者行MTX联合刮宫术者)40例,B2组(CSP 2型患者行UACE联合刮宫术)90例。对患者术后临床数据及随访结果进行统计分析。结果:A1、B1两组的刮宫术中出血量、术后第1天血β-hCG下降超过50%者的比例、肝功能异常率、子宫切除率、治疗成功率的差异均无统计学意义。但A1组患者的住院时间明显长于B1组,差异有统计学意义。A2组的刮宫术中出血量、住院时间、肝功能异常率、子宫切除率高于B2组,术后第1天血β-hCG下降超过50%者的比例、治疗成功率低于B2组,差异均有统计学意义。结论:MRI能够明确CSP诊断,并准确分型,对于治疗方式的选择有重要指导意义。UACE联合刮宫治疗CSP的效果优于MTX联合刮宫术,尤其是对于CSP 2型患者更能降低子宫切除率,保留生育功能,可作为CSP 2型患者的首选治疗方式。
子宫动脉栓塞术; 甲氨蝶呤; 疤痕妊娠; 磁共振成像
疤痕妊娠(cesarean scar pregnancy,CSP)是指是孕囊、受精卵或胚胎着床于前次剖宫产疤痕处的一种特殊类型的异位妊娠,发病少见[1]。CSP早期临床无特异性表现,发病前不易明确诊断,如处理不及时或处理不当,极易引起失血性休克,严重者危及患者生命[2]。
因CSP发病率低,目前临床对其诊断及治疗认识有限,在诊断方面:超声检查是CSP影像学诊断首选的检查方法,相关报道较多,但有关MRI的影像学特点、分型及对临床治疗的指导意义报道较少。在治疗方面:目前关于CSP的治疗方法尚无统一规范的方案[3-4]。药物治疗所需时间长,治疗过程中存在发生子宫大量出血,需切除子宫的潜在风险。外科手术创伤较大,主要用于无法控制的大出血及无生育要求的妇女。近年来,子宫动脉栓塞(uterine artery embolization,UAE)联合甲氨蝶呤(MTX)子宫动脉化疗栓塞(uterine artery chemoembolization,UACE)治疗CSP取得了良好的效果,它不仅可以用于预防刮宫术中大出血,亦可以用于治疗刮宫术中大出血,显著降低了子宫切除率,保留了患者的生育功能,提示其有可能成为治疗CSP的首选方案[5-6]。但关于不同MRI影像学分型CSP的治疗效果的研究尚少。本研究搜集我院收治的187例CSP患者的资料,探讨不同的MRI影像学表现及分型对其治疗的指导意义,同时对MTX联合刮宫及UACE联合刮宫治疗不同类型CSP的适应证、有效性和安全性进行评价。
资料与方法
一、一般资料
选取2014年1月—2016年1月于我院治疗的CSP患者187例,所有患者资料完整、均在我院接收MRI检查,入院前均未在他院接受治疗,无造影剂过敏、子宫破裂、失血性休克、严重凝血功能及心、肝、脑、肺、肾等重要脏器的严重合并症。根据患者治疗方式的不同,将患者分为A、B两组。A组85例,为MTX联合刮宫组,患者先经肌肉注射MTX 50 mg/m2后再行超声引导下刮宫术。B组102例,为UACE联合刮宫组,患者先行UACE后再行超声引导下刮宫术。两组患者治疗前一般资料差异均无统计学意义(P>0.05),见表1。
表1 两组患者的一般资料比较 ()、中位数或例(%)
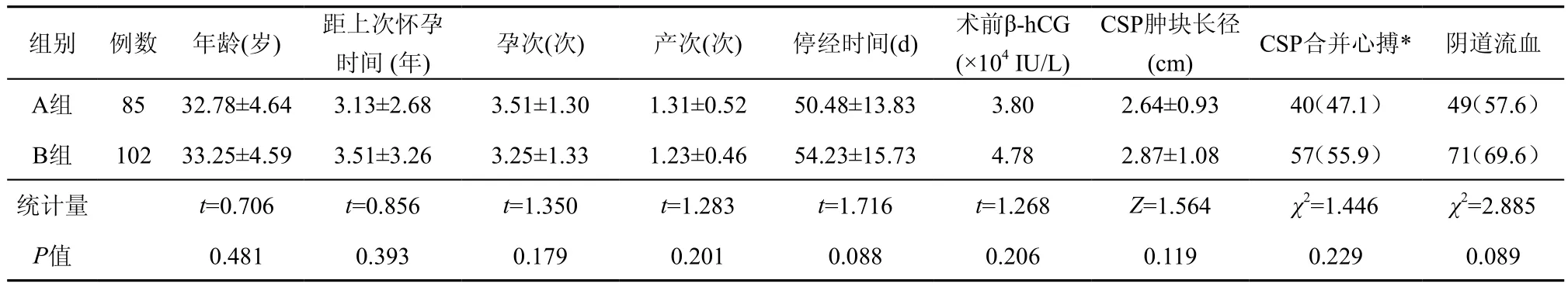
表1 两组患者的一般资料比较 ()、中位数或例(%)
注:β-hCG为β-人绒毛膜促性腺激素;CSP为疤痕妊娠。*心搏即入院时B超检查发现胚囊内的原始心脏搏动,代表活胎。
组别 例数 年龄(岁) 距上次怀孕时间 (年) 孕次(次) 产次(次) 停经时间(d) 术前β-hCG (×104IU/L) CSP肿块长径(cm) CSP合并心搏* 阴道流血A组 85 32.78±4.64 3.13±2.68 3.51±1.30 1.31±0.52 50.48±13.83 3.80 2.64±0.93 40(47.1) 49(57.6)B组 102 33.25±4.59 3.51±3.26 3.25±1.33 1.23±0.46 54.23±15.73 4.78 2.87±1.08 57(55.9) 71(69.6)统计量 t=0.706 t=0.856 t=1.350 t=1.283 t=1.716 t=1.268 Z=1.564 χ2=1.446 χ2=2.885 P值 0.481 0.393 0.179 0.201 0.088 0.206 0.119 0.229 0.089
二、CSP的诊断
CSP的诊断主要依据于以下标准[7]:(1)患者有剖宫产史;(2)停经,合并或不合并阴道不规则流血;(3)血β-hCG浓度升高;(4)典型的超声及MRI表现[8-9]:①妊娠物位于子宫前壁峡部剖宫产疤痕处;②宫腔内未见妊娠物;③宫颈形态正常,内外口紧闭,未见妊娠组织;④妊娠物与膀胱间的子宫肌层缺失或连续性中断。
三、CSP的MRI检查方法及分型
1.MRI仪器及扫描方法:使用GE Signa HDxt 1.5T磁共振扫描仪。主要扫描参数:横断面T2加权成像(T2WI)快速自旋回波(FSE)序列:扫描野(FOV) 36 cm×36 cm,层厚/间距5.5 mm/0.5 mm;横断面可变容积加速肝脏采集序列(LAVA-Flex):FOV36 cm×36 cm,层厚/间距5.5 mm/0.5 mm。矢状位T2WI FSE脂肪抑制序列:FOV21 cm×21 cm,层厚/间距5 mm/0.5 mm;部分病例进行增强扫描,采用钆喷酸葡胺注射液0.1 mmol/kg,经肘静脉注射,速度为2 ml/s,注射结束后进行LAVA-Flex增强横断位、矢状位及冠状位扫描。检查前最好饮水,使膀胱充盈。
2.MRI分型:Vial等[10]将CSP分为两型:1型,孕囊种植在子宫疤痕处,向子宫峡部或官腔生长(即为内生型);2型,孕囊种植在有缺陷的剖宫产子宫切口疤痕深部,深入肌层,朝向膀胱及腹腔生长(即为外生型)。由我院放射科3例经验丰富的诊断医师(1名主任医师,2名副主任医师,均有5~10年的MRI诊断经验)按照Vial标准进行诊断,187例患者中CSP 1型57例,CSP 2型130例。
四、治疗方法
1.MTX联合刮宫术:A组85例患者经肌内注射MTX(0.1 g冻干粉MTX溶于4 ml注射用水,重溶浓度为25 g/L)50 mg/m2,严密监测患者症状及体征,1周后行刮宫术。刮宫术后组织常规送病理检查。刮宫术后第1天复查血β-hCG浓度、肝肾功能及血常规。
2.UACE联合刮宫术:B组102例CSP患者先由3名经验丰富的放射科介入医生(2名主治医师和1名主任医师,均有10年以上介入手术经验)分别独立实施治疗的操作,具体操作过程:采用改良Seldinger技术行右股动脉穿刺置管,再行双侧子宫动脉超选择性插管至子宫动脉上行支,插管成功并造影证实后,分别于患者双侧子宫动脉内缓慢灌注术前核定剂量的MTX(0.1g冻干粉MTX溶于20 ml注射用水,重溶浓度为5 g/L)50 mg/m2,再用明胶海绵颗粒(直径560~710 μm,杭州艾立康公司)栓塞双侧子宫动脉上行支,直至DSA造影显示双侧子宫动脉完全栓塞(图1)。所有患者于UACE术后24~48 h内行超声引导下刮宫术。刮宫术后组织常规送病理检查。刮宫术后第1天复查血β-hCG浓度、肝肾功能及血常规。
五、病例亚组分组:
187例患者中CSP 1型者57例,CSP 2型者130例,依据患者MRI表现及治疗方式的不同,CSP 1型患者可再分为2个亚组,即:A1组(CSP 1型患者行MTX联合刮宫术者)45例,B1组(CSP 1型患者行UACE联合刮宫术)12例。CSP 2型患者可再分为2个亚组,即:A2组(CSP 2型患者行MTX联合刮宫术者)40例,B2组(CSP 2型患者行UACE联合刮宫术)90例。
六、住院观察指标及出院后随访指标
住院期间动态监测患者血β-hCG浓度、肝肾功能、血常规及CSP病灶大小,同时详细记录患者出血量、并发症(如:发热、呕吐、眩晕及疼痛等)。患者出院后3~6个月内每两周复诊1次,复诊内容包括:血β-hCG浓度、肝肾功能、血常规,腹部超声检查及临床症状评估(阴道流血量、月经恢复时间等)。并发症的评价参照美国国家癌症研究所-不良事件公共术语标准第三版(NCI-CTCAE V3.0)进行分级。
七、疗效评价
治疗成功的标准:治疗后无严重并发症(严重并发症指:出血量>500 ml,或需再次行子宫动脉栓塞术或子宫切除术),患者生育功能得以保留;无主诉症状;无发热;无阴道流血;血β-hCG浓度恢复正常;CSP病灶完全消失。
出院标准[11]:无主诉症状;无发热;无阴道流血或阴道流血明显少于正常月经量3日以上;血β-hCG浓度恢复正常或下降超过50%且持续下降;CSP病灶完全消失或持续缩小。
八、统计学处理
采用SPSS19.0统计软件分析数据,两组计量资料如术中出血量、住院时间比较采用t检验,非正态分布计量数据采用Mann-Whitney U检验,计数资料如术后第1天β-hCG 下降超过50%者所占比例、肝功能异常率、子宫切除率、治疗成功率等比较采用χ2检验,P<0.05为差异有统计学意义。
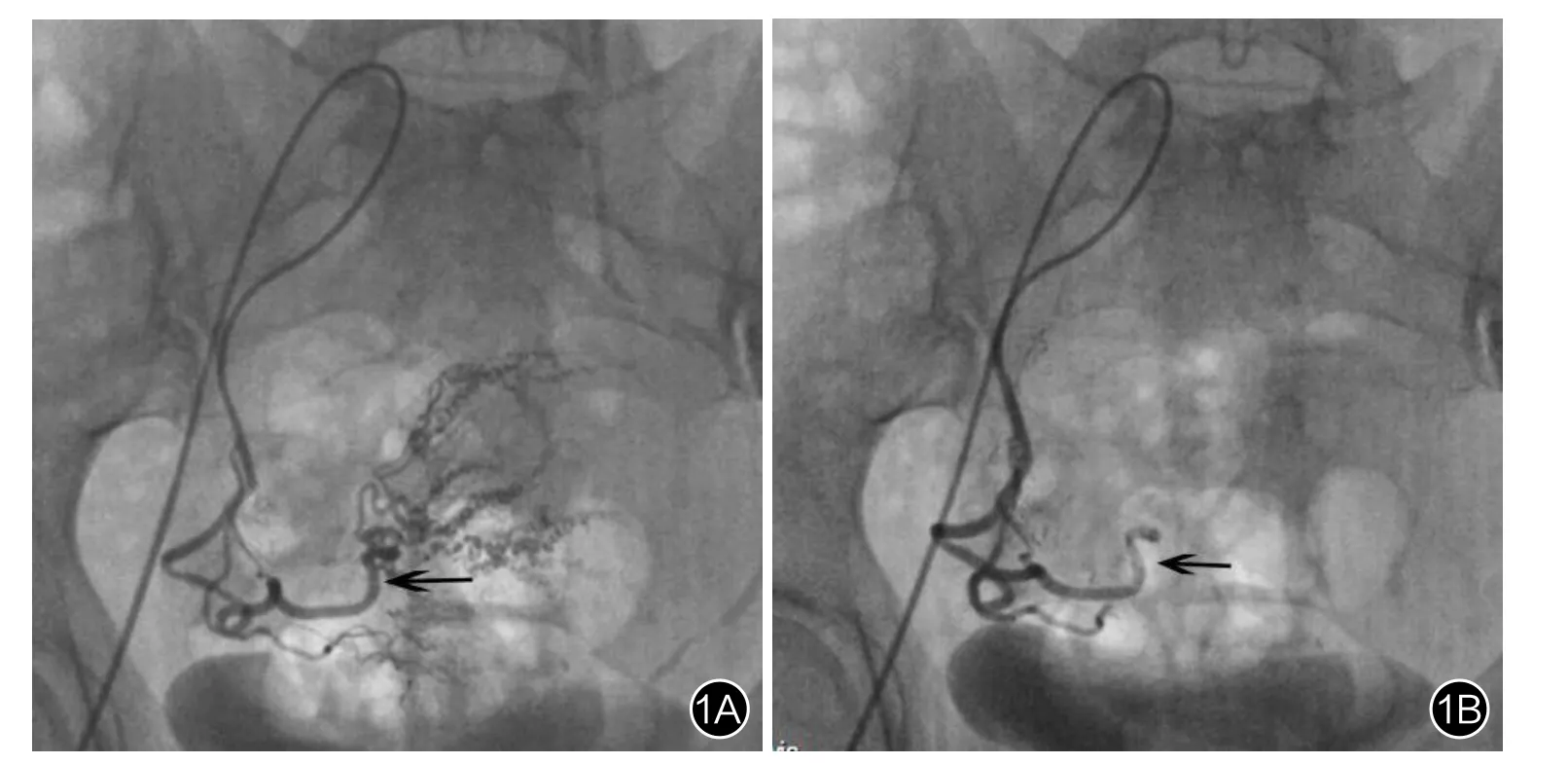
图1 疤痕妊娠患者UACE术前及术后子宫动脉造影
结 果
一、CSP患者的MRI表现
CSP 1型患者MRI多表现为单纯囊状影,呈类圆形、泪滴状及哑铃形,孕囊种植在子宫疤痕处,向子宫峡部或官腔生长,最小者长径约为0.9 cm,最大者约2.8 cm,距离子宫前壁浆膜层0.3~0.6 cm不等,T1WI上表现为低信号,T2WI上表现为边界清楚囊状高信号影,增强后T1WI上囊壁可见环形薄壁强化;囊内有时可见乳头状影及出血灶(图2A)。CSP 2型MRI多表现为混杂包块影,孕囊种植在有缺陷的剖宫产子宫切口疤痕深部,深入肌层,朝向膀胱及腹腔生长。最小者长径约1.0 cm,最大者约7.4 cm,T1WI呈等、低混杂信号,T2WI表现为长T2为主混杂信号包块,周围肌层内见增多迂曲的血管影,部分包块可见T1WI高信号出血灶,增强扫描在T1WI上见斑片状强化(图2B)。187例中19例妊娠囊突破子宫前壁浆膜层,与膀胱分界不清,其余168例孕囊距离子宫前壁浆膜层0.1~0.6 cm不等,187例患者超声首次检查时,33例患者未明确诊断,超声首次正确诊断率为82.35%(154/187),多误诊为先兆流产。但经超声复查后33例患者中有27例确诊为CSP,正确诊断率达96.79%(181/187),剩余6例患者误诊为宫颈肌瘤变性。本研究MRI首次正确诊断率为94.65%(177/187),常误诊为宫颈前壁出血灶。
二、A、B组患者治疗后的资料比较
A组术中出血量大于B组,差异有统计学意义,85例患者中21例于刮宫术中出血量超过500 ml,7例出血量超过1 500 ml;B组患者102例中13例于刮宫术中出血量超过500 ml,2例出血量超过1 500 ml。
A组的住院时间、肝功能异常率、子宫切除率高于B组,术后第1天血β-hCG下降超过50%者的比例和治疗成功率低于B组,差异均有统计学意义,见表2。
三、CSP 1型患者经两种方法治疗后的资料比较
A1、B1两组的刮宫术中出血量、术后第1天血β-hCG下降超过50%者的比例、肝功能异常率、子宫切除率、治疗成功率的差异均无统计学意义。但A1组患者的住院时间明显长于B1组,差异有统计学意义,见表3。
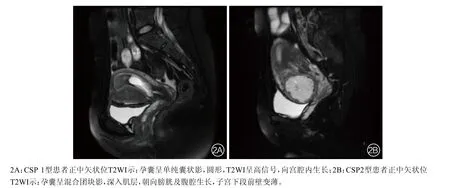
图2 2种类型CSP患者的MRI图像表现
表2 A、B组患者治疗后的资料比较 ()、中位数或例(%)

表2 A、B组患者治疗后的资料比较 ()、中位数或例(%)
组别 例数 术中出血量(ml) 住院时间 (d) 术后第1天血β-hCG 下降超过50%者 肝功能异常者 子宫切除 治疗成功A组 85 246.54 13.48±1.58 72(84.7) 15(17.6) 8(9.1) 64(75.3)B组 102 128.99 6.73±1.65 96(94.1) 3(2.9) 2(1.9) 89(87.3)统计量 Z=6.402 t=11.595 χ2=4.499 χ2=11.526 χ2=5.085 χ2=4.459 P值 <0.001 <0.001 0.034 0.001 0.024 0.035
四、CSP 2型患者经两种方法治疗后的资料比较
A2组的刮宫术中出血量、住院时间、肝功能异常率、子宫切除率高于B2组,术后第1天血β-hCG下降超过50%者的比例、治疗成功率低于B2组,差异均有统计学意义,见表4。
表3 CSP 1型患者经两种方法治疗后的资料比较 ()、中位数或例(%)

表3 CSP 1型患者经两种方法治疗后的资料比较 ()、中位数或例(%)
组别 例数 术中出血量(ml) 住院时间 (d) 术后第1天血β-hCG 下降超过50%者 肝功能异常者 子宫切除 治疗成功A1组 45 129.13 13.56±1.66 42(93.33) 8(17.78) 3(6.67) 41(91.11)B1组 12 162.92 7.33±1.83 11(91.37) 1(8.33) 0(0) 11(91.67)统计量 Z=0.060 t=5.307 χ2=0 χ2=0.124 χ2=0.037 χ2=0 P值 0.952 <0.001 1 0.725 0.848 1
五、并发症
住院期间共18例(A组15例,B组3例)患者出现MTX所致药物性肝功能损害(NCI-CTCAE1级),护肝治疗后好转;19例(A组5例,B组14例)患者有轻度发热,体温37~39℃(NCI-CTCAE1级),对症治疗后均好转。UACE术后患者多出现轻微盆腹腔疼痛(NCI-CTCAE1级),仅有6例患者出现严重臀部及腹部疼痛NCI-CTCAE2级),予以密切观察、对症治疗,1周内疼痛均明显好转或消失。
177例保留生育功能者,术后随访12~18个月不等,随访方式包括门诊复查及电话随访,87例患者于出院1个月后恢复月经周期,56例患者于出院2个月后恢复月经周期,B2组1例患者出现卵巢早衰及闭经,其余患者均于出院后1年内恢复月经周期,月经恢复平均时间为(2.00±1.56)个月。患者血β-hCG浓度恢复到正常的时间为刮宫术后(20.35±5.77)d,患者CSP病灶消失时间为刮宫术后(25.20±3.56)d,随访期间有5例患者再次妊娠。
表4 CSP 2型患者经两种方法治疗后的资料比较 ()、中位数或例(%)

表4 CSP 2型患者经两种方法治疗后的资料比较 ()、中位数或例(%)
组别 例数 术中出血量(ml) 住院时间 (d) 术后第1天血β-hCG 下降超过50%者 肝功能异常者 子宫切除 治疗成功A2组 40 378.63 13.40±1.50 30(75.00) 7(17.50) 5(12.50) 23(57.50)B2组 90 124.47 6.64±1.62 85(94.44) 2(2.22) 2(2.22) 78(86.66)统计量 Z=5.740 t=8.950 χ2=8.441 χ2=7.800 χ2=3.902 χ2=11.962 P值 <0.001 <0.001 0.004 0.005 0.048 0.001
讨 论
CSP是剖宫产后的远期并发症之一,发病率低,临床表现缺乏特异性,而体格检查常无明显阳性体征,早期即可导致难以控制的子宫大量出血,极为凶险[1-3]。早期正确诊断是其正确治疗的基础,血β-hCG浓度有助于妊娠的诊断而无助于CSP的确诊,主要用于监测治疗效果。因此,超声或MRI检查在CSP的诊断中起着非常重要的作用。超声是目前诊断CSP的首选影像学方法,具有无创、简便、可重复性等特点。但是,超声检查诊断CSP的特异性不强,难以与子宫颈妊娠及先兆流产鉴别诊断[12]。其次,超声仅能根据孕囊周围血流分布情况来间接预测其是否发生粘连或是植入,准确性较差。而且,超声很大程度上依赖于操作者的技术,易发生漏诊、误诊[13]。
而MRI具有较高软组织分辨率和多序列、多参数、多方位成像特点,在评估盆腔脏器结构方面具有独特优势[14]。相对于超声检查,MRI检查更加清晰,能够显示更多细节。MRI能清晰显示妊娠囊大小、与浆膜面间的距离及生长方式等。同时MRI能准确显示异位妊娠内部的出血情况,这是超声检查所不能发现的。此外,MRI检查可清晰显示孕囊在子宫前壁着床的位置及分型,病灶与周围组织的关系,周围血供的情况,可以为临床治疗方案选择提供更多有用信息,并决定手术方式的选择。本研究中187例患者首次超声检查正确诊断率仅为82.35%(154/187),复查超声正确诊断率可达96.79%,与MRI首次正确诊断率94.65%(177/187)相仿。Huang等[15]报道MRI及超声对CSP的正确诊断率分别为97.6%(41/42)和81%(34/42),重复超声检查后的正确诊断率为96.6%,与本研究结果相仿。因此,建议凡是可疑CSP的患者,在条件允许时均须行MRI检查或超声复查以明确诊断。
CSP治疗的目的是清除病灶、控制出血、保留生育能力[7]。但目前仍没有统一的治疗标准,临床多采用个性化的综合治疗,根据CSP大小、病灶血供及病灶类型选择治疗方案。传统治方法包括MTX化疗和清宫术。MTX化疗有全身用药和超声引导下孕囊内注射两种方式。超声引导下囊内注射MTX往往导致剖宫产后疤痕破裂,因此本研究中非UACE组患者均采用经肌肉注射MTX全身化疗的方式。MTX可抑制滋养细胞生长,使胚胎组织坏死脱落并吸收,但治疗时间长,文献报道,单纯使用MTX全身化疗,血β-hCG浓度恢复到正常的时间需要4~16周,CSP病灶的消失则需要数月至1年,且治疗过程中仍有阴道大出血的风险[16]。本研究中A组85例患者肌注MTX1周后仅40例患者的血β-hCG浓度下降至入院时的50%水平以下,同时Wu等[11]报道,MTX化疗后子宫切除和术中大出血发生率达76.1%。此外盲目清宫也是CSP治疗的禁忌,单纯清宫术导致子宫切除术及大出血的概率也高达70%[17]。因此单纯MTX化疗和刮宫术有较高的子宫切除率及大出血的概率。
近几年来随着介入医学的发展及技术革新,UAE术近年来广泛应用于治疗CSP,取得了良好的效果。它不仅可以用于预防刮宫术中大出血,亦可以用于治疗刮宫术中大出血,显著降低了子宫切除率,保留了患者的子宫以及生育功能。UAE通过暂时性的栓塞双侧子宫动脉,切断滋养细胞的血液供应,使之缺血缺氧而坏死;还能在刮宫术过程中辅助止血,从而避免大出血的发生,降低手术风险。更有学者认为,当妊娠滋养细胞侵犯至膀胱子宫间隙时,UAE是保留子宫的唯一可选择方式[18]。UAE术中如联合MTX动脉灌注(UACE)则能起到化疗杀伤和缺血损伤的双重作用,研究表明,UACE术中MTX在靶器官的浓度是MTX全身化疗时的9~68倍,药物可直接作用于孕囊,使其杀胚效果提高2~22倍[10]。此外,由于UAE的栓塞作用,靶器官内血流缓慢,进一步延长了MTX杀胚时间,提高了药物作用效率。因此,血管栓塞及局部药物浓度的提高两种作用相互协同进一步促进了滋养细胞的死亡,降低了刮宫术中及术后的出血风险,缩短了治疗观察周期。本研究中A组的住院时间、肝功能异常率、子宫切除率高于B组,术后第1天血β-hCG下降超过50%者的比例和治疗成功率低于B组,差异均有统计学意义,表示UACE联合刮宫术治疗CSP患者较MTX联合刮宫术疗效好,不良反应少,验证了此理论。
MTX联合刮宫术或UACE联合刮宫术治疗CSP 1型患者效果均较好,且无明显差异,这可能是因为CSP 1型患者孕囊未深入肌层,清宫术相对容易清除,极少有绒毛残留。因此,对于CSP 1型患者的治疗可选择MTX联合刮宫术或UACE联合刮宫术,但UACE联合刮宫术患者住院时间明显缩短,可优先考虑。CSP 2型患者孕囊植入较深,甚至穿透浆膜层,清宫较为困难,多有绒毛残留,本研究采用介入治疗仍无法完全避免刮宫术中大出血。UACE联合刮宫术治疗CSP 2型成功率较MTX联合刮宫术高,能尽快减少阴道持续出血,降低β-hCG水平,而且不良反应少,因此对于CSP 2型患者应首先采用UACE联合刮宫术。
值得注意的是177例患者经12~18个月随访,B组1例患者出现卵巢早衰和绝经症状,A组患者未出现绝经症状,提示MTX经动脉灌注可能会提高卵巢功能损伤的概率。究其原因可能与卵巢动脉-子宫动脉吻合支有关。UACE时,MTX及明胶海绵颗粒均可通过吻合支,直接杀伤卵巢组织或造成卵巢血流灌注量不足,导致卵巢功能下降。子宫动脉卵巢支较纤细,容易被孕囊丰富的血管所掩盖,如果经验不足,容易出现栓塞剂及化疗药物非靶性栓塞子宫动脉卵巢支,影响卵巢的微环境,使卵巢功能短暂性降低甚至永久性损伤[19]。娴熟的栓塞技术可以使UAE对卵巢的影响降至最低,栓塞时导管尽可能地置入子宫动脉上行支,避开子宫动脉卵巢支,控制MTX及明胶海绵颗粒灌注速度,避免损伤卵巢。本研究中仅1例出现卵巢早衰症状,发生率较低,或许无代表性,有必要在后续研究中增加样本数或延长随访时间排除其偶发性的可能。
总之,MRI能够明确CSP诊断,并准确分型,对于治疗方式的选择有重要指导意义,一旦超声提示CSP可能,可行MRI检查以明确诊断,并按照其分型选择合适的治疗方法,以减少并发症及术中出血量。UACE术后刮宫治疗CSP的治疗效果优于MTX肌肉注射后行刮宫术,尤其是对于CSP 2型患者更能降低子宫切除率,保留生育功能,应作为CSP 2型患者的首选治疗方式。
1 Jurkovic D, Hillaby K, Woelfer B, et al. First trimester diagnosis and management of pregnancies implanted into the lower uterine segment cesarean section scar[J]. Ultrasound Obstet Gynecol ,2003,21(3):220-227.
2 曹满瑞,何健龙,刘炳光,等.剖宫产疤痕妊娠的子宫动脉栓塞并清宫治疗[J].临床放射学杂志,2009,28(4):553-555.
3 Rotas MA, Haberman S, Levgur M. Cesarean scar ectopic pregnancies: etiology, diagnosis, and management[J]. Obstet Gynecol,2006,107(6):1373-1381.
4 Fylstra DL. Ectopic pregnancy within a cesarean scar: a review[J].Obstet Gynecol Surv,2002,57(8):537-543.
5 Yang XY, Yu H, Li KM, et al. Uterine artery embolisation combined with local methotrexate for treatment of caesarean scar pregnancy[J]. BJOG, 2010,117(8):990-996. doi: 10.1111/j.1471-0528.2010.02578.x.
6 Hois EL, Hibbeln JF, Alonzo MJ, et al. Ectopic pregnancy in a cesarean section scar treated with intramuscular methotrexate and bilateral uterine artery embolization[J]. J Clin Ultrasound,2008,36(2):123-127.
7 朱志韬,孙志先,祖茂衡,等.子宫动脉栓塞术预防疤痕妊娠清宫大出血的临床价值[J].中华介入放射学电子杂志,2017,5(1):13-16. doi:10.3877/cma.j.issn.2095-5782.2017.01.004.
8 车锦连, 谢锦兰, 严达,等. MRI在子宫疤痕妊娠诊断中的应用价值[J]. 海南医学, 2016, 27(5):748-750.doi:10.3969/ j.issn.1003-6350.2016.05.021.
9 Godin PA, Bassil S, Donnez J. An ectopic pregnancy developing in a previous caesarian section scar[J]. Fertil Steril, 1997, 67(2):398-400.
10 Vial Y, Petignat P, Hohlfeld P. Pregnancy in a cesarean scar[J]. Ultrasound Obstet Gynecol, 2000, 16(6):592-593.
11 Wu X, Zhang X, Zhu J, et al. Caesarean scar pregnancy: comparative efficacy and safety of treatment by uterine artery chemoembolization and systemic methotrexate injection[J]. Eur J Obstet Gynecol Reprod Biol, 2011, 161(1):75-79.
12 中华医学会计划生育学分会. 剖宫产瘢痕妊娠诊断与治疗共识[J].中华医学杂志, 2012, 92(25):1731-1733.
13 种轶文, 张坤, 周延,等. MRI检查在剖宫产术后子宫瘢痕妊娠诊治中的应用价值[J]. 中华妇产科杂志, 2014, 49(12):914-918.
14 崔璨,程悦, 沈文, 等.女性盆腔器官脱垂病人肛提肌的MRI评价[J].国际医学放射学杂志,2015,38(2):148-151.doi:10.3874/ j.issn.1674-1897.2015.02.Z0210.
15 Huang Q, Zhang M, Zhai R. Comparison of gadolinium‐enhanced magnetic resonance imaging with ultrasound in evaluation of cesarean scar pregnancy[J]. J Obstet Gynaecol Res, 2014, 40(7):1890-1893.
16 Li C, Li C, Feng D, et al. Transcatheter arterial chemoembolization versus systemic methotrexate for the management of cesarean scar pregnancy[J].Int J Gynaecol Obstet, 2011, 113(3):178–182.
17 Arslan M, Pata O, Dilek T U, et al. Treatment of viable cesarean scar ectopic pregnancy with suction curettage[J]. Int J Gynaecol Obstet, 2005, 89(2):163-166.
18 Litwicka K, Greco E. Caesarean scar pregnancy: a review of management options[J]. Curr Opin Obstet Gynecol, 2011, 23(6): 415-421.
19 Ryu RK, Siddiqi A, Omary RA, et al. Sonography of delayed effects of uterine artery embolization on ovarian arterial perfusion and function. [J]. AJR Am J Roentgenol,2003, 181(1):89-92.
(本文编辑:闫娟)
李奎,颜国辉,邹煜. 子宫动脉栓塞与甲氨蝶呤治疗不同MRI分型的剖宫产术后疤痕妊娠的疗效评价[J/CD]. 中华介入放射学电子杂志,2017,5(3):128-134.
更正声明
本刊2017年第5卷第2期第115-117页发表的白卫星等作者的论文《经颈内静脉途径治疗脑动静脉畸形一例》一文中,115页的“Onxy18胶(Microvention公司,美国)”公司名称有误,应该为“Onxy-18胶(Medtronic公司,美国)”,特此更正。
本刊编辑部
2017年7月15日
Uterine artery chemoembolization and systemic methotrexate in treating cesarean scar pregnancy of different MRI types
Li Kui, Yan Guohui, Zou Yu. Department of Radiology, Women’s Hospital, School of Medicine,Zhejiang University, Hangzhou 310006, China
Zou Yu,Email:Zouyuzju@Zju.edu.cn
Objective:To study various types of MRI imagings of cesarean scar pregnancy (CSP), and to evaluate their significance in clinical application. Also, the indications, efficacy and safety of methotrexate (MTX) combined with uterine curettage and uterine artery chemoembolization (UACE) combined with curettage in the treatment of different types of CSP were as well studied.Methods:Clinical data of 187 patients with CSP treated in our hospital were retrospectively analyzed. They were divided into four groups according to different MRI types and treatments: Group A1 (CSPI patients treated by MTX combined with curettage), 45 patients; group B1( CSPI patients treated by UACE combined with curettage ), 12 patients; group A2 (CSPII patients treated by MTX combined with curettage), 40 patients; and group B2 (CSPII patients treated by UACE combined curettage), 90 patients. Their relative clinical data and follow-up results were statistically analyzed.Results:The blood loss during curettage showed no difference in both group A1 and group B1, while the number of patients with β-hCG decreased by more than 50% in the first day after curettage, and abnormal liver function rate, hysterectomy rate and treatment success rate all showed no significant difference. However, hospital stay in group A1 was much longer than in group B1, with significant difference. Group A2 and group B2 were seen a significant difference in blood loss during curettage, hospital stay, abnormal liver function rate, hysterectomy rate, decreased β-hCG decreased in the first day after curettage and treatment success rate.Conclusion:MRI can not only diagnose CSP, but also can confirm its different types, thus, it has an important clinical significance for the treatment of CSP. UACE combined with curettage hadbetter effect than MTX combined with curettage in the treatment of CSP patients, especially for CSPII patients, and it should be the first choice for the patients with CSPII.
Uterine artery embolization; Methotrexate; Cesarean scar pregnancy; Magnetic resonance imaging
2017-06-03)
10.3877/cma.j.issn.2095-5782.2017.03.002
浙江省教育厅科研基金项目(Y201534762)
310006 杭州,浙江大学医学院附属妇产科医院放射科
邹煜,Email:Zouyuzju@Zju.edu.cn
