高效液相色谱法测定利福昔明混悬乳剂的含量
2017-08-09朱庆贺苗艳王爽陈曦王观悦史同瑞
朱庆贺,苗艳,王爽,陈曦,王观悦,史同瑞
(黑龙江省兽医科学研究所,齐齐哈尔 161006)
高效液相色谱法测定利福昔明混悬乳剂的含量
朱庆贺,苗艳,王爽,陈曦,王观悦,史同瑞*
(黑龙江省兽医科学研究所,齐齐哈尔 161006)
建立了测定利福昔明混悬乳剂含量的高效液相色谱法(HPLC)。采用C18色谱柱(4.6 mm×150 mm,5 μm),以甲醇-乙腈-0.075 mol/L磷酸二氢钾溶液-1 mol/L柠檬酸溶液(32∶28∶25∶4)为流动相,流速1.0 mL/min,检测波长236 nm,进样量20 μL,柱温25 ℃。利福昔明浓度在5~100 μg/mL时,其峰面积与浓度线性关系良好(r2=0.9996),无杂质干扰,稳定性高,回收率范围为98.4%~100.2%,RSD为0.58%~1.32%。本操作方法简便、分析快速、结果准确,适用于利福昔明混悬乳剂的含量测定。
利福昔明;混悬乳剂;高效液相色谱法;含量
利福昔明是利福霉素衍生物,是一种高效低毒的肠道抗生素。适用于革兰氏阳性菌及阴性菌、需氧及厌氧细菌所致急慢性肠道感染等症。在人类医学领域,利福昔明主要用于治疗肠道感染、腹泻、小肠结肠炎等病症[1-2]。但是,近年来兽医领域也有相关应用的报道,其药物剂型主要有干混悬剂、喷雾剂和混悬液[3-4]。而本实验室成功研制了利福昔明混悬乳剂,具备稳定性好,生物相容性好,缓释效果显著的特点,为利福昔明的兽医临床应用提供了一种新的药物剂型,首次建立了针对此剂型的HPLC含量测定法。该测定方法能够为利福昔明混悬乳剂剂型的开发提供一定的参考价值,对于该剂型的稳定性研究、药代动力学研究以及进一步的临床试验都具有重要意义。
1 材料与仪器
1.1 材料 利福昔明对照品,含量95.7%,中国兽医药品监察所;利福昔明混悬乳剂(自制),规格为:2%利福昔明混悬乳剂;乙腈/甲醇均为色谱纯,赛默飞世尔科技公司 ;磷酸二氢钾/柠檬酸,天津天力化学试剂有限公司。
1.2 仪器 电子分析天平,MS104TS/02型,梅特勒-托利多(上海)有限公司; InertSustain C18色谱柱(4.6 mm×150 mm,5 μm);高效液相色谱仪,LC-20AT SPD-20A,SHIMADZU;纯水仪,XYE2-20-H型,北京湘顺源科技有限公司;实验室PH计,FE20型,梅特勒-托利多(上海)有限公司。
2 方法与结果
2.1 色谱条件 色谱柱:C18(150 mm×4.6 mm,5 μm);注温:25 ℃;流速:1 mL/min;检测波长236 nm;进样量20 μL;流动相:甲醇-乙腈-0.075 mol/L磷酸二氢钾溶液-1 mol/L柠檬酸溶液(32∶28∶25∶4)。
2.2 溶液制备
2.2.1 对照品溶液制备 精密称取经105 ℃干燥至恒重的利福昔明对照品(p=95.7%)10 mg,置100 mL容量瓶中,加流动相稀释至刻度,摇匀,制成100 μg/mL的对照品储备液。精密量取对照品储备液2 mL,置10 mL容量瓶中,加流动相稀释至刻度,摇匀,得浓度为20 μg/mL的对照品溶液。
2.2.2 供试品溶液制备 精密量取样品适量(相当于利福昔明20 mg),置100 mL 容量瓶中,加流动相充分溶解并稀释至刻度,摇匀。精密量取此液1 mL置10 mL容量瓶中,加流动相稀释至刻度,摇匀,用0.45 μm微孔滤膜过滤,取续滤液作为供试品溶液。
2.2.3 阴性对照溶液制备 按配方比例量取与供试品相当的空白乳剂(与利福昔明混悬乳剂相比只是不含利福昔明,其他成分相同)适量,按照供试品溶液的制备方法制成阴性对照溶液。
2.3 系统适用性和专属性试验 分别量取利福昔明对照品溶液、供试品溶液和阴性对照溶液,按2.1项色谱条件测定,结果见图1。在该色谱条件下,利福昔明的保留时间k为6.9 min左右,阴性对照在此时间附近没有出峰,因此对利福昔明HPLC的测定没有影响,专属性能满足检测要求。
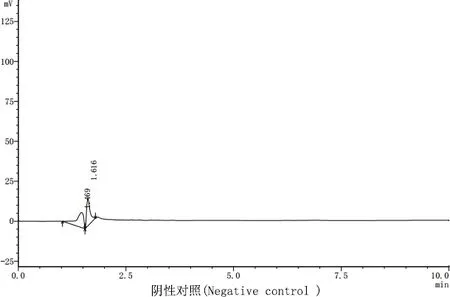

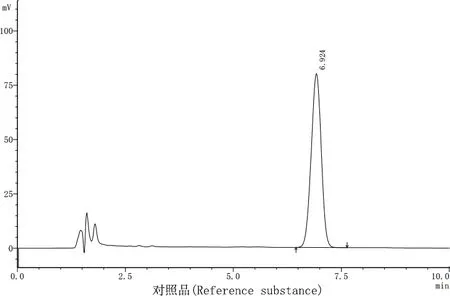
图1 HPLC图谱Fig 1 The HPLC chromatogram
2.4 线性试验 精密量取对照品储备液0.5、2.0、4.0、8.0、10 mL分别置10 mL容量瓶中,加流动相稀释至刻度,摇匀,配制成浓度分别为5、20、40、80、100 μg/mL的系列对照品溶液。按2.1项下色谱条件测定,以峰面积(y)对利福昔明的浓度(x,μg/mL)进行线性回归方程,方程为y=65047x+48715,r2=0.9996。结果表明利福昔明在5~100 μg/mL范围内线性关系良好。
2.5 回收率测定 取2.2.1项制备的100 μg/mL储备液,分别精密取适量储备液并添加配方剂量的空白悬浮乳剂基质,超声溶解后,用流动相稀释成低(L=10 μg/mL )、中(M=50 μg/mL)、高(H=80 μg/mL)3种理论浓度的对照品,每个浓度配制3份,按2.1项下色谱条件测定其含量,计算回收率,结果见表1。结果表明高、中、低浓度对照品的回收率范围为98.4%~100.2%,RSD为0.58%~1.32%。该方法回收率符合要求。
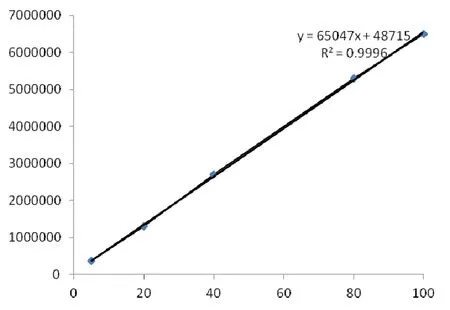
图2 利福昔明标准曲线Fig 2 The standard curve of rifaximin
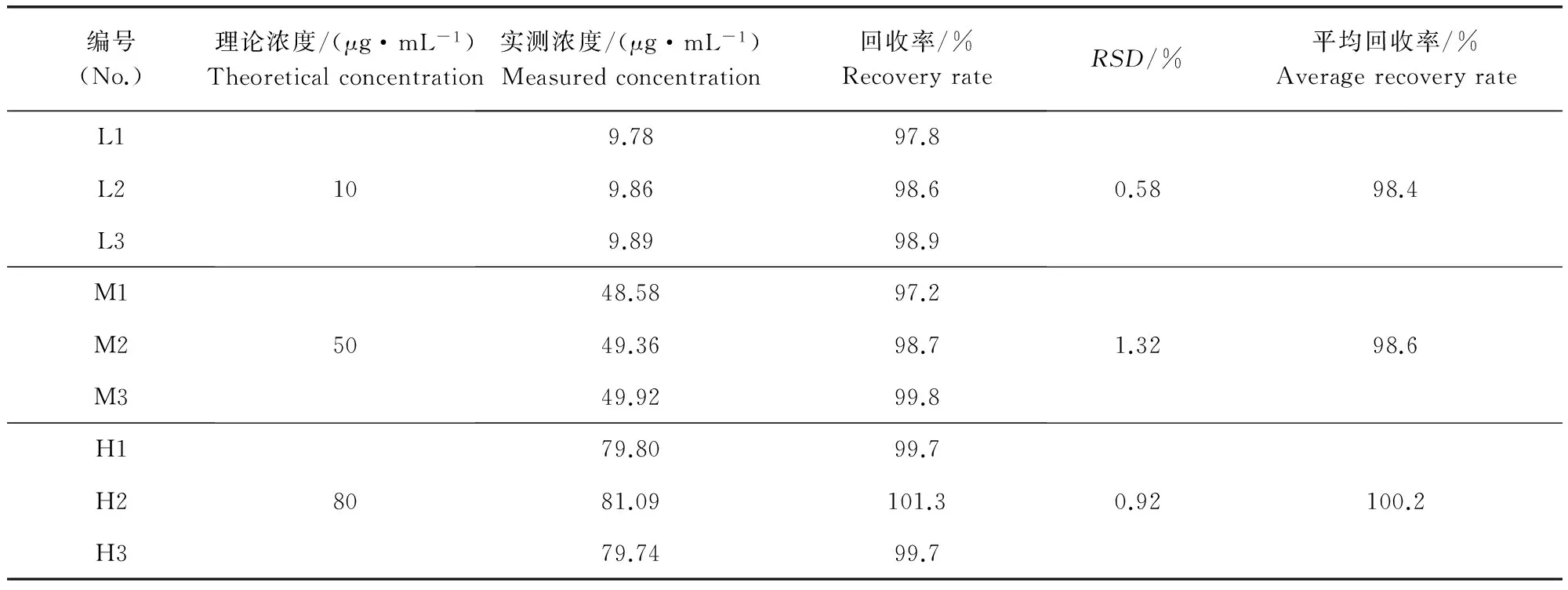
表1 利福昔明的回收率Tab 1 Recovery rate of Rifaximin
回收率R%=实测浓度/理论浓度×100%
2.6 精密度试验 取2.2.1项制备的100 μg/mL储备液,精密取适量储备液,用流动相稀释成20 μg/mL的标准溶液,按2.1项下色谱条件重复进样6次,分别测定其峰面积。结果表明RSD为0.97%,精密度良好。
2.7 稳定性试验 取2.2.1项制备的100 μg/mL储备液,精密取适量储备液,用流动相稀释成20 μg/mL的标准溶液,按2.1项下色谱条件分别于0、2、4、8、10、12 h测定其峰面积。结果表明平均峰面积为1298966,RSD为1.05%。表明本品在12 h内含量稳定。
2.8 样品含量测定 精密量取3批次的利福昔明混悬乳剂样品,每批次3份,按2.2.2项制成供试品溶液,进行含量测定。结果表明,批号为20141201、20160315、20161031的3批样品中利福昔明平均含量分别为标示量的96.22%、99.39%、101.22%,符合规定。
3 讨论与小结
3.1 测定波长和色谱柱的选择 根据文献报道[5-6],利福昔明在240 nm附近有较大吸收。因此初选240、254、236 nm波长下测定利福昔明混悬乳剂中利福昔明的含量。通过色谱结果的比较分析,在236 nm波长下测定,能够获得最大的灵敏度和抗干扰能力,本试验中选择236 nm作为利福昔明含量的检测波长。
色谱柱中C8和C18都是反相色谱柱的一种,适用于分析弱极性的物质,C8在弱极性较强的一侧,C18在极性较弱的一侧,但是差别并不是十分明显,在加上C18较C8具有更好的保留特性,本试验参考相关文献[7]方法选择了C18色谱柱。试验证明,利用C18色谱柱进行色谱分析分离度好,适用于利福昔明混悬乳剂含量的测定。
3.2 利福昔明混悬乳剂 利福昔明是人工半合成抗菌药[2],具有广谱杀菌作用,对革兰阳性菌,如金黄色葡萄球菌、停乳链球菌、无乳链球菌,以及革兰氏阴性菌,如大肠杆菌、巴氏杆菌均具有良好的杀灭效果,而这些细菌恰恰又是引起奶牛乳房炎发生的主要病原微生物。另一方面,利福昔明的药代动力学研究表明,利福昔明在口服后基本无系统吸收,只在局部发挥高效的抗菌作用。综上所述,利福昔明可以作为一种良好的奶牛乳房局部作用型抗菌药物。郭旭[8]等利用制备的利福昔明乳房注入剂对干奶期奶牛临床型乳房炎的预防效果进行了观察。结果表明,利福昔明高剂量组对干奶期奶牛临床型乳房炎的预防效果与空白对照组相比,差异极显著(P<0.01),说明利福昔明对临床型乳房炎有较好的预防效果。
本实验室成功研制了利福昔明混悬乳剂,兼具了利福昔明和混悬乳剂的共同优点,是奶牛乳房炎防治的一种创新剂型。建立了利福昔明混悬乳剂中利福昔明的HPLC的检测方法,本方法分离度好,利福昔明的保留时间在6.9 min左右,峰形好,基本无拖尾,杂质不干扰试验测定,而且采用外标法测定利福昔明混悬乳剂的含量操作简单,结果准确,回收率高,重现性好,是利福昔明悬浮乳剂中利福昔明含量测定的简便、快速、准确的方法。
[1] Steffen R, Sack D A, Riopel I,etal. Therapy of travelers diarrhea with rifaximin on various continents[J]. American Journal of Gastroenterology. 2003, 98: 1073-1078.
[2] Infante R M, Ericsson C D, Jiang Z D,etal. Eleroaggragative scherichia coli diarrhea intraverlers: response to rifaximin therapy[J]. Cli Gastroenterol Hepatol. 2004, 2(2): 135-138.
[3] 李晶. 利福昔明阴道栓和缓释阴道泡腾片的研制及评价[D]. 南京:南京农业大学,2011.
LI J. Research and development on the rifaximin baginal suppository and rifaximin sustained-release baginal effervescent tablets[D]. Nanjing: Nanjing Agricultural University, 2011.
[4] 尚士光. HPLC法测定利福昔明干混悬剂中利福昔明的含量[J]. 中国医药导报,2008,5(35):27-28.
SHANG S G. Determination of rifaximin in Rifaximin Dry Suspension by HPLC[J].China medical herald, 2008,5(35):27-28.
[5] 申兰慧,石涛,赵春才,等.利福昔明片的高效液相色谱分析[J]. 江苏药学与临床研究,2003,11(5):28-30.
SHEN L H, SHI T,ZHAO C C,etal.Determination of Rafaximin and Impurities in Rafaximin Tablets by HPLC[J]. Jiangsu Pharmacertical and Clinical Research,2003,11(5):28-30.
[6] 潘丽,廖慧琼,苏健强,等.利福昔明干混悬剂溶出度测定方法研究[J].亚太传统医药,2013,9(8):44-45.
PAN L, LIAO H Q,SU J Q,etal.Research on Dissolution Test Method of Rifaximin Dry Suspension[J].Asia-Pacfic Traditional Medicine, 2013,9(8):44-45.
[7] 张祖兵.利福昔明的结构确证和质量标准研究[D].成都:四川大学,2004.
ZHANG Z B.Study on the structure and quality criterion of rifaximin[D]. Chendu: Sichuan University, 2004.
[8] 郭旭,李培锋,关红,等.利福昔明乳房注入剂对干奶期奶牛临床型乳房炎预防效果观察[J].动物医学进展.2013,34(7):115-120.
GUO X, LI P F, GUAN H,etal.Observation of Rifaximin Intramammary Infusion on Prophylactic Efficacy of Clinical Mastitis in Dairy Cow of Dry Period[J].Progress in Veterinary Medicine.2013,34(7):115-120.
(编辑:陈希)
Content Determination of Rifaximin Suspo-emulsions by HPLC
ZHU Qing-he, MIAO Yan, WANG Shuang, CHEN Xi, WANG Guan-yue, SHI Tong-rui*
(HeilongjiangInstituteofVeterinaryScience,Qiqihar161006,China)
SHITong-rui,E-mail:systr@sina.com
A method for the content determination of rifaximin suspoemulsion by HPLC was established. HPLC system consisted of C18 column(5 μm, 4.6 mm×150 mm), methyl alcohol-acetonitrile-citric acid-potassium phosphate monobasic(32∶28∶25∶4) as mobile phase. The flow rate was 1.0 mL/min. The detection wave length was 236 nm. The injection volume was 20 μL and column temperature was room temperature. There was no interference occurred from inpurities. The calibration curve was linear in the range of 5~100 μg/mL(r2=0.9996).The recovery was 98.4%~100.2% andRSDwas 0.58%~1.32%. The method is rapid, simple and accurate for the content determination of rifaximin suspo-emulsions.
rifaximin;suspo-emulsions ;HPLC;content
黑龙江省应用技术研究与开发项(czznkt2016-2) 作者简介: 朱庆贺,研究实习员,硕士,从事兽药研究。
史同瑞。E-mail: systr@sina.com
10.11751/ISSN.1002-1280.2017.7.08
2016-11-25
A
1002-1280 (2017) 07-0042-05
S859.79
