高效液相色谱法测定卡巴匹林钙可溶性粉中卡巴匹林钙和游离水杨酸的含量
2017-08-09林仙军张航俊罗成江陈晓林徐晶许国强
林仙军,张航俊,罗成江,陈晓林,徐晶,许国强
(1.浙江省兽药饲料监察所,杭州 311101;2.浙江省诸暨市畜牧兽医局,浙江诸暨 311800)
高效液相色谱法测定卡巴匹林钙可溶性粉中卡巴匹林钙和游离水杨酸的含量
林仙军1,张航俊1,罗成江1,陈晓林1,徐晶2,许国强2
(1.浙江省兽药饲料监察所,杭州 311101;2.浙江省诸暨市畜牧兽医局,浙江诸暨 311800)
建立了一种可同时测定卡巴匹林钙可溶性粉中卡巴匹林钙和游离水杨酸含量的高效液相色谱方法。采用Agilent Zorbax XDB C18色谱柱,流动相为0.2%磷酸溶液-乙腈(70∶30,V/V),流速1.0 mL/min,检测波长228 nm,柱温30 ℃。结果表明卡巴匹林钙和水杨酸在0.1~100 μg/mL浓度范围内线性关系良好,相关系数r均大于0.999;卡巴匹林钙回收率为97.4%~101.1%,批内相对标准偏差为0.4%~1.3%,批间相对标准偏差为0.2%~0.5%;水杨酸回收率为96.9%~101.2%,批内相对标准偏差为0.5%~1.5%,批间相对标准偏差为0.2%~0.5%。方法操作简便、准确、可靠,可用于卡巴匹林钙可溶性粉的质量控制。
卡巴匹林钙;水杨酸;可溶性粉;高效液相色谱
卡巴匹林钙是乙酰水杨酸钙与尿素的络合物,在水中水解为乙酰水杨酸,从而发挥解热、镇痛、抗炎及抑制血小板聚集的作用[1]。卡巴匹林钙正逐步推广应用于畜禽养殖业,用于猪、鸡的发热和缓解疼痛等[2]。其制剂卡巴匹林钙可溶性粉质量标准收载于《兽药质量标准汇编》(2013年)[3],采用紫外分光光度法测定卡巴匹林钙的含量,结果准确,但专属性较差;水杨酸检查项供试品溶液配制不合理,结果不稳定。目前卡巴匹林钙或水杨酸的检测方法有毛细管电泳法[4]、高效液相色谱法[5-6]、高效液相色谱-串联质谱法[7]和超高效液相色谱法[8-9]。高效液相色谱法快速、准确,应用广泛,高效液相色谱法测定卡巴匹林钙可溶性粉中卡巴匹林钙和游离水杨酸的含量的方法未见报道。因此,本研究利用建立的方法进行实际样品检测,积累数据,以期为完善卡巴匹林钙可溶性粉的质量控制提供参考。
1 仪器与材料
1.1 主要仪器 Agilent 1260高效液相色谱仪,配VWD检测器(美国Agilent公司);AG-285电子天平(Mettler公司);SL502N电子天平(上海民桥精密科学仪器有限公司);KQ-500E型超声波清洗器(昆山市超声仪器有限公司);TU-1810紫外可见分光光度计(北京普析通用仪器有限公司)。
1.2 主要材料 乙腈、甲醇均为色谱纯,默克公司;磷酸为优级纯,浙江三鹰化学试剂有限公司;冰乙酸为分析纯;水为超纯水。
1.3 对照品和供试品 卡巴匹林钙对照品购于中国兽医药品监察所,批号H0691503,含量99.2%;水杨酸对照品,购于中国食品药品检定研究院,批号100106-201104,含量99.9%;卡巴匹林钙可溶性粉,浙江大飞龙动物保健品有限公司产品,规格为50%,批号为20160801,20160802,20160803;卡巴匹林钙原料为齐鲁晟华制药有限公司产品,批号502080780,含量为98.9%;乳糖为湖南尔康制药有限公司产品,批号20160701。
2 方法与结果
2.1 检测波长的选择 取卡巴匹林钙和水杨酸对照品适量,用甲醇溶解并稀释制成约50 μg/mL的溶液,在200~400 nm波长范围内进行扫描。结果卡巴匹林钙在228 nm和276 nm的波长处有最大吸收,在228 nm波长处吸收值较大;水杨酸在228 nm波长处也有较大吸收。综合考虑,选择228 nm作为检测波长。
2.2 流动相的选择 考察了乙腈-水、乙腈-磷酸溶液和乙腈-乙酸溶液等作为流动相。乙腈-水为流动相,卡巴匹林钙和水杨酸出峰较快,峰形差;乙腈-磷酸溶液较乙腈-乙酸溶液峰形较好。比较了乙腈与0.05%磷酸溶液、0.1%磷酸溶液、0.2%磷酸溶液和0.3%磷酸溶液作为流动相,各流动相保留时间一致,磷酸浓度越高峰形越好,而乙腈-0.3%磷酸溶液pH值为1.5,对色谱柱损害较大;比较了0.2%磷酸溶液-乙腈(70∶25,V/V)、0.2%磷酸溶液-乙腈(70∶30,V/V)和0.2%磷酸溶液-乙腈(70∶35,V/V)作为流动相,0.2%磷酸溶液-乙腈(70∶30,V/V)为流动相峰形对称,保留时间比较合适,分离较好。因此,选择0.2%磷酸溶液-乙腈(70∶30,V/V)作为流动相。
2.3 卡巴匹林钙对照品溶液的制备 取卡巴匹林钙对照品适量,精密称定,用流动相超声溶解并定量稀释制成每1 mL中约含50 μg的溶液,摇匀,作为对照品溶液。
2.4 水杨酸对照品溶液的制备 取水杨酸对照品适量,精密称定,用流动相超声溶解并定量稀释制成每1 mL中约含25 μg的溶液,摇匀,作为水杨酸对照品溶液。
2.5 卡巴匹林钙和水杨酸检测用供试品溶液的制备 取卡巴匹林钙可溶性粉适量,精密称定,用流动相超声溶解并定量稀释制成每1 mL中约含1 mg的溶液,摇匀,作为水杨酸测定供试品溶液;取5.00 mL置100 mL量瓶中,用流动相稀释至刻度,摇匀,作为卡巴匹林钙测定供试品溶液。
2.6 高效液相色谱条件和系统适应性 色谱柱:Agilent Zorbax XDB C18 5 μm,4.6×250 mm;检测波长228 nm;流速1.0 mL/min;进样量20 μL;柱温30 ℃;流动相为0.2%磷酸溶液-乙腈(70∶30,V/V)。卡巴匹林钙和水杨酸混合对照品溶液、卡巴匹林钙测定供试品溶液、水杨酸测定供试品溶液和辅料乳糖色谱图见图1~图4。卡巴匹林钙和水杨酸的分离度大于5.0,理论板数以卡巴匹林钙计大于3000。

图1 混合对照品溶液(1:卡巴匹林钙;2:水杨酸)Fig.1 Mixture of two reference substances(1.carbasalate calcium;2.salicylic acid)

图2 卡巴匹林钙测定供试品溶液(1:卡巴匹林钙)Fig.2 Carbasalate calcium determination solution (1.carbasalate calcium)

图3 水杨酸测定供试品溶液(1:卡巴匹林钙;2:水杨酸)Fig.3 Salicylic acid determination solution (1.carbasalate calcium;2.salicylic acid)

图4 辅料(乳糖)Fig.4 Accessories(lactose)
2.7 标准曲线及线性关系考察 分别取卡巴匹林钙和水杨酸对照品适量,用流动相超声溶解并稀释制成每1 mL中含卡巴匹林钙和水杨酸100 μg的溶液,摇匀,作为混合对照品溶液。分别取混合对照品溶液适量,用流动相稀释成浓度分别为0.1、0.5、2.5、5、10、50 μg/mL的溶液,与混合对照品溶液一起依照浓度由小到大的次序,按上述色谱条件进样分析,以系列标准溶液浓度为横坐标,峰面积为纵坐标绘制标准曲线,卡巴匹林钙和水杨酸在0.1~100 μg/mL浓度范围内线性关系良好,卡巴匹林钙线性方程Y=41.277X+11.205,相关系数r=0.9994;水杨酸线性方程Y=45.012X+0.1689,相关系数r=1.0000。
2.8 精密度试验 取卡巴匹林钙对照品溶液(50 μg/mL),按上述色谱条件重复连续进样6次,测得峰面积相对标准偏差为0.8%;取水杨酸对照品溶液(20 μg/mL),按上述色谱条件重复连续进样6次,测得峰面积相对标准偏差为0.5%。表明此方法的仪器精密度符合要求。
2.9 稳定性试验 取批号为20160801的卡巴匹林钙可溶性粉供试品溶液,分别于0、2、4、6、12、24 h进行测定,测得卡巴匹林钙峰面积相对标准偏差为1.1%,测得水杨酸峰面积相对标准偏差为1.4%。表明供试品溶液稳定性良好。
2.10 方法专属性 取卡巴匹林钙可溶性粉各0.1 g,分别加水、1 mol/L盐酸溶液、1 mol/L氢氧化钠溶液和5%过氧化氢溶液各1 mL,放置1 h,依法测定。卡巴匹林钙在水中较不稳定,水杨酸的量从1%升高到2%;在盐酸溶液中稳定(数据见稳定性试验);在氢氧化钠溶液中不稳定,99%以上已降解为水杨酸;在过氧化氢溶液中不稳定,约有20%降解为水杨酸。相应色谱图见图5~图8。

图5 水1 h(1:卡巴匹林钙;2:水杨酸)Fig.5 water 1 h (1.carbasalate calcium;2.salicylic acid)

图6 1 mol/L盐酸溶液1 h(1:卡巴匹林钙;2:水杨酸)Fig.6 1 mol/L hydrochloric acid solution 1 h (1.carbasalate calcium;2.salicylic acid)

图7 1 mol/L氢氧化钠溶液1 h(2:水杨酸)Fig.7 1 mol/L sodium hydroxide solution 1 h (1.carbasalate calcium;2.salicylic acid)

图8 5%过氧化氢溶液1 h(1:卡巴匹林钙;2:水杨酸)Fig.8 5% hydrogen peroxide solution 1 h (1.carbasalate calcium;2.salicylic acid)
2.11 卡巴匹林钙加样回收率试验 取批号为20160701的乳糖作为辅料,加入卡巴匹林钙原料配制成40%、50%和60%的卡巴匹林钙可溶性粉试样,依法进行测定。每个浓度连续3 d,每次做5份平行样,计算回收率、批内相对标准偏差和批间相对标准偏差。结果显示,回收率为97.4%~101.1%,批内相对标准偏差为0.4%~1.3%,批间相对标准偏差为0.2%~0.5%,结果见表1。
2.12 水杨酸加样回收率试验 由于水杨酸的限度为不得过1.5%,因此,取批号为20160701的乳糖作为辅料,加入水杨酸对照品适量,使成浓度约为0.5%、1.0%和1.5%的供试品,依法进行测定。每
个浓度连续3 d,每次做5份平行样,计算回收率、批内相对标准偏差和批间相对标准偏差。回收率结果为96.9%~101.2%,批内相对标准偏差为0.5%~1.5%,批间相对标准偏差为0.2%~0.5%,结果见表2。
2.13 实际样品测定 按照建立的检测方法,对浙江大飞龙动物保健品有限公司提供的卡巴匹林钙可溶性粉进行检测,规格为50%,批号为20160801、20160802和20160803。卡巴匹林钙的含量与紫外分光光度法一致;水杨酸的含量测定虽已考虑到在水中会降解的因素,加水溶解后立即测定,但结果还是较本法偏高。数据见表3和表4。
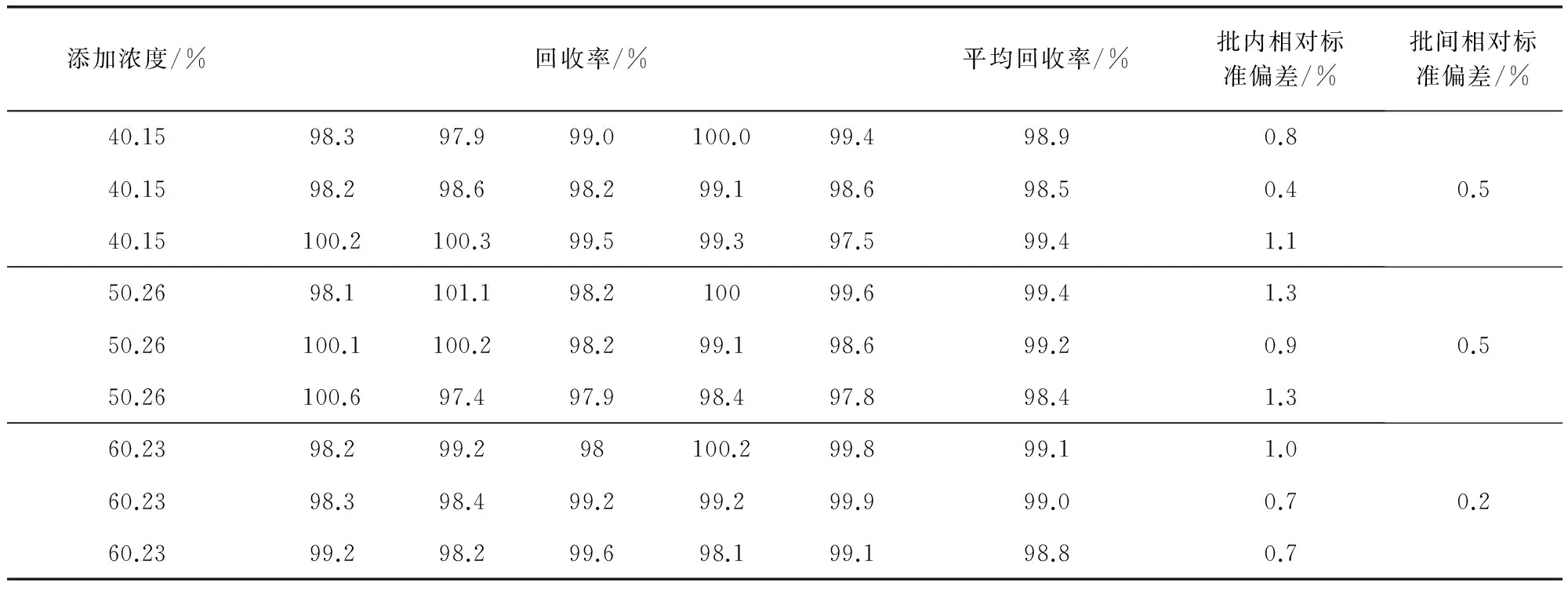
表1 卡巴匹林钙加样回收率试验结果(n=5)Tab 1 Carbasalate calcium results of recovery test(n=5)
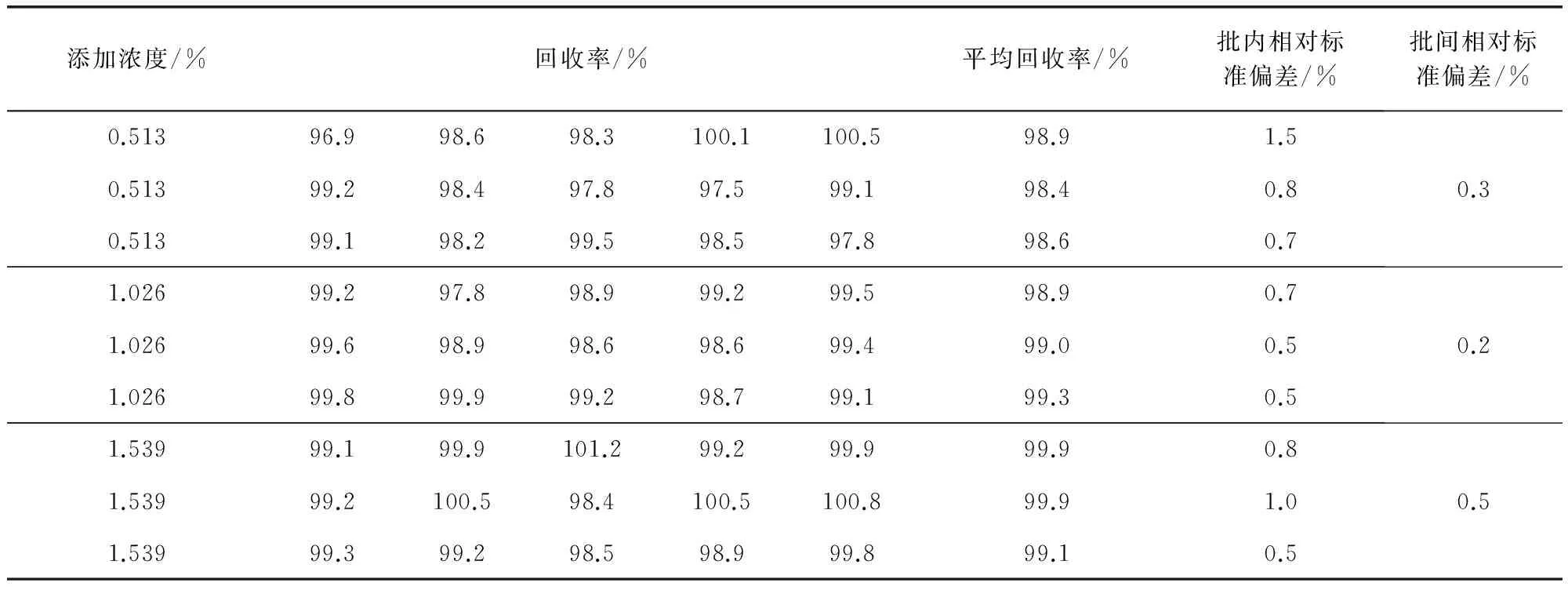
表2 水杨酸加样回收率试验结果(n=5)Tab 2 Salicylic acid results of recovery test(n=5)

表3 HPLC法与紫外分光光度法测定卡巴匹林钙含量结果比较(n=3)Tab 3 Comparison of HPLC and UV spectrophotometry for the determination of carbasalate calcium(n=3)
3 小 结
游离水杨酸是卡巴匹林钙的降解产物,需要严格控制。《兽药质量标准汇编》(2013年)规定卡巴匹林钙可溶性粉含水杨酸不得超过1.5%,采用标准规定的方法进行检测,供试品加水溶解后卡巴匹林钙即开始快速水解为水杨酸,结果偏大且不稳定,供试品溶液配制后放置1 h检测结果即可增加一倍,差异显著。合格的卡巴匹林钙可溶性粉水杨酸检查项目易误判为不合格,给生产、经营和检验等带来影响。

表4 HPLC法与紫外分光光度法测定水杨酸含量结果比较(n=3)Tab 4 Comparison of HPLC and UV spectrophotometry for the determination of salicylic acid(n=3)
[1] 侯曙光,魏树礼.卡巴匹林钙的性质及应用[J].中国药学杂志,1996,31(2):105-107.
HOU S G ,WEI S L. The properties and applications of carbasalate calcium[J]. Chinese Pharmaceutical Journal,1996,31(2):105-107.
[2] 郑文,陈洪亮,吴连勇.卡巴匹林钙的药理作用及其在养殖中的应用展望[J].家禽科学,2010,(9):48-49.
ZHEN W,CHEN H L,WU L Y.Pharmacological effects of Kaba Pilin and its application in aquaculture[J].Poultry Science,2010,(9):48-49.
[3] 农业部兽药评审中心.兽药质量标准汇编(2013年)[M].北京:中国农业出版社,2013.
Ministry of Agriculture veterinary drug evaluation center. Veterinary drug quality standards(2013)[M].Beijing:China Agriculture Press,2013.
[4] Zaugg S,Zhang X,Sweedler J.etal. Determination of salicylate,gen-tisic acid and salicyluric acid in human urine by capillary electrophoresis with laser-induced fluorescence detection[J].Chromatography,2001,(752):17-31.
[5] Shen C L,Huang X H. Development and validation of a RP-HPLC method for simultaneous determination of warfarin enantiomers,aspirin and salicylic acid in beagle plasma[J]. Application to Pharmacokinetic Study.Latin American Journal of Pharmacy,2013,(32):679-687.
[6] Eva-luise Hobl,Bernd Jilma,Josef Ebner,etal. Simultaneous determination of acetylsalicylic acid and salicylic acid in human plasma by isocratic high-pressure liquid chromatography with post-column hydrolysis and fluorescence detection[J]. Biomedical Chromatography,2013,27(6):695-698.
[7] Mullangi R,Sharma K,Srinivas N. Review of HPLC methods and HPLC methods with mass spectrometric detection for direct determination of aspirin with its metabolite(s) in various biological matrices[J]. Biomedical Chromatography:BMC,2012,26(8):906-941.
[8] Rubak P,Hardlei T F,Würtz M,etal. Low-doseacetylsalicylic acid therapy monitored with ultra high performance liquid chro-matography[J]. Clin Biochem,2013,(46):988-992.
[9] Castillo-García M L,Aguilar-Caballos M P,Gómez-Hens A. Determination of acetylsalicylic acid and its major metabolites in bovine urine using ultra performance liquid chromatography[J]. Journal of Chromatography,2015,985:85-90.
(编辑:侯向辉)
Determination of Carbasalate Calcium and Free Salicylic Acid in Carbasalate Calcium Soluble Powder by HPLC
LIN Xian-jun1, ZHANG Hang-jun1,LUO Cheng-jiang1,CHEN Xiao-lin1,XU Jing2,XU Guo-qiang2
(1.ZhejiangProvinceSupervisoryInstituteofVeterinaryDrugandFeed,Hangzhou,Zhejiang311101,China; 2.AnimalHusbandryandVeterinaryBureauofZhujiCountyinZhejiang,Zhuji311800,China)
A high performance liquid chromatography method was established for the determination of carbasalate calcium and free salicylic acid in carbasalate calcium soluble powder. Separation was performed on a reversed-phase Agilent Zorbax XDB C18 column. The mobile phase consisted of a mixture of 0.2% phosphoric acid solution and acetonitrile(70∶30,V/V) . The detection wavelength was 228 nm, the flow rate was 1.0 mL/min, and the column temperature was 30 ℃. A good linearity of the calibration curves was obtained with the range of 0.1~100 μg/mL for carbasalate calcium and free salicylic acid, the correlation coefficientr>0.999. The recoveries of carbasalate calcium were 97.4%~101.1%, the intra-assay coefficient of variation were 0.4%~1.3%, and the inter-assay coefficients of variation were 0.2%~0.5%. The recoveries of free salicylic acid were 96.9%~101.2%, the intra-assay coefficient of variation were 0.5%~1.5%, and the inter-assay coefficients of variation were 0.2%~0.5%. The method is simple, accurate and reliable in the determination of carbasalate calcium and free salicylic acid in carbasalate calcium soluble powder.
carbasalate calcium;salicylic acid;soluble powder;HPLC
林仙军,高级畜牧师,从事兽药、饲料和畜产品质量安全检测研究。E-mail: lxj1000@163.com
10.11751/ISSN.1002-1280.2017.7.06
2017-01-03
A
1002-1280 (2017) 07-0028-06
S859.2
