工业废水CODCr测定方法与技术发展过程分析
2017-08-08吕文英刘国光吴海珍韦朝海
韦 聪 李 磊 吕文英 刘国光 吴海珍 韦朝海
(1.广东工业大学环境科学与工程学院,广东 广州 510006;2.华南理工大学环境与能源学院,广东 广州 510006;3.华南理工大学生物科学与工程学院,广东 广州 510006)
工业废水CODCr测定方法与技术发展过程分析
韦 聪1,2, 李 磊1, 吕文英1, 刘国光1, 吴海珍3, 韦朝海2
(1.广东工业大学环境科学与工程学院,广东 广州 510006;2.华南理工大学环境与能源学院,广东 广州 510006;3.华南理工大学生物科学与工程学院,广东 广州 510006)
化学需氧量(chemical oxygen demand,COD)作为表征污水或废水污染程度的一个重要指标,在全球范围内被普遍采用。通过追踪COD方法发展的历史,以工业废水中最常用的重铬酸钾法为例,从氧化还原电位、催化作用等方面分析方法原理的特点、影响因素与适用范围,结合氧化剂的选择、定义的科学性、二次污染、COD成分的毒性以及干扰组分的存在5个方面讨论传统COD方法中存在的问题,指出方法创新和完善的方向;在方法原理基础上,论述微波消解技术、分光光度技术、库仑滴定技术等方面的COD技术化及其实际应用的动态,提出实现流程的标准化和样品的批量化可以提高效率的观点。通过对我国工业废水COD测定方法、技术应用的过程分析,指出COD方法及技术的创新性、可靠性、时效性对于我国未来的工业废水污染控制的稳定性与水环境管理的规范性将发挥重要的影响作用。
化学需氧量;重铬酸钾法;微波消解技术;分析方法;干扰组分
0 引 言
COD被列为我国水污染控制最重要的执行指标,也是水环境质量的核心评价指标,关于工业废水COD原理性发明的历史、传统测试方法存在的问题、COD测定技术的发展及其干扰组分的识别,可能从某种程度上支配我国的环境经济代价,从而构成对社会发展的潜在影响。COD是指废水或污水(下文称废水)中有机物和还原性无机物在强氧化剂作用下的氧化过程中所需氧的当量值。它最初是表征废水中有机污染程度的综合性指标,以生物分解有机物需要耗氧的原理获得启发,用氧化剂的氧化能力来替代水中生物分解有机物的能力。
在出现COD的定义之前,19世纪末,由Sawyer[1]和Barnett等[2]首先提出了通过测定生化需氧量(biological oxygen demand,BOD)来评估生活污水或者工业废水中污染物的含量或浓度。鉴于BOD测试过程需要较长的时间,学者们希望寻找一种测定结果等同于BOD,能够在短时间内评估废水污染程度的化学方法。由于不同废水中微生物的代谢速率不是一个常量,所以很难找到一种化学的测定方法与BOD相关联。然而,在很多情况下,常常需要在最短的时间内大致了解某种废水的耗氧能力,基于该想法,一些学者设想用某些氧化剂的氧化能力来代替水体中微生物分解有机物的能力,并通过测定氧化剂的消耗量来间接计算废水的耗氧量。尽管通过化学测定方法得出的耗氧量高于BOD值,但却可作为水污染程度的一个参考性判断标准,该方法渐渐得到了认可并结合各种技术加以推广应用。科学家们将运用化学的方法测定得到的废水耗氧量定义为化学需氧量,简称COD。目前在工业废水COD分析中,以重铬酸钾作为氧化剂的应用已经很广泛,在水环境管理方面发挥了重要作用。我国首次引入COD的概念发现于《水和废水化学分析方法手册》(1977年出版)的文献中,随着GB 11914——1989《水质化学需氧量的测定 重铬酸盐法》的颁布,COD作为水环境管理指标在1990年7月1日被推行。尽管COD在我国的水环境管理中占有非常重要的地位,但对原理的新发现和技术的发展进步方面,我国科学界贡献不大。
科学家们在最初的探索中,提出一些氧化剂来判断废水需氧量。基于稳定性与可靠性,Adeney和Dawson[3]于1926年首先开始基于重铬酸钾的COD分析方法实验;但现代COD的测定方法都是基于Muers[4]的工作,他于1936年首先使用Ag2SO4作为催化剂来促进重铬酸钾对挥发性脂肪酸的氧化。之后,Moore等[5-6]将COD测试应用于常规废水的分析;Dzyadzio[7]提出在约200℃和酸性条件下使用碘酸钾作为氧化剂,然后用碘量法测定过量的碘酸钾,与重铬酸钾法比较,以此计算出来的废水中选定有机物的耗氧量的误差均不超过3%。关于干扰误差的研究,Williams等[8]提出以HgSO4作为络合剂来减小Cl-的干扰。在方法原理方面,科学家们考虑批量分析、高通量检测、降低药剂消耗、降低能耗以及减少二次污染等的需求,发展了不少新的COD测定技术,如微波消解技术、分光光度技术、库仑滴定技术等,提高了工业废水COD测试的效率。
因此,本文把回顾工业废水COD方法原理与技术发展、传统COD分析方法存在的问题以及干扰组分的识别作为立论的观点,对方法和技术加以讨论,阐明COD分析技术在水环境管理中新的作用和面临的挑战。
1 工业废水COD测定原理
在工业废水中常用重铬酸钾法来测试COD值,COD分析的重铬酸钾法最初由Adeney和Dawson[3]提出,基于重铬酸钾分子的稳定性和强氧化性,容易制得分析纯以上的纯品也是其中的一个原因。通过一系列的研究明确COD的分析过程为[9]:在水样中加入已知浓度的重铬酸钾标准溶液,于强酸介质下以Ag2SO4作为催化剂,以HgSO4掩蔽Cl-,加温沸腾回流2h,冷却后以试亚铁灵为指示剂,用已标定的硫酸亚铁铵溶液滴定水样中未被还原的重铬酸钾,由消耗的硫酸亚铁铵的量求得重铬酸钾消耗量表达的COD值。重铬酸钾在强酸性介质中的氧化反应式为
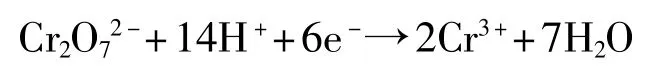
标准电极电位为

反应条件中,回流加热的温度约为146℃(419K),反应体系中浓硫酸浓度为9mol/L,重铬酸钾的浓度为0.25mol/L,根据能斯特方程,此时电对Cr2O72-/Cr3+的条件电极电位为
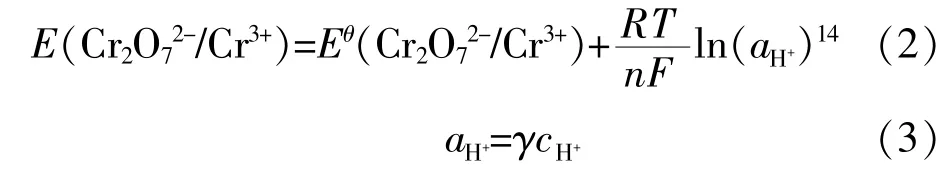
式中:E(Cr2O72-/Cr3+)——条件电极电位;
R——气体常数,8.314J/(K·mol);
T——热力学温度;
n——电极反应式中转移的电子数,n=6;
F——法拉第常数,96485C/mol。
为简化计算,假设浓硫酸的活度系数γ为1,因此,将该反应体系的数据代入条件电极电位的方程,有:
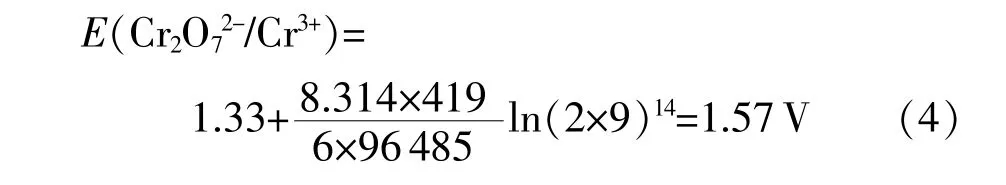
表1列举了部分工业中常见有机物的半波电位。从表中可见,常见有机物的半波电位处于-2.35~0.20V范围内,如果忽略其他条件因素,仅从氧化还原电位的角度来看,在上述反应条件下,重铬酸钾具有足够的氧化能力分解常见的有机化合物。标准方法中,0.25mol/L的重铬酸钾溶液可测定COD值介于50~700 mg/L的水样,0.025 mol/L的重铬酸钾溶液可测定COD值介于10~50mg/L的水样,在浓度的高端和低端都存在准确度变差的趋势,更高浓度的水样需要通过稀释进行分析,极端低浓度的水样则需要选用其他方法。
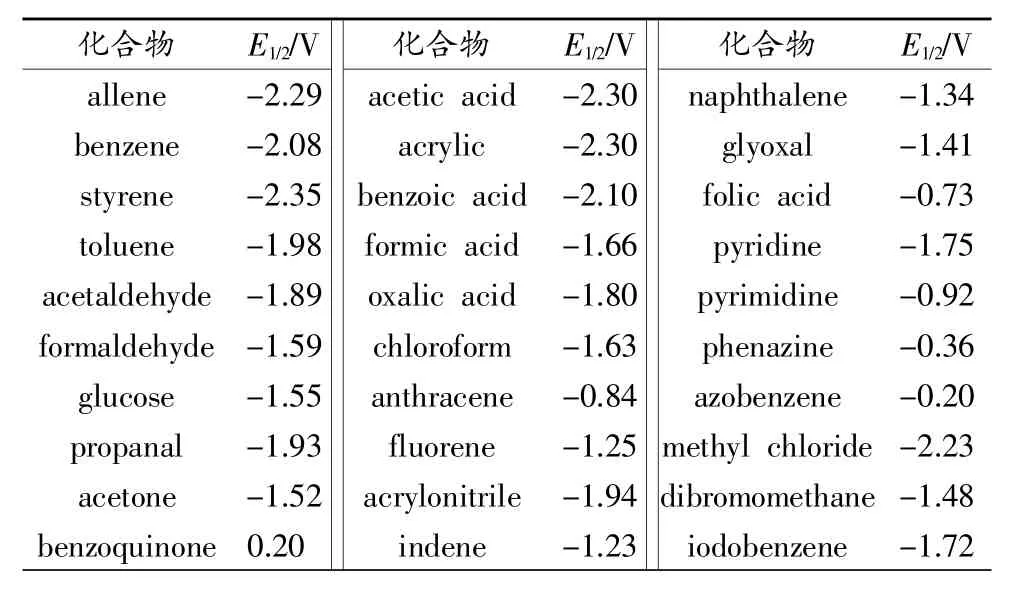
表1 25℃时工业中部分常见有机物的半波电位(相对于标准氢电极)
2 影响重铬酸钾法测定工业废水COD准确性的因素
2.1 催化剂
重铬酸钾法使用的催化体系是Ag2SO4-H2SO4溶液,以含羟基的脂肪族有机物为例,催化机理[10]为:有机物中含羟基的脂肪族有机化合物在强酸性介质中首先被重铬酸钾氧化为脂肪酸。这时,所生成的脂肪酸与硫酸银作用生成脂肪酸银,由于Ag+的作用,使羧基易断裂而生成CO2和H2O,并进一步生成新的脂肪酸银,脂肪酸分子中的碳原子较前者少了一个,如此重复循环,逐步使有机物全部氧化成CO2和H2O,反应过程可简略表示为:
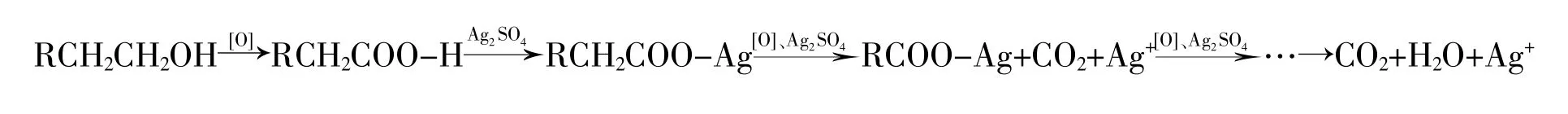
值得关注的是,标准重铬酸钾法中规定,当取20 mL待测水样时,则相应地加入30mL Ag2SO4-H2SO4溶液作为催化剂。刘爱鹰[11]在保持其他条件不变的情况下改变催化剂的加入量,发现催化剂适量少加时测定结果变化不大;当加入20mL Ag2SO4-H2SO4溶液时,测定COD的相对误差也仅为8.5%;但当加入量为60mL时,则COD分析的相对误差则高达292%。原因是重铬酸钾在酸性条件下分解为铬酸根,铬酸根与Ag+反应生成铬酸银沉淀。当Ag2SO4-H2SO4加入量大于30mL时,在酸性条件下,一方面,Ag+会与重铬酸钾形成铬酸银沉淀而影响滴定终点:
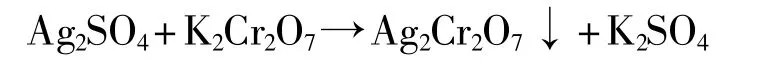
另一方面,Ag+与重铬酸钾反应,会导致溶液中重铬酸钾浓度降低,使E(Cr2O72-/Cr3+)的值变小,进而降低重铬酸钾的氧化能力,同时产生了隐形的重铬酸钾消耗。所以,催化剂Ag2SO4-H2SO4溶液的加入量是影响COD测试准确度的一个关键因素。
尽管通过Ag2SO4-H2SO4催化体系保证了重铬酸钾法能够对大多数有机物的完全氧化而被广泛应用,但是,人们已经意识到Ag2SO4的使用会导致COD分析费用过于昂贵,因此,国内外分析工作者在寻找Ag2SO4的替代物方面开展了一些研究。Selvapathy等[12]提出了用MnSO4来替代Ag2SO4作催化剂,经过几种有机废水的测试表明具有一定的可行性。Sun等[13]尝试了在H2SO4-H3PO4的混酸体系中,以Mn(H2PO4)2为催化剂,把 H2SO4-H3PO4、加入催化剂Mn(H2PO4)2量和回流时间作为正交试验法的控制条件,指出催化剂Mn(H2PO4)2的加入量是3个控制条件中影响COD分析准确度最主要的因素,而回流时间是最次要的因素,当控制加入催化剂Mn(H2PO4)2量为0.3g,H2SO4-H3PO4体积比为6∶1及回流时间为5min的条件时,标准物邻苯二甲酸氢钾的分析结果相对误差仅为0.39%,回流时间的缩短可以明显节能。在保证所有有机物彻底分解的前提条件下,催化剂应当在经济性与无二次污染方面寻求兼顾。
2.2 温 度
对于大部分化学反应来说,温度是一个至关重要的参数。Ramon等[14]以重铬酸钾法为原理,利用可控温的微波消解器代替标准方法使用的加热炉来消解样品,研究发现,在反应温度超过165℃时,重铬酸钾会发生如下的热分解反应:
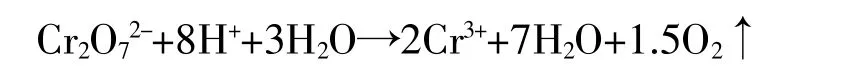
这将会使COD的测量带来正偏差,考虑到重铬酸钾的热稳定性,并通过对两种控温系统的控温效果对比实验,最终选定反应最高温度不超过170℃。Dasgupta等[15]以理论值为200mg/L的邻苯二甲酸氢钾标准溶液为测试对象,考察了温度对重铬酸钾与邻苯二甲酸氢钾反应的速率常数变化,当温度分别为100,110,130,140℃时,相对应的反应速率常数为2.51±0.08,3.56±0.10,6.68±0.18,11.60±0.84(mol/L)-1·s-1,表明温度的作用符合阿伦尼乌斯方程的规律。因此,如果一种新型COD方法仍需要在高温下消解样品,则不能忽视温度对结果的影响。
2.3 酸 度
重铬酸钾法分析水样COD的测定体系为强酸性介质,根据能斯特方程,酸度会显著影响重铬酸钾的条件电极电位,如果酸度太小,那么E(Cr2O72-/Cr3+)的值会降低,使得重铬酸钾的氧化能力不足以氧化所有的有机物,导致COD分析结果偏低;如果酸度太高,虽然E(Cr2O72-/Cr3+)的值会升高,增强了重铬酸钾的氧化能力,但是却增加了硫酸的消耗量,造成资源的浪费。为此,根据能斯特方程,表2列出了E(Cr2O72-/Cr3+)随硫酸浓度变化时的改变趋势。实际反应体系中浓硫酸浓度要求大于9 mol/L,追求稳定的氧化电位。

表2 不同硫酸浓度下,重铬酸钾条件电位的变化趋势
2.4 掩蔽剂
对于高氯含量废水,大量存在的Cl-会使COD测试的结果偏高,为了掩蔽Cl-,需要在重铬酸钾法中加入一定量的掩蔽剂如硫酸汞,使之与Cl-形成稳定性的络合物,阻止在酸性条件下Cl-对重铬酸钾的还原作用。沈澄英[16]探讨了掩蔽剂HgSO4用量对以邻苯二甲酸氢钾配制CODCr标准溶液作为分析样品测定的影响,当200mg/L的CODCr值水样中含有2000mg/L Cl-时,加入 10 倍 Cl-质量的 HgSO4后,仍然有546.6mg/L的Cl-没有被硫酸汞络合。经过一系列的重复实验发现,HgSO4与Cl-的质量比达到50∶1时才能彻底掩蔽Cl-,此时的测定值非常接近真值。因此,高盐水样的分析需要消耗大量的汞,二次污染非常严重。
3 传统工业废水COD分析方法中存在的问题
3.1 氧化剂的选择
以工业废水中最常用的国家标准重铬酸钾法为例,虽然重铬酸钾具有较高的氧化能力,但对于不同水质的水体(水样),其氧化程度受方法条件的影响,可能造成测量值与实际真值不符,尤其含有难降解有机物的工业废水,测得的COD值与理论值相差较大。用标准重铬酸钾法测定COD,直链脂肪族化合物可被完全氧化,但芳香烃如苯和甲苯氧化率低,吡啶则很难被氧化。分子结构分析指出,在基态下,苯分子的6个π电子都在成键轨道上,它们的动量要比3个孤立的π轨道中低得多,因此苯环是个很稳定的体系,在重铬酸钾分析COD的氧化体系中,其氧化率仅17%[17]。含有杂元素的吡啶环等杂环芳烃也有相似的稳定结构,大π键的形成降低了分子的反应活性,其氧化率也只有20%左右。若这些难氧化有机物恰恰是废水的主要污染成分,用COD来衡量浓度或污染程度就会偏离实际。早期的废水中难降解有机物含量少,COD值能够代表废水中有机物含量的真值,但随着工业的发展,进入水体中的难降解有机物逐渐增多,其氧化率也逐渐降低,可以预见,随着水体污染的加重,水体中难降解有机物含量的增加,单位COD值所造成的环境危害将会越来越大。寻求对水体环境产生生态风险的有机污染物能够彻底反应的氧化剂,阐明氧化原理,建立定量分析,是对传统COD分析方法的创新。
3.2 定义的科学性
COD的传统定义是指用强氧化剂氧化水中有机物而消耗的氧化剂的量,定义中并没有区分有机物和还原性无机物,实际上,COD包括了还原性无机物消耗氧化剂的量。因此,废水中的还原性无机物质应视为非目标物,基于污染的定义加以针对性讨论。在使用重铬酸钾法测试COD时,无机还原性物质如亚铁盐、硫化物、亚硝酸盐、亚硫酸盐、硫代硫酸盐、氯离子等均不同程度被氧化,其需氧量也被加到COD中。这时,用COD来表征有机污染程度会出现较大的偏差。同时,COD是用氧化剂的氧化能力来代替水中生物分解有机物的能力,而在不同地区,不同水质中,有着不同的生物群落,对有机物的降解能力也不一样,因此会导致等量的COD值引起的污染程度的不同。根据以上讨论,COD的定义应当建立在对水体构成实质性污染成分的耗氧量,不应当包括氯离子、锰离子、过氧化氢分子之类在天然水体中不被氧分子所氧化的成分,使概念更趋向于需氧量的自然属性。有机物和还原性物质在水体中构成污染的真正原因是消耗溶解氧,以最终产物为CO2和H2O标志,称之为有机污染物;消耗溶解氧但不转化为CO2和H2O的起始物,称之为无机污染物。
3.3 二次污染
标准方法COD的测定需要使用800 W左右的加热器材对一个待测水样加热2h(含循环冷却),使用催化剂Ag2SO4-H2SO4溶液(每100mL浓H2SO4中含有 1g Ag2SO4)30mL,0.25mol/L K2Cr2O7溶液 10mL和0.4g的掩蔽剂HgSO4,硫酸亚铁铵溶液若干,少量的蒸馏水和指示剂,外加人工,根据经验,一个样品分析的成本价约为15元人民币。假设我国每天所有的检测机构测试水样COD的样品数约为25000个,以分析一个COD理论值是500 mg/L的标准物邻苯二甲酸氢钾水样为例,可以求得我国COD分析的各种药剂、能源与费用,如表3所示,其中不包含仪器设备损耗费用。根据药剂消耗的当量值计算并且参考2014年我国环境保护部公布的相关废水排放数据可知,每天COD的分析又相当于向水环境排放0.012t COD,相当于2014年每天全国废水COD排放总量的约1.5%。根据表3还可估算出我国检测机构每年消耗在 COD 分析的 K2Cr2O7、Ag2SO4、HgSO4和(NH4)2Fe(SO4)2的总质量分别约为6.75,2.73,3.65,16.88t,因此,COD分析废液的排放呈现出解决环境污染过程中新增了环境问题。此外,标准重铬酸钾法并不是一个自动化的测试过程,要求实验操作人员具备熟练的操作技巧才能保证测试结果的重现性。二次污染的存在暴露出了传统COD分析方法在实际应用中的局限性。
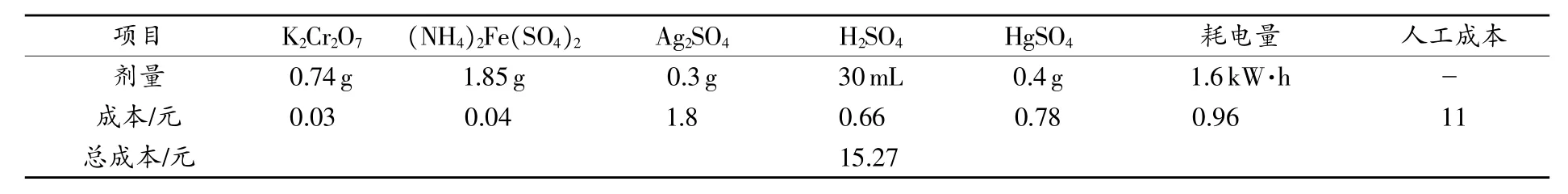
表3 测试单个理论COD值为500mg/L邻苯二甲酸氢钾标准溶液的成本
3.4 COD成分的毒性
COD分析作为频繁使用的传统指标之一,根据化学物质对人类的健康影响来制定,较少考虑对生态系统的影响,仅仅停留在宏观的阶段,虽然可以间接表征水中有机物的含量,但却不能反映水中具体物质组成和生物毒性。也就是说,COD值低,不能说明该浓度有机物的水质安全可用,以复杂、高毒性的焦化废水为例,即使COD达到了国家标准排放要求,外排水中仍然存在难降解的POPs,排放到环境中会存在潜在的环境风险,如Zhao和Wei等[18]研究中发现,已经达标的废水需要稀释8倍后才能达到天然水体的安全程度。因此,针对低COD值、毒性不明确的经过处理后的焦化废水尾水,或其他工业外排水,COD的行业排放限值需要结合环境毒理学原理,兼顾考虑生态风险水平和技术经济水平的共同目标。表4为工业废水中常见有机物的理论需氧量和半数致死量参数。
从表中可知,所列出有机物的ThOD在0~4mg/mg的范围内,其中ThOD最大的有机物是正己烷(3.53mg/mg),最小的是甲酰胺(0.35mg/mg)。值得注意的是,表中某些有机物之间的ThOD相近,假设它们都能被K2Cr2O7充分氧化,即这些有机物的化学需氧量值也应该相近,从化学层面来说,COD值相近的有机物的还原能力差别不大,进而误认为还原能力相似的有机物对水体的污染程度也相似,实际上,从毒理学参数的半数致死量(LD50)来看,虽然某些有机物的ThOD相近,但是LD50却有很大的差别。可见,水质安全保障还需要从毒理学方面来建立有机污染物的健康风险和生态风险评价体系。
随着废水中的污染物和衍生物种类增多,成分更趋于复杂,仅依靠COD来评价废水的污染程度已表现出明显的缺陷性,如能寻找到某种连接污染物浓度和毒性的归一化指标,将会对我国制定工业领域废水排放标准提供更趋于合理的参考依据。
4 工业废水COD测定技术
从COD方法原理可以看到,步骤多,流程长,耗能、耗药、耗材与耗时间,具有一定的劳动强度,这些,都是值得改进的地方。对此,实现流程的标准化、样品量的批次化、实时在线的高通量化以及全自动化(去人工化),成为由方法原理过渡到技术追求的发展方向。
4.1 微波消解技术及其改进
微波消解法的化学药剂体系和重铬酸钾法相似,其最大特点就是消解反应采用频率为2450MHz的电磁波能量来实现,在高频微波作用下,分子会产生摩擦运动,采用密封消解方式使消解罐压力迅速提高到203kPa,在高温高压条件下仅需要把样品消解15min,可同时消解12个样品,提高了COD的分析效率。Jardim等[19]最早开始微波消解测定COD的研究,他们采用硫酸-重铬酸钾消解体系,将样品与试剂加入聚四氟乙烯管中,消解后仍用硫酸亚铁铵对样品进行滴定,结果符合要求。然而,Del.Valle.M等[20]利用微波消解含邻苯二甲酸氢钾标准溶液的COD水样,观察到当消解时间大于5min时,得出的实验结果急剧上升并超过了标准溶液的理论值,指出随着微波消解时间的增加,导致重铬酸钾快速热分解。对实验条件优化后,与传统重铬酸钾法相比,将微波消解的时间缩短至5min得到的测试结果的重现率控制在91%~102%范围内。
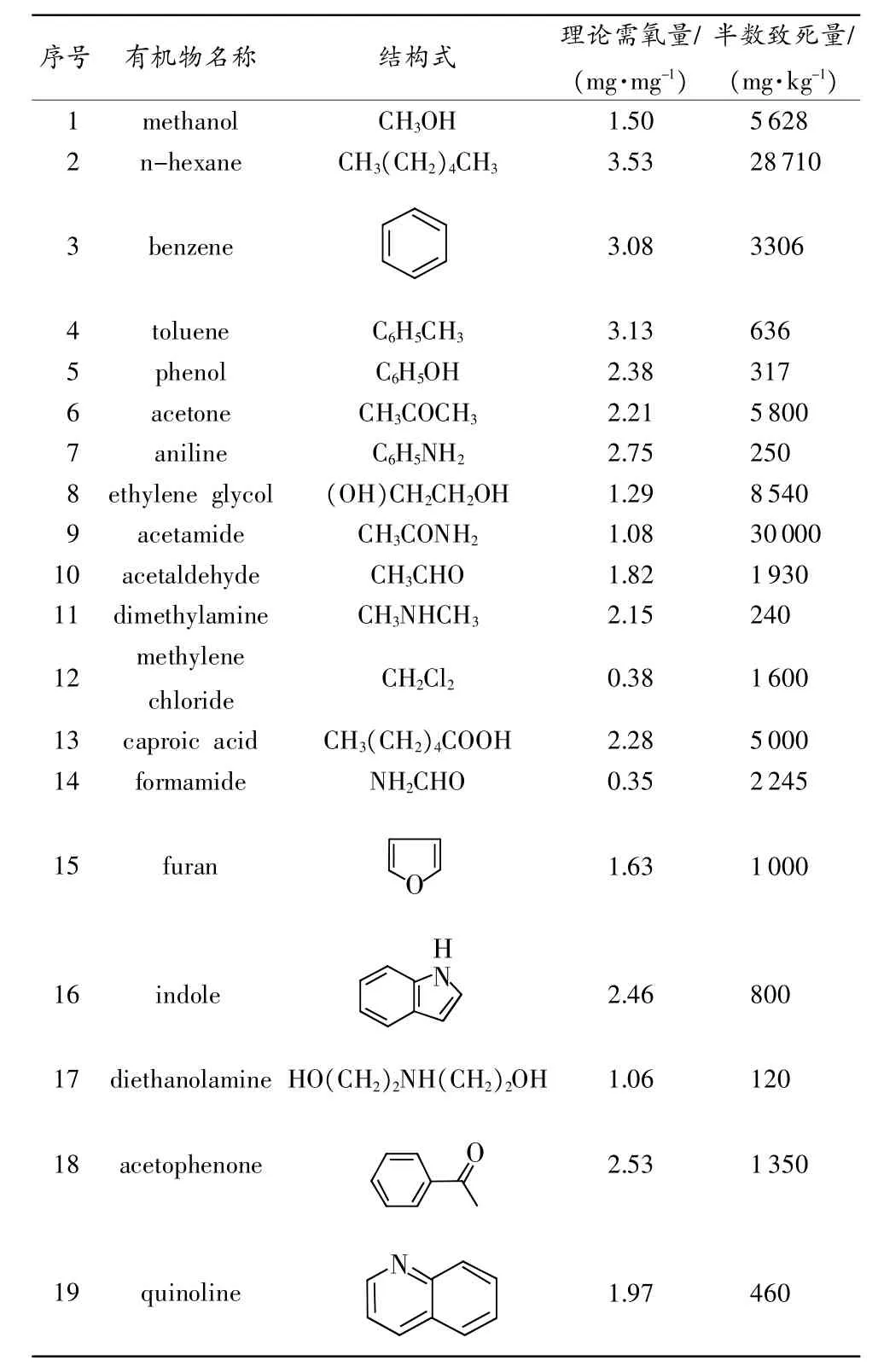
表4 工业中常见有机物的理论需氧量和半数致死量参数
目前改进的消解方法有:密封消解法、快速开管消解法、光催化消解法、微波消解法、声化学消解法等。Domini等[21]分别运用3种快速消解的COD测试方法(即密封消解法、快速开管消解法、超声消解法)对12种不同有机物的模拟废水及10个真实废水的样品进行测定,其测定结果与标准方法相符,且消解时间仅需约30min,从多方面提高了效率。
4.2 分光光度技术
试样中加入已知量的重铬酸钾标准溶液,在硫酸介质中,以Ag2SO4作为催化剂,HgSO4作为Cl-的掩蔽剂,经高温消解30 min后冷却,测定重铬酸钾中的六价铬[Cr(VI)]被还原产生的三价铬(Cr3+)在600nm[22]波长处的吸光度,而试样中COD值与三价铬(Cr3+)的吸光度增加值成正比例关系,将三价铬(Cr3+)的吸光度换算成试样的COD值。目前比较成熟的分光光度法测COD仪是美国哈希公司生产的DR/5000U分光光度计。
分光光度法适用于地表水、地下水、生活污水和工业废水中化学需氧量的测定。对未经稀释的水样,其COD测定下限为15mg/L,上限为1000mg/L,待测水样的Cl-浓度不应大于1000mg/L。对于化学需氧量大于1000mg/L或者Cl-含量大于1000mg/L的水样,可经适当稀释后进行测定。运用分光光度法测试水样COD时,Cl-仍然是主要的干扰成分,水样中含有Cl-会使测定结果偏高;此外,在酸性重铬酸钾条件下,一些芳香烃类有机物、吡啶等化合物难以被氧化,都会导致测定结果偏低。
4.3 库仑滴定技术
该技术的原理是水样以重铬酸钾为氧化剂,在10.2mol/L硫酸介质中回流15min,过量的重铬酸钾用电解产生的亚铁离子作为库仑滴定剂,进行库仑滴定,根据电解产生亚铁离子所消耗的电量,按照法拉第定律进行计算公式为

式中:Qs——标定重铬酸钾所消耗的电量,C;
Qm——测定过量重铬酸钾所消耗的电量,C;
V——水样的体积,mL。
标准方法中规定,当使用1mL,0.05mol/L重铬酸钾溶液进行测定时,最低COD检出浓度为2mg/L;当使用3mL,0.05mol/L重铬酸钾溶液进行标定值测定时,最低COD检出浓度为3 mg/L,其中测定上限为100mg/L。该技术适用于低COD值水样的测定,不需要其他标准物质进行对比,直接用电量进行定量测试,在一定程度上弥补了重铬酸钾法的不足。
5 工业废水中常见COD干扰组分的识别
探究水样中影响COD测定准确性的干扰组分和寻找如何降低或者消除干扰的方法,需从化学角度深入理解干扰组分作用的原理。判断一个化学反应自发进行的条件为吉布斯自由能变ΔrGm<0,又因为ΔrGm与电动势存在如下关系:

式中:z——反应中转移的电子数;
ΔE——原电池电动势。
当 ΔrGm<0 时,ΔE>0,氧化还原反应才能自发进行,又因为ΔE=E+-E-,如果两个电对的标准氧化还原电势的差值ΔE大于0.2V,就可以判断氧化反应进行的方向。以下列举5类工业废水中常见对COD分析造成干扰的组分及消除干扰的方法。
5.1 氯离子
Cl-对COD测试的干扰主要表现在两个方面:1)消耗催化剂Ag2SO4中一定量的Ag+,降低氧化剂的氧化效率,Ag+与Cl-反应生成AgCl白色沉淀会影响滴定终点的观测;2)从这两个半反应的标准电极电位(E0)来看:
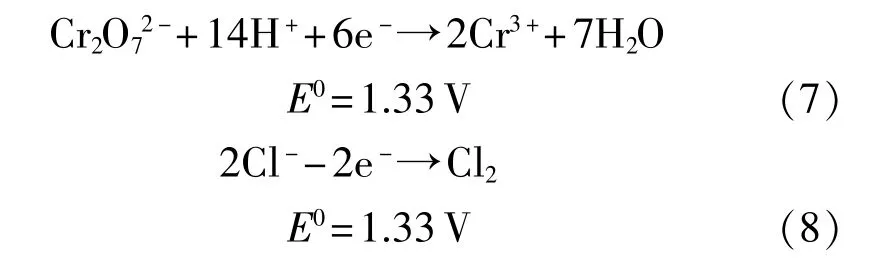
似乎Cl-应不被酸性重铬酸钾所氧化,但在CODCr的测定中,体系为强酸性介质,酸度大小直接影响K2Cr2O7氧化的条件电极电位,而酸度大小却与Cl-的条件电极电位无关。由前面所述可知,在测定CODCr时,体系中氧化剂的条件电极电位达1.55V,完全可使反应按以下方向进行:
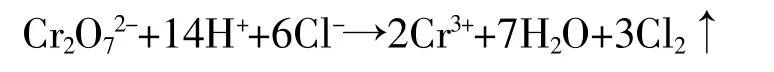
所以,K2Cr2O7在氧化有机物的同时也会氧化Cl-,从而影响COD测试的准确性。理论上,反应完全时1mg Cl-相当于 0.226mg COD。
对于高氯低COD值的工业废水,采用标准方法所测数据几乎不具有参考价值,长期以来广大环保工作者就如何消除Cl-的干扰进行了不懈的努力,先后提出了添加硫酸汞法[23]、标准曲线校正法[24]、吸收校正法[25]、密封消解法[26]、铋吸附剂除氯法[27]以及银盐沉淀法[28]等。
使用0.4 g硫酸汞络合氯离子的最高量可达40mg,如取用20mL水样,可以最高络合含2000mg/L氯离子浓度的水样,但为了保证准确性和减少误差,标准方法中规定,如果水样中氯离子浓度超过1000mg/L,必须先做定量稀释,才能进行测定。标准曲线校正法原理是通过检测水样中Cl-的浓度,从表观COD值中扣除Cl-对COD的贡献,即:而吸收校正法的原理是在消解时于体系中加入与标准方法相同的硫酸银作催化剂,以硫酸汞作掩蔽剂,加热结束后用充气泵吹出体系内滞留的氯气,然后用碘量法测定吹出的这部分氯气,从总COD中减掉这部分Cl2相当的COD值,两者的差值即为吸收校正法的COD值。
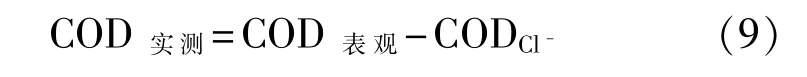
铋吸附剂除氯法是在COD测定消解前通过加入化学药剂使水样中的Cl-在酸性液中以HCl气体释放出来,然后被悬放在反应管中的铋吸附剂吸收而预先除去,以此来降低Cl-存在对测定结果的干扰。银盐沉淀法是对水样进行预处理,在消解前向水样中加入适量的硝酸银,然后取沉淀Cl-之后的上清液进行测定,加入硝酸银的量,应保证水样中的Cl-完全沉淀。
虽然上述消除氯离子干扰的方法都能起到掩蔽的效果,但是每一种方法仍存在一些缺点。其实,可以从另一角度思考,开发一种分离有机物和氯离子的吸附材料,分离后让氯离子留在待测水样中,通过测试有机物与氯离子未分离前的水样COD值减掉经过分离后仅含有氯离子的水样COD值,从而获得有机物的COD值。
5.2 溴离子
Br与Cl同属于第VII族,它们的离子具有相似的化学性质,如果某种工业废水中含有较高浓度的Br-时,则会影响重铬酸钾法分析COD的准确性。Br-不能通过加入硫酸汞来掩蔽,Belkin等[29]分别在不同浓度的邻苯二甲酸氢钾和葡萄糖标准溶液中加入一系列不同浓度的Br-,并加入不同量的硫酸汞验证Br-是否能被掩蔽,发现当Br-浓度一定时,有机物浓度越低,Br-对表观COD值的贡献越大;当有机物浓度一定时,Br-浓度越小,单位质量Br-对COD的贡献就越大;同时还验证了硫酸汞对Br-掩蔽的无效性。因此,在对含有Br-的工业废水进行COD分析时,还需要结合TOC分析技术来协同判断废水的有机物含量。此外,曹国民等[30]建议含溴废水中有机物的实际COD可通过表观COD与Br-对COD的贡献值之差进行估算,但是此方法的准确度还有待商榷。
5.3 过氧化氢
Fenton法是常用的废水处理高级氧化技术,用重铬酸钾法测定Fenton体系中的COD时,残余的H2O2与二价铁离子对结果产生正干扰。H2O2是一种氧化性物质,但遇到氧化性更强的物质如重铬酸钾时H2O2则充当还原剂的角色,使测定的COD值高于废水的实际值或者混淆滴定终点。H2O2与重铬酸钾的反应方程式为
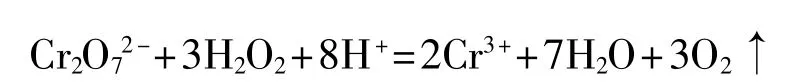
理论上,反应完全时1mg H2O2能引起0.471mg COD的变化。
使用二氧化锰作为催化剂加入含有H2O2的水样中催化分解H2O2,反应之后二氧化锰沉淀下来,既消除了H2O2对测试COD的干扰,也不会影响COD的测定,但二氧化锰催化H2O2所需时间长且操作复杂;此外,Kang等[31]通过建立H2O2浓度与COD关系的线性方程,用已经测得的COD结果扣除线性方程中相应浓度H2O2产生的对应COD值进而得到准确值来消除H2O2对COD测试的干扰,但在实际工业废水中常常含有多种有机物,H2O2还有可能与有机物或废水中其他成分发生复杂的化学反应,因此,有时利用COD-H2O2的线性关系来扣除H2O2的干扰不一定准确。
为了保证COD分析的客观性,当测试含有大量H2O2废水的COD时,建议同时采用几种消除干扰方法对同一水样进行平行分析,加以检验。
5.4 工业废水中其他常见还原性无机物
以化工行业为例,由于每一类化工工艺流程各异,导致排放废水的水质不同,复杂工业废水中含有多种影响COD分析准确性的还原性物质,曹臣等[32]以焦化废水生物处理出水中的组分为例,采用连续过滤分级方法对焦化废水生物处理出水进行物理组分分离,通过紫外可见光谱的变化和GC-MS定性分析各形态组分的有机组成特性,并运用化学分析手段考察还原性无机物的组成及含量,从而系统解析生物出水残余COD的构成特征,发现干扰COD分析的还原性物质除了 Cl-以外,还有 SCN-、CN-、Br-、I-、S2-、NH4+、NO2-、S2O32-、SO32-、Mn2+、Fe2+等。 而预测废水中某种还原性物质对COD分析的干扰程度,该物质的理论需氧量可作为一项初步的参考依据,表5列出了复杂工业废水中常见还原性物质的理论需氧量,图1同时列出了部分还原性物质的标准氢还原电位,根据这些物质的还原电位差异,可作为实现COD分质的理论参考依据。基于Cl-、NH4+准确的干扰去除方法仍然是个难题,需要结合生物技术的思考建立合理的校正方法。
5.5 悬浮物与胶体
天然水体以及废水中普遍含有悬浮物和胶体,如果待测水样中存在较多悬浮物,也会对COD的测定造成影响。悬浮物的COD主要由有机质贡献,如生物处理后出水中未分离完全的颗粒污泥中吸附的有机物和残留的菌胶团等,其贡献大小受泥水分离效果的影响,生物系统排泥不及时(SRT过长)或曝气量过大均可能增加悬浮物对COD的贡献。曹臣等[32]的研究工作中发现,生物出水中悬浮物和胶体成分分别占据COD值的25.9%~46.3%和18.7%~44.4%。

表5 工业废水中还原性物质的理论需氧量
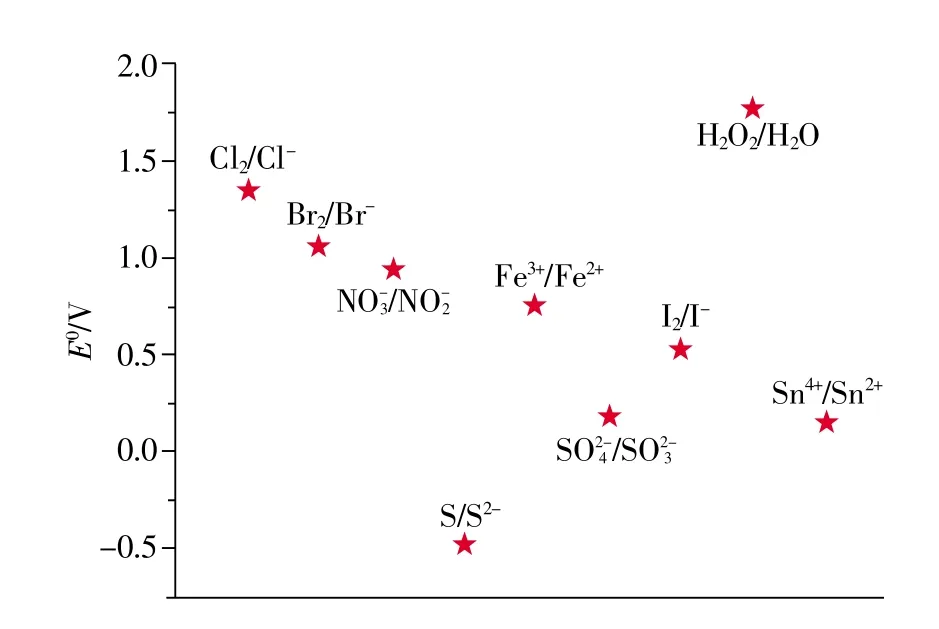
图1 工业废水常见还原性物质的标准氢电极电位
6 结束语
使用COD作为衡量水体有机物污染程度的指标已有将近90年的历史,其测定方法和评价标准已经形成了一套体系。但无论是国家标准还是其他优化的测试技术,都或多或少地使用了有毒的化学药剂,对环境造成二次污染。对此,未来COD测试的发展应致力于开发不使用有毒化学药品、消解时间短、效率高、无二次污染的新原理技术,如替代技术、原位技术、顶空技术、探针技术等,在瞬时性、灵敏性、高通量等方面取得突破。
解析COD构成与氧化还原电位的关系及影响COD分析准确性的干扰组分作用机理,力图找到废水对COD有贡献的物质的规律,提高废水COD分析的准确性,仍然是一件有意义的工作;COD背后隐藏着环境与经济的作用关系,利用不同氧化剂的氧化能力及GC-MS、离子色谱等辅助技术,对COD成分建立分质,如有机污染COD和无机污染COD,可以为水处理技术和水环境管理提供一种新的视角。
[1]SAWYER C N.Biological engineering in sewage treatment[J].Sewage Works Journal,1944,16(5):925-935.
[2]BARNETT J, DUPRÉ D J, HOLLOWAY B J, et al.Analogues of pantothenic acid.Part IV.Aryl derivatives of pantoyltaurine[J].Journal of the Chemical Society(Resumed),1944,24(8):94-96.
[3]ADENEY W E,DAWSON B B.The estimation of organic matter in water by means of potassium bichromate and sulphuric acid[J].Scientific Proceedings of the Royal Dublin Society,1926,18(1):199-202.
[4]MUERS M M.The biological purification of whey solutions[J].Journal of the Society of Chemical Industry,1936,55(3):71-72.
[5]MOORE W A, KRONER R C, RUCHHOFT C C.Dichromate reflux method for determination of oxygen consumed[J].Analytical Chemistry,1949,21(8):953-957.
[6]MOORE W A, LUDZACK F J, RUCHHOFT C C.Determination ofoxygen-consumed values of organic wastes[J].Analytical Chemistry,1951,23(9):1297-1300.
[7]DZYADZIO A M.The true oxygen consumption of sewage and a method for Its determination[J].Vodosnabzheniei Sanit Tekh(USSR),1938,9(3):117-120.
[8]DOBBS R A,WILLIAMS R T.Elimination of chloride interferencein thechemicaloxygen demand test[J].Analytical Chemistry,1963,35(8):1064-1067.
[9]魏复盛,毕彤,齐文启.水和废水检测分析方法[M].4版.北京:中国环境科学出版社,2002:211-213.
[10]沈叔平.水和废水监测分析方法指南(上册)[M].北京:中国环境科学出版社,1990:231-232.
[11]刘爱鹰.影响COD测定精度因素初探[J].当代化工,2006,35(4):295-298.
[12]SELVAPATHY P,STARLET J J.A new catalyst for COD determination[J].Indian Journal of Environmental Health,1991,33(1):96-102.
[13]SUN J H, XIA S Q, SUN R X.Rapid determination of wastewater COD using Mn(H2PO4)2as catalyst[J].Journal of Environmental Sciences,1996,8(2):212-217.
[14]RAMON R, VALERO F, DEL VALLE M.Rapid determination of chemical oxygen demand using a focused microwave heating system featuring temperature control[J].Analytica Chimica Acta,2003,491(1):99-109.
[15]DASGUPTA P K,PETERSEN K.Kinetic approach to the measurement of chemical oxygen demand with an automated micro batch analyzer[J].Analytical Chemistry,1990,62(4):395-402.
[16]沈澄英.掩蔽剂硫酸汞用量对水样中CODCr测定的影响[J].安徽化工,2014,40(6):96-98.
[17]李瑞祥,曾红梅,周向葛.无机化学[M].北京:化学工业出版社,2013:100-101.
[18]ZHAO J L, YAN B, WEI C H, et al.Multispecies acute toxicity evaluation of wastewaters from different treatment stages in a coking wastewater-treatment plant[J].Environmental Toxicology and Chemistry,2014,33(9):1967-1975.
[19]JARDIM W F,ROHWEDDER J J R.Chemical oxygen demand(COD) using micro-wave digestion[J]. Water Research,1989,23(8):1069-1071.
[20]DEL VALLE M, POCH M, ALONSO J, et al.Evaluation of microwave digestion for chemical oxygen demand determination[J].Environmental Technology,1990,11(12):1087-1092.
[21]DOMINI C E, HIDALGO M, MARKEN F, et al.Comparison of three opimized digestion methods for rapid determination of chemical oxygen demand:Closed microwaves,open microwaves and ultrasound irradiation[J].Analytica Chimica Acta,2006,561(1):210-217.
[22]NAKAMURA H, KOBAYASHI S, HIRATA Y, et al.A spectrophotometric biochemical oxygen demand determination method using 2,6-dichlorophenolindophenol as the redox color indicator and the eukaryote Saccharomyces cerevisiae[J].Analytical Biochemistry,2007,369(2):168-174.
[23]VYRIDES I,STUCKEY D C.A modified method for the determination of chemical oxygen demand(COD) for samples with high salinity and low organics[J].Bioresource Technology,2009,100(2):979-982.
[24]王方园,盛贻林,郑绍成.高浓度氯离子化工废水中COD测定方法比较[J].工业水处理,2006,26(5):72-74.
[25]黄荣富,周觅,俞建军,等.高氯低COD废水COD测定方法研究[J].精细化工中间体,2014,44(1):61-63.
[26]叶晓新,郭利群.COD测定中氯离子干扰消除方法的探讨[J].环境科学导刊,2011,30(5):95-97.
[27]VAIDYA B, WATSON S W, COLDIRON S J, et al.Reduction of chloride ion interference in chemical oxygen demand(COD) determinations using bismuth-based adsorbents[J].Analytica Chimica Acta, 1997,357(1):167-175.
[28]郭劲松,林佳琪,方芳,等.屏蔽氯离子干扰高盐榨菜废水中 COD的测定方法[J].重庆大学学报,2014,6(1):147-153.
[29]BELKIN S, BRENNER A, ABELIOVICH A.Effect of inorganic constituents on chemical oxygen demand-I.Bromides are unneutralizable by mercuric sulfate complexation[J].Water Research,1992,26(12):1577-1581.
[30]曹国民,盛梅,钟晨,等.工业废水中溴离子对COD测定的影响[J].中国给水排水,2007,23(20):85-88.
[31]KANG Y W, CHO M J, HWANG K Y.Correction of hydrogen peroxide interference on standard chemical oxygen demand test[J].Water Research,1999,33(5):1247-1251.
[32]曹臣,韦朝海,杨清玉,等.废水处理生物出水中COD构成的解析-以焦化废水为例 [J].环境化学,2012,31(10):1494-1501.
(编辑:李刚)
Analysis of the development of the industrial wastewater CODCrdetermination method and technology
WEI Cong1,2, LI Lei1, LÜ Wenying1, LIU Guoguang1, WU Haizhen3, WEI Chaohai2
(1.School of Environment Science and Engineering,Guangdong University of Technology,Guangzhou 510006,China;2.School of Environment and Energy,South China University of Technology,Guangzhou 510006,China;3.School of Bioscience and Bioengineering,South China University of Technology,Guangzhou 510006,China)
Chemical oxygen demand (COD) as an important indicator of water quality has been widely used for characterizing the pollution extent of sewage or wastewater.By tracking the history of COD analysis and taking the commonly-used potassium dichromate approach as an example,here the authors carry out a thorough review on(i) the principle of COD detection method, the key factors and the scope of its application; and (ii) the important issues related to the traditional method including the selection of oxidants, the scientific meaning of definition, the second pollution, the toxic components and the interferential components.In addition, we discuss the developmentand currentstatus ofthe microwave digestion technology, spectrophotometrytechnology and Coulomb titration technology,and propose the view of standardization and batch processing in order to improve the efficiency of COD determination.Lastly,we emphasize that the novelty, reliability, and timeliness of COD method/technology play significant roles in our country's industrial wastewater pollution control and water environment management.
chemical oxygen demand; potassium dichromate method; microwave digestion technology; analytical method; interferential components
A
:1674-5124(2017)07-0001-09
10.11857/j.issn.1674-5124.2017.07.001
2016-10-20;
:2016-12-15
国家自然科学基金重点项目(51278199);广东省应用型科技研发专项基金项目(2015B020235005)
韦 聪(1990-),男,广西河池市人,硕士研究生,专业方向为环境工程。
韦朝海(1962-),男,教授,博士,主要从事水污染控制理论与技术研究。
