吉非替尼一线治疗EGFR突变型晚期肺腺癌的临床研究
2017-08-07孙海凤郭亚焕
薛 静,孙海凤,吴 涛,郭亚焕,赵 征
(1西安交通大学第一附属医院呼吸与危重症医学科,西安 710061;2陕西省肿瘤医院内三科;*通讯作者,E-mail:xiaofeng2009ok@163.com)
吉非替尼一线治疗EGFR突变型晚期肺腺癌的临床研究
薛 静1,孙海凤2*,吴 涛2,郭亚焕2,赵 征2
(1西安交通大学第一附属医院呼吸与危重症医学科,西安 710061;2陕西省肿瘤医院内三科;*通讯作者,E-mail:xiaofeng2009ok@163.com)
目的 探索吉非替尼作为一线治疗对EGFR突变型晚期肺腺癌疗效、不良反应及预后的影响。 方法 收集陕西省肿瘤医院内三科和西安交通大学第一附属医院呼吸科经组织病理学证实的EGFR突变型晚期肺腺癌患者(Ⅲ/Ⅳ期)45例。二代测序检测EGFR阳性突变位点。评估吉非替尼作为一线治疗对EGFR突变型肺腺癌患者的疗效、生存期、不同突变类型生存差异及不良反应。 结果 45例患者CR 1例(2.2%),PD 2例(4.5%),PR 27例(60%),SD 15例(33.3%),疾病控制率(DCR)为95.5%,客观缓解率(ORR)为62.3%。EGFR阳性突变L858R 26例,19del 19例,两组患者的PR、SD、DCR和ORR均无统计学意义,而L858R CR和PD比例均显著高于19del患者;对所有患者进行3年的随访,无进展生存期(PFS)为(11.5±4.2)月,总生存期(OS)为(21.7±5.4)月。19del患者无进展生存期(13.2月)及总生存期(27.6月)显著高于L858R无进展生存期(9.8月)及总生存期(20.4月)。多因素生存分析示吉非替尼一线治疗EGFR突变阳型晚期肺腺癌的无进展生存期及总生存期与分化程度、临床分期、年龄、性别和吸烟无关,与突变位点有关。 结论 吉非替尼一线治疗EGFR突变型有较高的DCR和ORR,同时EGFR不同突变类型可能影响吉非替尼一线治疗晚期肺腺癌PFS和OS。
EGFR突变; 吉非替尼; 肺腺癌; 回顾研究
肺癌是当今世界上发生率和死亡率均居首位的恶性肿瘤,且发病率逐年上升,其中非小细胞肺癌(non-small cell lung cancer,NSCLC)约占85%,多数确诊时已经晚期[1]。目前,含铂双药化疗方案仍为一线治疗晚期NSCLC的标准方案,但晚期NSCLC的中位生存期仅为8-10个月[2]。表皮生长因子酪氨酸激酶抑制剂(epidermal growth factor receptor tyrosine kinase inhibitor,EGFR-TKI)作为一种治疗NSCLC的分子靶向药物,具有高效低毒的优势,为NSCLC的治疗指出了新的方向。吉非替尼是首个被应用于临床的EGFR-TKI。EGFR-TKI是一种小分子药物,它通过与ATP竞争结合于细胞膜表皮生长因子受体的酪氨酸区域,阻止酪氨酸磷酸化,抑制细胞内一系列与肿瘤细胞的形成、增殖、凋亡相关的信号通路联级反应,从而抑制肿瘤细胞的增殖[3]。EGFR-TKIs在临床应用上仍面临很多问题,譬如EGFR突变的患者一线EGFR-TKIs治疗是否比含铂两药方案化疗获益更多[4-8]。为了使EGFR-TKIs在临床应用中发挥出最大的优势,本研究对吉非替尼作为一线治疗EGFR突变型的晚期肺腺癌的药物的药效做比较分析,以更好地指导EGFR-TKIs在临床中的应用。
1 资料与方法
1.1 研究对象
收集2013-01-01~2016-01-01于陕西省肿瘤医院内三科和西安交通大学第一附属医院呼吸科经组织病理学证实的门诊及住院EGFR突变型晚期肺腺癌患者(Ⅲ/Ⅳ期)。纳入研究的共45例,患者均一线口服吉非替尼,其中男性20 例,女性25例;患者年龄43-73岁,中位年龄(64.5±16.3)岁。
纳入标准:①经组织病理学诊断证实的晚期(Ⅲ/Ⅳ期)肺腺癌患者;②患者年龄介于20-75岁;③根据美国东部肿瘤协作组制定的体力评分情况(performance status)PS[9](performance status,体能状态)评分≤2分的患者;④所有患者治疗前均采用NGS(Next-Generation Sequencing,二代测序技术)检测组织标本的EGFR基因检测;⑤至少有一个可测量病灶,根据实体瘤的疗效评价(response evaluation criteria in solid tumors,RECIST)1.1[10]定义的可测量病灶为靶病灶;⑥回访无进展生存期≥6个月;⑦治疗期间未采用其他抗肿瘤治疗。
排除标准:①合并其他部位肿瘤者;②肺纤维化、接受过大面积放疗和肺功能严重受损的患者;③临床资料不完整;④回访信息不全的患者。
1.2 治疗方法
组织病理学证实为肺腺癌的患者,均通过天津诺禾医学检验所的NGS肺癌9基因pannel检测组织标本的EGFR突变状态。对于EGFR敏感突变的患者一线EGFR-TKI,本研究中患者均给予吉非替尼250 mg/d,连续服用直至疾病爆发进展或不能耐受毒副作用为止。
1.3 疗效评价
患者口服吉非替尼3个月后进行疗效评价,按照RECIST1.1评价标准:完全缓解(complete response,CR)、部分缓解(partial response,PR)、稳定(stable disease,SD)、进展(progression disease,PD)。客观缓解率(objective response rate,ORR)包括CR和PR。疾病控制率(disease control rate,DCR)包括CR、PR 和SD。无病进展生存期(progression-free survival,PFS)为首次用药时间到疾病进展或任何原因引起死亡时间。按照WHO抗癌药物毒性表现及分级标准评价不良反应。随访:对纳入研究患者进行3年的随访,采用电话或门诊方式随访,末次随访时间为2016年5月30日。
1.4 统计学分析
应用SPSS 22.0进行统计分析,计数资料采用例数和百分数表示,组间比较采用卡方检验。单因素采用Kaplan-Meier法对生存资料进行分析,多因素生存分析数据使用COX回归模型。以P<0.05为差异有统计学意义。
2 结果
2.1 患者的基本资料
纳入本研究共45例患者,均为一线口服吉非替尼者,其中男性20例,女性25例;患者年龄43-73岁,中位年龄(64.5±16.3)岁;Ⅲa患者16例,Ⅲb期患者14例,Ⅳ期患者15例,其中骨转移9例,脑转移4例,肾上腺转移2例;PS评分为0-1分29例,PS 2分16例。各临床特征不同分类间,差异均无统计学意义(见表1)。
表1 患者临床基本资料
Table 1 Clinical basic information of patients
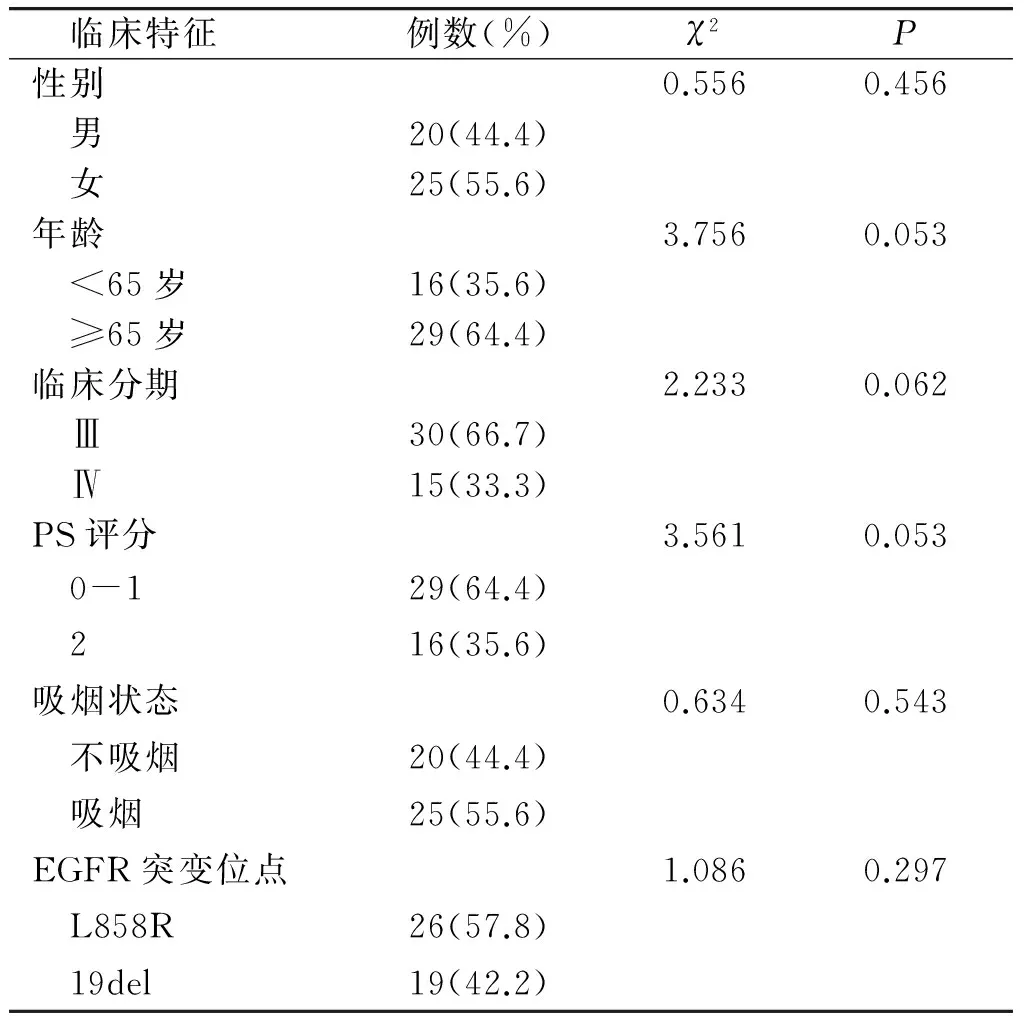
临床特征例数(%)χ2P性别0.5560.456 男20(44.4) 女25(55.6)年龄3.7560.053 <65岁16(35.6) ≥65岁29(64.4)临床分期2.2330.062 Ⅲ30(66.7) Ⅳ15(33.3)PS评分3.5610.053 0-129(64.4) 216(35.6)吸烟状态0.6340.543 不吸烟20(44.4) 吸烟25(55.6)EGFR突变位点1.0860.297 L858R26(57.8) 19del19(42.2)
2.2 吉非替尼一线治疗EGFR突变型的晚期肺腺癌的疗效评估
45例患者接受吉非替尼一线治疗,其中CR 1例(2.2%),PR 27例(60%),SD 15例(33.3%),PD 2例(4.5%),DCR为95.5%,ORR为62.3%。并对不同EGFR突变位点的患者的疗效做统计学分析,其中存在L858R的患者26例,19del的患者19例,两组患者的PR、SD、DCR和ORR均无统计学意义,而L858RCR和PD比例均显著高于19del患者,差异具有统计学意义(P<0.05,见表2)。
表2 不同EGFR敏感突变型的晚期肺腺癌的近期疗效 例(%)
Table 2 Short-term efficacy of advanced lung adenocarcinoma patients with different EGFR-sensitive mutations cases(%)

组别nCRPRSDPDDCRORR L858R组261(3.5)*14(53.8)9(34.6)2(7.6)*24(92.4)15(57.3) 19del组190(0) 13(68.4)6(31.8)0(0) 19(100)13(68.4)
与19del组比较,*P<0.05
2.3 吉非替尼一线治疗不同EGFR突变类型的晚期肺腺癌3年生存期的比较
吉非替尼一线治疗不同EGFR突变类型的晚期肺腺癌总的无进展生存期为(11.5±4.2)个月,总的3年生存期为(21.7±5.4)个月。根据EGFR突变状态将患者分为两组,做3年生存期分析,发现存在L858R的肺腺癌患者在一线服用吉非替尼的PFS为9.8个月,而19del的这类患者PFS为13.2个月,19del的PFS显著高于L858R;19del 的肺腺癌患者OS为27.6个月,显著高于L858R的20.4个月,差异具有统计学意义(均P<0.05,见图1)。
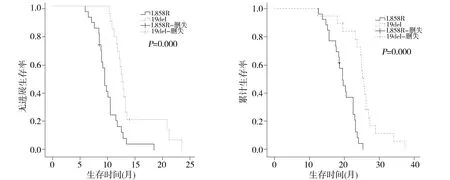
图1 不同EGFR突变类型的晚期肺腺癌3年生存期比较Figure 1 Comparison of 3-year survival of advanced lung adenocarcinoma patients with different EGFR mutation
2.4 吉非替尼一线治疗EGFR突变阳性的晚期肺腺癌多因素生存期分析
单因素分析EGFR突变类型可能会影响患者的预后,对患者的多个病理因素做生存分析数据的COX回归模型,吉非替尼一线治疗EGFR突变型晚期肺腺癌患者的PFS和OS,分别与分化程度、临床分期、年龄、性别及吸烟无关,突变位点可能影响吉非替尼一线治疗EGFR突变型晚期肺腺癌患者的PFS和OS(见表3,4)。
表3 吉非替尼一线治疗EGFR突变阳性的晚期肺腺癌PFS的COX回归模型
Table 3 COX regression model of gefitinib first-line treatment for PFS of EGFR-mutation-positive advanced lung adenocarcinoma
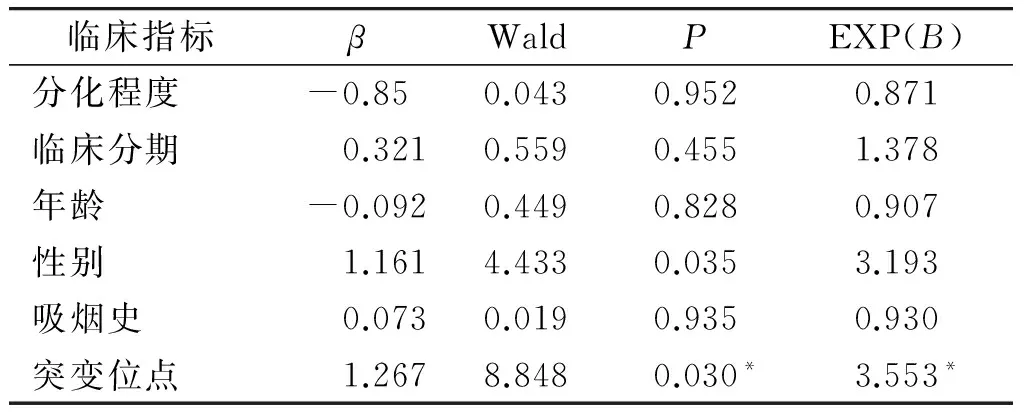
临床指标βWaldPEXP(B)分化程度-0.850.0430.9520.871临床分期0.3210.5590.4551.378年龄-0.0920.4490.8280.907性别1.1614.4330.0353.193吸烟史0.0730.0190.9350.930突变位点1.2678.8480.030*3.553*
*P<0.05
表4 吉非替尼一线治疗EGFR突变阳性的晚期肺腺癌OS的COX回归模型
Table 4 COX regression model of gefitinib first-line treatment for OS of EGFR mutant-positive advanced lung adenocarcinoma
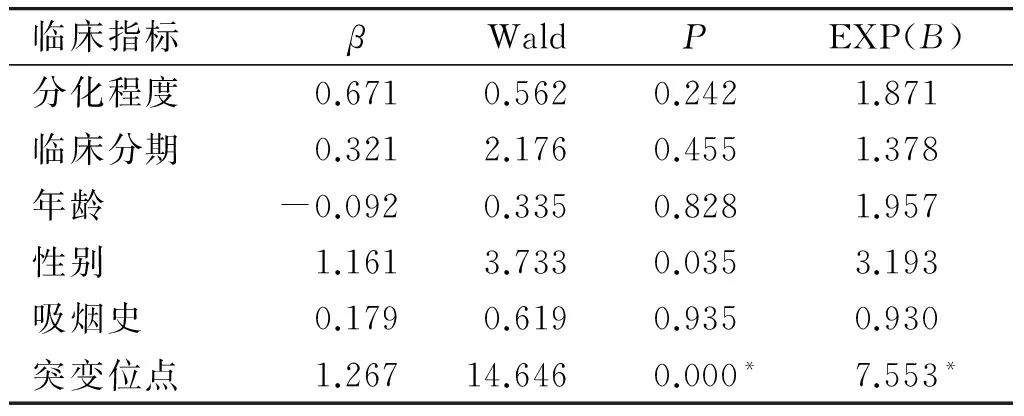
临床指标βWaldPEXP(B)分化程度0.6710.5620.2421.871临床分期0.3212.1760.4551.378年龄-0.0920.3350.8281.957性别1.1613.7330.0353.193吸烟史0.1790.6190.9350.930突变位点1.26714.6460.000*7.553*
*P<0.05
2.5 吉非替尼一线治疗EGFR突变型的晚期肺腺癌不良反应
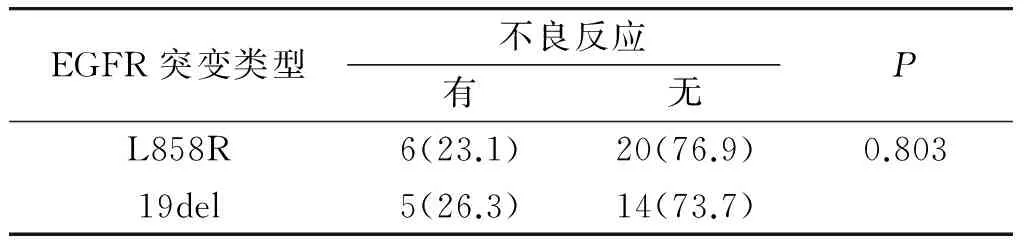
45例患者一线服用吉非替尼的总不良反应率为24.4%(11/45),其中皮疹(13.3%)较多,所有不良反应均为轻微级别,L858R和19del两组间不良反应无显著差异(见表5)。
表5 吉非替尼一线治疗EGFR突变型的晚期肺腺癌不良反应 例(%)
Table 5 Adverse reactions of gefitinib in treatment of advanced lung adenocarcinoma patients with EGFR mutation cases(%)
EGFR突变类型不良反应有无PL858R6(23.1)20(76.9)0.80319del5(26.3)14(73.7)
3 讨论
近年来,肺癌化疗的疗效并未取得突破性进展,而EGFR-TKI使晚期NSCLC患者生存期显著延长[5]。近10余年来,EGFR-TKI的研究已经取得了很多里程碑意义的结果。多项大型的国际多中心临床研究[11-13]均已证实:对于EGFR敏感突变的晚期NSCLC患者,EGFR-TKI治疗的PFS及ORR均优于传统细胞毒药物的化疗。随后几项大型研究[14-17]均通过EGFR-TKI一线治疗对比化疗,证实了其一线治疗在EGFR突变患者中的疗效。
本研究对纳入的45例EGFR突变的晚期肺腺癌患者,使用吉非替尼一线治疗疗效进行分析,结果显示,CR 1例(2.2%),PR 27例(60.0%),SD 15例(33.3%),PD 2例(4.5%),DCR为95.5%,ORR为62.3%。对纳入研究患者进行3年的随访,吉非替尼一线治疗不同EGFR突变类型的晚期肺腺癌总的无进展生存期为(11.5±4.2)个月,总的3年生存期为(21.7±5.4)个月。值得关注的是,发现存在L858R的肺腺癌患者在一线服用吉非替尼的PFS为9.8个月,而19del的这类患者PFS为13.2个月,19del 的PFS显著高于L858R;19del 的肺腺癌患者OS为27.6个月,显著高于L858R的20.4个月。
外显子19缺失突变和外显子21 L858R突变是EGFR的两种主要突变型。LUX-Lung 3研究的亚组分析[12]提示二代EGFR-TKI治疗EGFR敏感突变患者,中位PFS及中位OS在EGFR 19外显子缺失突变患者中较化疗组显著延长,而在EGFR 21错义突变患者中虽然有相对延长但无统计学差异。也有研究证实在一代EGFR-TKI吉非替尼与厄洛替尼治疗EGFR敏感突变患者中显示,19号外显子缺失患者的PFS比21号外显子L858R错义突变型患者的相对长,但两组之间PFS无统计学差异(P=0.072)[12-16]。柳菁菁等[16]研究发现对于中国NSCLC患者,不同EGFR敏感突变患者一线接受EGFR-TKI治疗的疗效和预后并不相同,19del组患者的中位PFS明显优于其他敏感突变类型,但中位OS与L858R突变组相似。TRIBUTE研究亚组分析得到的结果也提示EGFR突变状态与疗效有关[18,19]。这与本文的研究结果相似,本组研究提示19del突变患者的PFS(13.2个月vs9.8个月)和OS(27.6个月vs20.4个月)均长于L858R错义突变患者,但不同于其他研究的是,两者OS在统计学上亦有显著差异,这可能与本研究样本量较少有关。目前,尚缺乏对靶向药物治疗EGFR不同敏感突变之间的疗效作头对头的临床研究,可能有待进一步的相关研究证实。
[1] Chen W,Zheng R,Baade PD,etal.Cancer statistics in China,2015[J].CA Cancer J Clin,2016,66(2):115-132.
[2] Zhou C,Wu YL,Chen G,etal.Erlotinib versus chemotherapy as first-line treatment for patients with advanced EGFR mutation-positive non-small-cell lung cancer(OPTIMAL,CTONG-0802):a multicentre,open-label,randomised,phase 3 study[J].Lancet Oncol,2011,12(8):735-742.
[3] Rosell R,Carcereny E,Gervais R,etal.Erlotinib versus standard chemotherapy as first-line treatment for European patients with advanced EGFR mutation-positive non-small-cell lung cancer(EURTAC):a multicentre,open-label,randomised phase 3 trial[J].Lancet Oncol,2012,13(3):239-246.
[4] Mayo C,Bertran-Alamillo J,Molina-Vila M,etal.Pharmacogenetics of EGFR in lung cancer:perspectives and clinical applications[J].Pharmacogenomics,2012,13(7):789-802.
[5] Wu YL,Zhou C,Hu CP,etal.Afatinib versus cisplatin plus gemcitabine for first-line treatment of Asian patients with advanced non-small-cell lung cancer harbouring EGFR mutations(LUX-Lung 6):an open-label,randomised phase 3 trial[J].Lancet Oncol,2014,15(2):213-222.
[6] Han JY,Park K,Kim SW,etal.First-SIGNAL:first-line single-agent iressa versus gemcitabine and cisplatin trial in never-smokers with adenocarcinoma of the lung[J].J Clin Oncol,2012,30(10):1122-1128.
[7] Sequist LV,Martins RG,Spigel D,etal.First-line gefitinib in patients with advanced non-small-cell lung cancer harboring somatic EGFR mutations[J].J Clin Oncol,2008,26(15):2442-2449.
[8] Yang CH,Yu CJ,Shih JY,etal.Specific EGFR mutations predict treatment outcome of stage IIIB/IV patients with chemotherapy-naive non-small-cell lung cancer receiving first-line gefitinib monotherapy[J].J Clin Oncol,2008,26(16):2745-2753.
[9] Luersen GF1,Wei W,Tamm EP,etal.Evaluation of magnetic resonance(MR)biomarkers for assessment of response with response evaluation criteria in solid tumors:comparison of the measurements of neuroendocrine tumor liver metastases(NETLM)with various mr sequences and at multiple phases of contrast administration[J].J Comput Assist Tomogr,2016,40(5):717-722.
[10] Kadokura M,Ishida Y,Tatsumi A,etal.Performance status and neutrophil-lymphocyte ratio are important prognostic factors in elderly patients with unresectable pancreatic cancer[J].J Gastrointest Oncol,2016,7(6):982-988.
[11] Asami K,Koizumi T,Hirai K,etal.Gefitinib as first-line treatment in elderly epidermal growth factor receptor-mutated patients with advanced lung adenocarcinoma:results of a Nagano Lung Cancer Research Group study[J].Clin Lung Cancer,2011,12(6):387-392.
[12] Kato T,Yoshioka H,Okamoto I,etal.Afatinib versus cisplatin plus pemetrexed in Japanese patients with advanced non-small cell lung cancer harboring activating EGFR mutations:Subgroup analysis of LUX-Lung 3[J].Cancer Sci,2015,106(9):1202-1211.
[13] Zhao HY1,Chen GY,Huang Y,etal.Erlotinib plus capecitabine as first-line treatment for older Chinese patients with advanced adenocarcinomaof the lung(C-TONG0807):an open-label,single arm,multicenter phase II study[J].Medicine(Baltimore),2015,94(2):e249。
[14] De Grève J,Van Meerbeeck J,Vansteenkiste JF,etal.prospective evaluation of first-line erlotinib in advanced non-small cell lung cancer(NSCLC)carrying an activating EGFR mutation:a multicenter academic phase II study in Caucasian patients(FIELT)[J].PLoS One,2016,11(3):e0147599.
[15] Boye M,Wang X,Srimuninnimit V,etal.First-line pemetrexed plus cisplatin followed by gefitinib maintenance therapy versus gefitinib monotherapy in East Asian never-smoker patients with locally advanced or metastatic nonsquamous non-small-cell lung cancer:quality of life results from a randomized phase III trial[J].Clin Lung Cancer,2016,17(2):150-160.
[16] 柳菁菁,张爽,吴春娇,等.中国不同表皮生长因子受体敏感突变类型非小细胞肺癌患者接受表皮生长因子受体酪氨酸激酶抑制剂一线治疗的临床疗效比较[J].临床药物治疗杂志,2016,38(3):211-217
[17] Lim SM,Cho BC,Kim SW,etal.A multicenter phase II study of sorafenib in combination with erlotinib in patients with advanced non-small cell lung cancer(KCSG-0806)[J].Lung Cancer,2016,93:1-8.
[18] Gridelli C,De Marinis F,Di Maio M,etal.Gefitinib as first-line treatment for patients with advanced non-small-cell lung cancer with activating epidermal growth factor receptor mutation:review of the evidence[J].Lung Cancer,2011,71(3):249-257.
[19] Ellis PM,Coakley N,Feld R,etal.Use of the epidermal growth factor receptor inhibitors gefitinib,erlotinib,afatinib,dacomitinib,and icotinib in the treatment of non-small-cell lung cancer:a systematic review[J].Curr Oncol,2015,22(3):e183-215.
Clinical study of gefitinib as first-line treatment for EGFR-mutant advanced lung adenocarcinoma
XUE Jing1,SUN Haifeng2*,WU Tao2,GUO Yahuan2,ZHAO Zheng2
(1DepartmentofRespiratoryandCriticalCareMedicine,FirstAffiliatedHospitalofXi’anJiaotongUniversity,Xi’an710061,China;2Department3ofMedicalOncology,TumorHospitalofShaanxiProvince;*Correspondingauthor,E-mail:xiaofeng2009ok@163.com)
ObjectiveTo explore the therapeutic effects,adverse reactions and prognostic significance of gefitinib as first-line drug in treatment of EGFR-mutantion advanced lung adenocarcinoma.MethodsForty-five patients with EGFR-mutant advanced lung adenocarcinoma(stage Ⅲ/Ⅳ)confirmed by histopathology from department of respiratory of the First Affiliated Hospital of Xi’an Jiaotong University and third department of medical oncology of Tumor Hospital of Shaanxi Province were recruited.The EGFR mutation was evaluated by next-generation sequencing.The therapeutic effects,adverse reactions and prognostic significance of gefitinib were recorded.ResultsAmong the included patients,there was one case of CR(2.2%),2 cases of PD(4.5%),27 cases of PR(60.0%),and 15 cases of SD(33.3%).The disease control rate(DCR)and objective response rate(ORR)was 95.5% and 62.3%,respectively.A total of 26 patients were found L858R EGFR mutation and 19 patients were 19del EGFR mutant.PR,SD,DCR and ORR showed no statistical significance between mutation patients and non-mutantation patients,while the CR and PD rates in L858 patients were significantly higher than that of 19del patients.After follow-up for 3 years,the progression-free survival(PFS)and overall survival(OS)of all enrolled patients were(21.7±5.4)months and(11.5±4.2)months,respectively.The PFS and OS of 19del EGFR-mutant patients were significantly higher than those of L858R patients.By multivariate analysis,tumor differentiation,clinical stage,age,sex,smoking were not correlated with PFS and OS,but EGFR mutant sites affected the prognosis.ConclusionPatients with EGFR-mutant advanced lung adenocarcinoma treated with gefitinib as first therapy have a higher DCR and ORR,and different EGFR mutation types may affect the PFS and OS of advanced lung adenocarcinoma patients treated with first-line treatment.
EGFR mutation; gefitinib; lung adenocarcinoma; respective study
薛静,女,1984-04生,硕士,住院医师,E-mail:orangeabc@163.com
2016-12-19
R734.2
A
1007-6611(2017)04-0352-05
10.13753/j.issn.1007-6611.2017.04.011
