由4-甲基-1,2,3-噻二唑-5-甲酸构筑的过渡金属配合物的合成、晶体结构及与DNA作用
2017-08-07严世承胡未极沈金杯赵国良
严世承 胡未极 沈金杯 赵国良*,,
由4-甲基-1,2,3-噻二唑-5-甲酸构筑的过渡金属配合物的合成、晶体结构及与DNA作用
严世承1胡未极2沈金杯2赵国良*,1,2
(1浙江师范大学行知学院,金华 321004)
(2浙江师范大学化学与生命科学学院,金华 321004)
以4-甲基-1,2,3-噻二唑-5-甲酸(C4H4N2O2S,HL)分别与硫酸钴(CoSO4·7H2O)、氯化铜(CuCl2·2H2O)、硝酸银(AgNO3)反应合成了3个配合物[Co(L)2(H2O)4]·2H2O(1)、[CuNa(L)3]n(2)和[AgL]n(3),用元素分析、红外光谱、热重分析进行表征,用单晶X射线衍射测定了产物的结构。配合物1属于三斜晶系,空间群P1,Co2+的配位数为6,形成一个略为拉长的CoN2O4八面体,与理想的正八面体非常接近。配合物2属于三斜晶系,空间群P1。Cu2+离子的配位数为4,构成变形的平面四边形结构,Na+离子的配位数为6,构成一个略微变形的八面体结构,最终形成三维网状结构。配合物3属于单斜晶系,空间群P21/c,银离子为三配位,构成变形的平面三角形构型,具有二维网状结构。用溴化乙锭荧光探针法测定了配体和配合物与DNA作用的荧光光谱。
2-甲基-1,2,3-噻二唑-5-甲酸;过渡金属配合物;晶体结构;DNA作用
配位聚合物花样繁多、结构新颖、性能优异,在磁性、荧光、非线性光学、吸附、催化、分离、主客体化学、生物化学和生物制药等诸多领域有着广泛的潜在应用,因而倍受国内外化学家和材料学家的关注和重视[1-4]。配位聚合物的结构和功能的体现主要依赖于中心金属离子和配体的调控,因此,人们可以根据自己的设计思想来合成具有各种各样结构和功能的配位聚合物。
噻唑及其衍生物是一类重要的含N、S原子的杂环化合物,具有广泛的生物活性,表现出良好的抗菌、抗病毒、抗肿瘤、除草和调节植物生长等多种生物活性,在人类和其他生物的新陈代谢等过程中起到了重要的调节作用。该杂环系统具有丰富的电子,可与金属离子配位,易形成氢键、芳香堆积、静电和疏水作用等多种非共价键相互作用。这种结构赋予了噻唑类化合物许多特殊的性能,在农业、医药、生命科学、材料等领域具有广泛的潜在应用[5-13]。钴和铜作为机体的必需微量元素具有重要的生理作用[14];银的生理活性也为人们所熟知。银离子的配位数可以从2到7,有很大的弹性,表现出丰富的几何构型[15-16],所以银配位聚合物也是超分子化学和配位化学研究的热点之一。本文报道了4-甲基-1,2,3-噻二唑-5-甲酸(HL)的钴、铜和银配合物,并对其进行了晶体结构分析;同时测定了配体和配合物与DNA的作用,以期为过渡金属离子与生物活性物质作用及相应配合物有关性质的后续研究提供相关信息。
1 实验部分
1.1 仪器与试剂
金属含量用重量法测定,碳、氢、氮含量用德国Elementar公司Vario ELⅢ型元素分析仪测定;单晶X射线衍射用德国Bruker公司APEXⅡCCD单晶衍射仪测定;美国Nicolet公司NEXUS 670型傅立叶变换红外光谱仪(FTIR),KBr压片,测定范围为400~4 000 cm-1;美国Perkin Elmer公司的LS-55型荧光光谱仪。
HL用赫德-莫里法[17]制备。硫酸钴、氯化铜、硝酸银、氢氧化钠、氨水等试剂均为市售分析纯试剂,用前未做进一步处理。小牛胸腺DNA为生化试剂。
1.2 配合物的合成
1.2.1 配合物[Co(L)2(H2O)4]·2H2O(1)的合成
称取0.288 g(2.0 mmol)HL溶于15 mL去离子水中,用0.5 mol·L-1氢氧化钠溶液调节溶液的pH值为6~7;另称取0.281 g(1.0 mmol)七水硫酸钴溶于10 mL去离子水中,将其逐滴加入上述溶液中,室温搅拌反应4 h。将少许不溶物过滤,粉红色滤液于室温下自然挥发,40 d后得到适合于单晶分析的块状粉色晶体,过滤、洗涤、干燥收集产品。产率:41% (以金属盐计)。对产物(C8H18CoN4O10S2,Mr=453.33)进行元素分析,实验值(%):C,21.10;H,3.89;N,12.27;Co,12.77。计算值(%):C,21.19;H,4.00;N,12.36;Co,13.00。IR(KBr,cm-1):3 435(w),1 590(vs),1 352(vs),1 283(m),1 203(m),1 026(m),851(m),787(s),651(w),579(w),489(w)。
1.2.2 配合物[CuNa(L)3]n(2)的合成
称取0.288 g(2.0 mmol)HL溶于15 mL去离子水中,用0.5 mol·L-1氢氧化钠溶液调节溶液的pH值为7~8,室温搅拌2 h,另称取0.170 g(1.0 mmol)氯化铜溶于5 mL去离子水中,将其逐滴加入上述溶液中,室温搅拌反应8 h。将不溶物过滤,蓝色滤液于室温下自然挥发,3 d后得到适合于单晶分析的块状蓝色晶体,过滤、洗涤、干燥收集产品。产率:41%(以氯化铜计)。对产物 (C12H9CuN6NaO6S3,M r= 515.96)进行元素含量测定,实验值(%):C,27.71;H,1.72;N,16.12;Cu,12.17。计算值 (%):C,27.93;H,1.76;N,16.29;Cu,12.32。IR(cm-1):1 632(vs),1 502(w),1 442(w),1 387(vs),1 283(m),1 203(m),1 021(m),849(m),782(s),498(w)。
1.2.3 配合物[AgL]n(3)的合成
称取0.170 g(1.0 mmol)AgNO3溶于5 mL去离子水中,不断搅拌下逐滴加入3 mol·L-1氨水,直到最初生成的沉淀刚好溶解为止。另称取0.144 g(1.0 mmol)HL并加入3 mol·L-1氨水10 mL使其溶解,然后将其逐渐滴入上述溶液中,室温搅拌1 h,得到无色透明溶液,将滤液置于暗处缓慢挥发溶剂,1个月后得到无色单晶,产率:57%(以硝酸银计)。对产物(C4H3N2O2SAg,Mr=251.01)进行元素含量测定,实验值(%):C,19.25;H,1.25;N,11.27;Ag,43.11。计算值(%):C,19.14;H,1.20;N,11.16;Ag,42.97。IR(cm-1):1 640(vs),1 499(w),1 435(w),1 381(vs),1 288(m),1 205(m),1 027(m),843(m),788(s),650(w),487(w)。
1.3 配合物与DNA作用的荧光光谱
将小牛胸腺DNA(ct-DNA)用0.1 mol·L-1的NaCl溶液配成200μg·mL-1(cDNA=3.72×10-4mol·L-1),经纯度测定A260/A280=1.8~2.0,符合实验测试要求,置于4℃温度下保存,在4 d之内使用;Tris-HCl缓冲溶液(5 mmol·L-1Tris-HCl/50 mmol·L-1NaCl)按常规方法配制,其中 Tris-HCl的浓度为 0.0l mol·L-1,pH= 7.40。
在10 mL比色管中加入1.0 mL 200μg·mL-1的DNA溶液、1.0 mL 200μg·mL-1EB溶液以及2.0 mL pH=7.40的Tris-HCl缓冲溶液,在室温下放置2 h。然后向混合溶液中依次加入不同量的浓度为5× 10-4mol·L-1化合物溶液,用Tris缓冲溶液定容,在4℃下反应4 h后,在美国Perkin Elmer公司的LS-55型荧光光谱仪上,激发波长λex=251 nm,扫描混合溶液在520~700 nm范围的荧光光谱。
1.4 晶体结构分析方法
选用大小适宜的配合物单晶,在德国Bruker SMART APEXⅡCCD单晶衍射仪上进行衍射实验。用Mo Kα射线(λ=0.071 073 nm)在设定的2θ范围内收集衍射数据。衍射数据用程序SADABS[18]进行经验吸收校正,晶体结构用SHELXS-97[19]程序由直接法解出,对所有非氢原子坐标及其各向异性温度因子用SHELXL-97程序[20]进行全矩阵最小二乘法修正至收敛。除水上的氢原子外,其余氢原子均为理论加氢,水上的氢原子通过差值 Fourier合成得到。主要晶体学数据列于表1,主要的键长和键角列于表2~4。
CCDC:1526276,1;1526277,2;1434529,3。

表1 配合物的晶体学数据Table 1 Crystallographic data for the complexes

表2 配合物1的主要键长(nm)和键角(°)Table 2 Selected bond lengths(nm)and bond angles(°)of complex 1

续表2

表3 配合物2的主要键长(nm)和键角(°)Table 3 Selected bond lengths(nm)and bond angles(°)of complex 2

表4 配合物3的主要键长(nm)和键角(°) Table 4 Selected bond lengths(nm)and bond angles(°)of complex 3
2 结果与讨论
2.1 配合物的晶体结构
2.1.1 配合物[Co(L)2(H2O)4]·2H2O(1)的晶体结构
图1为配合物的配位环境图,其晶体结构单元由1个4-甲基-1,2,3-噻二唑-5-甲酸根和2个配位水分子,1个游离水分子所组成,其它的部分可由晶体学上的倒反对称中心操作产生,整个化合物是电中性结构。每个Co都处于结晶学上的倒反中心,与2个4-甲基-1,2,3-噻二唑-5-甲酸根中噻二唑环上的2个N原子和4个配位水上的O原子配位,形成一个完美的CoN2O4八面体几何构型。来自配位水分子的4个O原子(O1W,O1WA,O2W,O2WA)处于八面体的赤道平面,键长范围为0.205 5(2)~0.206 2(2)nm,∠O1W-Co1-O2WA=∠O1WA-Co1-O2W= 89.88(8)°,∠O1W-Co1-O2W=∠O1WA-Co1-O2WA= 90.12(8)°,4个键角之和等于360°,可见这4个O原子与金属Co原子共平面并构成了一个平行四边形;同时,轴向位置被2个噻二唑环上的N原子占据(dCo1-N1=dCo1-N1A=0.218 1(2)nm),∠O1W-Co1-O1WA=∠O2W-Co1-O2WA=∠N1-Co1-N1A=180.0°,说明O1W,Co1,O1WA;O2W,Co1,O2WA;N1,Co1,N1A各组内 3个原子分别处于同一条直线上。因此,CoN2O4配位多面体是个略为拉长的八面体,与理想的正八面体非常接近,也与文献报道的相似配体钴配合物的基本情况相近[21-24]。

图1 配合物1的配位环境图Fig.1 Coordination environment of complex 1
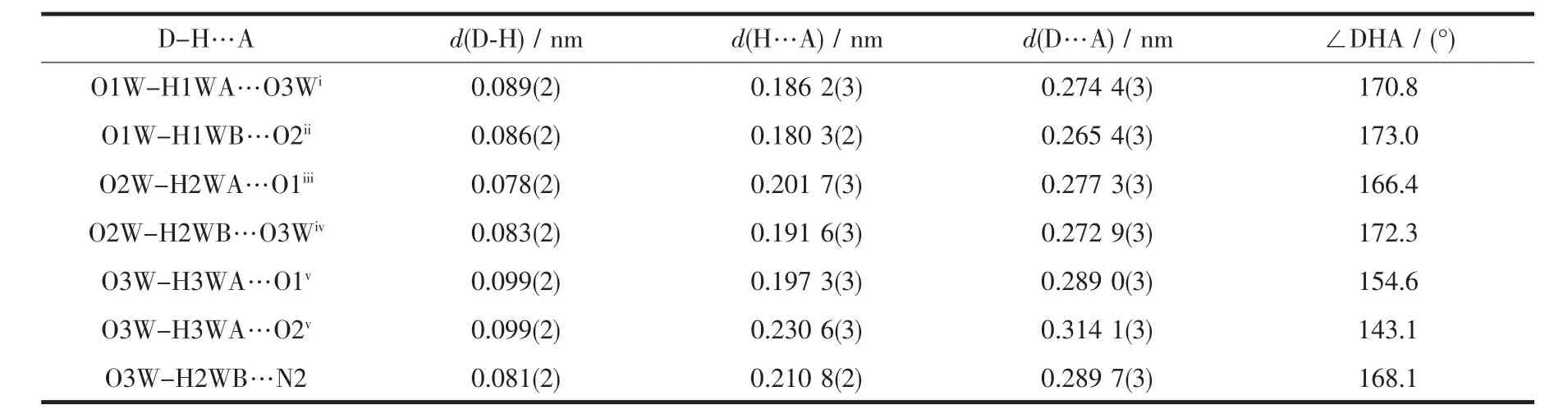
表5 配合物1中的氢键数据Table 5 Hydrogen bond geometry of complex 1
配合物是具有层状结构的三维超分子体系,如图2所示。在每一层结构中,通过羧基上的氧原子与配位水以O-H…O氢键(表5)将独立的结构单元与周围4个结构单元相连,形成类似等号形状的二维平面结构。其中,独立的结构单元中的配位水分子存在2种连接方式:处于对角关系的一对水分子分别与其周围的一个结构单元通过1个O-H…O氢键相连,而另一对水分子均与其周围的晶格水O3W和一个结构单元通过2个O-H…O氢键相连;晶格水O3W通过O-H…O,O-H…N氢键噻唑甲酸根上的2个氧原子和1个氮原子相连,从而得到了一个由O-H…O,O-H…N氢键连接起来的三维超分子体系。

图2 配合物1沿a轴方向的三维层状结构图Fig.2 Three dimensional layered structure of complex 1 viewed along a axis
2.1.2 配合物[CuNa(L)3]n(2)的晶体结构
[CuNa(L)3]n的最小不对称单元包括晶体学独立的 1个 Cu离子,1个 Na离子,3个 4-甲基-1,2,3-噻二唑-5-甲酸根配体。如图3所示,Cu2+离子处于四配位的环境中,由4个噻二唑甲酸根离子提供的3个氧原子(O2,O4,O6)和1个氮原子(N5)构成变形的平面四边形结构。Cu-O键长范围在0.191 7~0.194 2 nm,Cu-N键长为0.200 8 nm,与文献[25]报道的铜配合物接近,中心离子Cu偏离四边形平面0.007 2 nm。金属Na离子为八配位结构,与来自6个配体的3个羧基氧原子(O1,O3,O5)和3个氮原子(N2,N4,N6)配位形成一个略微变形的八面体构型。其中,O1,O3,O5和N6处于八面体的赤道位置,中心钠原子偏离赤道平面0.008 99 nm,N2,N4处于八面体的轴向位置,N2-Na1-N4的键角为173.61(1)°,接近于直线。Na-N键的距离为0.257 0(5)~0.261 5(5)nm,Na-O键的距离为0.227 5(4)~0.240 6(4)nm,键长略长于文献[26]报道的钠配合物的相应键长,明显短于另一文献[27]报道的有关键长。
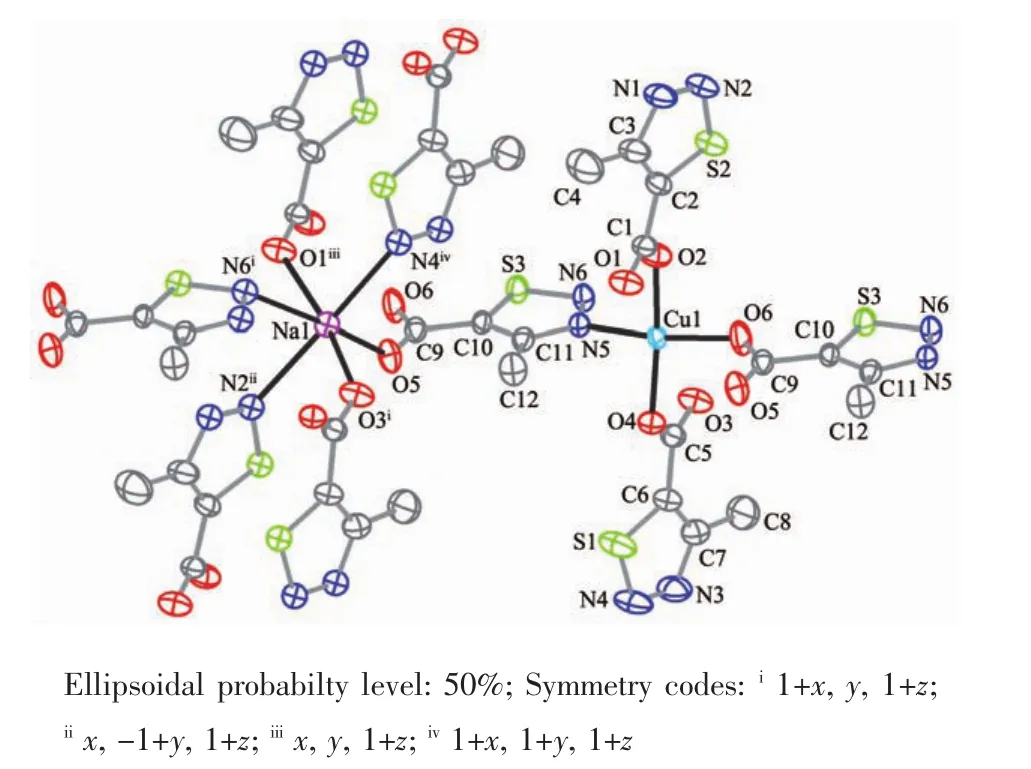
图3 配合物2的配位环境图Fig.3 Coordination environment of complex 2
在配合物2中,配体L-中的羧基都是去质子化的,并以2种不同的配位方式(图3)和金属Na、Cu离子配位:第一种方式是配体通过1个氮原子和羧基上的2个氧原子三齿桥连2个Na离子和1个Cu离子,该类配体间的夹角为4.712(2)°,几乎相互平行;第二种方式为配体通过2个氮原子和羧基上的2个氧原子四齿桥连2个Na离子和2个Cu离子,该类配体间的夹角为0°,与第一类配体之间的夹角为86.65(3)°,几乎相互垂直。Cu离子与相邻 2个 Na离子之间的距离分别为0.381 2(6)nm和0.399 5(7)nm。
另外,相邻噻二唑环间的距离为:0.348 49 nm,质心距离为:0.369 2 nm,存在着强的π-π堆积作用。配体通过2种首尾连接的配位方式连接相邻的金属Cu,Na离子,最终形成一个从a,b,c三个轴向看,如同“井”字形的二维层状结构(图4),孔道大小0.778 1 nm×0.833 4 nm。从拓扑角度分析,该配合物可以简化为一个双节点的(4,6)-连接的三维拓扑网络(图5)。
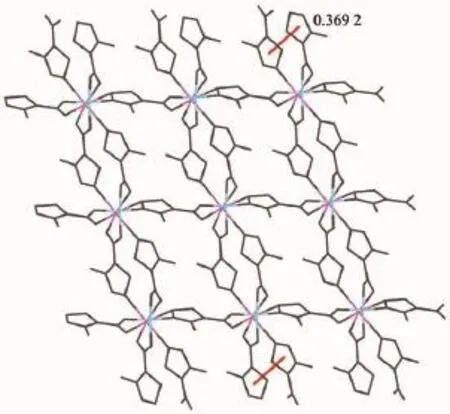
图4 配合物2的二维层状结构Fig.4 Two dimensional layer of complex 2
2.1.3 配合物[AgL]n(3)的晶体结构

图5 配合物2的三维拓扑网络Fig.5 Three dimensional topology network of complex 2
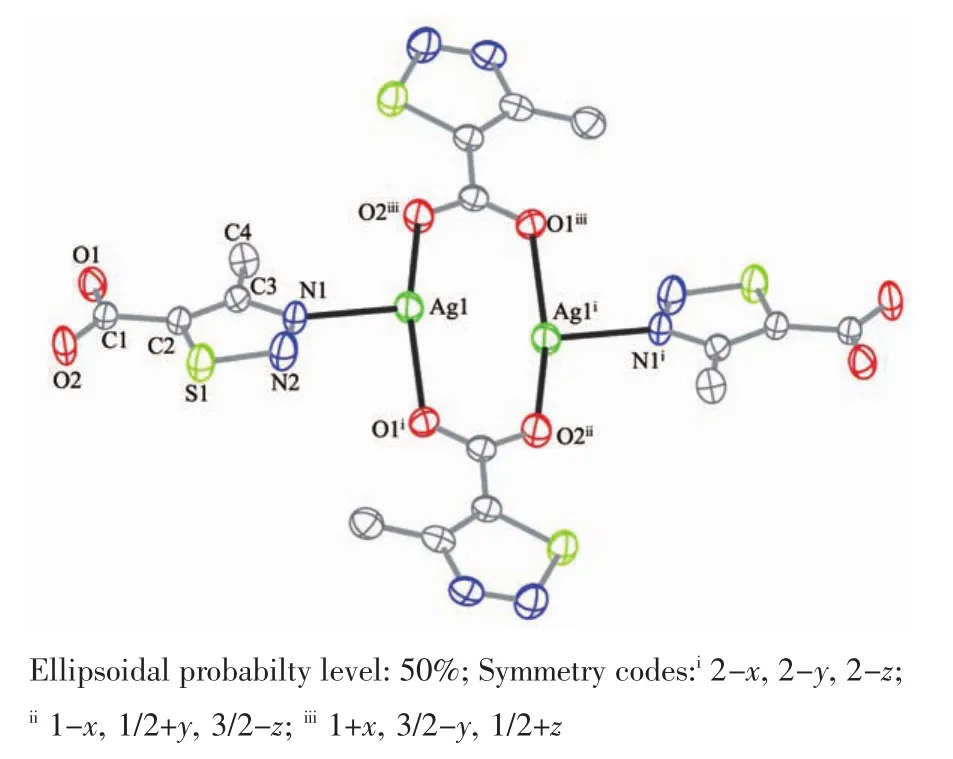
图6 配合物3的配位环境图Fig.6 Coordination environment of complex 3
配合物3属于单斜晶系,中心对称,P21/c空间群,具有二维网状结构,其最小不对称单元包括1个Ag离子,1个4-甲基-1,2,3-噻二唑-5-甲酸根离子(L-)。银离子为三配位,分别与来自3个噻二唑甲酸根离子中的1个氮原子和2个氧原子配位,构成变形的平面三角形构型(图6)。中心离子Ag偏离由N1、O2和O1所构成的平面三角形0.037 78 nm。Ag-O键长为0.224 3(3)~0.229 7(3)nm,Ag-N键长是0.237 4(3)nm,N-Ag-O、O-Ag-O的键角范围是89.35(7)°~150.15(11)°,与文献[28-30]报道的银配合物相近;相邻Ag…Ag间的距离为0.306 6(6)nm,未超过它们间的范德华力半径之和(0.344 nm),表明存在弱的金属键作用。
由于没有氢键给体,因此配合物中不存在典型的氢键,但是由于配合物存在较多的噻唑环,且相邻噻唑环所在平面的夹角为 0°,平均距离为0.343 0(3)nm,质心距为0.373 1(2)nm,所以噻唑环之间存在着较强的π-π堆积作用。在π-π堆积作用下,二维格子状层面结构形成了波形三维超分子结构(图8)。

图7 配合物3的4-连接的二维拓扑结构Fig.7 Four-connected 2D topology structure of complex 3
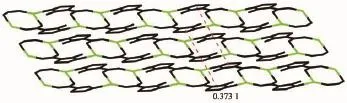
图8 配合物3的三维波形堆积图Fig.8 Three dimensional wave-like framework of complex 3
2.2 配合物的红外光谱
游离配体中羧基的伸缩振动出现在1 703 cm-1处,当形成配合物后此峰消失,分别出现了羧基的反对称伸缩振动νas(COO-)和对称伸缩振动νs(COO-)峰。配合物1中羧基的2个振动峰出现在1 582和1 352 cm-1处,与配体钠盐的振动峰相近,说明羧基并未参与配位;3 435和579 cm-1处的振动峰表明有水。配合物2中羧基的2个振动峰出现在1 632和1 442 cm-1处,说明羧基以单齿方式与中心金属离子配位。配合物3中羧基的振动峰出现在1 640和1 499 cm-1处,说明羧基以双齿桥式与中心金属离子配位[31]。这些均与单晶结构分析结果相吻合。
2.3 配合物的热重分析
图9为配合物的热重(TG)曲线,从图中可知:配合物1在72~160℃之间有1个大失重台阶,质量损失为23.62%,与理论值(23.72%)相吻合;从212℃之后配体逐渐氧化分解,至452℃左右基本分解完全,期间总的质量损失率为59.90%,理论失重59.83%,推断残余物可能是CoO,最终残留量为16.48%,(理论值:16.46%)。配合物2在239℃之前无任何失重,说明产物不含溶剂分子,这与单晶结构结果一致,之后配体逐渐氧化分解,至458℃左右基本分解完全,期间总的质量损失率为74.09%,理论失重74.31%,推断残余物可能是CuO+Na2CO3,最终残留量为25.91%,(理论值:25.69%)。配合物3在168℃之前也无任何失重,说明产物中也无溶剂分子,之后配体逐渐氧化分解,至545℃ 左右基本分解完全,期间总的质量损失率为55.90%,理论失重57.03%,推断残余物可能是Ag,最终残留量为44.10%,(理论值:42.97%)。
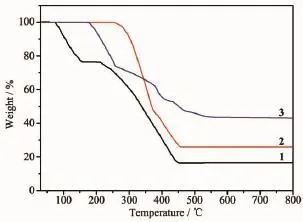
图9 配合物的热重曲线Fig.9 TG curves of the complexes
2.4 配体、配合物与DNA作用
图10是化合物(配体和配合物)与DNA浓度的比值 r分别为 0,0.13,0.27,0.40,0.54,0.67的情况下,化合物对EB-DNA复合体系的荧光猝灭图。由图可见,在590 nm处,EB-DNA体系能发出强烈的荧光,随着所加的化合物浓度的增加,EB-DNA复合体系的荧光发生了不同程度的猝灭。由此假设,在EB-DNA复合体系中,由于配体分子中的噻唑环的嵌入,使嵌入DNA中的部分EB由结合态变成自由态。根据实验数据,结合Stem-Volmer方程[32],算出这4个化合物与DNA作用的结合常数Ksq分别为0.24,0.43,0.31,0.13。Ksq的大小定量地反映了化合物与DNA插入作用的强弱。通过比较结合常数我们可以看出,配合物1和2的插入作用强于配体,而配合物3的作用不如配体。

图10 化合物对DNA-EB复合体系的荧光猝灭图Fig.10 Influence ofthe compounds on the fluorescence spectra of EB-DNA system
[1]SHI Pei(石沛),SHEN Wei(沈伟),YU Yu-Ye(余玉叶),et al. Chinese J.Inorg.Chem.(无机化学学报),2015,31(1):45-53
[2]Zhang X H,Qin J H,Ma L F,et al.Cryst.Growth Des., 2012,12(6):4649-4657
[3]Zhao J,Wang X L,Shi X,et al.Inorg.Chem.,2011,50(11): 3198-3205
[4]Ma Z B.Coord.Chem.Rev.,2011,255:1623-1641
[5]CUI Shen-Feng(崔胜峰),WANG Yan(王艳),LÜJin-Song(吕敬松),et al.Sci.Sin.Chim.(中国科学:化学),2012,42(8): 1105-1131
[6]LIU Yu-Ting(刘玉婷),YAN Hui-Xin(晏会新),YIN Da-Wei (尹大伟),et al.Fine Chem.Intermed.(精细化工中间体), 2009,39(1):8-12
[7]HU De-Yu(胡德禹),SONG Bao-An(宋宝安),HE Wei(何伟), et al.Chin.J.Synth.Chem.(合成化学),2006,14(4):319-328
[8]DAI Hong(戴红),LIU Jian-Bin(刘建兵),ZHANG Xin(张欣), et al.Chin.J.Org.Chem.(有机化学),2009,29(1):123-127
[9]Lubitz I,Zikich D,Kotlyar A.Biochemistry,2010,49(17): 3567-3574
[10]HUANG Guang(黄光),YANG Ji-Chun(杨吉春),LIHui-Chao (李慧超),et al.Agrochemicals(农药),2011,50(2):79-82
[11]Cui Y,Qian G,Chen L,et al.Dyes Pigm.,2008,77(1):217-222
[12]PuS Z,Li H,Liu G,et al.Tetrahedron Lett.,2010,51(27): 3575-3579
[13]Yamamoto T,Otsuka S I,Fukumoto H,et al.J.Polym.Sci. Part A,2011,49(6):1508-1512
[14]YANG Ke-Di(杨克敌),ZHANG Tian-Bao(张天宝),WANG Ai-Guo(王爱国),et al.Trace Elements and Health(微量元素与健康).Beijing:Science Press,2003:151
[15]Liang Z L,Mak T C W.Inorg.Chem.,2009,48(14):6480-6489
[16]Han L L,Zheng X Y,Chen J S,et al.Cryst.Growth Des., 2014,14(5):2230-2239
[17]Hurd C D,MoriR I.J.Am.Chem.Soc.,1955,77:5359-5364
[18]Scheldrick G M.SADABS,Program for Empirical Absorption Correction of Area Detector Data,University of Göttingen, Germany,1996.
[19]Sheldrick G M.SHELXS-97,Program for the Solution of Crystal Structure,University of Göttingen,Germany,1997.
[20]Sheldrick G M.SHELXL-97,Program for the Refinement of Crystal Structure,University of Göttingen,Germany,1997.
[21]CHEN Yan-Hui(陈艳辉),LI Chao-Zhu(李超柱),LI Jia-Ming (李家明).Chin.J.Synth.Chem.(合成化学),2010,18(3):328 -331
[22]Aakeroy C B,Despera J,Levin B,et al.Inorg.Chim.Acta, 2006,359(4):1255-1262
[23]Jia H B,Yu J H,Xu J Q,et al.J.Mol.Struct.,2002,641(1): 23-27
[24]Zou R Q,Cai L Z,Guo G C.J.Mol.Struct.,2005,737(2): 125-129
[25]HU Wei-Ji(胡未极),WU Da-Ling(武大令),SHEN Jin-Bei (沈金杯),et al.Chinese J.Inorg.Chem.(无机化学学报), 2016,32(8):1467-1475
[26]CHEN Yan-Min(陈延民),XIE Qing-Fan(解庆范).J.Synth. Cryst.(人工晶体学报),2013,42(11):2449-2454
[27]ZHAO Zeng-Bing(赵增兵),TAIXi-Shi(台夕市),CHEN Yuan -Tao(陈元涛).Chem.Reagents(化学试剂),2010,32(7):588-590
[28]HUANG Yon-Qing(黄永清),ZHOU Xia-Ying(周夏英), SHEN Zhong-Liang(沈忠良),et al.Acta Chim.Sinica(化学学报),2007,65(14):1381-1384
[29]WANG Ji-Jiang(王记江),HE Xiang-Yang(何向阳),CAO Pai-Xiang(曹培香),etal.Chinese J.Inorg.Chem.(无机化学学报),2012,28(4):829-832
[30]HAO Xiao-Min(郝晓敏),GU Chang-Sheng(谷长生),JI Li-Li (纪丽丽),et al.Chinese J.Inorg.Chem.(无机化学学报), 2015,31(5):1063-1070
[31]Nakamoto K,Translated by HUANG De-Ru(黄德如),WANG Ren-Qing(汪仁庆).Infrared and Raman Spectra of Inorganic and Coordination Compounds(无机和配位化合物的红外和拉曼光谱).Beijing:Chemistry Industry Press,1986.
[32]Lakowicz JR,Weber G.Biochemistry,1973,12(21):4161-4170
Syntheses,Crystal Structures and DNA Binding of Transition Metal Complexes Constructed by 4-Methyl-1,2,3-thiadiazol-5-carboxylic Acid
YAN Shi-Cheng1HU Wei-Ji2SHEN Jin-Bei2ZHAO Guo-Liang*,1,2
(1Xingzhi College,Zhejiang Normal University,Jinhua,Zhejiang 321004,China)
(2College of Chemistry and Life Science,Zhejiang Normal University,Jinhua,Zhejiang 321004,China)
Three transition metalcomplexes[Co(L)2(H2O)4]·2H2O(1),[CuNa(L)3]n(2)and[AgL]n(3)were synthesized from 4-methyl-1,2,3-thiadiazol-5-carboxylic acid(C4H4N2O2S,HL),CoSO4·7H2O,CuCl2·2H2O,and AgNO3.They were characterized by elemental analysis,infrared spectrum,thermogravimetricanalysis (TGA).The crystal structures of the complexes were confirmed by single X-ray diffraction method.Complex 1 crystallizes in triclinic system with space group P1,Co2+ion is six-coordinated to constitute a slightly deformation octahedral structure. Complex 2 crystallizes in triclinic system with space group P1.Cu2+ion is four-coordinated to form a quadrilateral plane structure deformation,and Na+ion is six-coordinated to constitute a slightly deformation octahedralstructure, eventually forming a three-dimensional network structure.Complex 3 crystallizes in monoclinic system with space group P21/c,and its coordination number is three,forming a deformation plane triangle configuration with 2D network structure.In addition,DNA-binding of the ligand and complexes was studied by EtBr fluorescent probe method.CCDC:1526276,1;1526277,2;1434529,3.
4-methyl-1,2,3-thiadiazol-5-carboxylic acid;transition metalcomplex;crystalstructure;DNA-binding
O614.81+2;O614.121;O614.122
A
1001-4861(2017)08-1381-09
10.11862/CJIC.2017.177
2017-01-20。收修改稿日期:2017-06-28。
浙江省公益性技术应用研究计划项目(No.2014C32014)资助。
*通信联系人。E-mail:sky53@zjnu.cn
