多系统萎缩患者24 h动态血压变化及影响因素
2017-07-25张映
张映
[摘要] 目的 研究多系统萎缩(MSA)患者动态血压变化的特点及其影响因素。 方法 选取我院2015年1月~2016年9月收治的20例MSA患者作为MSA组,选择同期健康体检者40例为对照组,采用无创性携带式动态血压监测仪分别进行24 h动态血压监测,对比两组动态血压及血压变异性指标;同时对MSA进行Hoehn-Yahr 严重程度分级(H-Y分级),探讨MSA患者病情严重程度与血压变异性的关系。 结果 MSA组动态血压中的夜间收缩压(nSBP)、夜间舒张压(nDBP)较对照组明显升高(P均<0.05);血压变异性中24 h收缩压标准差(24hSBPSD)、日间收缩压标准差(dSBPSD)和夜间收缩压标准差(nSBPSD)较对照组明显升高(P均<0.05),且MSA患者的H-Y分级与收缩压的血压变异性呈正相关(P<0.05)。 结论 MSA患者存在夜间血压升高现象,收缩压的血压变异性(SBPV)与MSA的严重程度相关。
[关键词] 多系统萎缩;动态血压;血压变异性;H-Y分级
[中图分类号] R741 [文献标识码] A [文章编号] 1673-9701(2017)18-0009-03
The change of twenty-four hour ambulatory blood pressure and the related factors in MSA
ZHANG Ying
Department of Neurology, Jinhua Municipal Central Hospital in Zhejiang Province, Jinhua 321000, China
[Abstract] Objective To investigate the ambulatory blood pressure profile in patients with multiple system atrophy (MSA) and its influencing factors. Methods A total of 20 cases with MSA in our hospital from January 2015 to September 2016 were selected as the MSA group, 40 cases of healthy person during the same period were selected as the control group. All subjects were tested respectively on 24 hours ambulatory blood pressure monitoring, blood pressure(BP)and blood pressure variability(BPV) indexes of the two groups were compared; The severity of MSA was assessed using Hoehn-Yahr stage(H-Y stage), the correlation between BPV and severity of MSA were explored. Results The nSBP、nDBP of BP in the MSA group were significantly higher than those in the control group(P<0.05); the 24hSBPSD, d SBPSD, nSBPSD of BPV in the MSA group were significantly higher than those in the control group(P<0.05); SBPV in MSA patients was positively correlation with H-Y stages (P<0.05). Conclusion MSA patients had a high prevalence of supine hypertension, the SBPV was correlated with the severity of MSA.
[Key words] Multiple system atrophy; 24 h ambulatory blood pressure monitoring; Blood pressure variability; H-Y stage
多系統萎缩(multiple system atrophy,MSA)是一种原因不明、成年后散发的进行性神经系统变性病,临床症状主要表现为对左旋多巴类药物不敏感帕金森综合征、小脑共济失调及自主神经功能障碍等[1,2]。其中自主神经功能障碍是MSA的重要特征,也是患者就医的常见原因。既往研究MSA的心血管自主神经功能检查[3-5]如直立倾斜试验、卧立位血压等均提示有显著异常。本研究通过动态血压监测观察MSA患者血压节律及变异性的特点,以评价MSA患者心脏自主神经功能衰竭情况,同时探讨血压变异性与病情严重程度的关系。
1 资料与方法
1.1一般资料
1.1.1 MSA组 选取2015年1月~2016 年9月在我院诊断的可能MSA患者20例,其中男12例,女 8例;年龄56~80岁,平均(68.14±8.29)岁;病程3个月~8年,平均(4.9±2.6)年;同时根据Hoehn-Yahr分级[1],将MSA组分为早期(H-Y 分级1.0~1.5级,8例)、中期(H-Y分级2.0~3.0级,6例)及晚期(H-Y 分级>3 级,6 例)三个亚组,其中8例口服美多巴治疗,5例因症状改善不明显自行停药。所有入选患者的诊断均符合Gilman S等[6]在2008年提出的可能MSA诊断标准:(1)30岁后起病,缓慢加重,出现帕金森病或小脑症状;(2)其他疾病不能解释的排尿异常,男性性功能勃起障碍,其中至少符合一项;(3)至少包括以下一项附加特征:可能的MSA-P型(左旋多巴不敏感、帕金森病症状加重、壳核代谢减少、MRI表现壳核萎缩、病理征阳性或腱反射亢进);可能的MSA-C型(小脑症状,MRI提示小脑、脑干萎缩,小脑代谢减少,病理征阳性或腱反射亢进)。排除其他严重神经系统疾病、精神疾病、严重的心、肝、脑、肾及内分泌、代谢、血液系统疾病。
1.1.2 对照组 选取同期健康体检者40例,其中男22例,女18例;年龄52~78岁,平均(67.80±7.64)岁;无高血压、糖尿病、冠心病、严重躯体疾病、精神疾病及其他引起自主神经功能障碍的疾病。
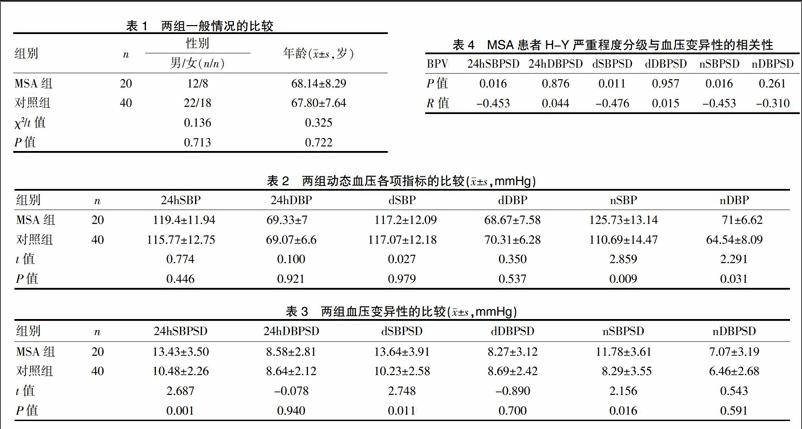
各组受试者的年龄、性别相匹配。见表1。
1.2方法
24 h動态血压监测:所有患者均采用无创动态血压监测仪(ABMP)记录24 h动态血压的变化。将测压袖带放置在左上臂,日间(6:00~22:00)每30 min测量1次,夜间(22:00~6:00)每60 min测量1次。受试者的日常活动不受限,24 h有效测量次数>80%。记录动态血压指标包括:24 h平均收缩压(24hSBP)、24 h平均舒张压(24hDBP)、日间平均收缩压(dSBP)、日间平均舒张压(dDBP)、夜间平均收缩压(nSBP)、夜间平均舒张压(nDBP)。同时测量各个时段血压的标准差作为血压的变异性:即24hSBPSD、24hDBPSD、dSBPSD、dDBPSD、nSBPSD、nDBPSD。
1.3 统计学方法
采用SPSS21.0统计软件进行统计学分析,计量资料用均数±标准差(x±s)表示,两组间均数比较采用t检验,方差齐性检验用Levene检验,用Spearman相关分析来评估动态血压与病情严重程度(H-Y分级)的相关性,P<0.05提示差异具有统计学意义。
2 结果
2.1两组动态血压各项指标的比较
两组动态血压中的nSBP、nDBP指标比较,差异均有统计学意义(P<0.05),而24hSBP、24hDBP、dSBP、dDBP指标比较,差异均无统计学意义(P均>0.05),见表2。
2.2两组血压变异性的比较
两组动态血压中的24hSBPSD、dSBPSD、nSBPSD的指标比较,差异均有统计学意义(P均<0.05),而24hDBPSD、dDBPSD、nDBPSD指标比较,差异均无统计学意义(P均>0.05)。见表3。
2.3 MSA患者H-Y严重程度分级与血压变异性的相关性
根据Spearman相关分析表明:血压变异性中的24hSBPSD、dSBPSD、nSBPSD与MSA的严重程度呈正相关,差异有统计学意义(P<0.05),而24hDBPSD、dDBPSD、nDBPSD与MSA的病情不相关,差异无统计学意义(P>0.05)。见表4。
3 讨论
MSA是一种罕见的神经变性病,好发年龄为54~62岁,男性发病率高于女性[7]。目前MSA分为2型,即以帕金森病症状为突出表现的MSA-P型及以小脑共济失调为突出表现的MSA-C型[8]。它们均伴有明显的自主神经功能障碍,且多在疾病的早期出现,其自主神经功能障碍表现为直立性低血压(75%)、尿便障碍(83%)[9]、男性勃起障碍(97%)[10、11]、睡眠结构改变[12]等。故有学者认为自主神经功能障碍是诊断MSA必备的特征。本研究通过动态血压监测MSA患者是否存在血压节律及异常血压变化,推测MSA患者自主神经功能障碍后的血压变化,同时探讨血压变异性与疾病严重程度的关系。
动态血压是动态监测一段时间内血压波动的情况,能较准确地反映血压的特点及昼夜节律变化,是评价心脏自主神经功能的重要方法。一般正常血压的波动呈双峰一谷的杓型[13],即清晨起床后血压开始上升,8、9点出现第一个高峰后下降,午后2、3点再次上升,至下午5、6点达第二个峰值后再次下降,凌晨2、3点达到底谷,且收缩压的波动大于舒张压,日间血压波动大于夜间;它受神经、体液及多种因素影响,而神经对血压的影响是通过自主神经的紧张反射完成的[14、15];当自主神经功能异常时,即出现血压节律改变及夜间高血压等改变[16,17]。MSA是一种节前交感神经元变性的疾病:主要累及脊髓中间外侧细胞核、迷走神经脊核及脑干网状结构[18,19],同时损伤骶髓2、3腹外侧前角细胞等[20],故MSA患者同时存在交感及副交感神经的损害。而本实验结果显示,与对照组相比,MSA患者的nSBP、nDBP较对照组明显升高(P<0.05),这与Schmit C[21]的实验结果相符,表明MSA患者存在血压昼夜节律改变及夜间血压偏高等自主神经功能损伤表现。
血压变异性反映个体一段时间内血压的波动程度,体现自主神经对心血管调节的动态平衡,一般用动态血压变化的标准差来表示。研究发现:血压变异性增大可能由于动脉压力感受器敏感性降低、失去调节血压的能力所导致的[22]。Vichayanrat E等[23]发现MSA患者收缩压的变异性较帕金森病组及对照组明显升高(P<0.01),而舒张压的变异性无明显差异(P>0.05);而本实验研究显示MSA患者血压变异性指标中24hSBPSD、nSBPSD、dSBPSD较对照组明显升高(P均<0.05),其余各项血压变异性指标与对照组比较,差异无统计学意义(P>0.05),证实MSA患者因自主神经功能损伤,失去有效调节血压的能力,且以对收缩压的调节能力下降为主。
一般情况下,血压变异性越大,疾病越严重,靶器官损伤也越明显。朱静等[24]发现MSA患者的心脏自主神经功能与疾病的病程、严重程度正相关。而本研究通过Spearman方法对血压变异性与疾病的严重程度进行相关性分析,发现MSA组的24hSBPSD、nSBPSD、dSBPSD与疾病的严重程度呈正相关,其余各项指标与疾病的严重程度不相关。表明MSA患者收缩压变异性的增高是提示病情加重的指标之一。
综上所述,MSA患者存在夜间血压升高现象,而收缩压的变异性与MSA患者病情的严重程度相关。但因血压变异性与神经内分泌因素、环境因素、对压力反射敏感性及自主神经的调节相关。它们之间的关系还有待进一步研究及证实。
[参考文献]
[1] 马凯,李勇杰.帕金森病改良Hoehn-Yahr分级的临床应用[J].首都医科大学学报,2002,23(3):260-261.
[2] Watanabe H,Riku Y,Nakamura T,et al. Expanding concept of clinical conditions and symptoms in multiple system atrophy[J]. Rinsho Shinkeigaku,2016,56(7):457-464.
[3] Brisinda D,Sorbo AR,Di Giacopo R,et al. Cardiovascular autonomic nervous system evaluation in Parkinson disease and multiple system atrophy[J]. Neurol Sci,2014, 336(1):197-202.
[4] Baschieri F,Calandra-Buonaura G,Doria A,et al. Cardiovascular autonomic testing performed with a new integrated instrumental approach is useful in differentiating MSA-P from PD at an early stage[J]. Parkinsonism Relat Disord,2015,21(5):477-482.
[5] Low PA,Reich SG,Jankovic J,et al. Natural history of multiple system atrophy in North America:A prospective cohort study[J]. Lancet Neurol,2015,14(7):710-719.
[6] Gilman S,Wenning GK,Low PA,et al. Second consensus statement on the diagnosis of multiple system atrophy [J].Neurology,2008,71(9):676-679.
[7] Schrag A,Wenning GK,Quinn,et al. Survival in multiple system atrophy[J]. Mov Disord,2008,23(2):294-296.
[8] Roncevic D,Palma JA,Martinez J,et al. Cerebellar and parkinsonian phenotypes in multiple system atrophy:Similarities,differences and survival[J]. Neural Transm 2014,121(5):507-512.
[9] Stefanova N,Bücke P,Duerr S,et al. Multiple system atrophy:An update[J]. Lancet Neurol,2009,8(12):1172-1178.
[10] Papasoris AG,Papapetropoulos S,Singer C,et al. Urinary and erectile dysfunction in multiple system atrophy(MSA)[J]. Neurourol Urodyn,2008,27(1):22-27.
[11] Jecmenica-Lukic M,Poewe W,Tolosa E,et al. Premotor signs and symptoms of multiple system atrophy[J]. Lancet Neurol,2012,11(4):361-368.
[12] 趙馨,张玉虎,冯淑君,等. 多系统萎缩患者的主客观睡眠障碍[J]. 中华神经科杂志,2016,49(4):294-298.
[13] 孙玉青,骆雷鸣. 血压节律改变与靶器官损害[J]. 中国循环心血管医学杂志,2015,7(3):429-430.
[14] 魏芳芳.自主神经功能对血压变异性的影响[D].中国医科大学,2012.
[15] Ishikawa J,Watanabe S,Harada K.Awakening blood pressure rise in a patient with spinal cord injury[J]. Am J Case Rep,2016,20(17):177-181.
[16] Biaggioni I.The pharmacology of autonomic failure:From hypotension to hypertension[J]. Pharmacol Rev,2017,69(1):53-62.
[17] Goldstein DS,Pechnik S,Holmes C,et al. Association between supine hypertension and orthostatic hypotension in autonomic failure[J]. Hypertensio,2003,42(2):136-142.
[18] Lodice V,Lipp V,Ahlskog JE,et al. Autopsy confirmed multiple system atrophy cases:Mayo experience and role of autonomic function tests[J]. Neurol Neurosurg Phychiatry,2012,83(4):453-459.
[19] Jellinger KA,Wenning GK. Multiple system atrophy:Pathogenic mechanisms and biomarkers[J].Neural Transm(Vienna),2016,123(6):555-572.
[20] Sakaribara R,Uchiyama T,Yamanishi T,et al. Sphincter EMG as a diagnostic tool in autonomic disorders[J]. Clin Auton Res,2009,19(1):20-31.
[21] Schmidt C,Herting B,Prieur S,et al. Autonomic dysfunction in different subtypes of multiple system atrophy[J].Mov Disord,2008,23(12):1766-1772.
[22] Roy S,Jaryal AK,Srivastava AK,et al.Cardiovagal baroreflex sensitivity in parkinsons disease and multiple system atrophy[J]. Clin Neurol,2016,12(2):218-223.
[23] Vichayanrat E,Low AD,Lodic V,et al. Twenty-four-hour ambulatory blood pressure and heart rate profiles in diagnosing orthostatic hypotension in Parkinson's disease and multiple system atrophy[J]. Eur J Neurol,2017,24(1):90-97.
[24] 朱静,李胜. 多系统萎缩自主神经功能障碍研究的新进展[J]. 临床神经病学杂志,2016,29(4):315-317.
(收稿日期:2017-02-15)
