UPLC-MS/MS法同时测定糖尿病模型大鼠血浆中沙格列汀及其代谢产物5-羟基沙格列汀浓度
2017-07-03倪善红汤道权肖冰心李艳丽孙增先徐州医科大学附属连云港医院连云港市第一人民医院药学部江苏连云港00徐州医科大学药物分析教研室江苏徐州004
倪善红,汤道权,董 洁,,肖冰心,刘 云,李艳丽,孙增先#(.徐州医科大学附属连云港医院/连云港市第一人民医院药学部,江苏连云港 00;.徐州医科大学药物分析教研室,江苏徐州 004)
UPLC-MS/MS法同时测定糖尿病模型大鼠血浆中沙格列汀及其代谢产物5-羟基沙格列汀浓度
倪善红1,2*,汤道权2,董 洁1,2,肖冰心1,刘 云1,李艳丽1,孙增先1#(1.徐州医科大学附属连云港医院/连云港市第一人民医院药学部,江苏连云港 222002;2.徐州医科大学药物分析教研室,江苏徐州 221004)
目的:建立同时测定糖尿病模型大鼠体内沙格列汀及其代谢产物5-羟基沙格列汀血药浓度的方法。方法:采用超高效液相色谱-串联质谱法。色谱柱为Waters BEH Shield RP18,流动相为10mmol/L乙酸铵-乙腈(70∶30,V/V),流速为0.3m L/m in,柱温为30,进样量为10μL;扫描模式为多反应监测,正离子模式,各离子对为m/z 316.2→180.2(沙格列汀)、m/z332.3→196.2(5-羟基沙格列汀)、m/z304.2→153.9(维格列汀,内标)。取6只SD大鼠,复制糖尿病模型后,ig沙格列汀0.53mg/kg,于给药前及给药后0.25、0.5、0.75、1.0、1.5、2.0、4.0、6.0、8.0、12.0、24.0 h经眼眶取血0.25m L,测定血浆中沙格列汀及其代谢物5-羟基沙格列汀的浓度,采用Win Nonlin 6.1软件计算药动学参数。结果:沙格列汀和5-羟基沙格列汀的质量浓度线性范围为0.1~100(r=0.997 2)、0.2~200 ng/m L(r=0.996 5),定量限分别为0.1、0.2 ng/m L,日内(n=5)、日间(n=3)RSD均小于12%,准确度为94.1%~105.4%、91.0%~103.6%,提取回收率分别为72.4%~87.3%、107.0%~115.3%(RSD均小于13.6%,n=6),基质效应分别为105.9%~107.8%、83.5%~88.2%(RSD均小于10.3%,n=6),稳定性的RSD≤11.0%(n=5);药动学参数cmax分别为(49.97±11.14)、(16.87±7.35)ng/m L,t1/2分别为(2.88±0.21)、(4.21±0.95)h,AUC0-24h分别为(90.95±7.06)、(49.13±5.33)ng·h/m L(n=6)。结论:本方法简便、准确、专属性强,适用于沙格列汀及其代谢物5-羟基沙格列汀在大鼠体内的药动学研究。
沙格列汀;5-羟基沙格列汀;血药浓度;药动学;大鼠;超高效液相色谱-串联质谱法

图1 二级碎片全扫描质谱图Fig 1 Full scanning production spectra of the secondary fragments
2.3 混合血浆样品和质控样品的制备
精密吸取沙格列汀及5-羟基沙格列汀标准工作液各10μL,加入空白血浆80μL,涡旋混匀30 s,制成含沙格列汀质量浓度为0.1、1、5、10、20、40、50、80、100 ng/m L及5-羟基沙格列汀质量浓度为0.2、2、10、20、40、80、100、160、200 ng/m L的系列混合血浆样品。
同法制备含沙格列汀低、中、高(0.4、25、75 ng/m L)及含5-羟基沙格列汀低、中、高(0.8、50、150 ng/m L)3个质量浓度的混合质控样品。
取100μL血浆样品于1.5m L离心管中,分别加入50 ng/m L内标溶液50μL、乙腈500μL,涡旋2min,以13 500 r/m in离心10m in;移取上清至1.5m L离心管中,室温下氮气吹干,残留物用200μL 10%甲醇复溶,涡旋1m in,以13 500 r/m in离心5min,取上清液10μL,进样测定。
2.5 专属性考察
分别取6只大鼠空白血浆样品(不加内标)、空白血浆加入沙格列汀和5-羟基沙格列汀、大鼠给药0.5 h后收集的血浆样品,均按“2.4”项下方法处理后,按“2.1”项下色谱条件进样分析。结果,沙格列汀、5-羟基沙格列汀及内标的保留时间分别为1.29、1.09、1.15m in;在保留时间0.74min处,发现内源性物质峰,但不干扰沙格列汀、5-羟基沙格列汀及内标的测定,为了尽量减少内源性物质对仪器的污染,0.8min之前的组分切到质谱外,色谱图见图2。
2.6 标准曲线与定量下限考察
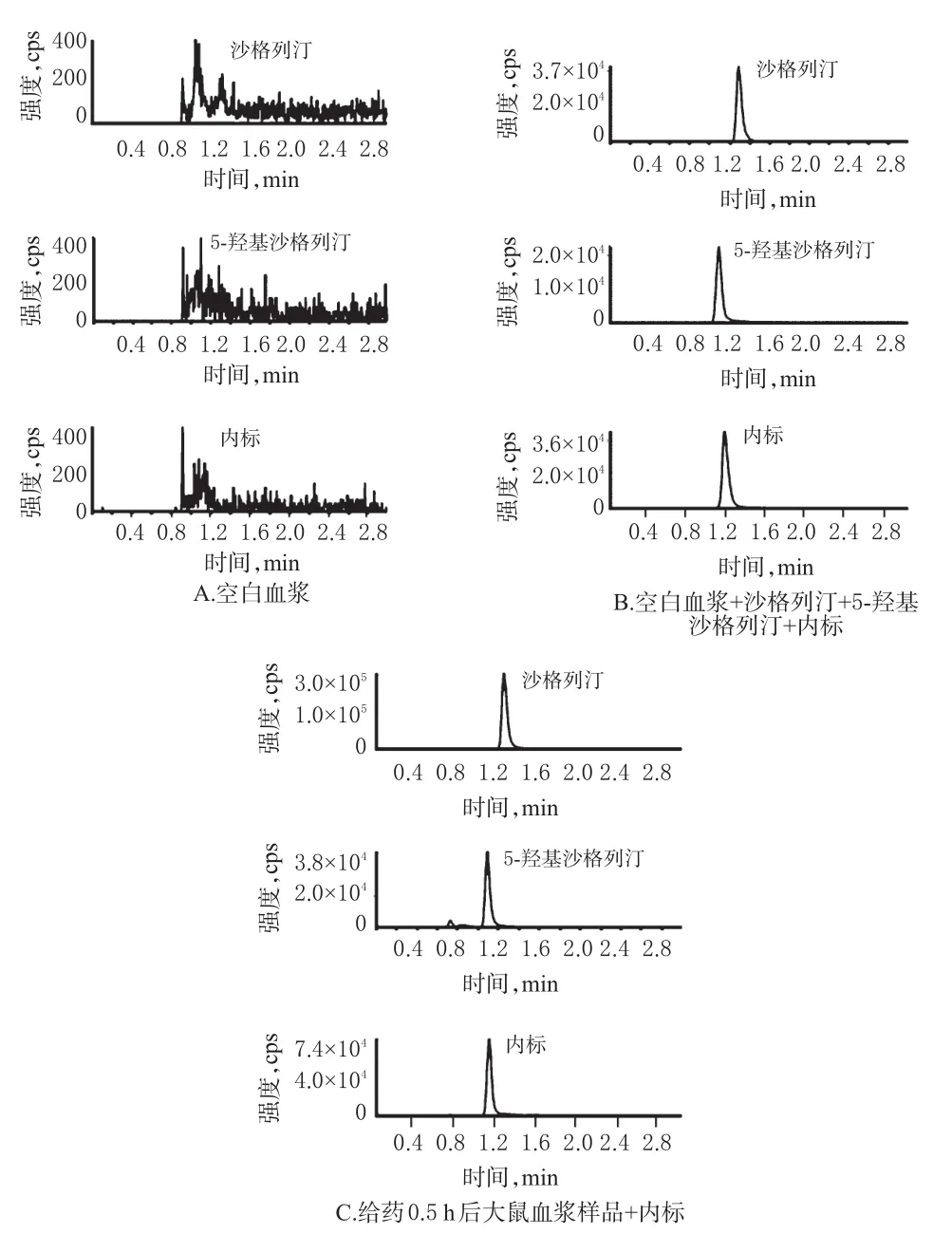
图2 超高效液相色谱图Fig 2 UPLC chromatogram s
取“2.3”项下系列混合血浆样品,按照“2.4”项下方法处理后,按“2.1”项下色谱条件进样测定,以待测物质量浓度(ng/m L)为横坐标(x)、待测物与内标的峰面积比值为纵坐标(y)进行线性回归。结果,沙格列汀、5-羟基沙格列汀的回归方程分别为y=4.7×10-3x-5.63×10-5(r=0.997 2)、y=1.06×10-3x+5.53×10-(7r=0.996 5),线性范围分别为0.1~100、0.2~200 ng/m L,定量下限分别为0.1、0.2 ng/m L。
2.7 精密度、准确度、提取回收率、基质效应与稳定性试验
按照相关要求进行操作。结果,沙格列汀和5-羟基沙格列汀的日内(n=5)、日间(n=3)精密度试验峰面积的RSD均小于12%;准确度为94.1%~105.4%、91.0%~ 103.6%;提取回收率分别为72.4%~87.3%、107.0%~115.3%(RSD均小于13.6%,n=6);基质效应分别为105.9%~107.8%、83.5%~88.2%(RSD均小于10.3%,n=6);稳定性试验(室温放置24 h、-80和室温下反复冻融3次、-80冻存90 d及吹干后残渣在室温放置24 h)峰面积的RSD≤11.0%(n=5)。
2.8 药动学研究
贾荣林[31]根据PID算法原理设计了空气源热泵热水器中电子膨胀阀的控制测试系统,并取得了良好的控制效果,极好地解决了系统的适应性和运行的节能性,从应用的角度证明了电子膨胀阀在空气源热泵热水器系统中的优越性。
取6只大鼠,高脂饲料喂养1个月后,ip链脲佐菌素诱导T2DM模型。造模前禁食、自由饮水12 h。按临床上沙格列汀给药剂量进行换算,ig 0.53mg/kg沙格列汀溶液,分别于给药前和给药后0.25、0.5、0.75、1.0、1.5、2.0、4.0、6.0、8.0、12.0、24.0 h经大鼠眼眶静脉丛取血0.25m L,置于经抗凝处理的离心管中,3 500 r/m in离心5m in,分离血浆,置于-80冰箱保存,备用。采用超高效液相色谱-串联质谱(UPLC-MS/MS)法测定不同时间点的沙格列汀和5-羟基沙格列汀的血药浓度,药-时曲线见图3。采用Win Nolin 6.1软件按照非房室模型进行处理,计算药动学参数,结果见表1。
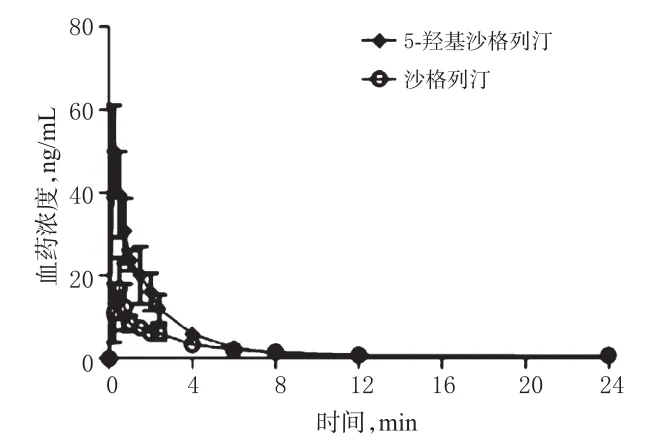
图3 沙格列汀与5-羟基沙格列汀在糖尿病模型大鼠体内的药-时曲线Fig 3 Concentration-time curvesof saxagliptin and 5-hydroxy saxagliptin in diabeticmodel rats in vivo
表1 沙格列汀与5-羟基沙格列汀在糖尿病模型大鼠体内的药动学参数(±s,n=6)Tab 1 Pharm cokinetic parameters of saxagliptin and 5-hydroxy saxagliptin in diabeticmodel rats in vivo(±s,n=6)

表1 沙格列汀与5-羟基沙格列汀在糖尿病模型大鼠体内的药动学参数(±s,n=6)Tab 1 Pharm cokinetic parameters of saxagliptin and 5-hydroxy saxagliptin in diabeticmodel rats in vivo(±s,n=6)
药动学参数t1/2,h tmax,h cmax,ng/mL AUC0-24h,ng·h/mL AUC0-∞,ng·h/mL沙格列汀2.88±0.21 0.25±0.01 49.97±11.14 90.95±7.06 91.72±7.57 5-羟基沙格列汀4.21±0.95 0.54±0.10 16.87±7.35 49.13±5.33 51.85±4.85
3 讨论
本文建立了稳定性好、通用性强、可灵敏快速测定大鼠血浆中沙格列汀及其代谢物5-羟基沙格列汀血药浓度的方法,并成功地应用于大鼠药动学研究。本实验起初采用BEH C18色谱柱,使用甲醇作为流动相,结果5-羟基沙格列汀的定量下限达不到检测要求;在流动相中添加乙腈后5-羟基沙格列汀的响应值提高,但检测物峰形变差。使用Waters BEH Shield RP18色谱柱摸索方法时流动相水相尝试过0.1%甲酸、0.1%甲酸-5mmol/L甲酸铵,但是随着水相比例的增加检测物的峰形变差且分叉成双峰,故选择不添加甲酸,且试验发现添加乙酸铵比添加甲酸铵灵敏度高、响应好,故最终选择10mmol/L乙酸铵-乙腈作为流动相体系。
样品处理时考虑到沙格列汀游离碱在水中微溶,在二氯甲烷及乙酸乙酯中溶解,但5-羟基沙格列汀的水溶性好,用乙酸乙酯、二氯甲烷基本无法提取,因此液液萃取同时提取两者比较困难,常规的液液萃取处理方法不适合该血浆样品的处理。而乙腈蛋白质沉淀法处理血浆样品的基质效应及提取回收率均满足相关的要求[11],故最终采用乙腈蛋白质沉淀法预处理。
综上所述,本研究建立的方法简便、准确、专属性强,适用于沙格列汀及其代谢产物5-羟基沙格列汀在大鼠体内的药动学研究。
[1] Boulton DW.Clinical pharmacokinetics and pharmacodynam ics of saxagliptin,a dipeptidyl peptidase-4 inhibitor [J].Clin Pharmacokinet,2017,56(1):11-24.
[2] Rose A,Jennifer H,JeffreyWS.Pharmacokinetic,pharmacodynamic and clinical evaluation of saxagliptin in type 2 diabetes[J].Expert Opin Drug Metab Toxicol,2016,12(4):467-473.
[3] Neumiller JJ,Campbell RK.Saxagliptin:a dipeptidyl peptidase-4 inhibitor for the treatmentof type 2 diabetesmellitus[J].Am JHealth Syst Pharm,2010,67(18):1515-1525.
[4] 陆菊明.2型糖尿病治疗新药沙格列汀的药理及临床评价[J].中国新药杂志,2011,20(21):2039-2043.
[5] Larry KG,Caitlin CD,M ichael TM.Comparative clinical pharmacokinetics of dipeptidyl peptidase-4 inhibitors[J]. Clin Pharmacokinet,2012,51(8):501-514.
[6] 刁幼林,于建华,王娟.沙格列汀联合二甲双胍治疗2型糖尿病的临床观察[J].中国药房,2015,26(27):3761-3763.
[7] Scheen AJ.Pharmacokineticsof dipeptidylpeptidase-4 inhibitors[J].DiabetesObes Metab,2010,12(8):648-658.
[8] Xu XS,Demers R,Gu H,et al.Liquid chromatography and tandem mass spectrometry method for the quantitative determination of saxagliptin and itsmajor pharmacologically active 5-monohydroxymetabolite in human plasma:method validation and overcom ing specific and nonspecific binding at low concentrations[J].J Chromatogr B,2012,doi:10.1016/j.jchromb.2012.01.033.
[9] Batta N,PilliNR,Derangula VR,etal.A rapid and sensitive LC-MS/MSassay for the determ ination of saxagliptin and its activemetabolite 5-hydroxy saxagliptin in human plasma and its application to a pharmacokinetic study[J]. Drug Res,2015,65(3):133-140.
[10] Shah PA,Shah JV,Sanyal M,et al.LC-MS/MS analysis ofmetform in,saxagliptin and 5-hydroxy saxagliptin in human plasma and its pharmacokinetic study w ith a fixeddose formulation in healthy Indian subjects[J].Biomed Chromatogr,2016,doi:10.1002/bmc.3809.
[11] 国家药典委员会.中华人民共和国药典:四部[S].2015年版.北京:中国医药科技出版社,2015:363-368.
(编辑:刘明伟)
Simultaneous Concentration Determ ination of Saxagliptin and Its M etabolite 5-hydroxy Saxagliptin in Plasma of Diabetic M odel Rats by UPLC-MS/M S
NIShanhong1,2,TANG Daoquan2,DONG Jie1,2,XIAO Bingxin1,LIU Yun1,LIYanli1,SUN Zengxian1(1.Dept.of Pharmacy,Lianyungang Hospital Affiliated to Xuzhou Medical University/the First People’s Hospital of Lianyungang City,Jiangsu Lianyungang 222002,China;2.Teaching and Research Section of Drug Analysis,Xuzhou Medical University,Jiangsu Xuzhou 221004,China)
OBJECTIVE:To establish amethod for the simultaneous concentration determ ination of saxagliptin and itsmetabolite 5-hydroxy saxagliptin in diabetic model rats in vivo.METHODS:UPLC-MS/MSwas performed on the column of Waters BEH
沙格列汀(Saxagliptin,SAX)是一种强效、具有选择性的二肽基肽酶4(DPP-4)抑制剂,用于治疗2型糖尿病(T2DM)[1-2]。DPP-4可裂解肠促胰素,肠促胰素主要包括胰高血糖素样肽1(GLP-1)和葡萄糖依赖的促胰岛素分泌多肽(GIP),GLP-1具有葡萄糖依赖性促胰岛素分泌的特性,可在血糖升高时发挥促胰岛素分泌作用,在血糖恢复正常时消失;同时,GLP-1还可促进胰岛B细胞增殖,改善其功能[3]。体内产生的GLP-1半衰期仅为1.5~2min,其氨基末端前2个氨基酸可被DPP-4快速裂解而失去促胰岛素分泌活性,使GLP-1无法在体内达到治疗浓度[4]。DPP-4抑制剂通过竞争性结合DPP-4活化部位,降低酶的催化活性,抑制GLP-1降解,提升内源性GLP-1的浓度,促进餐后胰岛素分泌,改善T2DM患者的血糖水平[5-6]。
沙格列汀在体内经细胞色素P4503A4/5代谢,主要代谢产物为5-羟基沙格列汀(5-hydroxy saxagliptin),其代谢产物也是一种选择性DPP-4抑制剂,活性是沙格列汀的50%[7]。目前,同时检测生物样品中沙格列汀及其代谢产物5-羟基沙格列汀的文献报道较少[8-10]。因此,本研究建立超高效液相色谱-串联质谱法(UPLC-MS/MS)同时测定沙格列汀和5-羟基沙格列汀在大鼠体内的血药浓度,计算相关药动学参数,为其进一步应用提供参考。
1 材料
1.1 仪器
Eksigent Ekspert Ultra LC110 XL超高效液相色谱(UPLC)仪、AB Qtrap 4500质谱仪(美国Applied Biosystems公司);T1氮气发生器(瑞士普利赛斯公司);AE-240电子天平(瑞士梅特勒-托利多仪器有限公司);Peqlab多功能高速离心机(德国Deutschland公司,离心半径:8.4 cm)。
1.2 药品与试剂
沙格列汀一水合物(以下简称沙格列汀)对照品(郑州华文化学品有限公司,批号:SG-31504001,纯度:94.36%);5-羟基沙格列汀对照品(批号:20160303,纯度:95.6%)、维格列汀对照品(内标,批号:20151203,纯度:99.5%)均购自江苏豪森药业有限公司;链脲佐菌素(美国Sigma公司,批号:B57426,纯度:99.89%);乙腈为色谱纯;乙酸铵为分析纯。
1.3 动物
SPF级SD大鼠,♂,体质量为80~120 g,由徐州医科大学实验动物中心提供,购自上海斯莱克实验动物有限责任公司(实验动物许可证号:SCXK[沪]2013-0016)。
2 方法与结果
2.1 色谱条件与质谱条件
色谱柱:Waters BEH Shield RP1(8100mm×2.1mm,1.7μm);流动相:10 mmol/L乙酸铵-乙腈(70∶30,V/ V);流速:0.3m L/m in;柱温:30;进样量:10μL。
采用电喷雾电离源(ESI),以多反应监测(MRM)模式扫描,正离子方式检测。离子化电压:5 500 V;温度:550;喷雾气(N2)压力:50 psi(1 psi=6.859×10-3MPa);辅助加热气(N2)压力:60 psi;气帘气体(N2)压力:35 psi;碰撞气模式:Medium;扫描时间:100ms。用于定量分析的离子对为:m/z 316.2→180.2(沙格列汀)、m/z 332.3→196.2(5-羟基沙格列汀)、m/z 304.2→153.9(内标),取“2.2”项下标准工作液进样测定,质谱图见图1。
2.2 溶液的制备
精密称取沙格列汀对照品、5-羟基沙格列汀对照品各适量,用50%乙腈溶解并稀释,制成质量浓度均为1 mg/m L的对照品贮备液,置于4冰箱保存。对照品贮备液用10%甲醇稀释成相应质量浓度的标准工作液,备用。
精密称取维格列汀(内标)对照品适量,用50%乙腈溶解并稀释,制成质量浓度为1mg/m L的内标贮备液。内标贮备液用10%甲醇稀释成质量浓度为50 ng/m L的 Shield RP18w ith mobile phase of 10 mmol/L ammonium acetate-acetonitrile(70∶30,V/V)at a flow rate of 0.3 m L/m in,column temperature was 30,and injection volume was 10μL.Scanning mode was multi-reactive monitoring w ith positive ion mode,and each ion pair was m/z 316.2→180.2(saxagliptin),m/z 332.3→196.2(5-hydroxy saxagliptin)and m/z 304.2→153.9(vildagliptin,internal standard).6 SD rats were selected and intragastric adm inistred saxagliptin 0.53 mg/kg after inducing diabetic models.Blood sample 0.25 m L was taken from eyes before administration and after 0.25,0.5,0.75,1.0,1.5,2.0,4.0,6.0,8.0,12.0,24.0 h of adm inistration.Plasma concentration of saxagliptin and itsmetabolite 5-hydroxy saxagliptin were determ ined,and Win Nonlin 6.1 software was used to calculate the pharmacokinetic parameters.RESULTS:The mass concentration of saxagliptin and 5-hydroxy saxagliptin ranged in 0.1-100,0.2-200 ng/m L(r=0.997 2,0.996 5);lim its of quantitation were 0.1,0.2 ng/m L;inter-day and intra-day RSDs were less than 12%(n=5,3);accuracy was 94.1%-105.4%,91.0%-103.6%;extraction recoveries were 72.4%-87.3%,107.0%-115.3%(RSD<13.6%,n=6);matrix effects were 105.9%-107.8%,83.5%-88.2%(RSD<10.3%,n=6);RSD of stability was less than 11.0%(n=5),respectively;and pharmacokinetic parameters as cmaxwere(49.97± 11.14),(16.87±7.35)ng/m L,t1/2were(2.88±0.21),(4.21±0.95)h,AUC0-24hwere(90.95±7.06),(49.13±5.33)ng·h/m L(n=6).CONCLUSIONS:Themethod is simple,accurate,specific,and suitable for the pharmacokinetics research of saxagliptin and itsmetabolite 5-hydroxy saxagliptin in diabetic rats in vivo.
Saxagliptin;5-hydroxy saxagliptin;Plasma concentration;Pharmacokinetics;Rat;UPLC-MS/MS内标溶液,置于4冰箱保存,备用。
R917
A
1001-0408(2017)16-2201-04
2016-12-29
2017-04-13)
*硕士研究生。研究方向:体内药物分析。电话:0518-85605518。E-mail:nshwp@126.com
#通信作者:主任药师,博士。研究方向:体内药物分析。电话:0518-85605518。E-mail:sunzx715@163.com
DOI10.6039/j.issn.1001-0408.2017.16.11
