建泽泻盐炙工艺优化及其HPLC指纹图谱的建立Δ
2017-07-03丘建芳黄小强李小艳吴水生福建中医药大学药学院福州35022福建中医药大学生物医药研发中心福州35022
陈 莹,丘建芳,黄小强,许 文,2,李小艳,吴水生#(.福建中医药大学药学院,福州 35022;2.福建中医药大学生物医药研发中心,福州 35022)
建泽泻盐炙工艺优化及其HPLC指纹图谱的建立Δ
陈 莹1*,丘建芳1,黄小强1,许 文1,2,李小艳1,吴水生1#(1.福建中医药大学药学院,福州 350122;2.福建中医药大学生物医药研发中心,福州 350122)
目的:优化建泽泻盐炙工艺并建立其高效液相色谱(HPLC)指纹图谱。方法:以23-乙酰泽泻醇B、总三萜含量和外观性状综合评分为指标,采用单因素试验和正交试验,优化建泽泻盐炙工艺中用盐量、炒制温度和炒制时间3个因素的水平。采用HPLC法分别在208、245 nm波长下建立10批建泽泻盐炙品的指纹图谱,经软件比较其与对照图谱的相似度。结果:最优工艺为每100 kg泽泻加10 kg水溶解的2 kg盐,闷润1 h,在100 ℃下炒制8min。验证试验中,3批盐炙品外观性状均符合要求,综合评分平均值为93.94(RSD=6.63%,n=3);23-乙酰泽泻醇B和总三萜含量稳定,RSD分别为7.41%、7.39%(n=3)。在208、245 nm波长下分别标定了建泽泻盐炙品的17、10个共有峰;10批样品指纹图谱相似度均大于0.9。结论:优化的建泽泻盐炙工艺合理可行、重现性好;建立的指纹图谱共有峰稳定,可用于建泽泻盐炙品的质量评价。
建泽泻;盐炙工艺;正交试验;高效液相色谱;指纹图谱;23-乙酰泽泻醇B;三萜类化合物
泽泻为泽泻科植物泽泻[Alisma orientale(Sam.)Juzep.]的干燥块茎,别名水泻、水泽等,味甘、性寒,归肾、膀胱经,是具有利水渗湿、泄热、化浊降脂作用的传统中药材[1]。泽泻在福建地区具有悠久的栽培历史[2],宋代《本草图经》和明代《本草乘雅半偈》均记载福建产泽泻、清代《本草精汇品要》记载闽产泽泻为道地药材,称“建泽泻”。从古至今泽泻有多种炮制方法,如《雷公炮炙论》首载的酒浸法[3]及后炙、盐水伴、盐水炒焦、麸炒、土炒等炮制方法[4]。其中盐泽泻能引药下行,具有增强滋阴、利水的作用,为目前临床使用的主要泽泻炮制饮片[5]。现代化学和药理研究表明,泽泻利尿、降血脂的主要有效成分为原萜烷型四环三萜[6]。目前对泽泻炮制工艺的研究以盐炙为主,已有以23-乙酰泽泻醇B为指标对泽泻盐炙工艺进行优化的文献报道[7],但是已有研究表明不同炮制温度和时间下泽泻三萜成分易发生相互转化[8],故单一指标难以全面反映泽泻盐炙品的内在品质。同时建泽泻作为道地药材,以成品的外观性状作为炮制工艺的参考指标难以做到客观、可控、稳定和可重复,且其盐炙炮制工艺和盐炙品指纹图谱均少见文献报道,故有必要开展建泽泻规范化炮制工艺及其炮制品指纹图谱的评价研究。
本试验以2015年版《中国药典》(一部)泽泻项下指标23-乙酰泽泻醇B及建泽泻4种主要三萜(23-乙酰泽泻醇B、泽泻醇B、23-乙酰泽泻醇C、泽泻醇C,以下称总三萜)的总和、外观性状为综合指标,采用单因素试验和多指标正交试验法,考察炮制用盐量、温度和时间3个因素的最优水平,优化建泽泻盐炙工艺,并在此基础上建立建泽泻盐炙饮片高效液相色谱(HPLC)指纹图谱,分别对208 nm和245 nm波长下的共有峰进行标定和指认,从多指标和整体成分群定性的角度综合评价建泽泻盐炙品,为其炮制和质量评价提供试验依据。
1 材料
1.1 仪器
LC-20AT HPLC仪(日本岛津公司);FY135中草药粉碎机(天津市泰斯特仪器有限公司);DV215CD十万分之一分析天平(美国奥豪斯公司);KQ-500E台式超声波清洗器(昆山市超声仪器有限公司);CCFG-160B电炒锅(福建省邵武市永乐无线电厂);M illi-Q超纯水机(美国默克密理博公司)。
1.2 药材、药品与试剂
10批生泽泻饮片(购于福建省金山医药实业集团有限公司,来自福建建瓯泽泻药材生产质量管理规范基地,批号分别为:130110、130115、130121、130127、130211、130219、130227、130309、130316、130325,编号为S1~S10)经福建中医药大学范世明高级实验师鉴定为泽泻科植物泽泻[Alisma orientale(Sam.)Juzep.]的干燥块茎,样本存放于福建中医药大学药学院药用植物标本室;23-乙酰泽泻醇B对照品(中国食品药品检定研究院,批号:111846-201102,纯度:≥98.5%);泽泻醇B、23-乙酰泽泻醇C、泽泻醇C对照品(批号分别为:YAO02、YAO03、YAO08,纯度:>98.5%)和泽泻醇F、11-去氧泽泻醇B、16-羰基泽泻醇A、16-羰基-23-乙酰泽泻醇A、16-羰基-24-乙酰泽泻醇A、泽泻烯醇对照品(批号分别为:YAO046、YAO07、YAO11、YAO12、YAO13、YAO04)均由福建中医药大学药学院制备,供指纹图谱定性对比使用;乙腈为色谱纯,水为超纯水,其余试剂均为分析纯,盐为食用级。
2 方法与结果
2.1 4种三萜类化合物含量测定
2.1.1 色谱条件 色谱柱:Ultimate XB-C1(8150mm× 4.6 mm,5µm);流动相:乙腈-水(73∶27);流速:1.0 m L/m in;检测波长:208、245 nm;柱温:30;进样量:10 µL。
2.1.2 对照品溶液的制备 分别取23-乙酰泽泻醇B、泽泻醇B、23-乙酰泽泻醇C、泽泻醇C对照品适量,精密称定,加入乙腈溶解并定容,分别制备成质量浓度为151.7、152.5、196.0、156.5μg/m L的单一对照品贮备液。试验所用其他质量浓度的对照品溶液分别由乙腈稀释贮备液得到。
2.1.3 供试品溶液的制备 取过40目筛的泽泻样品粉末(批号:130110)约0.5 g,精密称定并置于具塞锥形瓶中,精密加入乙腈25m L,密塞,称定质量,超声(功率:250W,频率:50 kHz)提取30m in,放冷,再称质量,用乙腈补足减失的质量,摇匀,经0.45μm微孔滤膜滤过,取续滤液备用,即得。
2.1.4 专属性考察 取上述对照品和供试品溶液进样测定,2个波长下色谱峰分离良好,见图1。

图1 高效液相色谱图Fig 1 HPLC chromatograms
2.1.5 线性关系考察 分别取“2.1.2”项下方法制备的各对照品贮备液,用乙腈稀释,制备成7个系列质量浓度的各对照品溶液。精密吸取10µL,进样测定,以峰面积(y)对分析物质量浓度(x)作线性回归,结果见表1。

表1 4种三萜类成分线性关系考察结果Tab 1 Results of linear relationship of 4 kinds of triterpenoids
2.1.6 精密度、重复性、稳定性、加样回收率试验 按相关方法进行考察。结果,精密度试验中4种成分峰面积的RSD均未超过1.47%(n=6),表明精密度良好;重复性试验中4种成分含量的RSD均未超过1.63%(n=6),表明方法重复性良好;稳定性试验中4种成分峰面积的RSD均未超过1.56%(n=6),表明供试品溶液在24 h内稳定;加样回收率试验中4种成分的平均回收率分别为100.18%、96.59%、97.56%、97.79%(RSD均未超过2.70%,n=6),表明方法准确度良好。
2.1.7 含量测定方法 分别取对照品溶液和供试品溶液,进样测定峰面积,采用外标法计算含量。
2.2 单因素试验考察盐炙工艺
2.2.1 综合评分标准 以23-乙酰泽泻醇B、总三萜含量为内在指标,外观性状为外在指标,应用综合加权评分法处理数据。中药饮片的外观性状评分参照《中国药典》对盐泽泻性状的要求[1],即外观性状总分为饮片表面色泽、质地与气味评分之和,具体评分标准见表2。

表2 外观性状评分标准Tab2Appearanceandcharacterscoringcriterion
[9],确定各指标权重为23-乙酰泽泻醇B含量50%、总三萜含量35%、外观性状15%。评分方法:各项评分均为y=xi/xmax×权重系数×100(xmax为各项指标中含量或外观性状评分最高值,xi为对应各项指标或外观性状评分值),总分为各项指标评分的总和。
2.2.2 用盐量的考察在预试验的基础上,分别称取0.6、0.8、1.0、1.2、1.4g盐,分别加入4g水溶解,闷润泽泻,使盐水渗入泽泻饮片内部,饮片润湿程度基本相同。取泽泻5份,每份40g,闷润1h后,100下炒制12 min,考察用盐量。将上述泽泻盐炙品粉碎后过40目筛,评价各指标。结果,用盐量为0.8g时,综合评分最高,随后逐渐下降,详见表3。

表3 单因素试验考察结果Tab3Resultsofsinglefactortest
2.2.3 炒制温度的考察2015年版《中国药典》(四部)0213炮制通则规定盐炙法以文火加热,将待炮炙品炒至规定程度。已有报道指出文火温度为80~120[10],而温度过高泽泻易出现焦斑,故选择80~160考察炒制温度。取泽泻5份,各40g,分别用4g水溶解0.8g盐量制备的盐溶液闷润1h后,经不同温度(80、100、120、140、160)炒制12min后取出,放凉。将上述泽泻盐炙品粉碎后过40目筛,评价各指标。结果,随着炒制温度的升高,综合评分值先上升后下降,100时最高,详见表3。
2.2.4 炒制时间的考察取泽泻5份,各40g,分别用4 g水溶解0.8g盐量制备的盐溶液闷润1h,炒制温度为100,分别炒制不同时间(4、8、12、16、20min),取出放凉。将上述泽泻盐炙品粉碎后过40目筛,评价各指标。结果,炒制时间为12min时综合评分值最高,详见表3。但考虑到4min炮制时间过短,饮片外观性状不佳,结合此结果,选择将正交试验设计中时间的3个水平分别设为8、10、12min。
2.3 正交试验优化盐炙工艺
根据单因素试验考察结果,确定A(用盐量,g)、B(炒制温度,)、C(炒制时间,min)3因素为正交试验考察因素,每个因素拟定3个水平,以综合评分为指标,采用L(934)正交表设计试验。因素与水平见表4,正交试验设计与结果见表5,方差分析结果见表6。
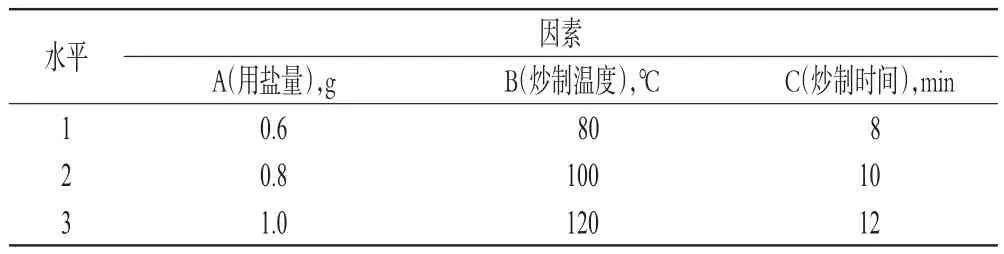
表4 因素与水平Tab4Factorsandlevels
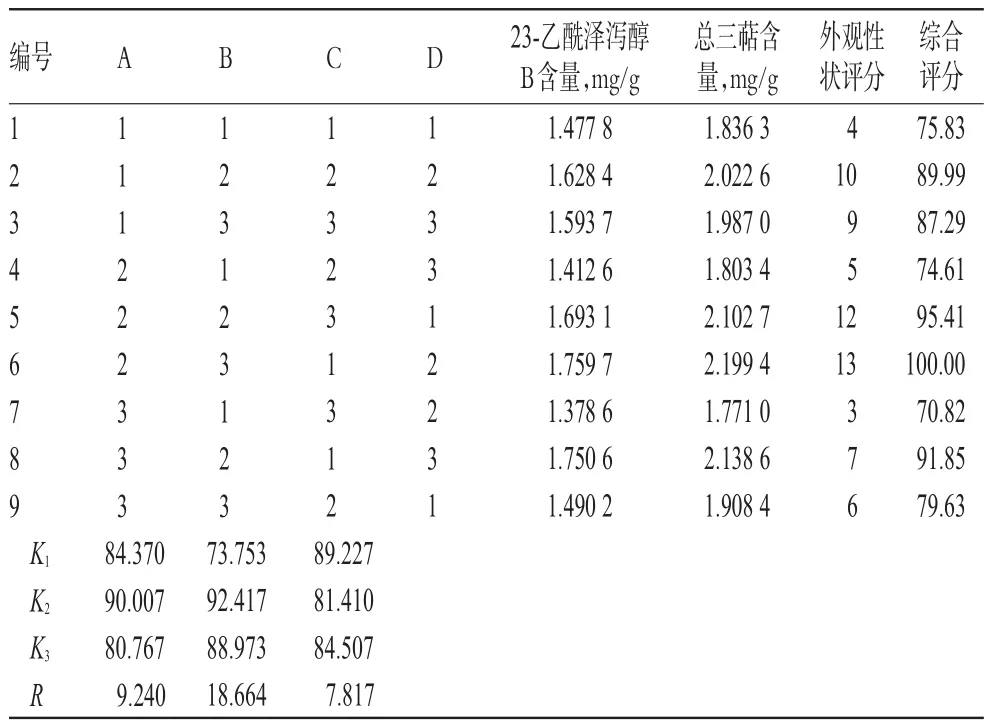
表5 正交试验设计与结果Tab5Designandresultsoforthogonaltest
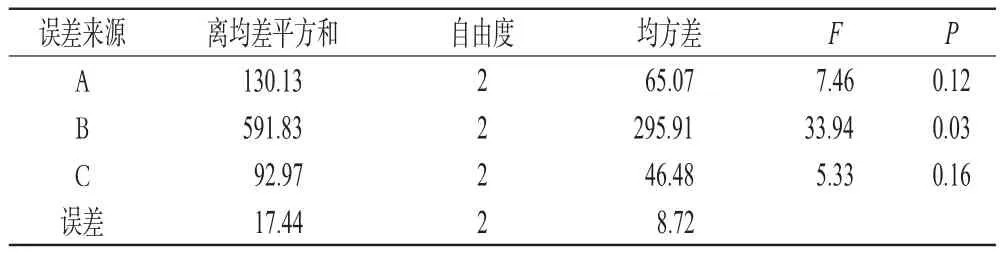
表6 方差分析结果Tab6Resultsofvarianceanalysis
表5结果表明,对综合评分影响大小依次为B(炒制温度)>A(用盐量)>C(炒制时间)。方差分析结果表明,因素B对试验结果有显著影响,而A和C无显著影响。选取最优盐炙工艺为A2B2C1,即每40g泽泻加4g水溶解的0.8g盐(每100kg泽泻加10kg水溶解的2kg盐),闷润1h,在100下炒制8min。
2.4 中试验证试验
取3份大小均匀的干燥生泽泻饮片,每份40kg,在中试设备上按上述优化的盐炙工艺条件制备3批盐泽泻饮片,验证工艺的可靠性。结果制备的3批盐泽泻外观性状均符合《中国药典》标准,各指标综合评分均大于87,批间RSD小于7.41%(n=3)。另外,对每批盐泽泻的指标均平行测定3次,结果,批次内的泽泻指标含量相对接近,批内RSD小于3%(n=3);且外观性状评分稳定,RSD小于4%(n=3),均符合《中国药典》要求。这表明优化的工艺稳定可行,得到的成品质量稳定。验证试验结果见表7。

表7 验证试验结果(n=3)Tab 7 Resu ltsof verification test(n=3)
2.5 建泽泻盐炙品指纹图谱研究
2.5.1 色谱条件 色谱柱:Ultimate XB-C1(8150 mm× 4.6mm,5μm);流动相:乙腈(A)-水(B),梯度洗脱(0~5min,35%A;5~20min,35%A~55%A;20~35m in,55%A~65%A;35~45m in,65%A~75%A;45~55m in,75%A~85%A;55~65m in,85%A);流速:1m L/min;检测波长:208、245 nm;柱温:30;进样量:10μL。
2.5.2 供试品溶液的制备 按优化的建泽泻盐炙工艺制备10批盐泽泻饮片,精密称取过40目筛盐炙品粉末2.0 g,置于50m L具塞锥形瓶中,其余操作同“2.1.3”项。
2.5.3 混合对照品溶液的制备 取23-乙酰泽泻醇B、泽泻醇B、23-乙酰泽泻醇C、泽泻醇C、泽泻醇F、11-去氧泽泻醇B、16-羰基泽泻醇A、16-羰基-23-乙酰泽泻醇A、16-羰基-24-乙酰泽泻醇A、泽泻烯醇对照品适量,精密称定,分别加入乙腈溶解并稀释制备成约1.0μg/m L对照品溶液并混合,供定性分析使用。
2.5.4 方法学考察 (1)系统适用性及专属性试验。精密吸取混合对照品溶液和供试品溶液各10μL,按“2.5.1”项下色谱条件进样,记录色谱图。结果在2个检测波长下各化合物与其相邻峰的分离度均大于1.5,拖尾因子为0.95~1.05,理论板数以各色谱峰计均大于10 000,表明该条件下方法专属性良好。(2)精密度、稳定性、重复性试验。取批号为130110的泽泻盐炙品供试品溶液,按相关方法进行考察。结果,精密度试验中各共有峰相对保留时间的RSD为0.16%~0.34%(n=6),相对峰面积的RSD为0.45%~3.87%(n=6),表明仪器精密度良好;稳定性试验中各共有峰相对保留时间的RSD为0.12%~0.27%(n=6),相对峰面积的RSD为1.13%~4.99%(n=6),表明供试品溶液在24 h内稳定性良好;重复性试验中各共有峰相对保留时间的RSD为0.04%~0.12%(n=6),相对峰面积的RSD为2.81%~4.96%(n=6),表明方法重复性良好。
2.5.5 泽泻盐炙品指纹图谱建立 (1)参照峰的选择。取“2.5.2”项制备的10批泽泻盐炙品供试品溶液各10 μL,按“2.5.1”项下色谱条件测定,得到10批泽泻盐炙品的HPLC图谱。选择指纹图谱中保留时间适中且峰面积较稳定的色谱峰为参照峰。结果表明,在208 nm波长下13号峰(23-乙酰泽泻醇B)和245 nm波长下6号峰(23-乙酰泽泻醇C)与相邻色谱峰分离良好、基线稳定,并且在泽泻中含量较高,故分别确定为208 nm和245 nm波长下的参照峰。(2)共有峰的标定及指认。将10批(S1~S10)泽泻盐炙品HPLC图谱导入中国药典委员会“中药色谱指纹图谱相似度评价系统”软件(2004A版)中进行色谱峰匹配,经多点校正后进行峰自动匹配,计算并生成对照图谱R。图谱在208 nm波长下共标定17个共有峰,经对照品定性,指认6个峰,其中5、6、8、10、13、15号峰分别为泽泻醇F、23-乙酰泽泻醇C、泽泻烯醇、泽泻醇B、23-乙酰泽泻醇B、11-去氧泽泻醇B;245 nm波长下共标定10个共有峰,指认5个峰,其中1、2、3、4、6号峰分别为16-羰基泽泻醇A、16-羰基-23-乙酰泽泻醇A、16-羰基-24-乙酰泽泻醇A、泽泻醇C、23-乙酰泽泻醇C。2个波长下共有峰峰面积总和均占各自波长下所有检出色谱峰峰面积总和的95%以上。(3)相似度评价。应用“中药色谱指纹图谱相似度评价系统”软件(2004A版),将10批泽泻盐炙品的HPLC图谱导入并计算相似度。结果,10批泽泻盐炙品相似度在208 nm波长下分别为0.999、0.999、0.999、0.997、0.998、0.998、0.994、0.998、0.998、0.999,在245 nm波长下分别为0.993、0.999、0.994、0.998、0.985、0.996、0.996、0.997、0.991、0.946,均大于0.9,表明各批药材质量稳定,批次间差异较小。生成的对照图谱和双波长HPLC指纹图谱见图2。
3 讨论
建泽泻是闽产道地药材之一,为临床常用大宗中药,文献记载有酒制、盐制、清蒸、麸制、土制等诸多炮制方法,“健脾生用或酒炒用,滋阴利水盐水炒”[11]。泽泻甘寒,入肾、膀胱经;盐味咸,引药入肾与膀胱,能够增强泽泻的利水渗湿、泄热通淋之功。因而开展泽泻的盐制炮制机制研究、制定盐制工艺标准有积极的现实意义。
3.1 工艺优化指标的选择
首先,泽泻化学成分主要为三萜类成分[12],是其利尿[13]、降脂[14]、降糖[15]等作用的有效物质基础。《中国药典》将23-乙醇泽泻醇B作为指标性成分[1],因此,本试验将其作为炮制工艺优化的指标之一。其次,泽泻三萜化合物性质不稳定,具体表现在产地加工、炮制等过程中会发生化学成分的转化,因此选择4种三萜化合物的总含量[16]作为总三萜评价指标。此外,由于外观性状评价与炮制程度有相关性[4],笔者同时参考文献[6],设置了色泽、质地、粉性、焦斑情况及味咸情况等外观性状指标。
3.2 2个试验中色谱条件及方法学考察项目的区别

图2 高效液相指纹图谱Fig 2 HPLC fingerprint
在4种成分的含量测定和建泽泻盐炙品指纹图谱的建立中,流动相分别采用了等度洗脱和梯度洗脱。等度洗脱可将4个化合物进行分离和洗脱,但在建立指纹图谱时,由于泽泻中成分复杂,等度洗脱不能达到较多成分基线分离的效果,而梯度洗脱则可,并可得到更多分离度良好的色谱峰,故后者采用梯度洗脱。另外,在指纹图谱的建立中,方法学考察的项目主要是根据国家食品药品监督管理总局印发的《中药注射剂指纹图谱研究的技术要求(暂行)》和文献[17]设立的,而含量测定的方法学考察项目则是根据2015年版《中国药典》方法学验证指导原则设立的,故二者考察项目不同。
3.3 建泽泻盐炙品的指纹图谱研究
本试验在优化建泽泻盐炙工艺的基础上,首次研究并建立了福建道地药材泽泻盐炙品的双波长(208 nm和245 nm)指纹图谱,各共有峰稳定性较好,相似度分别在0.994和0.946以上,符合指纹图谱建立的要求,故该方法可以对建泽泻盐炙品进行有效的质量评价。
参考文献
[1] 国家药典委员会.中华人民共和国药典:一部[S].2015年版.北京:中国医药科技出版社,2015:229.
[2] 蔡沓栗,杨成梓,林青青.建泽泻[J].生命世界,2015(10):14.
[3] 宋·唐慎微.重修政和经史证类备用本草:影印版[M].北京:人民卫生出版社,1957:162.
[4] 谢一辉,余无双,周丽姣,等.泽泻不同炮制工艺及评价方法的研究[J].中成药,2010,32(10):1736-1740.
[5] 徐硕,夏路风,金鹏飞,等.泽泻的化学成分及生物活性研究进展[J].中国医药导报,2015,12(27):47-51.
[6] 龚千峰.中药炮制学[M].北京:中国中医药出版社,2003:212-213.
[7] 陈天兴,陶忠增,盖雪.盐泽泻最佳炮制工艺的探讨[J].山东中医药大学学报,2005,29(5):385-387.
[8] 谢雪,许枬,张宏达.泽泻盐炙过程中化学成分转化研究[C]//中华中医药学会中药炮制分会2011年学术年会论文集.贵阳:中华中医药学会中药炮制分会,2011:381-387.
[9] 钟凌云,龚千锋,段启,等.多指标正交试验法优选泽泻盐炙炮制工艺[J].中成药,2006,28(1):45-47.
[10] 张敏娜.泽泻饮片炮制条件与质量评价研究[D].济南:山东大学,2007.
[11] 吴水生.泽泻的药学与临床研究[M].北京:中国中医药出版社,2007:4-5.
[12] 许枬,张宏达,谢雪.泽泻中的新三萜成分[J].中草药,2012,43(5):841-843.
[13] Hikino H,Iwakawa T,Oshima Y,etal.Diuretic principles of alisma plantago aquatica var orientale rhizomes[J]. Shoy-akugaku Zasshi,1982,36(2):150-153.
[14] 吴永平,王梦,卢定强.乙酰泽泻醇B与洛伐他汀对大鼠降血脂作用的比较[J].华西药学杂志,2011,26(3):243-244.
[15] 许文,罗奋熔,赵万里,等.泽泻降糖活性提取物化学成分研究[J].中草药,2014,45(22):3238-3245.
[16] Zhao W,Huang X,Li X,et al.Qualitative and quantitative analysis of major triterpenoids in Alismatis rhizoma by high performance liquid chromatography/diode-array detector/quadrupole-time-of-flightmass spectrometry and ultra-performance liquid chromatography/triple quadrupole mass spectrometry[J].Molecules,2015,20(8):13958-13981.
[17] 宋潇,谢昭明,黄丹,等.茯苓皮药材的HPLC指纹图谱研究[J].中国药房,2015,26(15):2109-2111.
Technology Optim ization of Stir-bake w ith Saltwater Processing for Fujian A lismatis Rhizoma and Establishm ent of Its HPLC Fingerprint
CHEN Ying1,QIU Jianfang1,HUANG Xiaoqiang1,XU Wen1,2,LIXiaoyan1,WU Shuisheng1(1.School of Pharmacy,Fujian University of Traditional Chinese Medicine,Fuzhou 350122,China;2.Biomedical Research and Development Center,Fujian University of Traditional Chinese Medicine,Fuzhou 350122,China)
OBJECTIVE:To optim ize the stir-bake w ith saltwater processing technology for Fujian A lismatis rhizoma,and establish its HPLC fingerprint.METHODS:Using 23-acetyl alisol B,total triterpenoids contents and appearance as comprehensive indexes,single factor experiment and orthogonal testwere employed,3 factors’levels including the quantity of salt,processing temperature and time were optimized.HPLC was used to develop fingerprints of 10 batches of Fujian Alismatis rhizoma atwavelength of 208,245 nm;the sim ilarity between fingerprints and control profile was compared by using software.RESULTS:The optimal technology was as follow as 2 kg salt dissolved w ith 10 kg water for each 100 kg Fujian A lismatis rhizoma,moistening for 1 h,stir-frying for 8 minutes under 100 ℃.In verification test,the appearance of 3 batches of processed products were all in line w ith requirements,average comprehensive score was 93.94(RSD=6.63%,n=3);23-acetyl alisol B and total triterpenoids contents were stable(RSD=7.41%,7.39%,n=3),respectively.Totally 17 and 10 common peaksweremarked in 208 nm and 245 nm respectively;sim ilarities of 10 batches of samples’fingerprintswere higher than 0.9.CONCLUSIONS:Optim ized stir-bake w ith saltwater technology is reasonable,feasible,and reproducible;the stability of common peaks of established fingerprints can conduct effective quality evaluation for Fujian Alismatis rhizoma processed by saltwater.
Fujian A lismatis rhizoma;Stir-bake w ith saltwater technology;Orthogonal test;HPLC;Fingerprint;23-acetyl alisol B;Triterpenoids
R283
A
1001-0408(2017)16-2244-05
2016-09-01
2016-10-17)
(编辑:刘 萍)
国家自然科学基金资助项目(No.U1205022);国家科技支撑计划课题(No.2011BAI01B06);国家中医药管理局国家中药标准化项目(No.ZYB2H-Y-FJ-09);福建省教育厅中青年教师教育科研项目(No.JA15242)
*硕士研究生。研究方向:中药药效物质基础及作用机制。电话:0591-22861135。E-mail:chenying578119815@163.com
#通信作者:教授。研究方向:中药复方药效物质及其作用机制。电话:0591-22861135。E-mail:wushuishengwss@163.com
DOI10.6039/j.issn.1001-0408.2017.16.23
