香椿芽苗中含硫化合物对其风味物质的影响
2017-07-01李楠王浩宇赵芳刘常金
李楠,王浩宇,赵芳,刘常金
(天津科技大学食品工程与生物技术学院,天津300457)
香椿芽苗中含硫化合物对其风味物质的影响
李楠,王浩宇,赵芳,刘常金*
(天津科技大学食品工程与生物技术学院,天津300457)
通过采用顶空固相微萃取的方法(HS-SPME)对香椿中的香气成分进行富集,并结合气相色谱-质谱(GCMS)法、气相色谱-嗅闻-质谱GC-O-MS对其特征性风味物质进行分析鉴定,从而进一步探究香椿中的香气组成成分。结果表明:在香椿芽苗的生长过程中,第一次得到反式-1-丙烯基双二硫化物,该化合物在一定基础上可以转化为香椿中所含有的1-丙烯基硫醇和3,4-二甲基噻吩。通过对比含硫化合物的结构式发现,香椿与大蒜在很大基础上存在一致性,而导致两者拥有特征性风味的物质在一定基础上也有所相似。
香椿;风味物质;气相色谱-嗅闻-质谱;反式-1-丙烯基双二硫化物
香椿 Toona sinensis(A.Juss.)Roem。又名春芽树、椿、椿树,在《植物名实图考》中称为红椿,属楝科(Meliaceae)香椿属(Toona)落叶乔木。香椿材菜兼用,在我国具有悠久的栽培历史,不但是我国特有速生用材树种,而且被国外称为“绿色保健菜”[1]。每年的三、四月份,是香椿上市的季节,也是香椿市场尤为兴盛的时期,且价格居高不下,但仍受大众所喜爱。究其原因,主要是香椿极其浓郁的香气和特殊的风味深受人们的青睐,并因此得名。因而近几年来,香椿越发成为广泛栽培的对象。随着对其需求的不断增加,人们在关注香椿产品的同时,对香椿风味的组成、形成机理、影响因素以及保藏方式亦或代替产品更加关注,也因此成为了大众想要探究的热点问题。
对于香椿香气成分的确定,目前国内外研究相对较少。李聚英等[2]研究发现:温度越高,香椿特征香气降低越迅速[3]。并得到两种明显呈现香椿特征香气的化合物,但由于质谱谱库检索尚不能与已知物质谱图吻合,初步推断为这两种化合物为噻吩衍生物或为唑衍生物的同分异构体。在此之前,Mu等[4]采用MAEHS-SPME(微波辅助顶空固相微萃取)法提取香椿挥发性成分,经GC-MS分析得到与本试验相似的离子流图,给出的明显呈香椿特征性风味的两种物质分别是2-乙基噻唑和5-乙基噻唑。但这与李聚英等购买的相应的噻吩和噻唑衍生物标准品通过质谱对比所得到的保留时间以及质谱图均不符。张杰等[5]第一次确定了2-巯基-3,4-二甲基-2,3-二氢噻吩的正反同分异构体是香椿挥发性化合物的关键物质,与Eric.Bliock等[6]所提出的二巯基-克莱森重排中的中间物相呼应。
香椿特征性风味目前被认定为一种易挥发性不稳定物质,而且香气成分复杂,究竟是哪种化学成分给予了香椿的特征性风味,且在采摘贮存、加工过程中香气的成分又是如何变化,对于香椿品质都有具大的影响。本研究采用HS-SPME对香椿香气进行富集并结合气相色谱-质谱(GC-MS)法、气相色谱-嗅闻-质谱GC-O-MS对其特征性风味物质的检测方法进行优化,从而进一步探究香椿中的香气组成成分,为香椿替代物的研制生产提供理论依据。
1 材料与方法
1.1 材料
香椿嫩叶采自天津经济技术开发区十一大街农产品种植园,香椿在园中自然健康的生长,具有浓厚的香椿特征性香气;香椿芽苗为天津科技大学农产品开发与物流保鲜实验室恒温培养。
1.2 试剂与仪器
SPME手动进样手柄(65 μm DVB/PDMS萃取头):美国Supelco公司;40 mL带有PTPE/硅橡胶平垫的透明萃取瓶:上海安谱公司;400 gHK-08粉碎机:广州市旭朗机械设备有限公司;85-2恒温磁力加热搅拌器:金坛市荣华仪器制造有限公司;Varian 4000GC/MS气相色谱-质谱联用仪:美国瓦里安公司;Agilent 7890气相色谱-质谱联用仪(配有FID检测器):美国安捷伦公司;Sniffer 9000嗅闻仪:瑞士Brechbühler公司;SG 350A匀浆机:上海天航电器有限公司。
1.3 试验方法
1.3.1 GC-MS分析条件
Varian 4000GC/MS气相色谱-质谱联用仪,使用毛细管柱(30 m×0.25 mm×0.25 μm);进样口温度 150℃,分流比5∶1,载气为氦气,色谱柱载气流速为1 mL/min;FID检测器温度为250℃、全出线温度280℃、电离方式EI、扫描方式为全扫描、扫描范围为43 aum~500 aum、离子阱温度220℃;程序升温:初温40℃,保持3 min,以4℃/min升至150℃,保持8 min,以8℃/min升至250℃,保持2 min;检索图库为NIST05库。
1.3.2 GC-O-MS分析条件
1.3.2.1 GC-O条件
Agilent 7890气相色谱仪,流出物在毛细管末端以1∶1的分流模式分别进入质谱仪和嗅辩仪;使用19091S-433(30 m×0.25 mm×0.25 μm)。分流比 5 ∶1;载气为 He(99.99%),柱前压 74.4 kPa,流速为 1 mL/min。
1.3.2.2 MS条件
检测器温度260℃,穿梭线温度280℃,电离方式EI,扫描方式为全扫描,扫描范围为33 aum~350 aum;离子阱温度220℃;检索图库为NIST08库。
1.3.3 嗅闻分析方法
选择5人对色谱峰进行嗅闻分析,其中3名女性,2名男性,每个成员都熟悉样品香气,每位成员对同一试验样品嗅闻两次,共10份数据用于统计分析。同一色谱峰有6次以上记录时,才被用来分析[7]。
1.3.4 香椿特征性香气的富集
称取香椿原料15.00 g于组织搅碎机中,按照1∶3(g/mL)的比例加入去离子水45 mL,打浆1 min至固液均匀。称取11.00 g左右的匀浆置于40 mL的萃取瓶中。将待用的样品放于60℃恒温磁力加热搅拌器中,水浴平衡30 min后,顶空萃取40 min,进样时热解析15 min,同时采集数据,每个样品平行3次。
2 结果与分析
2.1 香椿芽苗的GC-O-MS、GC-MS分析
香椿为热敏性物质,在加热的过程中其风味物质可能会发生分解、交联等其他反应,因而,温度是探究香椿气相质谱分析结果中的一大因素。近几年的研究发现,香椿与大蒜的呈味物质在一定基础上可能存在相似之处,故研究将含硫化合物作为探究是香椿特征性风味的目标物质。
将香椿样品按照1.3.4的方法进行香气的富集,并于气相色谱质谱联用、气相色谱-嗅闻-质谱联用仪中进行检测。经过多次试验结果表明:有15个色谱峰具有明显的气味,其中从21 min左右开始出现香椿特征性香气,到23 min左右香椿香气逐渐减弱至消失。在此期间,7号色谱峰(保留时间为21.946 min)呈现明显的蒸煮香椿风味,且强度较大,最为明显。将嗅辨结果统计整理,如表1所示。

表1 香椿样品香气成分GC-O-MS结果Table 1 The GC-O-MS results of aroma compounds from Toona sinensis

续表1 香椿样品香气成分GC-O-MS结果Continue table 1 The GC-O-MS results of aroma compounds from Toona sinensis
由气相色谱-嗅闻的结果可以看出,7号色谱峰是香椿特征性香气的关键成分,因而针对这一结果进行质谱分析。为了更为准确地对这15个色谱峰进行化学结构的定性,将香椿样品进一步作GC-MS检测分析,并将GC-O-MS的谱图与GC-MS的谱图进行对比分析,如图1所示。
由于方法1.3.1和1.3.2略有区别,因此所得色谱峰的保留时间以及峰面积也存在一定的差异,但两种方法所得到的图谱基本相同。通过谱库检索及定性分析发现,这15个色谱峰中有11个为含硫化合物。将这11个色谱峰的结果整理,如表2所示。

图1 香椿芽苗香气成分的GC-O-MS、GC-MS谱图Fig.1 GC-O-MS and GC-MS chromatograms of aroma compounds from Toona sinensis
这11个化合物与之前报道的研究结果大致相同[8],由表2可以看出含硫化合物在香椿挥发性化合物中所占百分比较低,但却是在嗅闻过程中主要表现香椿特有风味的物质。尤以7号色谱峰为主,在嗅闻过程中味道较为强烈,经谱库检索发现,该物质为3,4-二甲基-2,3-二氢噻吩,这与之前张杰等[5]的研究相符。但7号色谱峰呈现的为蒸煮香椿风味,而不是刚采摘过后的香椿原有风味,参考以往文献推断,3,4-二甲基-2,3-二氢噻吩并不是香椿中本身所含有的物质,而是受热发生了转化所引起[9]。
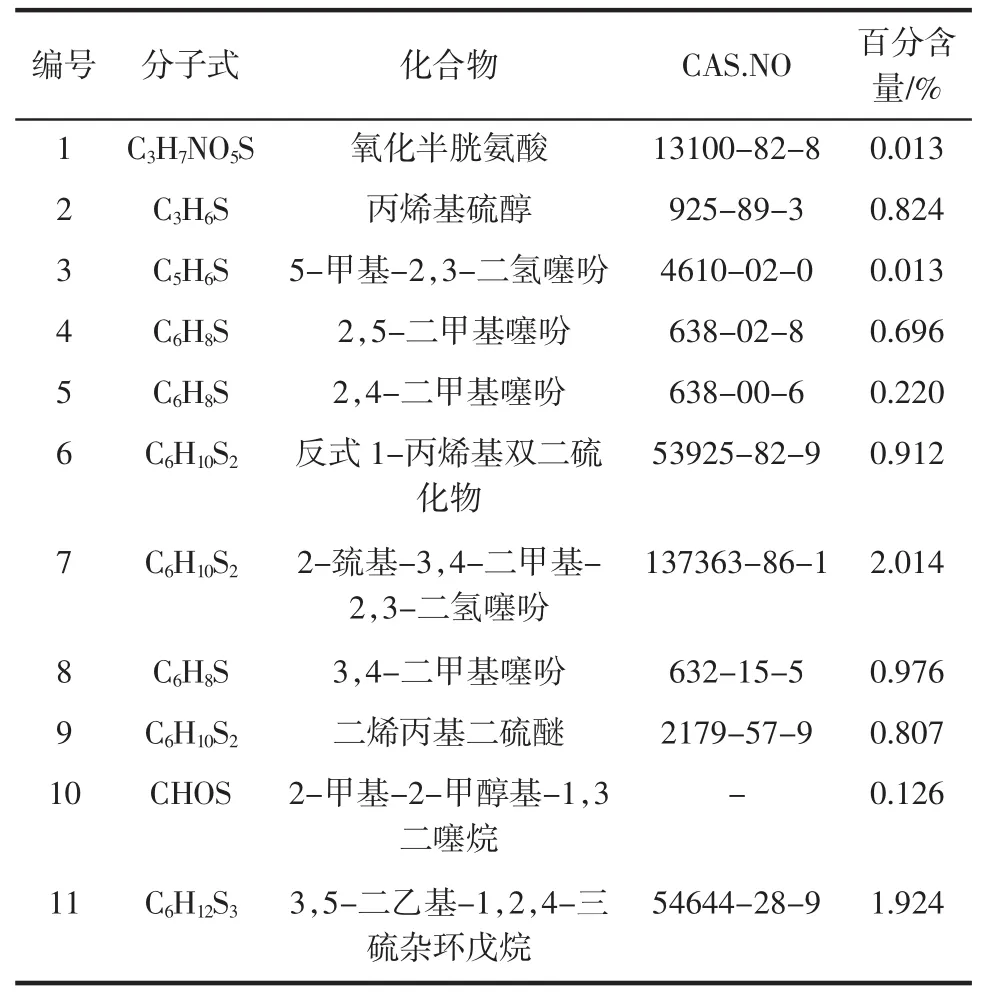
表2 主要呈味物质的质谱分析结果Table 2 The results of main flavor substance
6号色谱峰经谱库检索,分析鉴定为反式-1-丙烯基双二硫化物(trans-bis-(1-propenyl)disulfide),这是在香椿芽苗生长过程所鉴定出来的含硫化合物,也是第一次在香椿中检测出来的挥发性物质。反式-1-丙烯基双二硫化物分子质量为146.273 6,密度为1.024 g/cm3,折射率为1.557,闪点为71.3℃,在101.3 kPa下沸点为186.1℃,因而是一种不稳定的含硫化合物。此外,该化合物还存在3种同分异构体如图2。

图2 反式-1-丙烯基双二硫化物及其同分异构体Fig.2 Trans-bis-(1-proenyl)disulfide and its isomers
2号色谱峰为1-丙烯基硫醇,分子量为74.144 7,密度为0.864 g/cm3,在101.3 kPa下沸点为68.3℃。
2.2 香椿与大蒜的特征性风味物质在一定程度上存在一致性
将这11中含硫化合物与Daniela A.Locatelli等[10]所做的关于大蒜样品中含硫机化合物的结果进行对比,可以看出,香椿与大蒜十分相似,含硫化合物皆为两者特征性风味形成的关键因素。此外,结果显示,香椿挥发性物质中还含有2-巯基-3,4-二甲基-2,3-二氢噻吩及3,4-二甲基噻吩,这与E.Block等[6]提出的二巯基-克莱森重排在一定程度上极为相近,其具体反应式如图3。

图3 二巯基-克莱森重排Fig.3 Dithio-Claisen rearrangement
2号色谱峰为1-丙烯基硫醇(prop-1-ene-1-thiol),它与反式-1-丙烯基双二硫化物(a)在一定条件下可以发生转化,并可产生附属产物2-甲基噻吩、噻吩等其他物质,具体反应式如图4。

图4 反式-1-丙烯基双二硫化物转化生成1-丙烯基硫醇Fig.4 The transformation from trans-bis-(1-proenyl)disulfide to prop-1-ene-1-thiol
而2-甲基噻吩和噻吩在一定条件下又可以合成3,4-二甲基噻吩(b),产生附属产物 2,3-二甲基噻吩,具体反应式如图5。
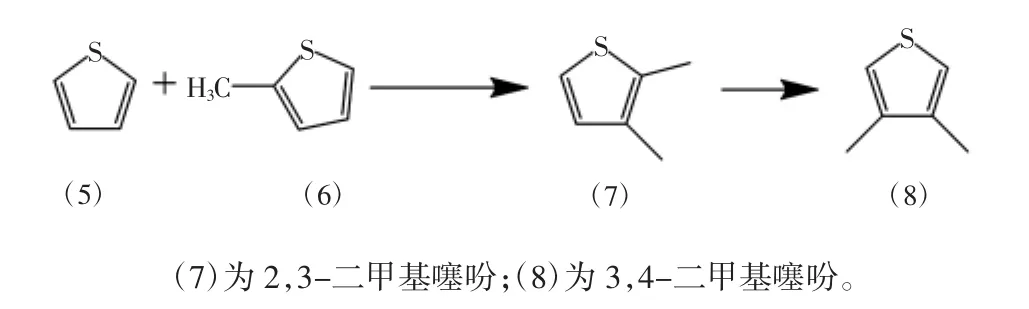
图5 2-甲基噻吩与噻吩合成3,4-二甲基噻吩Fig.5 Synthesis of 3,4-dimethythiophene from 2-methylthiophene and thiophene
关于 2-巯基-3,4-二甲基-2,3-二氢噻吩(c)的记录较少,没有发现其可以合成的路径,因而无法证明反式-1-丙烯基双二硫化物在加热的条件下可以直接转化为2-巯基-3,4-二甲基-2,3-二氢噻吩,但GCMS分析结果中却同时含有a、b、c这3种化合物,在一定程度上契合了E.Block提到的二巯基-克莱森重排。
根据表1可以看出,在对香椿嫩叶、芽苗的GCO-MS分析中,多次出现大蒜,洋葱的风味,且对其进行质谱分析过程中得到了二烯丙基二硫醚,这是大蒜中的主要物质之一,它可以与大蒜素进行相互转化。因而,又在另一方面证明了香椿与大蒜的一致性。
3 结论
通过对香椿生长过程中的芽苗进行GC-O-MS、GC-MS嗅闻分析,第一次发现香椿中含有反式-1-丙烯基双二硫化物,并在一定条件下可以转化为3,4-二甲基噻吩。此外,香椿中还含有2-巯基-3,4-二甲基-2,3-二氢噻吩,这3种物质在香椿中同时存在,这与E.Block所提到的二巯基-克莱森重排相契合。
对香椿进行嗅闻试验过程中,多次出现大蒜风味,且谱库检索得到的含硫化合物也存在于大蒜样品中,在一定程度上更加证明了香椿与大蒜的一致性。
[1] 陈丛瑾,黄克瀛,李姣娟,等.不同方法提取香椿芽挥发油的比较研究[J].分析实验室,2009,28(1):30-35
[2] 李聚英.香椿特征香气成分及其在加工、贮藏中的变化[D].北京:中国农业大学,2011
[3] 李聚英,王军,戴蕴青,等.香椿特征香气组成及其在贮藏中变化的研究[J].北京林业大学学报,2011,33(3):127-131
[4] MUR,WANGXR,LIUS X,et al.Rapid determination of volatile compounds in Toona sinensis(A.Juss)Roem By MAE-HS-SPMEFollowed by GC-MS[J].Chromatographia,2007,65(7/8):463-467
[5] Changjin Liu,Jie Zhang,Zhongkai Zhou,et al.Analysis of Volatile Compounds and Identification of Characteristic Aroma Components of Toona sinensis(A.Juss.)Roem.Using GC-MS and GC-O[J].Food and Nutrition Sciences,2013,4(3):305-314
[6] Eric Block,Shu Hai Zhao.Onion essential oil chemistry.Cis-and trans-2-mercapto-3,4-dimethyl 2,3-dihydrothiophene from pyrolysis of bis(1-propenyl)disulfide[J].Tetrahedron Letters,1992,31(35):4999-5002
[7]FALCAO L D,REVEL G D,ROSIER J P,et al.Aroma impact components of Brazilian Cabernet Sauvignon wines using detection frequency analysis(GC-olfactometry)[J].Food Chemistry,2008,107:497-505
[8] 陈丛瑾,杨国恩,袁烈江,等.HS-SPME/GC-MS法分析香椿芽、叶的挥发性化学成分[J].精细化工,2009,26(11):1080-1084
[9] 刘常金,李楠,王浩宇,等.香椿特征性风味化合物的鉴定及其生物合成机理研究[C].第三届食品感官科学国际学术研讨会论文集,2014:6
[10]Daniela A,Locatelli a b,Jorgelina C,et al.Solid phase microextraction coupled to liquid chromatography.Analysis of organosulphur compounds avoiding artifacts formation[J].Food Chemistry,2014,157:199-204
Effects of Sulfur Compounds of Toona sinensis Seedlings on the Aroma Compounds
LI Nan,WANG Hao-yu,ZHAO Fang,LIU Chang-jin*
(College of Food Engineering and Biotechnology,Tianjin University of Science and Technology,Tianjin 300457,China)
Characteristic flavor substance were condensed and analyzed by using Headspace Solid-phase Microextraction (HS-SPME)followed by Gas Chromatography-Mass Spectrometry (GC-MS)and Gas Chromatography-Olfactometry-Mass Spectomety(GC-O-MS).This research studied the chemical composition of the volatile compounds of Toona sinensis.The study got trans-bis-(1-proenyl)disulfide firstly which could transform into prop-1-ene-1-thiol and 3,4-dimethylthiophene from Toona sinensis at the growth stage.The sulfur compounds structure of Toona sinensis was similar to the Allium plants in the aspect of chemical composition,which lead to have same characteristic flavor substances between Toona sinensis and Allium plants.
Toona sinensis;characteristic flavor substance;GC-O-MS;trans-bis-(1-proenyl)disulfide
2016-09-02
李楠(1993—),女(汉),硕士研究生,食品工程专业。
*通信作者:刘常金(1969—),男(汉),副教授,博士,研究方向:农产品加工与贮藏工程。
10.3969/j.issn.1005-6521.2017.13.008
