不同比例PLLA/PDLLA/5%HA复合物体外降解性能的研究
2017-07-01徐高祥张鲁鲁高华丽金志恩
徐高祥,张鲁鲁,高华丽,杨 雪,姜 秋*,金志恩
(1.吉林大学口腔医院 儿童口腔科 吉林 长春130021;2.吉林省牙发育及颌骨重塑与再生重点实验室 吉林 长春130021)
不同比例PLLA/PDLLA/5%HA复合物体外降解性能的研究
徐高祥1,2,张鲁鲁1,高华丽1,杨 雪1,姜 秋1,2*,金志恩1
(1.吉林大学口腔医院 儿童口腔科 吉林 长春130021;2.吉林省牙发育及颌骨重塑与再生重点实验室 吉林 长春130021)
目前,乳牙残冠残根的修复治疗方法主要有常规的充填修复,金属预成冠及前牙透明冠、短桩修复等,而最近可吸收乳牙根管桩成为国内外学者的研究热点。而聚乳酸(polyactic acid,PLA)因其具有良好的生物相容性、降解性和无毒性[1],且易于加工成型[2]已经成为应用于生物医学的可降解材料的首选聚合物。聚乳酸存在三种立体构型,即:聚左旋乳酸(PLLA),聚右旋乳酸(PDLA)聚消旋乳酸(PDLLA)。其中PLLA和PDLA是两种具有光学活性的规则立构型聚合物,分子链排列比较规整,有较高的结晶度和机械强度,而PDLLA是无定形非晶态材料,具有良好的生物相容性和可吸收性[3]。由于PLLA具有易结晶及结晶度较高的特点,用 PLLA 制备的试件脆性高,物理性能不理想,而作为植入材料在体内降解时产生的乳酸易引发炎症,同时还具有x-射线下不显影等缺陷[4],因此,单纯将PLLA作为乳牙根管桩的材料并不理想。羟基磷灰石(HA),因其晶体结构与自然骨无机成分相似,能够与人体细胞膜表层蛋白质和多糖以氢键结合[5],还具有抗菌、抑菌性及良好的细胞黏附特性,目前是口腔医学中最常用的生物陶瓷材料。本课题组之前将PLLA与HA混合,通过溶液共混法和热压成型法制备PLLA/HA复合材料,得出HA质量分数为5%的PLA/HA复合物具有最优的力学性能,并且符合生物安全性要求。
另外,乳牙牙根生理性吸收一般为2-4年,但PLLA因其纤维结构较规整,具有较高的结晶度(83.5%),因此降解时间长,一般完全降解为2-6年,若使用单纯PLLA作为可吸收乳牙根管桩,不能完全满足与乳牙根同步吸收的要求,而非晶态的PDLLA降解速度较PLLA快的多[6]。因此,在保证力学性能的基础上,本实验将PDLLA与PLLA、HA按一定的比例共混复合来调控复合物的降解速度,以期找到一种合适的复合物比例,实现与乳牙牙根生理性吸收的同步。
1 材料与方法
1.1 主要材料与仪器
PLA-5%HA(质量分数PLLA:PDLLA为80:15,75:20,70:25)板块(上海丽昂化学有限公司合成),规格为50 mm*10 mm*4 mm;JF1004电子分析天平(跃平科学仪器有限公司,上海);电热恒温培养箱(科伟实验仪器有限公司,北京);冷场发射扫描电子显微镜(日本电子株式会社);便携PH计(哈纳,意大利);万能材料试验机(岛津公司,香港);X线多晶衍射仪(日本理学电子株式会社);DZF-6050真空恒温干燥箱(新诺仪器设备有限公司,上海);凝胶渗透色谱仪(岛津公司,香港)。
1.2 实验方法
1.2.1 磷酸盐缓冲液(PBS)中降解 将准确称取质量后的三种比例PLLA/PDLLA/5%HA及单纯PLLA试件放入盛有50 ml PBS(pH约为7.4,浓度为0.1 mol/L)的试管中,每个试管中放入1个试件,置于(37℃±1℃)的恒温箱中,每组设3个平行组,每1周更换一次PBS液,保持pH值恒定,分别于2,4,6,8,10个月取出试件,用滤纸吸去试件表面的水分后,真空干燥至恒重。
非缓冲溶液中降解 将准确称取质量后的三种比例PLLA/PDLLA/5%HA及单纯PLLA试件放入盛有50 ml蒸馏水(pH为6.4)的试管中,每个试管中放入1个试件,置于(37℃±1℃)的恒温箱中,每组设3个平行组,分别于相同时间点测定浸泡液体的pH值。
1.2.2 试件大体观察 取出不同时间点的试件,肉眼观察试件表面形态,色泽以及透明度的变化。
1.2.3 SEM形貌分析 将不同时间点取出的试件断口喷金,进行扫描电镜分析,与材料的原始形貌对比,观察材料的降解情况。
1.2.4 分子量测定并计算降解率 取出不同时间点的试件干燥至恒重,以氯仿为溶剂,采用GPC仪来测定试件的重均分子量(Mw)。将降解前试件的分子量记为Mw0,降解后的分子量记为Mwn。
降解率=(Mw0-Mwn)/Mw0*100%
1.2.5 力学性能测试 将不同时间点的试件利用电子万能试验机进行三点弯曲测定,跨距为40 mm,加载速度为1 mm/s,测得试件的最大断裂力值,并计算出其弹性模量及弯曲强度。
1.3 统计学方法
采用SPSS17.0统计学软件对数据进行统计学分析,以P<0.05为差异有统计学意义。
2 结果
2.1 试件大体观察
纯PLLA初始呈近透明状,光泽度良好[图1(B1)],PLA/HA复合材料呈乳白色,光泽度良好且不透明[图1(A1、C1、D1)];2个月后,复合材料表面开始变白,变白程度70%PLLA-25%PDLLA-5%HA>75%PLLA-20%PDLLA-5%HA>80%PLLA-15%PDLLA-5%HA,而单纯PLLA在第4个月时开始部分变白且透明度变低[图1(B3)]。70%PLLA-25%PDLLA-5%HA复合材料在第6个月、75%PLLA-20%PDLLA-5%HA复合材料在第8个月时,基本上完全变成了白色,表面稍变粗糙,并出现少量微裂纹[图1(C4、D5)];10个月时,80%PLLA-15%PDLLA-5%HA复合材料完全变白,出现裂纹,而75%PLLA和70%PLLA组复合材料表面逐渐开始剥脱;纯PLLA完全变白,失去光泽。[图1(A6、C6、D6、B6)]。
2.2 扫描电镜形貌分析
PLLA/PDLLA/5%HA复合物的初始形貌[图2(D、G、J)],可见到HA微球直径约为5 μm,与PLA结合紧密,结合界面良好,但断面有片层错落的现象,是一种脆性断裂。4个月时[图2(E、H、K)]可见部分HA包裹在基质中,部分颗粒从基质断面脱落,HA颗粒降解变小,直径约为2.5 μm,复合材料断面开始出现大小较为均一,直径约为1 μm的孔隙;纯PLLA[图2(B)]由于自身降解作用,断口表面也出现大量大小不等的孔隙,且呈明显的不规则形。到第10个月时,纯PLLA和80%PLLA-15%PDLLA-5%HA材料断面[图2(C、F)]空隙变大,数量较4月份时的更多;75%PLLA-20%PDLLA-5%HA和70%PLLA-25%PDLLA-5%HA复合材料[图2(I、L)]断口表面出现许多絮状物,逐渐无成型的聚乳酸结构。

A为80%PLLA-15%PDLLA-5%HA复合物大体观察,B为单纯PLLA大体观察,C为75%PLLA-20%PDLLA-5%HA复合物大体观察,D为70%PLLA-25%PDLLA-5%HA复合物大体观察
图1 试件大体观察
2.3 PLA/HA复合物与PLA力学性能的变化
图3、4显示,初始状态下各组的弹性模量、弯曲强度接近,70%PLLA-25%PDLLA-5%HA最小。随着降解时间的延长,各组PLLA/PDLLA/5%HA复合物与单纯PLLA的弹性模量均有所衰减。在第8个月之前,80%PLLA-15%PDLLA-5%HA和75%PLLA-20%PDLLA-5%HA的弹性模量、弯曲强度一直高于单纯PLLA,8个月之后,各组PLLA/PDLLA/5%HA复合物的弹性模量、弯曲强度均开始大幅度下降,第10个月时,70%PLLA-25%PDLLA-5%HA已经失去强度。而单纯PLLA弹性模量始终以一个较为一致速度的衰减。
2.4 分子量测定及生物降解率
各组PLLA/PDLLA/5%HA和单纯PLLA的初始重均分子量差别不是很大,单纯PLLA略高于PLLA/PDLLA/5%HA复合物。前4个月单纯PLLA的分子量下降较PLLA/PDLLA/5%HA略快。4个月后,各组材料的生物降解率均开始变快,8个月后PLLA/PDLLA/5%HA复合物的降解率开始变慢,但单纯PLLA总体降解速度较为一致。降解10个月时,单纯PLLA的降解率为70.5%,80%PLLA-15%PDLLA-5%HA为79.6%,75%PLLA-20%PDLLA-5%HA和70%PLLA-25%PDLLA-5%HA的降解率达到了90%左右。
2.5 PLLA/PDLLA/5%HA复合物及单纯PLLA非缓冲液pH的变化
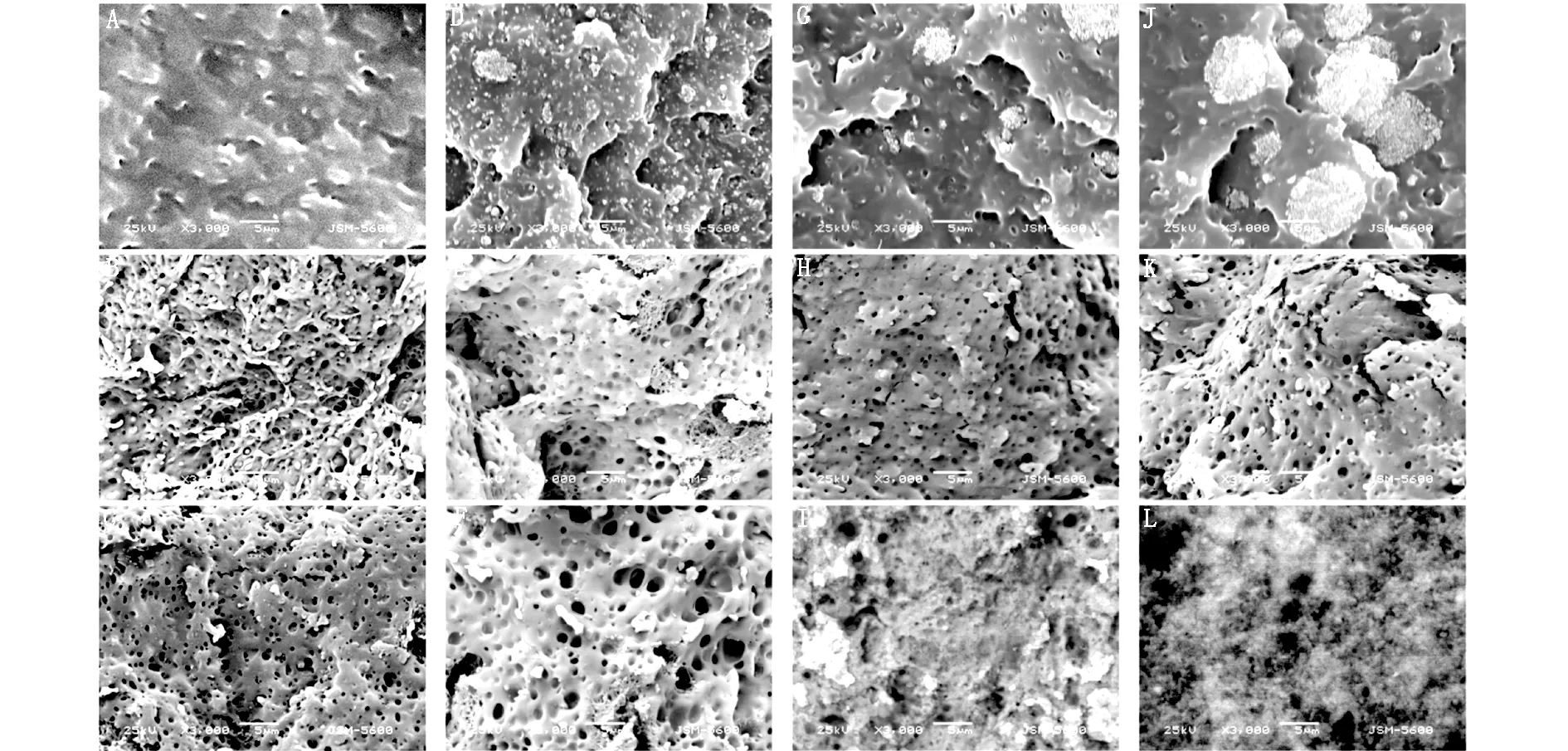
A、B、C为纯PLLA原始形貌及降解4个月、10个月形貌;D、E、F为80%左旋聚乳酸复合物初始形貌及降解4个月、10个月形貌;G、H、I为75%左旋聚乳酸复合物初始形貌及降解4个月、10个月形貌;J、K、L为70%左旋聚乳酸复合物初始形貌及降解4个月、10个月形貌
图2 PLLA/PDLLA/5%HA复合物与PLA断口形貌.SEM (*3000)
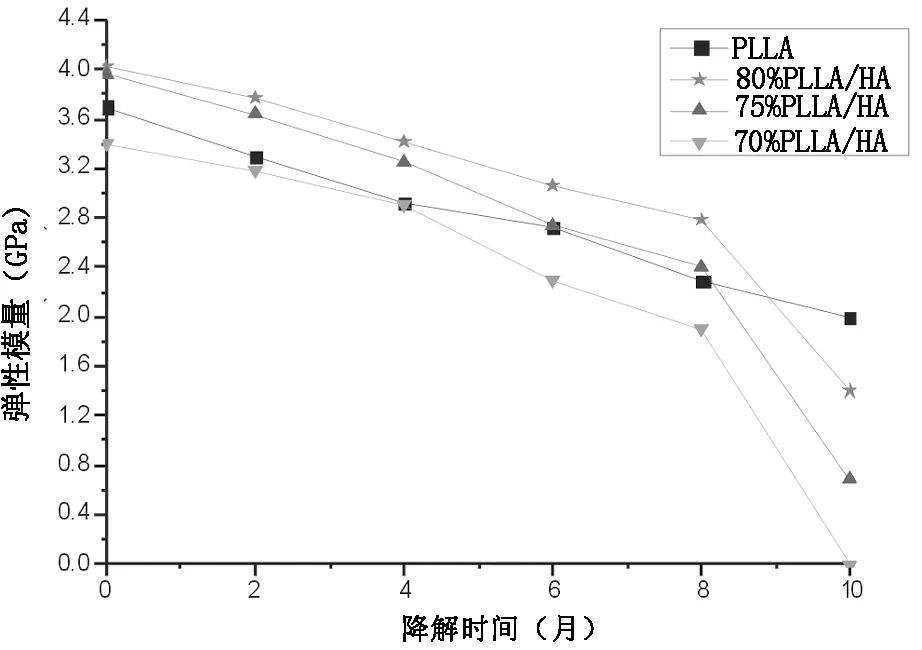
图3 PLLA/PDLLA/5%HA复合物与PLA弹性模量随时间变化
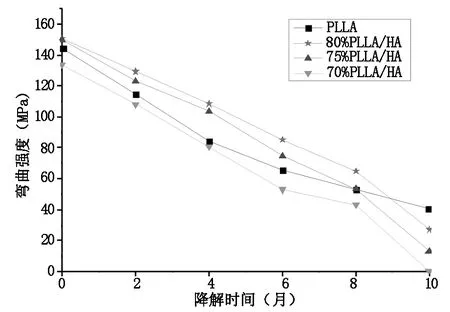
图4 PLLA/PDLLA/5%HA复合物与PLA弯曲强度随时间变化
由图5可见,在整个体外降解过程中,PLLA/PDLLA/5%HA复合物及单纯PLLA的pH值曲线均呈倒“S”形,4个月以前,各组均下降缓慢,但单纯PLLA的pH下降比PLLA/PDLLA/5%HA复合物略快;5-7个月,四组pH值均开始明显下降,且单纯PLLA的pH值比PLLA/PDLLA/5%HA复合物降低更为显著;7-10个月时,四组的pH下降趋于平缓。
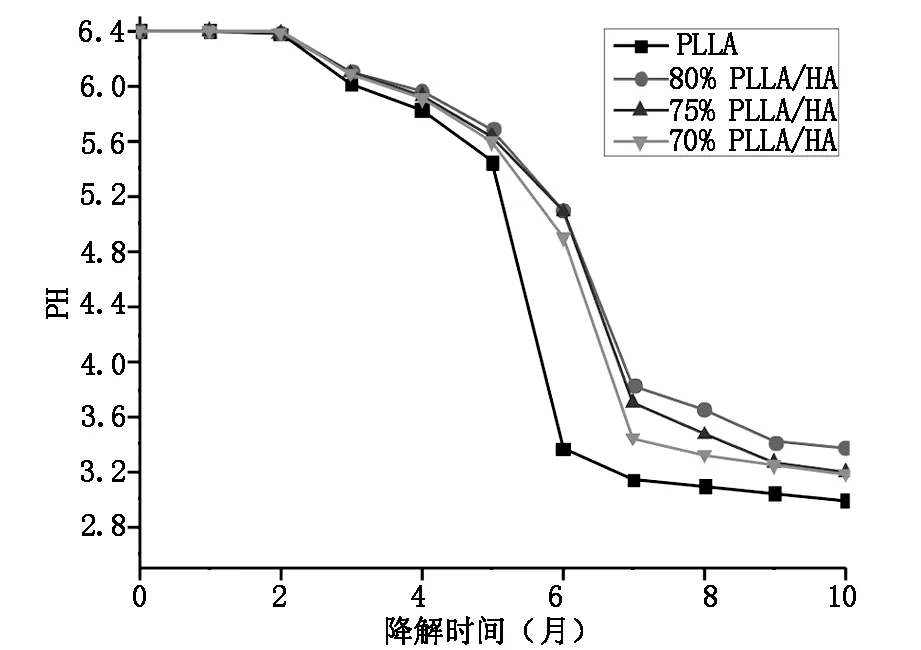
图5 降解液pH值随时间的变化
3 讨论
目前,因聚乳酸具有良好的生物相容性、降解性和无毒性,且易于加工成型,已经广泛作为生物医学可降解材料的首选聚合物,为实现能与乳牙牙根同步吸收的修复方法提供了思路。如果单独采用左旋聚乳酸(PLLA),因其结晶度高(83.5%),降解时间较长,一般完全降解需要2-6年,无法满足乳牙牙根生理性吸收的要求。而非晶态的外消旋聚乳酸(PDLLA)降解速度较PLLA快的多。因此本实验在保证力学性能的基础上,将PDLLA与PLLA、HA按一定的比例共混来调控复合物的降解速度,寻找与乳牙根同步吸收的混合比。
聚乳酸的降解主要分为吸水、酯键断裂、可溶性寡聚物扩散和碎片溶解的4个过程。通过水解作用可造成酯键的水解,高分子链发生断裂,降解为乙醇酸和乳酸进入三羧酸循环,最终代谢为CO2和水而排出[7]。随着观察时间的延长,我们发现PLLA/PDLLA/5%HA复合物中部分HA颗粒从基质断面脱落,基质表面出现了细小的空隙,水分子可能会通过这些孔隙进入材料的内部,催化水解反应。而且,有学者认为聚乳酸的降解是由于分子链端羧基引起的自催化水解,材料吸水后,PLA分子链上的酯键发生水解逐渐断裂,从而造成末端羧基基团的增多,可导致局部pH降低[8]。
我们看到前4个月,各组pH均下降缓慢,且分子量的变化也相对较缓,降解率相差不大。这可能是因为,前4个月水分子只是通过亲水力或其他作用力与聚乳酸结合,而未改变聚乳酸的化学结构。而这一阶段,单纯PLLA的pH值和分子量的下降比PLLA/PDLLA/5%HA复合物略快。究其原因,一方面可能是由于HA在中性介质中的溶解度很低[9],复合材料表面均匀分布着HA微粒阻挡了部分水分子向材料内的扩散 ,延缓了材料水解的速度[10];另一方面,随着材料的降解,HA在酸性环境中的溶解度逐渐增加,并有轻度Ca2+析出,Ca2+与聚合物的链端羧基形成离子键,自由链端羧基浓度减少[11],PLA的自催化速度有所抑制,降低了材料内部降解物质的自催化反应,同时对周围的酸性产物起到了一定的缓冲,同时这也是PLLA/PDLLA/5%HA组的pH始终高于单纯PLLA组的原因。在第5-7个月时,各组介质中的pH值均开始明显的下降,而7个月后,四组的pH均趋于稳定。这可能是因为PLA发生了酯的水解作用,分子链发生断裂,引起了低聚物和乳酸单体的浓度逐渐增加,7个月后PLA酯键断裂趋势有所下降,所释放的乳酸单体的浓度变化不大,从而使得pH下降幅度有所减缓[12]。HA与PLLA/PDLLA降解时的协同效应导致了单纯PLLA及PLLA/PDLLA/5%HA复合物的分子量、降解率和pH在降解过程中呈现出不均匀的状态。
本实验中80%PLLA-15%PDLLA-5%HA的初始弯曲强度为150.5MPa、75%PLLA-20%PDLLA-5%HA为149.9MPa、70%PLLA-25%PDLLA-5%HA为133.6MPa、纯PLLA为144.2MPa,均高于ISO4049标准中的复合树脂标准的弯曲强度80MPa,表明初始状态的PLLA/PDLLA/5%HA复合材料及纯PLLA的强度可以满足临床中残根残冠修复的抗折性要求。有研究表明[6,13],PDLLA质量分数<20%时PDLLA与PLLA共聚物的结晶度变化不大,但高于20%后结晶度则迅速降低;同时HA的加入也会影响PLA的结晶度,引起分子量的下降。复合材料的力学强度会随着PDLLA质量分数的增加迅速减小(由图3、4 可看出),本实验中随着PDLLA含量的增多,复合物力学性能的下降速度也相对变快。前8个月,80%PLLA-15%PDLLA-5%HA和75%PLLA-20%PDLLA-5%HA的弯曲强度和弹性模量均高于单纯PLLA,而70%PLLA/HA因其PDLLA的含量高,结晶度低导致降解速度较快,很快失去强度。HA的加入,延缓了复合材料早期的降解速度,有利于材料初始强度的保持[13]。威廉[14]等认为理想的根管桩材料应与牙本质的机械性能相似,PLLA/PDLLA/5%HA与单纯PLLA初期的弯曲强度与牙本质(102-138 MPa)较为接近,而弹性模量3.3~4.3GPa与牙本质(12-18GPa)仍存在不少差距。根据力学原理,当外力作用于一个复合体时,力总是从弹性模量高的材料向弹性模量低的材料传递,聚乳酸根管桩材料比牙本质的弹性模量小,可减少应力集中,使根管治疗后脆性变大的牙齿不易折断[15]。据文献记载[16,17]3-5.5岁儿童的咬合力为213.17±43.97N,牙合接触面积为129.52±31.12 mm2,计算得出乳牙单位面积的最大力约为2.61 MPa。降解10个月后,除了70%PLLA-25%PDLLA-5%HA组失去力学强度外,其他三组最低值为12.63 MPa仍大于2.61 MPa(乳牙单位面积最大力),说明降解10个月后的聚乳酸材料若应用于乳牙根管可以承受儿童的最大咬合力。这仅是我们观察了10个月的PLA/HA复合物的体外降解行为,根据其弯曲强度和弹性模量曲线来推测达到乳牙的最大咬合力值仍需很长一段时间,由此可看出PLLA/PDLLA/5%HA复合物可以成为理想的乳牙根管桩材料。
通常,可降解材料在体内降解时除了材料自身的降解作用,还会受到体内细胞、酶、机械应力等对材料的介导作用,因而材料在体内降解的速度可能会较体外更快。而本实验所研究的聚乳酸乳牙根管桩的应用环境是相对干燥的根管腔,因此复合材料的降解速度会较体外实验时缓冲液中的速度更慢。本实验的结果显示,单纯PLLA虽然在十个月的时间内力学性能下降不大,但是根据降解曲线分析,待其完全降解仍需很长时间,可能很难满足乳牙牙根同步吸收的要求;70%PLLA-25%PDLLA-5%HA的复合体材料降解速度最快,十个月的时间已经失去其力学性能,不能耐受咬合力的作用;75%PLLA-20%PDLLA-5%HA复合材料虽然降解速度较70%PLLA-25%PDLLA-5%HA更慢,但是其力学性能也维持不了更长的时间;而80%PLLA-15%PDLLA-5%HA的降解速度适中,力学性能维持的时间相对更久。因此,80%PLLA-15%PDLLA-5%HA复合物为能够满足乳牙牙根生理性吸收的理想根管桩材料的研究提供了方向。但是,其究竟能否真正实现与乳牙牙根吸收的同步还有需要进一步的体内实验。
[1]Lee BK,Yun Y,Park K.PLA Micro-and Nano-Particles[J].Advanced Drug Delivery Reviews,2016,42:105.
[2]Lopes MS,Jardini AL,Maciel FR.Poly(lactic acid) production for tissue engineering applications[J].Procedia Engineering,2012,42:1402.
[3]李延红.可降解聚乳酸/羟基磷灰石有机无机杂化材料的制备及性能研究[D].合肥工业大学,2005.
[4]Yanagida H,Okada M,Masuda M,et al.Cell adhesion and tissue response to hydroxyapatite nanocrystal-coated poly(l-lactic acid) fabric[J].Journal of Bioscience & Bioengineering,2009,108(3):235.
[5]Kalita SJ,Bhardwaj A,Bhatt HA.Nanocrystalline calcium phosphate ceramics in biomedical engineering.Materials Sci Eng C,2007,27:441.
[6]廖凯荣,全大萍,高建文,等. PLLA/PDLLA共混物的力学性能及体外降解特性研究[J]. 中山大学学报自然科学版,2002,41(1):51.
[7]Lee JB,Ko Y G,Cho D,et al.Modification of PLGA nanofibrous mats by electron beam irradiation for soft tissue regeneration[J].Journal of Nanomaterials,2015,20(3):405.
[8]babu Valapa R,Pugazhenthi G,Katiyar V.Hydrolytic degradation behaviour of sucrose palmitate reinforced poly (lactic acid) nanocomposites[J].International journal of biological macromolecules,2016,89:70.
[9]Nair NR,Sekhar VC,Nampoothiri KM.Augmentation of a Microbial Consortium for Enhanced Polylactide (PLA) Degradation[J].Indian Journal of Microbiology,2016,56(1):59.
[10]Furukawa T,Matsusue Y,Yasunaga T,et al.Biodegradation behavior of ultra-high-strength hydroxyapatite/poly (L-lactide) composite rods for internal fixation of bone fractures[J].Biomaterials,2000,21(9):889.
[11]Cai K,Yao K,Lin S,et al.Poly(D,L-lactic acid) surfaces modified by silk fibroin:effects on the culture of osteoblast in vitro.[J].Biomaterials,2002,23(4):1153.
[12]黄福龙,戴红莲,方 园,等.HA/PDLLA 复合材料的制备及其降解性能研究[J]. 无机材料学报,2007,22(2):333.
[13]全在萍,李世普.聚DL—丙交酯/羟基磷灰石(PDLLA/HA)复合材料(Ⅰ):制备及力学性能[J].中国生物医学工程学报,2001,20(6):485.
[14]Cheung W.A review of the management of endodontically treated teeth:post,core and the final restoration[J].The Journal of the American Dental Association,2005,136(5):611.
[15]Goto Y,Nicholls J I,Phillips K M,et al.Fatigue resistance of endodontically treated teeth restored with three dowel-and-core systems[J].The Journal of prosthetic dentistry,2005,93(1):45.
[16]陈爱华,黄 华.聚乳酸可吸收根管桩修复残根后的抗折力研究[J].牙体牙髓牙周病学杂志,2014(10):592.
[17]王亚林,朱 玲,张静露.儿童牙合接触面积及牙合力的研究[J].中国儿童保健杂志,2006,14(6):637.
吉林省工信厅项目(编号:2013220101000394)
*通讯作者
1007-4287(2017)06-1067-05
徐高祥(1990-),男,硕士,主要从事儿童口腔医学研究工作。
2016-11-14)
