流动注射化学发光法测定利福喷丁
2017-06-29张琰图
徐 通,张琰图,张 绪
(延安大学 化学与化工学院,陕西 延安 716000)
实验技术
流动注射化学发光法测定利福喷丁
徐 通,张琰图*,张 绪
(延安大学 化学与化工学院,陕西 延安 716000)
基于碱性介质中利福喷丁能增敏鲁米诺-铁氰化钾体系的化学发光这一现象,结合流动注射分析技术,建立了流动注射化学发光法测定利福喷丁的新方法。在最佳实验条件下,利福喷丁检测浓度的线性范围为0.008~0.88 mg/L,检出限(3σ)为1.2×10-3mg/L。对6.0×10-2mg/L的利福喷丁进行平行测定,其相对标准偏差(RSD,n=11)为1.9%。该方法已用于测定胶囊和血浆中利福喷丁的含量,结果满意。
流动注射;化学发光;鲁米诺;铁氰化钾;利福喷丁
利福喷丁(Rifapentine,RFT)是一种利福霉素衍生物,在血液中具有较长的半衰期,与利福平相比,其抗结核分枝杆菌性更强[1-2],加之用药频率少且疗效显著,在临床上广泛用于结核病的治疗,在动物模型中也显示出良好的治疗潜伏性结核病的前景[3-5]。但该药具有肝肾毒性,尤其损害肝功能,过量或长期服用还可能导致贫血、脱发等症状[6],故建立此药品含量的简单、快速、灵敏的检测方法十分必要。
目前测定RFT的主要方法有高效液相色谱(HPLC)法[7]、反相高效液相色谱(R-HPLC)法[8]、液相色谱-质谱联用(LC-MS)法[9]以及薄层色谱-紫外分光(TLC-UV)法[10]等。其中,HPLC法样品处理复杂且仪器价格昂贵,且其流动相中的非挥发性缓冲盐很难去除,导致LC-MS 联用技术的应用受到限制;TLC-UV法虽仪器设备简单,测定结果较为准确,但灵敏度低,操作繁琐[11]。流动注射化学发光法(FI-CL)作为流动注射技术与化学发光相结合的一种新的分析方法[12],因分析成本低、分析速度快、灵敏度高、操作简单,近年来被广泛应用于医药[13]、环境[14]、食品[15]等各个领域。
研究发现,在碱性介质中,RFT的加入能明显增强鲁米诺-铁氰化钾体系的化学发光,且RFT在一定质量浓度范围内与增强的化学发光强度呈良好的线性关系。本文结合流动注射分析技术,建立了一种测定利福喷丁含量的新方法。本方法线性范围宽,检出限较文献 [7]降低了1 000倍,已成功应用于药物胶囊和人血浆中RFT含量的分析。
1 实验部分
1.1 仪器与试剂
IFFM-E型流动注射化学发光分析仪(西安瑞迈公司);AUY220分析天平(日本岛津公司);KQ-250B型超声波清洗器(上海精密仪器仪表有限公司);H1650台式高速离心机(湖南湘仪实验室仪器开发有限公司);F-4500荧光分光光度计(日本日立公司);8453型紫外-可见分光光度计(美国安捷伦公司)。
RFT(中国药品生物制品检定所)标准溶液(0.1 g/L):准确称量10.0 mg RFT标准品于烧杯中,加适量甲醇溶解后用水定容至100 mL容量瓶中,摇匀后置于冰箱中4 ℃储存备用,使用时逐级稀释至所需浓度。
Luminol储备液(0.01 mol/L ):称取0.443 0 g鲁米诺固体,用0.1 mol/L NaOH溶解后加水定容至250 mL棕色容量瓶中,置于冰箱中4 ℃下保存,避光放置1周后使用。
K3Fe(CN)6储备液(0.01 mol/L):称取0.329 3 g铁氰化钾固体,用水溶解并定容至100 mL 棕色容量瓶中,使用时逐级稀释。
本实验所用试剂均为分析纯,实验用水为二次蒸馏水。

图1 流动注射化学发光分析法测定RFT流路图Fig.1 Schematic diagram of the flow injection chemilumine-scence determination of RFTP1,P2:peristaltic pump;V:sample valve;F:flow cell;PMT: photomultiplier;PC:computer;W:waste;a:carrier(water); b:K3Fe(CN)6;c:luminol;d:NaOH
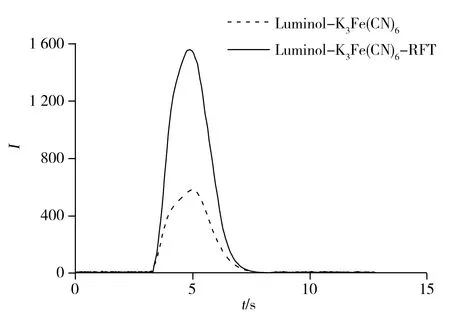
图2 化学发光动力学曲线Fig.2 Kinetic curves of CL reactions c(luminol)=1.0×10-4 mol/L;c[K3Fe(CN)6]=5.0×10-5 mol/L;c(NaOH)=0.4 mol/L;ρ(RFT)=1.0 mg/L
1.2 实验方法
启动流动注射分析系统,将各溶液按图1所示分别泵入相应管道,待基线稳定后,注入样品溶液。溶液经六通阀(V)混合,在流通池(F)发生反应,产生的化学信号经光电倍增管(PMT)放大检测,以相对发光强度(ΔI=IS-I0)进行定量分析。其中I0为未加入样品时的化学发光强度,IS为加入样品后的化学发光强度。
2 结果与讨论
2.1 化学发光动力学曲线
图2为Luminol-K3Fe(CN)6和Luminol-K3Fe(CN)6-RFT混合液的化学发光动力学曲线。从图中可以看出,RFT的加入可使Luminol-K3Fe(CN)6体系的发光强度明显增强3倍左右。
2.2 实验条件的选择
2.2.1 反应物混合方式的选择 实验发现,反应物的混合方式会对化学发光强度产生一定影响,为了使RFT对Luminol-K3Fe(CN)6体系的增敏程度最大,考察了以下3种进样方式的影响:①[RFT+K3Fe(CN)6]+(Luminol+NaOH);②(RFT+NaOH)+[Luminol+K3Fe(CN)6];③(RFT+Luminol)+[NaOH+K3Fe(CN)6]。结果表明,第1种进样方式获得的相对发光强度最大,因此实验选择第1种混合进样方式。
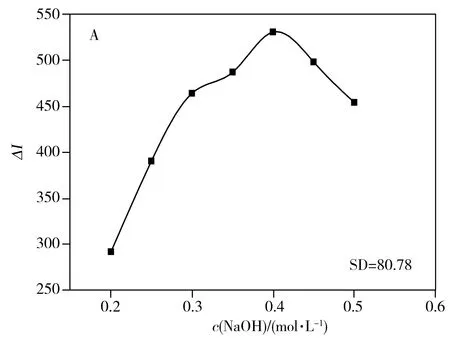
2.2.2 试剂浓度及流速的选择 对该体系所用试剂的浓度及流速进行了优化。对于NaOH溶液,固定K3Fe(CN)6浓度为5.0×10-5mol/L,Luminol浓度为4.0×10-4mol/L,配制0.2~0.5 mol/L范围内的一系列NaOH溶液,观察ΔI的变化。发现随着NaOH浓度的增大,ΔI也增大,当NaOH浓度达到0.4 mol/L时,ΔI最大。此后,ΔI随NaOH浓度的继续增大而减小(图3A)。因此实验选择NaOH的最佳浓度为0.4 mol/L。
K3Fe(CN)6作为本反应的氧化剂,其浓度会对发光强度产生一定影响。考察了K3Fe(CN)6浓度为1.0×10-5~1.5×10-4mol/L时ΔI的变化,结果发现,ΔI随K3Fe(CN)6浓度的增大而增大,当K3Fe(CN)6浓度超过5.0×10-5mol/L时,ΔI迅速减小,见图3B。这可能是由于铁氰化钾本身有颜色,会吸收光辐射[16]所致。因此选择K3Fe(CN)6浓度为5.0×10-5mol/L。
Luminol作为应用最广泛的化学发光试剂[17],其浓度对化学发光强度具有很大影响。实验考察了Luminol浓度在1.0×10-5~1.4×10-4mol/L范围时对ΔI的影响,发现当Luminol浓度增大到1.0×10-4mol/L时,ΔI也增至最大,继续增大其浓度ΔI反而减小。因此选择Luminol的最佳浓度为1.0×10-4mol/L。
由于试剂流速决定溶液中发光部分在光电倍增管的停留时间和扩散情况[18],因此改变试剂的流速也会对化学发光强度产生一定的影响。考察了试剂流速在0.8~3.2 mL/min 范围内时ΔI的变化,结果显示当流速低于2.4 mL/min时,ΔI随着流速的增大而增大,当流速高于2.4 mL/min时,ΔI开始减小,因此选择最佳流速为2.4 mL/min。
2.3 线性范围、精密度与检出限
在优化实验条件下,配制了一系列不同浓度的RFT溶液,发现RFT的质量浓度(ρ,mg/L)在0.008~0.88 mg/L范围内与相对化学发光强度(ΔI)呈良好的线性关系,其回归方程为ΔI=752.94ρ+81.01,r=0.992 4。对6.0×10-2mg/L的RFT标准溶液连续平行测定11次,计算得到其相对标准偏差(RSD)为1.9%。根据IUPAC建议,计算得本法的检出限(3σ)为1.2×10-3mg/L。
2.4 干扰实验
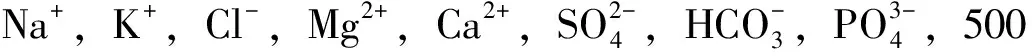
2.5 样品的测定
取同一批次的利福喷丁胶囊10粒,于研钵中研磨混匀后,准确称取相当于0.15 g的利福喷丁药粉,加适量甲醇溶解后定容至100 mL容量瓶中,充分摇匀并过滤,得到一定浓度的样品溶液。按照“1.2”方法,将其稀释至线性范围内进行加标回收试验以检测该方法的准确性。计算表明:胶囊中的回收率为98.6%~103.7%,相对标准偏差(RSD)为1.2%~2.8%(表1)。
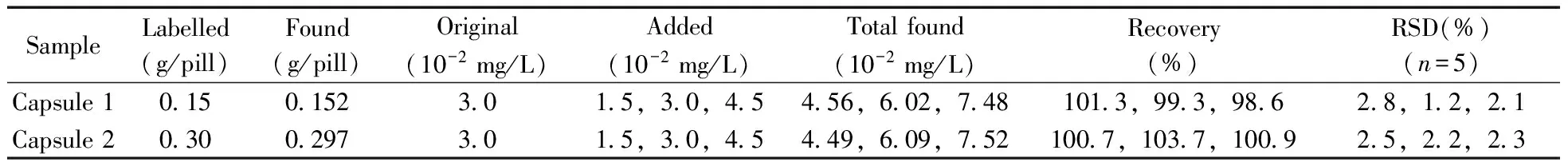
表1 胶囊中RFT的测定结果
实验所用健康志愿者血浆购于延安大学附属医院,吸取高、中、低3个不同浓度的RFT标准溶液加入3个等量的血浆样品中,均加入2 mL乙腈沉淀蛋白,振摇,放入离心机离心10 min(3 000 r/min)后,取上清液用N2流吹干,复溶后用水稀释到线性范围内进行分析,结果见表2。从表2可以看出,血浆中利福喷丁的回收率为99.6%~102.0%,表明此法可用于血浆中利福喷丁的测定。
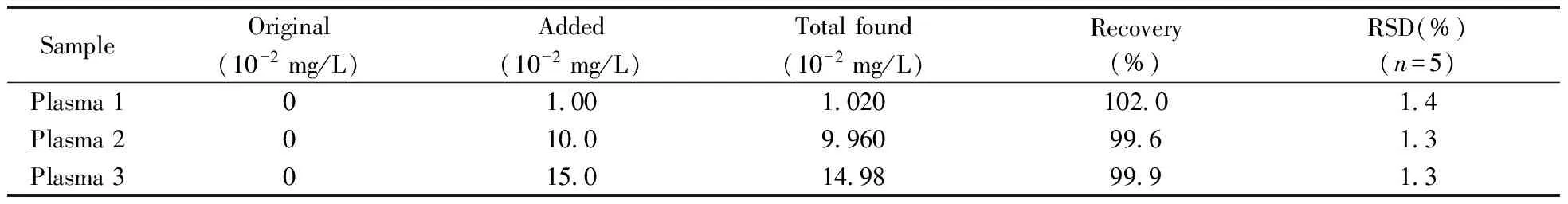
表2 血浆中RFT的测定结果
3 结 论
本文基于碱性介质中利福喷丁能增敏鲁米诺-铁氰化钾体系的化学发光,利用流动注射技术,提出了一种简单、快速测定利福喷丁的新方法。通过测定胶囊及人血浆中利福喷丁的含量,表明该方法准确、灵敏度高,有望进一步应用于临床上利福喷丁的血药浓度监测。
[1] Rosenthal I M,Williams K,Tyagi S,Peloquin C A,Vernon A A,Bishai W R,Grosset J H,Nuermberger E L.Am.J.Respir.Crit.Care.Med.,2006,174:94-101.
[2] Zvada S P,Van Der Walt J S ,Smith P J,Fourie B,Roscigno G,Mitchison D,Simonsson U S H,McIlleron H M.Antimicrob.AgentsChemother.,2010,54(8):3390-3394.
[3] Guo C B.Pro.Clin.Med.(郭存炳.临床医药实践),2016,25(5):341-343.
[4] Winchester L C,Podany A T,Baldwin J S,Robbins B L,Fletcher C V.J.Pharm.Biomed.Anal.,2015,104:55-61.
[5] Sterling T R,Villarino M E,Borisov A S,Shang N,Gordin F,Bliven-Sizemore E,Hackman J,Hamilton C D,Menzies D,Kerrigan A,Weis S E,Weiner M,Wing D,Conde M B,Bozeman L,Horsburgh C R,Chaisson R E.NewEngl.J.Med.,2011,365(23):2155-2166.
[6] Huang B Y,Deng L D.Chin.Pharm.(黄必义,邓立东.中国药师),2005,8(2):129-131.
[7] Wang Y Z.Str.Pharm.J.(王勇忠.海峡药学),2002,14(3):26-27.
[8] Xia Z G.GuangZhouMed.(夏志高.广州医药),2010,41(2):59-61.
[9] An J,Dong Z J,Zhang X D,Liu H T.Chin.J.Pharm.Anal.(安静,董占军,张笑丹,刘洪涛.药物分析杂志),2016,36(2):208-216.
[10] Editorial Committee of the Pharmacopeia of the People's Republic of China.ThePharmacopeiaofPeople'sRepublicofChina(PartⅡ).Beijing:ChemicalIndustryPress(中华人民共和国药典委员会.中华人民共和国药典.2部.北京:化学工业出版社),1995:300-302.
[11] Zhang J X,Wang X Y,Tang K H.Chin.J.Antibio.(张静霞,王欣瑜,唐克慧.中国抗生素杂志),2009,34(10):588-592.
[12] Khataee A,Hasanzadeh A,Iranifam M,Joo S W.Sens.ActuatorsB,2015,215(2015):272-282.
[13] Liu H,Zhang Y T,Shuang H J,Song F X.J.Instrum.Anal.(刘欢,张琰图,双海军,宋馥馨.分析测试学报),2016,35(4):497-500.
[14] Khataee A,Iranifam M,Fathinia M,Nikravesh M.Spectrochim.ActaA,2014,134(2015):210-217.
[15] Ma Y,Zhang Y T,Liu H M,Liu H,Shuang H J.Chin.J.Anal.Lab.(马媛,张琰图,刘宏美,刘欢,双海军.分析试验室),2015,34(4):442-446.
[16] Yang W P,Zhang Y T,Zhang Z J.ActaChim.Sin.(杨维平,张琰图,章竹君.化学学报),2003,61(2):303-306.[17] Shao X D,Li Y.Chem.Res.(邵晓东,李瑛.化学研究),2010,21(1):102-112.
[18] Rose A L,Waite T D.Anal.Chem.,2001,73(24):5909-5920.
Determination of Rifapentine by Flow Injection Chemiluminescence Method
XU Tong,ZHANG Yan-tu*,ZHANG Xu
(College of Chemistry and Chemical Engineering,Yan′an University,Yan′an 716000,China)
A novel method of flow injection chemiluminescence for the determination of rifapentine was proposed based on the phenomenon that the chemiluminescence intensity of the luminol-K3Fe(CN)6system could be enhanced by rifapentine in alkaline medium,combined with flow injection analysis technique.Under the optimal experimental conditions,the linear range of rifapentine's detection concentration was 0.008-0.88 mg/L,the detection limit(3σ) was 1.2×10-3mg/L,and the relative standard deviation(RSD,n=11) was 1.9% for rifapentine at 6.0×10-2mg/L.The method was applied in the determination of rifapentine in both capsules and plasma with satisfactory results.
flow injection;chemiluminescence;luminol;potassium ferricyanide;rifapentine
2017-01-07;
2017-01-21
陕西省高水平大学建设专项资金(2013SXTS03);陕西省重大基础研究项目(2016ZDJC-19);延安市科技创新团队项目(2015CHTD-04)
10.3969/j.issn.1004-4957.2017.06.018
O657.3;TQ460.72
A
1004-4957(2017)06-0805-04
*通讯作者:张琰图,博士,教授,研究方向:化学发光分析,Tel:0911-2333193,E-mail:zhyt1969@163.com
