血小板功能试验监测P2Y12受体拮抗剂的抗血小板聚集效果研究进展
2017-06-29孔繁强任静门剑龙
孔繁强,任静,门剑龙
血小板功能试验监测P2Y12受体拮抗剂的抗血小板聚集效果研究进展
孔繁强,任静,门剑龙△
P2Y12受体拮抗剂广泛应用于心脑血管疾病的预防和治疗中,而监测治疗后血小板功能变化有助于改善患者的预后。血小板功能试验是评估抗血小板聚集治疗后残留血小板高反应性的重要方法,主要包括透射光法血小板聚集试验(LTA)、电阻抗法血小板聚集试验(WBIA)、血管舒张剂刺激磷酸蛋白(VASP)、血栓弹力图(TEG)、血小板功能分析仪-100型(PFA-100)和VerifyNow系统。这些试验监测抗血小板聚集治疗后血小板残留反应性的能力各不相同,评估效果也各有不同。其中,LTA是评估抗血小板药物疗效的经典方法,便捷而廉价,但易受操作和环境干扰;WBIA临床应用较少,缺乏评估临界值;VASP对血小板功能变化敏感,但试验复杂且成本高;TEG能监测药物对血小板的抑制率,但指导治疗的安全性还需要验证;PFA-100监测抗血小板聚集药物的敏感性和特异性尚不明确;VerifyNow有效可靠,但成本过高。临床研究证据显示,LTA、VASP和VerifyNow系统能敏感反映P2Y12受体拮抗剂抗血小板聚集的效果,且与心血管疾病患者主要不良心脏事件(MACE)风险相关。
预后;综述;P2Y12受体拮抗剂;血小板功能试验;实验室临界值
用血小板功能试验(platelet function tests,PFTs)监测抗血小板聚集药物的作用效果是目前临床研究的热点。随着氯吡格雷、普拉格雷和替格瑞洛等P2Y12受体拮抗剂的普及使用,治疗后血小板残留高反应性(high platelet reactivity,HPR)与主要不良心脏事件(major adverse cardiac events,MACE)的关系研究得到普遍重视。大规模队列研究发现,通过PFTs监测P2Y12受体拮抗剂的抗血小板聚集效果(即残留HPR)以指导治疗可有效改善患者的临床结局[1]。另一方面,PFTs通常在外科手术前用于评估患者停用P2Y12受体拮抗剂后血小板功能的恢复情况,有助于降低术中出血风险。2015年欧洲心脏病学会(ESC)和2016年美国心脏病学会/美国心脏协会(ACC/AHA)在其发布的冠心病相关治疗指南中均对利用PFTs监测P2Y12受体拮抗剂的抗血小板聚集效果表现出积极的态度[2-3]。本文旨在对PFTs在监测P2Y12受体拮抗剂治疗中的临床价值和应用效果相关研究进行综述,以期为临床提供参考。
1 可用于P2Y12受体拮抗剂监测的PFTs
目前,在临床上可用于监测P2Y12受体拮抗剂的PFTs可分为实验室检测和床旁检测两类,前者主要包括透射光法血小板聚集试验(light transmission aggregometry,LTA)、电阻抗法血小板聚集试验(whole blood impedance aggregometry assay,WBIA)和血管舒张剂刺激磷蛋白试验(vasodilatorstimulated phosphoprotein,VASP),后者主要包括血栓弹力图(thrombelastogram,TEG)、血小板功能分析仪-100型(platelet function analyzer-100,PFA-100)和 VerifyNow 系统,这些检测方法均有商品化试剂,且均积累了一定临床经验,见表1。这些试验中,临床共识是:LTA一直是评估血小板功能的“金标准”,对P2Y12受体拮抗剂有足够的敏感性,缺点是实验结果易受环境及检验操作等多种因素的影响;VASP和VerifyNow系统对P2Y12受体拮抗剂治疗后的血小板功能变化更为敏感,并有较为充分的循证依据,被认为是目前有效且可靠的检测方法,但其在国内的试验成本过于昂贵;其他如WBIA、TEG和PFA-100等试验,临床实践证据正在逐步积累验证。
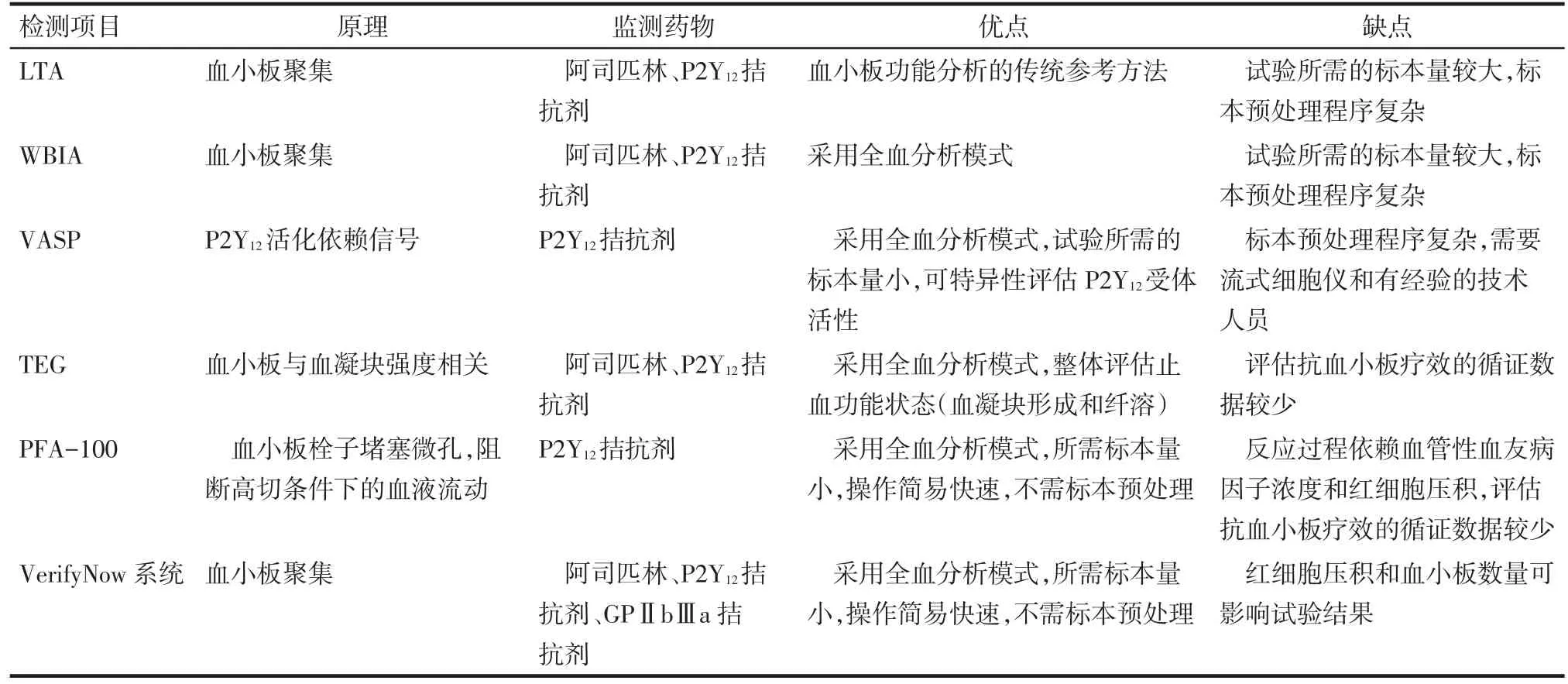
Tab.1 The primary platelet function tests表1 主要的血小板功能试验
2 实验室监测血小板功能的临床实践进展
2.1 LTA 传统的LTA采用富含血小板的血浆作为标本,以光散射法检测血小板在诱导剂刺激下发生活化聚集的过程。监测氯吡格雷、普拉格雷和替格瑞拉等P2Y12受体拮抗剂的抗血小板聚集效果时,采用二磷酸腺苷(adenosine diphosphate,ADP)作为诱导剂。通常情况下,诱导剂浓度对试验结果影响显著,浓度过高可产生药物抵抗的假象,会使医生不适当地上调药物剂量或使用替代药物;浓度过低可造成血小板抑制假象,易误导医生下调剂量或延长外科择期术前的等待时间。Parodi等[4]研究表明,LTA能够敏感地反映不同P2Y12受体拮抗剂对心脏介入治疗患者术后血小板聚集抑制率的差异,低抑制率与患者的不良临床结局相关。Bernlochner等[5]研究发现,LTA可敏感地反映氯吡格雷和普拉格雷药物剂量变化引起的HPR的波动,以及两类药物治疗后HPR的差异;该研究显示,通过上调识别HPR的临界值,LTA可更为准确地预测氯吡格雷低反应患者的MACE复发风险。Reny等[6]纳入了13项前瞻性研究数据的荟萃分析显示,6 478例接受氯吡格雷治疗的患者在危险因素存在的情况下(如年龄>75岁、急性冠脉综合征、糖尿病和高血压),HPR与MACE风险增加之间关联性显著增强(P=0.04);在无风险因素的患者中,未发现两者间存在关联性(P=0.48);该研究显示,在有1个风险因素的患者中,HPR与MACE风险的风险比(hazard ratio,HR)为 3.2(P=0.001);在有≥2个风险因素的患者中,患者的HPR与MACE的风险比开始增加(HR=3.7,P=0.000 3),由此认为,LTA 能够敏感反映 HPR,其与MACE风险间的关联强度明显依赖于患者自身的心血管风险因素数量。
总体而言,LTA可敏感反映P2Y12受体拮抗剂的抗血小板聚集效果,可帮助医生评估MACE风险,且检测成本低廉,因此该试验仍是抗血小板聚集疗效评估的重要监测方法。
2.2 WBIA WBIA采用水蛭素抗凝试管(而非枸橼酸钠抗凝)对血液标本进行抗凝,采用多电极血小板聚集分析仪记录一定时间内(如15 min)的电阻抗变化[7]。目前,有关WBIA的一些研究主要集中于对氯吡格雷的监测方面,该试验检测环境更接近循环血液环境,但存在样本需要量大、耗时长等问题。较早期的研究显示,该试验能够识别有MACE风险和出血风险的患者[8]。Amann等[9]在纳入了 400例心脏介入患者的注册研究中发现,通过设置相应的诊断临界值,WBIA可有效预测患者的缺血和出血风险,而且在不同年龄、糖尿病和体质指数亚组中均有相近的诊断效能。但该试验也存在着尚需解决的问题,如没有设置被广泛接受的风险评估临界值、临床应用难以推广、缺乏足够的循证证据,因此还需要大型的前瞻性队列研究完成临床数据积累。
2.3 VASP 用流式法测定ADP特异性的VASP仅需少量全血标本即可监测抗血小板聚集治疗后的血小板活化情况,测定结果以血小板反应指数(platelet reactivity index,PRI)表达。该试验能够高度特异性地反映氯吡格雷、普拉格雷等P2Y12受体拮抗剂抑制血小板聚集的效果,有效抑制时PRI值处于低水平;如抑制效果差,PRI则处于高水平,MACE风险增加[10-11]。Aradi等[12]采用系统分析显示,采用 VASP 试验能反映氯吡格雷和普拉格雷对血小板功能的影响,可指导临床调整抗血小板聚集治疗方案,结论认为,建立在VASP监测基础上的强化抗血小板聚集治疗能降低心血管疾病的死亡率和PCI术后支架内血栓形成的风险。Mallouk等[13]的系统评价显示,通过调整诊断临界值可提高对氯吡格雷低反应性患者的检出率。
VASP的另一个优势是对患者的监测依从性要求较低。近期随机对照研究显示,接受心脏介入治疗的患者在应用氯吡格雷的最初6个月中,不同的监测依从性与监测效果间并无显著关联,但该研究也发现,氯吡格雷初始治疗有效的患者,如在随后治疗中监测依从性差,更容易导致PRI偏低,使出血风险增加[14]。另外需注意的是,采用不同试验原理的检测方法对VASP数据的可靠性有一定影响,如流式法VASP监测P2Y12受体拮抗剂时与LTA测定结果的变化趋势接近,而采用ELISA法的VASP与LTA测定结果间存在明显差异[15-16]。此外,与其他PFTs不同,VASP试验对时间的要求不高,从而更有利于保证实验数据的准确性。Rollini等[17]研究显示,从护士采集血液标本到检测之间的耗时可对LTA和VerifyNow系统监测抗血小板聚集药物的效果产生影响,两种方法在血样采集后30 min至2 h可基本维持数据稳定,4 h后数值均开始降低,但对VASP影响很小(在所有时间点均维持数据稳定)。
综上所述,关于VASP监测P2Y12受体拮抗剂的循证证据已非常充分,VASP可作为评估抗血小板聚集效果的可靠试验,但制约该试验普及应用的瓶颈是检测过程相对复杂和成本较高。
3 床旁监测血小板功能的临床实践进展
3.1 TEG TEG是一种整体观察血液凝固过程,动态观测血凝块生成、凝块强度和纤维蛋白溶解的试验方法。多年来,TEG的主要用途是分析创伤、心脏手术和肝脏手术患者的出血风险和出血原因,以指导成分输血。近年来,TEG及其血小板图(TEG-platelet mapping,TEG-PM)被逐渐用于监测抗血小板聚集治疗后的血小板残留高反应性。临床实践中,以ADP作为诱导剂的TEG和TEG-PM更多地作为反映P2Y12受体拮抗剂抗血小板聚集效果的试验方法。Fu等[18]通过调整TEG-PM的诊断临界值实现了对支架内再狭窄风险的有效预测;研究显示,患者对氯吡格雷低反应性是导致支架内再狭窄的独立风险因素。Liu等[19]研究显示,TEG能识别应用了氯吡格雷的CYP2C19*2基因多态性患者的血小板残留高反应性。Lv等[20]研究显示,TEG可用于评估P2Y12受体拮抗剂的治疗效果,如血小板残留反应性高时可致卒中风险增加。
目前,关于用TEG监测P2Y12受体拮抗剂的研究以国内数据为主,多数结论认为TEG有助于评估治疗后的HPR,但由于相关研究多为病例对照研究,缺乏前瞻性的多中心研究,因此TEG指导临床治疗的安全性仍有待更多研究验证。另一方面,TEG-PM还被用于评估择期外科手术患者术前停用抗血小板聚集药物的时机和安全性。Kasivisvanathan等[21]研究显示,对于非心脏手术患者,TEG-PM能敏感地反映术前7 d内应用氯吡格雷所致的术中出血风险;该研究认为,ADP诱导的血小板聚集抑制率为34%,可作为提示出血风险的临界值。
对于择期外科手术患者,术前抗血小板聚集药物停药时间与安全性的关系仍未形成共识。国内指南推荐的术前停药时间(不伴有心血管缺血风险患者,氯吡格雷和替格瑞洛5 d,普拉格雷 7 d)与欧洲指南相近[2,22],但对疑似有出血疾病或风险、长期使用抗血小板聚集药物、高龄和口服某些中成药的患者,出血风险评估非常困难,因此这种状态下,用PFTs评估血小板功能是更为安全的选择。TEG和TEG-PM对术前停药患者的检测往往是在LTA结果无法解释或无法获得时的替代手段,但由于TEG和TEG-PM检测成本较高,不建议作为常规手段。
3.2 PFA-100 PFA-100是一种床旁出血时间检测设备,主要用于对出血性疾病如血管性血友病、血小板无力症和巨大血小板综合征等的诊断。在较早时期,PFA-100检测结果与氯吡格雷治疗相关性差,不能对血小板抑制状态进行准确评估。近年来出现的专用型检测试剂(如INNOVANCE®PFA P2Y)提高了该设备对P2Y12受体拮抗剂诊断的敏感性。已有少量研究显示,该试验有助于评估心脑血管疾病患者应用P2Y12受体拮抗剂后的HPR[23-24],能够帮助临床预测这些患者心血管事件复发的风险,并提高临床对短暂性脑缺血发作或缺血性卒中后二级预防的有效性[25]。另一方面,PFA-100的临床价值也存在争议。Bartels等[26]研究显示,PFA-100监测抗血小板聚集药物的敏感性和特异性均较低(分别为48.6%和74.8%),不能作为指导药物剂量调整的手段;Teuber等[27]研究显示,PFA-100不能敏感反映较低剂量氯吡格雷抑制血小板的效果。此外,PFA-100由于缺乏公认的参考范围和评估疗效的临界值[28],因此其在临床实践中应用较少,临床应用仍在摸索中。
3.3 VerifyNow检测系统 VerifyNow检测系统检测法是一种简单易行的床旁血小板功能监测试验,可检测患者血小板聚集功能,评价抗血小板聚集药物的疗效。该试验的优点包括:仅需要少量全血标本,检测过程快速(3~5 min),特异性高,其检测环境与人体循环血液环境相近,检测结果与LTA结果变化趋势相关性好,用于监测P2Y12受体拮抗剂是安全有效的[29]。VerifyNow系统监测氯吡格雷的试验结果以P2Y12反应单位(P2Y12reaction units,PRU)的形式报告,存在HPR 时,PRU 水平增高[30]。Cattaneo 等[31]研究显示,PRU 水平增高往往提示MACE风险增加;Lemesle等[32]的前瞻性研究显示,VerifyNow系统能评估患者对氯吡格雷的反应性,且被VerifyNow系统提示异常的患者中,有47%的患者的LTA和VASP表现出相同的趋势,该研究认为VerifyNow系统与其他试验联合应用时效果可能更佳。
近期的研究显示,VerifyNow系统在急性冠脉综合征患者的治疗监测和风险预测中表现出良好的性能。Li等[33]研究发现,在接受心脏介入治疗的患者中,该试验联合GRACE评分能有效预测心脏病患者在1年内发生MACE的风险。Guimarães等[34]研究显示,在对 PRU 进行连续监测时,其与LTA的检测结果间具有良好的趋势相似性,该研究表明,VerifyNow系统不但可用于指导对急性冠脉综合征患者进行氯吡格雷剂量的调整,同时也可有效监测普拉格雷和替格瑞洛在初始治疗时的抗血小板聚集效果;另外,该研究也发现,对于某些合并复杂情况的患者(如高GRACE分值),单纯VerifyNow系统无法满足对抗血小板聚集药物的监测。
综上所述,目前VerifyNow系统是监测P2Y12受体拮抗剂治疗的可靠方法,循证证据充分,可在医院床旁和家庭实施操作,但缺点是该试验在国内的成本过高,并不适合作为主要的检测手段。
4 展望
目前,对于心脑血管疾病患者是否使用PFTs指导临床抗血小板聚集治疗一直存在争议,某些试验有助于临床对预后进行评估。目前,已有包括系统评价和荟萃分析证据支持LTA、VASP和VerifyNow系统用于评估抗血小板聚集药物对心血管疾病一、二级预防的安全性,但仍缺少足够的前瞻性多中心随机对照试验,尚不足以证明PFTs的安全性和有效性。因此,未来仍需更多研究证明PFTs与患者临床结局间的相关性,并在诊断临界值等问题上形成共识。此外,降低检测成本也将是改善这些试验临床可获得性的重要因素。
[1]Mayer K,Schulz S,Bernlochner I,et al.A comparative cohort study on personalised antiplatelet therapy in PCI-treated patients with high on-clopidogrel platelet reactivity.Results of the ISAR-HPR registry[J].Thromb Haemost,2014,112(2):342-351.doi:10.1160/TH13-10-0874.
[2]Roffi M,Patrono C,Collet JP,et al.2015 ESC Guidelines for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation:Task Force for the Management of Acute Coronary Syndromes in Patients Presenting without Persistent ST-segment Elevation of the European Society of Cardiology(ESC)[J].Eur Heart J,2016,37(3):267-315.doi:10.1093/eurheartj/ehv320.
[3]Levine GN,Bates ER,Bittl JA,et al.2016 ACC/AHA guideline focused update on duration of dual antiplatelet therapy in patients with coronary artery disease:A report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines[J].J Thorac Cardiovasc Surg,2016,152(5):1243-1275.doi:10.1016/j.jtcvs.2016.07.044.
[4]Parodi G,Marcucci R,Valenti R,et al.High residual platelet reactivity after clopidogrel loading and long-term cardiovascular events among patients with acute coronary syndromes undergoing PCI[J].JAMA,2011,306(11):1215-1223.doi:10.1001/jama.2011.1332.
[5]Bernlochner I,Mayer K,Morath T,et al.Antiplatelet efficacy of prasugrel in patients with high on-clopidogrel treatment platelet reactivity and a history of coronary stenting[J].Thromb Haemost,2013,109(3):517-524.doi:10.1160/TH12-08-0552.
[6]Reny JL,Fontana P,Hochholzer W,et al.Vascular risk levels affect the predictive value of platelet reactivity for the occurrence of MACE in patients on clopidogrel.Systematic review and metaanalysis of individual patient data[J].Thromb Haemost,2016,115(4):844-855.doi:10.1160/TH15-09-0742
[7]Dugan G,O’Donnell L,Hanbury DB,et al.Assessment of Multiplate platelet aggregometry using citrate,heparin or hirudin in Rhesus macaques[J].Platelets,2015,26(8):730-735.doi:10.3109/09537104.2014.988694.
[8]Siller-Matula JM,Delle-Karth G,Lang IM,et al.Phenotyping versus genotyping for prediction of clopidogrel efficacy and safety:the PEGASUS-PCI study[J].J Thromb Haemost,2012,10(4):529-542.doi:10.1111/j.1538-7836.2012.04639.x.
[9]Amann M,Ferenc M,Valina CM,et al.Validation of a P2Y12-receptor specific whole blood platelet aggregation assay[J].Platelets,2016,27(7):668-672.doi:10.3109/09537104.2016.1153620.
[10]Deharo P,Quilici J,Bonnet G,et al.Is platelet inhibition correlated with time from last intake on P2Y12 blockers after an acute coronary syndrome?A pilot study[J].Platelets,2016,27(8):791-795.doi:10.1080/09537104.2016.1190006.
[11]Cattaneo M.High on-treatment platelet reactivity--definition and measurement[J].Thromb Haemost,2013,109(5):792-798.doi:10.1160/TH12-10-0758.
[12]Aradi D,Komócsi A,Price MJ,et al.Tailored Antiplatelet Treatment Study Collaboration.Efficacy and safety of intensified antiplatelet therapy on the basis of platelet reactivity testing in patients afterpercutaneous coronary intervention:systematic review and meta-analysis[J].Int J Cardiol,2013,167(5):2140-2148.doi:10.1016/j.ijcard.2012.05.100.
[13]Mallouk N,Labruyère C,Reny JL,et al.Prevalence of poor biological response to clopidogrel:a systematic review[J].Thromb Haemost,2012,107(3):494-506.doi:10.1160/TH11-03-0202.
[14]Forni Ogna V,Menetrey I,Muller O,et al.Effect of long-term adherence to clopidogrel on the VASP-PRI after elective coronary stent implantation:a randomized controlled study[J].Br J Clin Pharmacol,2016,82(6):1486-1497.doi:10.1111/bcp.13071.
[15]Danese E,Fava C,Beltrame F,et al.Relationship between pharmacokinetics and pharmacodynamics of clopidogrel in patients undergoing percutaneous coronary intervention: comparison between vasodilator-stimulated phosphoprotein phosphorylation assay and multiple electrode aggregometry[J].J Thromb Haemost,2016,14(2):282-293.doi:10.1111/jth.13197.
[16]Abtan J,Silvain J,Kerneis M,et al.Identification of poor response to P2Y12 inhibitors in ACS patients with a new ELISA-based vasodilator- associated stimulated phosphoprotein (VASP)phosphorylation assay[J].Thromb Haemost,2013,110(5):1055-1064.doi:10.1160/TH13-03-0203.
[17]Rollini F,Franchi F,Singh K,et al.Impact of timing from blood sampling to pharmacodynamic assessment on measures of platelet reactivity in patients treated with P2Y12 receptor inhibitors[J].Thromb Haemost,2016,116(6):1060-1069.doi:10.1160/TH16-05-0377.
[18]Fu Z,Dong W,Shen M,etal.Relationship between hyporesponsiveness to clopidogrel measured by thrombelastography and in stent restenosis in patients undergoing percutaneous coronary intervention[J].Clin Biochem,2014,47(16/17):197-202.doi:10.1016/j.clinbiochem.2014.08.009.
[19]Liu J,Nie XY,Zhang Y,et al.CYP2C19*2 and other allelic variants affecting platelet response to clopidogrel tested by thrombelastography in patients with acute coronary syndrome[J].Chin Med J(Engl),2015,128(16):2183-2188.doi:10.4103/0366-6999.162515.
[20]Lv HH,Wu S,Liu X,et al.Comparison of VerifyNow P2Y12 and thrombelastography for assessing clopidogrel response in stroke patients in China[J].Neurol Sci,2016,37(2):277-282.doi:10.1007/s10072-015-2407-7.
[21]Kasivisvanathan R,Abbassi-Ghadi N,Kumar S,et al.Risk of bleeding and adverse outcomes predicted by thromboelastography platelet mapping in patients taking clopidogrel within 7 days of non-cardiac surgery[J].Br J Surg,2014,101(11):1383-1390.doi:10.1002/bjs.9592.
[22]中华医学会外科学分会.中国普通外科围手术期血栓预防与管理指南[J].中国实用外科杂志,2016,36(5):469-474.Chinese MedicalAssociation.Chinese guideline forprevention and management of thrombosis in perioperative period of general surgery[J].Chin J Prac Surg,2016,36(5):469-474.doi:10.7504/CJPS.ISSN 1005-2208.2016.05.01.
[23]Santos MT,Madrid I,Moscardo A,et al.The administration of a loading dose of aspirin to patients presenting with acute myocardial infarction while receiving chronic aspirin treatmentreduces thromboxane A2-dependent platelet reactivity[J].Platelets,2014,25(4):268-273.doi:10.3109/09537104.2013.816671.
[24]Lim ST,Coughlan CA,Murphy SJ,et al.Platelet function testing in transient ischaemic attack and ischaemic stroke:A comprehensive systematic review of the literature[J].Platelets,2015,26(5):402-412.doi:10.3109/09537104.2015.1049139.
[25]Jover E,Rodríguez JM,Bernal A,et al.High on-treatment platelet reactivity in patients with ischemic cerebrovascular disease:assessment of prevalence and stability over time using four platelet function tests[J].Blood Coagul Fibrinolysis,2014,25(6):604-611.doi:10.1097/MBC.0000000000000118.
[26]Bartels A,Sarpong Y,Coberly J,et al.Failure of the Platelet Function Assay(PFA)-100 to detect antiplatelet agents[J].Surgery,2015,158(4):1012-1018.doi:10.1016/j.surg.2015.07.011.
[27]Teuber M,Mischke R.Influence of a low dosage of clopidogrel on platelet function in cats as measured by the platelet function analyser PFA-100 and the multiplate analyser[J].Res Vet Sci,2016,109:149-156.doi:10.1016/j.rvsc.2016.09.011.
[28]Kuiper GJ,Houben R,Wetzels RJ,et al.The use of regression analysis in determining reference intervals for low hematocrit and thrombocyte count in multiple electrode aggregometry and platelet function analyzer 100 testing of platelet function[J].Platelets,2017,28(1):1-8.doi:10.1080/09537104.2016.1257782.
[29]Trenk D,Stone GW,Gawaz M,et al.A randomized trial of prasugrel versus clopidogrel in patients with high platelet reactivity on clopidogrel after elective percutaneous coronary intervention with implantation of drug-eluting stents:results of the TRIGGERPCI(Testing Platelet Reactivity In Patients Undergoing Elective Stent Placement on Clopidogrel to Guide Alternative Therapy With Prasugrel)study[J].J Am Coll Cardiol,2012,59(24):2159-2164.doi:10.1016/j.jacc.2012.02.026.
[30]Saucedo JF,Angiolillo DJ,DeRaad R,et al.SWAP Investigators.Decrease in high on-treatmentplateletreactivity (HPR)prevalence on switching from clopidogrel to prasugrel:insights from the switching anti-platelet(SWAP)study[J].Thromb Haemost,2013,109(2):347-355.doi:10.1160/TH12-06-0378.
[31]CattaneoM.Responsevariabilitytoclopidogrel:istailored treatment,based on laboratory testing,the right solution?[J].J Thromb Haemost,2012,10(3):327-336.doi:10.1111/j.1538-7836.2011.04602.x.
[32]Lemesle G,Landel JB,Bauters A,et al.Poor agreement between light transmission aggregometry,Verify Now P2Y12and vasodilatator-stimulated phosphoprotein forclopidogrellowresponse assessment:a potential explanation of negative results of recent randomized trials[J].Platelets,2014,25(7):499-505.doi:10.3109/09537104.2013.840363.
[33]Li S,Liu H,Liu J,et al.Improved predictive value of GRACE risk score combined with platelet reactivity for 1-year cardiovascular risk in patients with acute coronary syndrome who underwent coronary stent implantation[J].Platelets,2016,27(7):650-657.doi:10.3109/09537104.2016.1153618.
[34]Guimarães LF,Généreux P,Silveira D,et al.P2Y12 receptor inhibition with prasugrel and ticagrelor in STEMI patients after fibrinolytic therapy:Analysis from the SAMPA randomized trial[J].Int J Cardiol,2017,230:204-208.doi:10.1016/j.ijcard.2016.12.173.
(2017-02-16收稿 2017-03-29修回)
(本文编辑 陆荣展)
Research progress of platelet function tests in antiplatelet effect on monitoring P2Y12receptor antagonist
KONG Fan-qiang,REN Jing,MEN Jian-long△
Medical Laboratory,Tianjin Medical University General Hospital,Tianjin 300052,China△
and Reviser E-mail:thromhaemo@126.com
The P2Y12receptor antagonist is used widely in prevention and treatment of cardiovascular and cerebrovascular disease.Monitoring changes of platelet function after treatment can improve the prognosis of patients.The platelet function test is the important way to evaluate high residual platelet reactivity after antiplatelet treatment,including light transmission aggregometry(LTA),whole blood impedance aggregometry assay(WBIA),vasodilator-stimulated phosphoprotein(VASP),thrombelastogram(TEG),platelet function analyzer-100(PFA-100)and VerifyNow system(VerifyNow).It is very different for the reflecting ability with residual reactivity of platelets among these tests after antiplatelet therapy,and also significant difference for assessment effect.Among them,LTA is a classic method for the curative effect evaluation of anti-platelet agents,which is convenient and cheap,but it is susceptible to the operating and environment interference.The clinical application of WBIA is less,and which lacks threshold value for assessment.VASP is sensitive for the changes of platelet function,but the test is complex and expensive.TEG can monitor the inhibition ratio of drugs on anti-platelets,but it needs to verify the safety of treatment.It is not clear for sensitivity and specificity with monitoring anti-platelet agent by PFA-100.VerifyNow is effective and reliable,but the cost is high.The evidence of clinical study shows that LTA,VASP and VerifyNow can reflect the effect of platelet inhibition of P2Y12receptor antagonists sensitively,and is associated with the risk of major adverse cardiac events(MACE)in patients with cadiovascular diseases.
prognosis;review;P2Y12receptor antagonists;platelet function test;laboratory critical values
R446.114.5
:A
10.11958/20170185
天津市科技计划项目(16KPXMSF00170)
天津医科大学总医院医学检验科(邮编300052)
孔繁强(1974),男,副主任技师,主要从事血液学实验室诊断及相关研究
△通讯作者及审校者 E-mail:thromhaemo@126.com
