术中超声辅助神经导航技术在颅脑手术中的应用
2017-06-29赵四军通讯作者王重韧
赵四军 赵 明(通讯作者) 徐 欣 尤 宇 王重韧 韩 磊
郑州大学附属肿瘤医院神经外科 郑州 450008
术中超声辅助神经导航技术在颅脑手术中的应用
赵四军 赵 明(通讯作者) 徐 欣 尤 宇 王重韧 韩 磊
郑州大学附属肿瘤医院神经外科 郑州 450008
目的 探讨术中超声辅助神经导航技术在颅脑手术中的应用价值。方法 选取2013-04—2014-12我院收治的50例颅脑内病变(高级别胶质瘤、低级别胶质瘤、炎性和胶质增生、脑膜瘤、转移瘤等)患者临床资料为研究样本,回顾性分析其临床资料。术中均使用神经导航技术,按是否使用术中超声辅助将其分为观察组和对照组各25例,根据术后影像学结果比较2组病灶全切率,并比较2组病例术后并发症发生率。结果 观察组病灶全切率88.00%与对照组60.00%比较明显较高(P<0.05)。观察组并发症发生率(0)较对照组(16.00%)低(P<0.05)。结论 术中超声辅助神经导航技术可实时、准确判断肿瘤边界,提高全切除率,减少并发症发生率,值得在临床推广应用。
术中超声;神经导航;颅脑手术
颅脑手术因有颅骨保护,且人脑功能复杂、重要,手术暴露及术中操作有其困难性。因此术前选择有效方法设计开颅方式,术中采取有效技术指导临床外科医师进行颅脑手术并提高病灶全切率,对患者预后有重要意义[1-2]。随微创神经外科发展,精确定位病灶已成为手术成功与否关键,术中超声检查可实时显示病变质地与轮廓,向医师反馈诊断与治疗信息,指导医师最大限度切除病灶,同时可减少手术损伤,但超声检查不能很好穿透颅骨,无法完成术前精确定位,而神经导航技术具有准确的导航定位功能,术前定位精准,但伴随手术操作,术中会出现漂移误差,两者结合,可互相弥补不足,但术中超声辅助神经导航技术对颅脑手术的应用价值现报道较少[3-4]。本文选取我院收治的50例颅脑内病变患者为研究对象,分析超声辅助神经导航技术在其颅脑手术中的应用价值,现报告如下。
1 资料与方法
1.1 一般资料 选取2013-04—2014-12我院收治的50例颅脑内病变患者为研究对象,其中高级别胶质瘤18例,低级别胶质瘤9例,炎性和胶质增生2例,脑膜瘤8例,转移瘤8例,海绵状血管瘤3例,脑脓肿2例,均符合颅脑手术适应证。排除标准:(1)合并严重肿瘤、血液系统、免疫系统及精神性疾病者;(2)存在严重心、肝、肾等重要脏器功能不全者;(3)家属配合依从性差,不完全支持本研究者。本研究经本院伦理委员会同意,且所有患者知情同意并签署知情同意书。根据术中是否行神经导航辅助技术将其分为观察组和对照组各25例,观察组男14例,女11例;年龄39~71(54.19±1.43)岁。对照组男13例,女12例;年龄40~69(54.20±1.41)岁,2组在性别、年龄等一般资料方面比较差异无统计学意义(P>0.05),具有可比性。
1.2 方法 术前完善检查,无需剃发,取平卧位,行头部MRI常规序列扫描,T1、T2、弥散张量成像、增强扫描,并加做T1增强1.5 mm薄层扫描,必要时加做T2平扫薄层扫描及CT薄层扫描。数据录入光盘,并放置好参考架,妥善固定。对照组采取单纯神经导航技术(美敦力StealthStation导航系统):(1)将影像资料通过光盘传至神经导航系统工作站显示和重建颅脑与病灶的三维模型;(2)应用红外线定位,使用Tracer轮廓注册法,注册成功后,选择鼻尖、内眦、眉心等处确认导航准确度,应用导航仪精确定位病灶在头皮的投影,设计最佳手术入路,并设计切开皮层方案。观察组在对照组基础上加用术中超声操作与超声诊断:开颅后的术野平面位于最高点并和地面平行,选择最大直径为2~3 cm的矩形探头,频率:(1)5 MHz,深度达7 cm;(2)10 MHz,深度4 cm,对位置表浅病灶选用高频率,对位置较深病灶选择低频率,术中重复使用超声探测,提示肿瘤何处残留及术野有无渗血变化。术者仔细辨认术中超声图像,多次使用超声帮助术者判断病灶位置及残余大小,纠正脑移位,病灶切除后,应用超声验证是否有残留。
1.3 观察指标 (1)统计患者术后并发症的发生率:较术前出现明显肢体活动障碍、言语障碍、视力视野障碍等均视为并发症,仅出现一过性肢体活动障碍、言语障碍等,经治疗后很快恢复不视为并发症。(2)比较2组病灶全切除率:根据术毕超声影像及术后CT或MRI复查结果评估肿瘤切除程度,分为全部切除,大部分切除,部分切除。

2 结果
2.1 2组并发症发生率比较 观察组仅有1例术后出现短暂肢体活动障碍,经治疗后很快恢复。对照组1例出现较严重肢体活动障碍,经治疗后生活可自理,3例出现言语障碍,虽可与人交流,但仍有不便。对照组并发症发生率16.0%(4例)明显高于观察组(P<0.05)。
2.2 2组病灶全切除率比较 观察组病灶全切率明显高于对照组(P<0.05)。见表1。
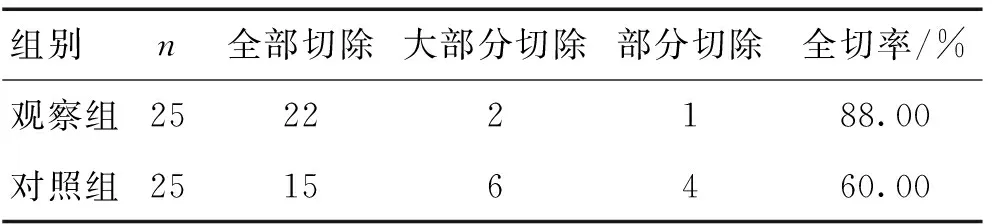
表1 2组病灶全切除率比较 (n)
3 讨论
传统神经外科手术中,术者多根据术前影像学信息如CT、MRI等设计开颅,开颅后依靠术者经验及对影像资料的理解,观察脑表面颜色变化及触觉而确定脑穿刺部位,这难免会出现偏差,导致术中寻找病灶困难,尤其是微小病灶,手术时间延长,增加了病人术后颅脑及全身并发症。因此选择有效的开颅方式,应用先进技术指导术者进行颅脑手术仍是临床研究的热点[5]。神经导航系统是传统立体定向、现代计算机技术、影像学技术及微侵袭技术相结合的产物,具有准确性、灵活性、微创性、快速性特点,能对脑深部或颅底较小病变或周围正常脑组织外观极为相似的病变进行准确定位,集影像-导向-手术为一体,因此在术中具有较好的定位、定向作用[6-7]。术中实时超声可提示脑实质与颅内病灶形态方向,指导术者选择最近皮层距离、最小皮层切口方法进行入路,同时进入手术后对检出率高的颅内病变部位进行动态、多方向定位,但其对颅骨的穿透性差,需打开骨窗后使用,无法在开颅前指导定位,此外术中图像是二维的,术者需有一定空间定位经验才可确定病灶三维定位,同时肿瘤切除后,切缘内壁附有双极所致创面电凝物的干扰无法鉴别肿瘤边界[8]。因此将神经导航与术中超声联合应用于颅脑手术中,方能取得更大价值。程伟等[9]在分析超声神经导航技术在颅脑手术中的应用价值时发现超声诊断对胶质瘤、髓母细胞瘤、脑膜瘤、海绵状血管瘤、转移癌、血管母细胞瘤等具有较好定位作用,但其不能很好地穿过颅骨,无法完成术前精确定位,当肿瘤或异常组织和正常脑组织的超声信号相近时难以辨认,而神经导航可做到,采用超声技术与神经导航技术结合后,能准确设计小切口与小骨瓣,尤其能定位颅内小病灶。林建虎等[10]将神经导航技术应用于95例基底节区高血压脑出血手术中,结果显示3例患者出现术后再出血再次手术,2例患者钻孔引流后出现颅内感染,经抗感染后控制良好。本研究结果显示术中超声辅助神经导航技术应用于颅脑手术后,患者病灶全切率明显提高,并发症发生率降低,这与上述研究结果相似,因此术中超声辅助神经导航技术可为选择神经外科手术入路、设计皮肤切口、指导手术进程度、判断手术结果提供客观依据,因而可明显缩短手术时间,减少手术并发症,从而提高手术质量。
综上,术中超声辅助神经导航技术在颅脑手术中具有较高应用价值,值得在临床上推广应用。
[1] 吴琼.神经外科手术颅内感染的危险因素分析及与脑脊液中细胞因子水平变化相关性研究[J].中国实验诊断学,2014,18(7):1 082-1 083.
[2] 饶克成,高飞,李琳,等.颅脑手术后颅内感染的治疗分析[J].中国实用神经疾病杂志,2014,17(4):77-78.
[3] 贾磊,李刚.颅脑手术中超声检查对手术的指导作用[J].山东医药,2014,54(46):101-103.
[4] 徐沛金,陈妙钿.神经导航应用于颅脑手术的护理配合[J].中国实用医药,2014,9(3):221;222.
[5] 闫飞,高媛媛.盐酸氨溴索对行颅脑手术老年患者全身麻醉机械通气期间呼吸功能的影响[J].中国实用神经疾病杂志,2015,18(19):91-92.
[6] 符雅君,吴邓娃.神经导航仪辅助颅脑肿瘤显微切除的护理配合[J].实用临床医药杂志,2013,17(12):1-3.
[7] 尤宇,赵明,徐欣,等.显微外科手术辅以导航技术切除矢状窦旁脑膜瘤的疗效[J].中国实用神经疾病杂志,2013,16(13):32-34.
[8] 李斌,谭卫,冯屹,等.术中超声在神经外科手术中的应用[J].医学综述,2014,20(11):2 062-2 063.
[9] 程伟,牛朝诗.术中超声神经导航技术在颅脑手术中的应用[J].中华神经医学杂志,2013,12(3):318-321.
[10] 林建虎,陆川,蔡建勇,等.神经导航在基底节区高血压脑出血手术中的应用[J].实用医学杂志,2014, 30(15):2 512-2 513.
(收稿2016-11-04)
R651.1+1
B
1673-5110(2017)05-0090-02
