莲子心的HPLC指纹图谱研究*
2017-06-24曾建伟褚剑峰李西海蔡巧燕林珊朱晓勤陈达鑫吴锦忠
曾建伟褚剑峰李西海蔡巧燕林珊朱晓勤陈达鑫吴锦忠#
(1福建中医药大学中西医结合研究院 福州 350122;2福建省中西医结合老年性疾病重点实验室 福州 350122)
●中西药苑●
莲子心的HPLC指纹图谱研究*
曾建伟1,2褚剑峰1,2李西海1,2蔡巧燕1,2林珊1,2朱晓勤1,2陈达鑫1,2吴锦忠1,2#
(1福建中医药大学中西医结合研究院 福州 350122;2福建省中西医结合老年性疾病重点实验室 福州 350122)
目的:建立莲子心的HPLC指纹图谱,为莲子心的品质评价提供可靠的方法。方法:采用Agilent HC C18(4.6 mm×250 mm,5 μm)色谱柱,以乙腈-0.1%三乙胺溶液(10∶90)为流动相,梯度洗脱,流速为1.0 ml/min,检测波长为284 nm,柱温为30℃,建立莲子心的HPLC指纹图谱,并进行相似度评价。结果:10个产地的莲子心在指纹图谱的相似度上达0.90以上,说明这10个产地的莲子心其主要化学成分基本一致。结论:该方法能较好地反映莲子心的化学成分信息,且操作简单,重复性好,为科学评价莲子心品质提供了参考。
莲子心;HPLC;指纹图谱;相似度
莲子心为睡莲科植物莲(Nelumbo Nucifera Gaertn)成熟种子的干燥幼叶及胚根,味苦性寒,具有清心安神,交通心肾,涩精止血之功效,用于热入心包,神昏谵语,心肾不交,失眠遗精,血热吐血等症的治疗[1],历版《中国药典》均有收载。莲子心主要含有生物碱[2]、黄酮[3]、多糖[4]等活性成分,具有降血糖[5]、抗心律失常[6]、抗肿瘤[7]和抗氧化[4,8~9]等活性。莲子心主产于湖南、湖北、江西、福建、浙江等江南水乡,素有湘莲、赣莲、建莲等名品,除上述主产地外,全国多地均有分布。本文采用高效液相色谱法,建立了莲子心的指纹图谱,从化学层面考察了全国各产地莲子心的品质差异,为科学评价莲子心的整体品质提供了实验依据。现报告如下:
1 仪器与材料
1.1 仪器Agilent 1200高效液相色谱仪(包括G1311A四元泵,G1329A自动进样器,G1316A柱温箱,G1315D二极管阵列检测器,Chemstation工作站),MS105DU十万分之一电子天平(梅特勒-托利多公司),AR2130千分之一电子天平(奥豪斯仪器有限公司),KQ-500DE型超声波清洗器(昆山市超声仪器有限公司),Millipore超纯水机(Millipore公司)。
1.2 材料莲心碱、异莲心碱、甲基莲心碱(对照品)均购自北京捷成生物工程技术公司,乙腈、甲醇(色谱纯),三乙胺、甲醇(分析纯)均购自国药集团化学试剂有限公司,超纯水为实验室自制。莲子心样品分别采自全国各主产地,分别编号为S1:河南南阳,S2:福建建宁,S3:湖北洪湖,S4:湖南湘潭,S5:江苏洪泽湖,S6:江西广昌,S7:山东微山湖,S8:浙江龙游,S9:重庆石祝,S10:安微芜湖,均经福建中医药大学杨成梓教授鉴定为莲(Nelumbo nucifera Gaertn)的干燥幼叶及胚根。
2 方法
2.1 色谱条件色谱柱:Agilent HC C18(4.6 mm× 250 mm,5 μm),流动相:乙腈-0.1%三乙胺溶液(10∶90),梯度洗脱,0~20 min:乙腈10%~50%;20~25 min:乙腈50%~80%;25~35 min:乙腈80%;流速:1.0 ml/min;检测波长:284 nm;进样量:10 μl;柱温:30℃。
2.2 溶液配制
2.2.1 对照品溶液配制取莲心碱,异莲心碱,甲基莲心碱适量,精密称定,加甲醇使溶解,制成浓度分别为20、40和60 μg/ml的对照品溶液。
2.2.2 供试品溶液配制取莲子心粉末(过四号筛)约1 g,精密称定,置具塞锥形瓶中,精密加入25 ml 30%乙醇,称定重量,浸泡30 min,加热回流提取60 min,放冷,再次称定重量,用30%乙醇补足减失的重量,过孔径为0.45 μm微孔滤膜滤过,取续滤液,即得。
2.3 方法学考察
2.3.1 精密度试验取同一供试品溶液,连续进样6次,各共有峰的相对保留时间的RSD<0.42%,相对峰面积RSD≤1.50%,相似度均大于0.98,表明该仪器的精密度良好。
2.3.2 稳定性试验取同一供试品溶液,分别于0 h,2 h,4 h,8 h,12 h,24 h进样检测,各共有峰的相对峰面积RSD≤2.56%,相似度大于0.96,表明样品溶液在24 h内基本稳定。
2.3.3 重复性试验取同一批莲子心药材共6份,精密称定,按“2.2.2”项下方法制备成供试品溶液,按“2.1”项色谱条件下进行测定,各共有峰的相对峰面积RSD≤2.81%,相似度大于0.97,表明该分析方法重现性良好。
2.4 指纹图谱的建立与共有指纹峰的确认
2.4.1 指纹图谱的建立取10批来自不同产地莲子心药材,按“2.2.2”项下方法制备成供试品溶液,按“2.1”项色谱条件下进行分析,记录各产地莲子心的HPLC色谱图,导入药典委员会颁布的《中药色谱指纹图谱相似度评价系统A版》,经系统自动匹配后,生成莲子心的指纹图谱。见图1。
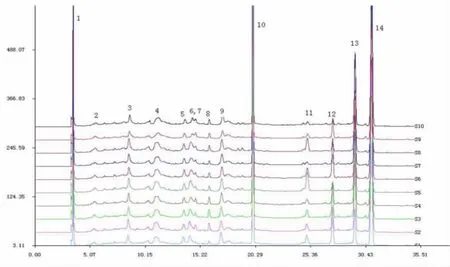
图1 莲子心HPLC指纹图谱
2.4.2 共有峰的确定从莲子心HPLC指纹图谱中确定出14个共有峰,选择保留时间适中且与相邻色谱峰分离较好的12号色谱峰作为参照峰,计算各共有峰的保留时间和峰面积与同一图谱中参照峰的保留时间和峰面积的比值,得到相对保留时间和相对峰面积。见表1~表2。

表1 莲子心HPLC指纹图谱中共有峰的相对保留时间

表2 莲子心HPLC指纹图谱中共有峰的相对峰面积
2.4.3 部分共有峰的鉴定为进一步阐明莲子心的化学成分组成,采用与现有对照品比对的方法,根据保留时间和紫外光谱,初步鉴定出指纹图谱中的12,13,14号色谱峰分别为莲心碱、异莲心碱和甲基莲心碱。
2.5 相似度评价采用中药色谱指纹图谱相似度评价系统,计算10批莲子心药材的HPLC指纹图谱的相似度,以生成的共有模式为对照图谱,计算相似度,结果表明各产地莲子心具有良好的相似性。见表3。

表3 10批莲子心的相似度评价结果
3 讨论
我们在试验过程中选择了不同浓度的乙醇作为提取溶剂,采用索氏提取、超声提取和回流提取作为提取方法,并选择不同的提取时间,对莲子心药材进行提取得到了不同的样品溶液,并进行了HPLC检测,根据检测结果分析了色谱峰的峰形、峰数、分离度和基线等,最终确定以30%乙醇为提取溶剂,超声提取30 min是最佳提取条件。
将样品溶液在全波长200~400 nm范围内进行扫描,结果显示,样品3D色谱图在284 nm处,峰数较多,峰面积较大,基线平稳。这既是莲子心生物碱成分的最大吸收波长,也是黄酮成分的第二大吸收波长,该波长能最大限度地检测出莲子心的主要成分,故选择284 nm作为检测波长。
此外,莲子心的主要成分为生物碱成分呈碱性,为降低拖尾现象,我们在水相中加入了0.1%的三乙胺作为扫尾剂。实验中我们还发现,采用等度洗脱,色谱图中间较长一段时间无峰,为节约分析时间,我们采用了梯度洗脱并优化了流动相的变化比例,使出峰均匀,峰的分离度良好。
莲子心含有多种化学成分,药典标准中仅测定莲心碱一个成分的含量,已不能全面反映莲子心的整体质量,因此建立能全面、系统地反映其化学成分的指纹图谱,将为其品质评价和质量控制提供一个有效的参考方法。本文在优化提取方法和色谱条件的基础上,建立了莲子心的HPLC指纹图谱,确定了莲子心的14个共有峰,其中峰12、13、14分别鉴定为莲心碱、异莲心碱和甲基莲心碱。相似度计算结果表明,各批样品指纹图谱的色谱峰整体上基本一致,相似度均在0.90以上,共有峰的相对保留时间RSD均小于0.71%,而共有峰的相对峰面积RSD却相差很大,在63.68%~111.9%之间。由此可见,不同产地的莲子心所含化学成分的种类虽然基本一致,但其含量差异仍然较大,提示莲子心药材的品质可能与产地的生长环境、采收加工等因素有关。
[1]国家药典委员会.中华人民共和国药典(一部)[M].北京:中国医药科技出版社,2015.273
[2]李萍,杨光明,张玉玲,等.莲子心脂溶性生物碱的分离、鉴定[J].食品与生物技术学报,2016,35(1):19-27
[3]邵建,刘艳丽,李笑然,等.莲子心的化学成分研究[J].中草药,2016,47 (10):1661-1664
[4]俞远志,吴亚林,潘远江.莲子心多糖的提取、分离和抗氧化活性研究[J].浙江大学学报(理学版),2008,35(1):48-51
[5]李秋哲.莲子心黄酮结构分析及其降血糖活性研究[D].福州:福建农林大学,2015.18
[6]王瑞芳,欧来良.莲子心提取物抗心律失常作用及其急性毒性研究[J].中草药,2008,39(3):413-415
[7]曾建伟,谢勇,林忠宁,等.莲子心抗肿瘤活性部位的筛选研究[J].实用中西医结合临床,2014,14(1):87-88
[8]杨小青,宋金春,谢顺岚,等.莲子心中酚性与非酚性生物碱体外抗氧化活性比较[J].医药导报,2015,34(12):1579-1583
[9]张俊生,陈莉华,杨顺清,等.超声波辅助乙醇提取莲子心总黄酮及其抗氧化活性的研究[J].食品工业科技,2012,33(3):220-223
Study on the HPLC Fingerprint of Nelumbinis Plumula
ZENG Jian-wei1,2,CHU Jian-feng1,2,LI Xi-hai1,2,CAI Qiao-yan1,2,LIN Shan1,2,ZHU Xiao-qin1,2,CHEN Da-xin1,2,WU Jin-zhong1,2#
(1Institute of Integrated Traditional Chinese and Western Medicine,Fujian University of Traditional Chinese Medicine,Fuzhou350122; 2Key Laboratory of Integrated Traditional and Western Medicine for Senile Diseases of Fujian Province,Fuzhou350122)
Objective:To establish the HPLC fingerprint of Nelumbinis Plumula,in order to provide a reliable method for the quality evaluation of Nelumbinis Plumula.Methods:Used Agilent HC C18(4.6 mm×250 mm,5 μm)column,with acetonitrile-0.1% triethylamine solution(10∶90)as mobile phase,gradient elution,flow rate was 1 ml/min,the detection wavelength was 284 nm,the column temperature is 30℃,established the HPLC fingerprint of Nelumbinis Plumula,and evaluated the similarity.Results:The similarity of 10 batches of Nelumbinis Plumula from different regions reached more than 0.90.which shows that the main chemical components of these 10 batches of Nelumbinis Plumula from different regions were basically identical.Conclusion:This method can preferably reflect the chemical composition information of Nelumbinis Plumula,and it is simple and reproducible.It provides a reference for the scientific evaluation of the quality of Nelumbinis Plumula.
Nelumbinis Plumula;HPLC;Fingerprint;Similarity
R914
B
10.13638/j.issn.1671-4040.2017.03.100
2017-02-07)
福建中医药大学校管课题-科研创新平台专项(编号:X2015022)
#通讯作者:吴锦忠,E-mail:jinzhongfj@126.com
