QuEChERS-HPLC-MS/MS快速测定染色黄鱼中3种碱性橙类染料
2017-06-22孙稚菁王灵芝任国杰张国翠卢熠川
孙稚菁,王灵芝,任国杰,张国翠,卢熠川
(大连市产品质量检测研究院,辽宁大连116630)
QuEChERS-HPLC-MS/MS快速测定染色黄鱼中3种碱性橙类染料
孙稚菁,王灵芝,任国杰*,张国翠,卢熠川
(大连市产品质量检测研究院,辽宁大连116630)
采用高效液相色谱-串联质谱法建立快速检测染色黄鱼中碱性橙Ⅱ,碱性橙21和碱性橙22的分析方法。将待测样品经QuEChERS法进行预处理,选用乙腈溶液超声提取,经氯化钠和C18粉末净化,以10 mmol/L的醋酸铵溶液(含有0.1%甲酸)-乙腈(含有0.1%甲酸)作为流动相,经Agilent poroshell 120 EC-C18(2.7 μm,2.1 mm×50 mm)色谱柱分离,采用多反应检测模式(MRM)检测。用标准曲线外标法进行定量。在优化条件下,目标物的线性范围为1 μg/L~100 μg/L,相关系数均大于0.999。该3种碱性橙类染料的定量下限为5 μg/kg。在3个浓度水平下,各目标物的回收率均大于85%,相对标准偏差(RSD)均低于5%。方法准确、快速、简便、灵敏、可靠。可用于染色黄鱼中此3种碱性橙类染料的快速测定。
QuEChERS;高效液相色谱-串联质谱法;碱性橙;黄花鱼
碱性橙Ⅱ(Basic OrangeⅡ)是一种偶氮类碱性工业染料,俗名“王金黄”、“块黄”等,主要用于纺织品、皮革制品及木制品的染色[1]。由于在中性或偏碱性条件下,碱性橙Ⅱ与蛋白质吸附较牢固,比其他水溶性染料如柠檬黄、日落黄等更易于在豆类制品以及鲜海鱼上染色且不易褪色,因此一些不法商贩用碱性橙Ⅱ对豆腐皮、黄鱼进行染色,以次充好,以假冒真,欺骗消费者。另外碱性橙21和碱性橙22也是常见的碱性橙类工业染料。由于这些工业染料具有致癌、致畸变性,会对人体造成严重的危害,因此在卫生部和农业部等公布的《151种食品和饲料中非法添加物质名单》中禁止碱性橙染料在食品中使用。
通过文献和标准检索发现,这3种碱性橙染料的检测方法主要为高效液相色谱法[2-6]、高效液相色谱-串联质谱法[7-14],另外还有气相色谱-串联质谱质谱法[15]和薄层色谱法[16]等方法。通过文献分析发现,这些方法多数前处理比较复杂,费时费力,多为关于碱性橙Ⅱ的检测,且多侧重于豆制品中碱性橙类染料的检测,关于碱性橙21和碱性橙22的检测方法较少。本文针对频发的染色黄鱼现象,通过试验开发了一种基于QuEChERS快速前处理方法基础上的高效液相色谱-串联质谱法。该方法操作简单、灵敏度高,结果准确可靠,回收率和重现性良好,保证了消费者的安全,提高了市场监督的效率,为食品安全监管部门提供技术参考和支持。
1 试验部分
1.1 试剂与仪器
碱性橙Ⅱ、碱性橙21、碱性橙22(纯度均大于98%):德国CNW公司;醋酸铵(色谱纯):美国Alfa Aesar公司;乙腈和甲醇(色谱纯):德国Merck公司。
Agilent 6490高效液相色谱-串联质谱仪(ESI源):安捷伦;BSA224S电子天平:赛多利斯科学仪器有限公司;KQ-250DB超声波清洗器:昆山市超声仪器有限公司;3-18KS离心机:Sigma公司;IKA T18均质器:Basic公司;XW-80A漩涡混合器:上海精科实业有限公司。
1.2 溶液配制
1.2.1 标准储备溶液
称取碱性橙Ⅱ、碱性橙21、碱性橙22各10 mg(精确至0.1 mg),分别置于50 mL容量瓶中,加入适量甲醇超声溶解,冷却后用甲醇定容至刻线,配制成浓度为0.2 mg/mL的标准储备溶液。
1.2.2 标准溶液的配制
准确移取3种标准储备液适量,用甲醇逐级稀释配制100、80、50、25、10、1 μg/L的系列混合标准溶液,用于标准曲线的绘制。
1.3 试样制备
称取粉碎好的鱼糜样品5.0g,加入乙腈25 mL,均质,超声10min,加入NaCl 2 g,涡旋混匀,经5 000 r/min离心处理3 min,取上清液2 mL加入C18粉末0.1 g,涡旋1 min,经0.22 μm微孔滤膜滤过,待测。
1.4 仪器分析条件
1.4.1 液相分离条件
色谱柱:Agilent poroshell 120 EC-C18(2.7 μm,2.1 mm×50 mm)。流动相:A 10 mmol/L的醋酸铵溶液(含有0.1%甲酸);B乙腈(含有0.1%甲酸)。梯度洗脱条件:0~3 min,40%~95%B;3 min~4 min,95%~40% B;4 min~6 min,40%B。柱温:35℃。流速:0.2 mL/min。进样量:2 μL。
1.4.2 质谱分析条件
离子源:电喷雾电离源(ESI源);离子源温度:300℃;检测方式:多反应监测(MRM);雾化气:氮气,30 psi;干燥气:氮气,流速:14 L/min;鞘气温度:350℃,流速:11 L/min;碰撞气:氮气;毛细管电压:3 500 V;碰撞电压:380 V;其他质谱参数见表1。
1.5 定性分析与定量测定
1.5.1 定性分析
分别将试样溶液与标准溶液按“1.4仪器分析条件”进行检测,比较在相同条件下获得的样品溶液与标准物质的分离谱图。以目标化合物色谱峰的保留时间与目标化合物两个离子的丰度比进行定性分析。
1.5.2 定量测定
移取“1.2.2”系列标准溶液,按照“1.4”色谱条件进行仪器分析,以系列标准溶液的质量浓度为横坐标,峰面积为纵坐标,制作标准曲线,用于定量计算。
2 结果与讨论
2.1 样品前处理条件的优化
经试验发现乙腈对于碱性橙类着色剂具有良好的提取效果,但在已经提取溶液中会含有大量的水及其水带入的大极性杂质,氯化钠的加入可以有效地分离出水分和大极性杂质,由于鱼类产品含有一定的脂类物质,经乙腈提取后这些脂类的存在会影响目标物的测定,降低色谱柱的寿命,C18粉末的加入很好地能吸附这些小极性的杂质。经试验验证发现,样品经乙腈提取后,经过氯化钠和C18粉末的纯化后,可以在保证目标物提取效率的前提条件下获得较为纯净的提取溶液。
2.2 液相色谱条件的优化
2.2.1 色谱柱的选择
试验通过考察3种目标成分在C18色谱柱上的分离效果,发现目标物在普通C18色谱柱上峰型严重拖尾,为了保证目标物的正模式响应,流动相中酸的存在又加剧了目标物的拖尾现象。鉴于这3种化合物的结构性质,推测造成拖尾的原因可能是目标物与固定相上残余硅羟基之间的相互作用所致。尝试选择Aiglent poroshell 120 EC-C18色谱柱用于改善3种目标化合物的色谱分离。研究显示,在优化的色谱条件下,可以获得良好的色谱分离效果,试验最终选择Aiglent poroshell 120 EC-C18作为色谱柱进行分离。
2.2.2 流动相中洗脱溶剂及改性剂的优化
液相色谱-串联质谱分析中的流动相通常为乙腈或甲醇和水,为了保证化合物的离子响应通常会加入甲酸、乙酸、乙酸铵等不同的改性剂,经过试验验证发现,乙腈-水系统可以获得良好的分离效果,加入甲酸的溶剂系统能明显提高离子响应,在酸性条件下醋酸铵的加入可以改善离子响应强度,并能保持良好的峰型,经过多次试验验证,以10 mmol/L的醋酸铵溶液(含有0.1%甲酸)和乙腈(含有0.1%甲酸)作为流动相系统进行梯度洗脱可以获得良好的分离图谱。
2.3 质谱条件的优化
将3种目标物的标准溶液在质谱上进行全扫描,在ESI(+)模式下得到3种目标化合物的分子离子峰。通过优化碰撞能等参数,得到3种化合物的子离子,每种物质选择2个子离子,将响应值高的离子作为定量离子,另一个作为定性离子。3种着色剂的MRM质谱参数见表1。
在该优化仪器条件下,3种标准物质的多反应检测谱图如图1所示(各标准物质浓度为5 μg/L)。
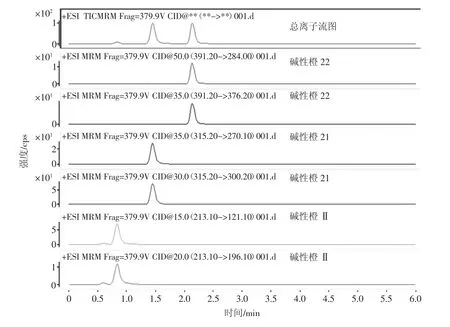
图1 3种着色剂的多反应检测谱图Fig.1 MRM chromatograms of 3 colorants
2.4 线性范围与相关系数
移取浓度分别为100、80、50、25、10、1 μg/L的系列混合标准溶液,在优化色谱条件下进行分析。研究结果表明:各目标物在1 μg/L~100 μg/L范围内具有良好的线性关系,相关系数均大于0.999。各目标物的线性回归方程及相关系数如表2所示。
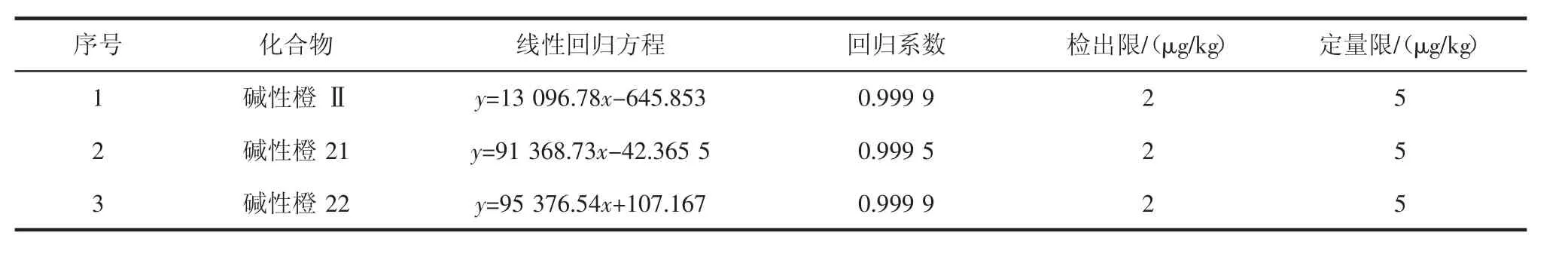
表2 3种着色剂的线性方程,相关系数,检出限与定量限Table 2 Linear equations,correlation coefficients(r),LODs and LOQs of 3 colorants
2.5 回收率与定量下限
向不含目标物质的空白样品基质中定量添加混合标准溶液,进行加标试验,计算信噪比(S/N)。以S/ N>3为检出限,以S/N>10为定量下限,具体试验结果见表3。对3种目标物分别在5、50、500 μg/kg 3个浓度水平下进行加标回收试验,每个水平测定6个样品,其回收率与相对标准偏差见表3。
由表3可知,各目标物的加标回收率为89.45%~99.49%,相对标准偏差(RSD)均低于5%。方法显示了良好的回收率与精密度。
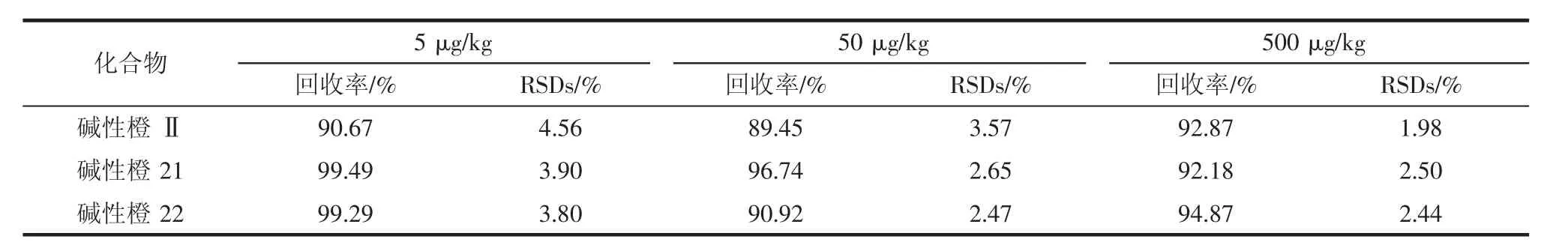
表3 3种着色剂的加标回收率与相对标准偏差Table 3 The average recoveries and RSDs of 3 colorants
2.6 实际样品测试
应用本法对72个市售黄花鱼样品进行测定。通过对测定结果统计分析发现,共有1个检出碱性橙Ⅱ,通过对阳性样品的分离图谱进行分析发现,分析图谱中所存在的干扰很少,该方法适用于实际样品的分析测定。
3 结论
本文采用QuEChERS-高效液相色谱-串联质谱法建立了染色黄鱼中3种碱性橙类着色剂的快速替换方法。空白样品加标试验及实际样品测定结果表明,该方法准确、简便、灵敏、可靠,可用于染色黄鱼中3种碱性橙类着色剂的快速替换和测定,能够为政府法规的执行和市场的质量监管提供有效的技术支持和保障。
[1]REBANE,I LEITO,S YURCHENKO,et al.A review of analytical techniques for determination of Sudan I-IV dyes in food ma-trixes [J].Journal of Chromatography A,2010,1217(17):2747-2757
[2]中华人民共和国国家质量监督检验检疫总局,中国国家标准化管理委员会.GB/T 23496-2009食品中禁用物质的检测碱性橙染料高效液相色谱法[S].北京:中国标准出版社,2009
[3]安徽省质量技术监督局.DB34/T 1107-2009豆制品中碱性橙的测定高效液相色谱法[S].合肥:安徽省质量技术监督局,2009
[4]朱浩,李小平,陈晓红,等.固相萃取-高效液相色谱法同时测定豆制品中的碱性嫩黄O、酸性橙Ⅱ和碱性橙Ⅱ[J].分析实验室, 2013,32(9):63-67
[5]赵宏,图雅,胡芬.高效液相色谱法测定辣椒粉中的碱性橙[J].中国卫生检验杂志,2012,22(1):19-20
[6]陈林,温佳欣,雷毅,等.高效液相色谱法同时快速检测腌腊肉制品中20种非法添加合成色素[J].分析测试学报,2015,34(9):1008-1013
[7]福建省质量技术监督局.DB35/T897-2009食品中碱性橙、碱性嫩黄O和碱性桃红T含量的测定[S].福州:福建省质量技术监督局,2009
[8]吉林省卫生厅.DBS22/008-2012食品中酸性橙、碱性橙2和碱性嫩黄的测定液相色谱-串联质谱法[S].长春:吉林省卫生厅, 2012
[9]浙江省质量技术监督局.DB33/T 703-2008食品和农产品中多种碱性工业染料的测定液相色谱-串联质谱法[S].杭州:浙江省质量技术监督局,2008
[10]张燕,舒平,张妮妮,等.QuEChERS前处理高效液相色谱-串联质谱法同时测定食品中6种工业染料[J].食品安全质量检测学报,2016,7(7):2790-2796
[11]刘思洁,范明,姜楠,等.超高效液相色谱-串联质谱法测定食品中酸性橙Ⅱ、碱性橙2和碱性嫩黄[J].中国卫生检验杂志,2013, 32(9):63-67
[12]林黛琴,万承波,邱萍,等.液相色谱-串联质谱法快速测定食品中4种黄色工业染料[J].质谱学报,2013,34(3):170-178
[13]林奕云,付强,蔡大川,等.UPLC-MS/MS法测定食品中四种碱性工业染料[J].食品工业,2016,37(5):278-282
[14]赵珊,张静,丁晓静,等.超高效液相色谱电喷雾串联四极杆质谱法检测豆制品中12种禁用工业染料[J].分析测试学报,2016, 35(4):432-437
[15]高鸣翔,张家树,蔡颖,等.GC/MS测定腐皮中碱性橙Ⅱ的含量[J].化学世界,2012(1):30-31
[16]夏立娅,韩媛媛,匡林鹤,等.薄层色谱扫描法同时检测豆制品中碱性橙、皂黄、柠檬黄和日落黄以及辣椒粉中酸性橙Ⅱ、丽春红2R和罗丹明B[J].分析实验室,2010,29(6):15-18
Determination of 3 Basic Orange in Dyed Yellow Croaker by QuEChERS-High Performance Liquid Chromatography-Tandem Mass Spectrometry
SUN Zhi-jing,WANG Ling-zhi,REN Guo-jie*,ZHANG Guo-cui,LU Yi-chuan
(Dalian Institute of Product Quality Supervision&Inspection,Dalian 116630,Liaoning,China)
A high performance liquid chromatography-tandem mass spectrometry(HPLC-MS/MS)method was developed for the rapid determination of 3 basic orange in dyed yellow croaker.To pass through the QuEChERS method under test sample preprocessing,ultrasonic extraction with acetonitrile solution,purification by sodium chloride and C18powder,the extract was separated on an Agilent poroshell 120 EC-C18(2.7 μm,2.1 mm×50 mm)using a gradient elution program with mobile phase of 10 mmol/L ammonium acetate(containing 0.1%formic acid)-acetonitrile(containing 0.1%formic acid),with multiple reactions monitoring(MRM)mode for testing.Using external standard method for the quantitative standard curve.The linear ranges of 3 analytes were in the range of 1 μg/L-100 μg/L,with correlation coefficients more than 0.999.The limits of quantiation(LOQs)were 5 μg/kg.The average recoveries at three spiked levels were greater than 85%,with RSDs less than 10%.This method is accurate,simple,sensitive and reliable,and can be used for analysis of 3 basic orange in dyed yellow croaker.
QuEChERS;high performance liquidchromatography-tandem mass spectrometry;basic orange;croaker
10.3969/j.issn.1005-6521.2017.12.031
2017-03-06
孙稚菁(1972—),女(汉),高级工程师,本科,研究方向:食品和化工产品质量安全监测。
*通信作者:任国杰(1987—),男(汉),工程师,硕士,研究方向:食品、药品以及化妆品检测方法的研究与开发。
