双膦镍络合物/EADC催化乙烯齐聚与Friedel-Crafts烷基化的串联反应
2017-06-05孟雪姣陈延辉
孟雪姣, 张 乐, 陈延辉, 姜 涛
(天津科技大学 化工与材料学院, 天津 300457)
双膦镍络合物/EADC催化乙烯齐聚与Friedel-Crafts烷基化的串联反应
孟雪姣, 张 乐, 陈延辉, 姜 涛
(天津科技大学 化工与材料学院, 天津 300457)
合成并表征了二苯基膦甲基-二苯基膦基-二甲基硅烷络合物(C1);考察了反应温度、nAl/nNi及溶剂的种类等对C1/EtAlCl2催化乙烯齐聚行为的影响。结果表明,以二氯乙基铝(EADC)为助催化剂、甲基环己烷为溶剂时,C1/EADC催化乙烯齐聚的活性可达4.32×106g/(molNi·h),产物为C4和C6馏分,其中C4馏分中1-丁烯的选择性大于94%;以甲苯为溶剂时,C1/EADC催化乙烯齐聚得到的短链烯烃与甲苯发生原位Friedel-Crafts烷基化反应,产物为多取代烷基甲苯;EADC在该催化体系中起到了双功能的作用,一是齐聚反应的助催化剂,二是烷基化反应的催化剂。
镍络合物; EADC; 乙烯齐聚; Friedel-Crafts烷基化; 烷基苯
烷基苯是生产洗涤剂和驱油剂的重要原料,可通过苯类化合物与线性α-烯烃(LAO)在酸性催化剂作用下发生Friedel-Craft烷基化反应制得。乙烯齐聚是制备LAO的重要反应,所用的催化剂包括金属铝系、钛系、镍系、锆系、铁系、铬系等,其中镍系催化剂在Shell公司的SHOP工艺中首次得到应用。1995年Brookhart小组发现2-亚胺镍配合物的催化活性,这一开创性的研究使镍基烯烃聚合催化剂的开发受到重新关注[1-3]。同时镍系催化剂因具备价廉易得、催化活性高、低碳α-烯烃线性选择性高和反应条件温和等优点,成为学术界的研究热点。近年来对乙烯齐聚镍配合物催化剂的研究工作集中在催化剂的结构调控上,主要围绕改变配体的种类和配体取代基展开。根据配位体的不同,镍系催化剂可分为 P∧O 配位型、N∧N 配位型、N∧O 配位型、N∧P 配位型和 P∧P 配位型等[4-13]。Song等[14]研究报道了PNP型的镍(II)配合物在助催化剂EtAlCl2(EADC)或MAO的作用下可以催化乙烯齐聚反应的发生,生成物主要为丁烯(96%)和少量的己烯低聚物。文献[14-16]采用镍系催化剂和EtAlCl2可以实现乙烯齐聚与烷基化的串联反应,一步合成烷基苯化合物,为齐聚催化方面的研究提供了新思路。但该方向的研究鲜有报道。
在本研究中,通过改变中心原子的种类以及配体骨架的长度对PNP型配体进行改造,合成并表征了新型的双膦镍络合物C1,研究了配体结构对乙烯齐聚行为的影响,考察了助催化剂种类、nAl/nNi、溶剂种类以及温度等因素对乙烯齐聚与Friedel-Craft烷基化串联反应的影响。
1 实验部分
1.1 试剂与仪器
二苯基氯化磷(质量分数98%)、二苯基膦(质量分数98%)、(氯甲基)二甲基氯硅烷(质量分数99%)、三乙基铝、甲基铝氧烷(MAO,1.4 mol/L甲苯溶液)、正丁基锂(2.4 mol/L己烷溶液)、一氯二乙基铝(DEAC,1.0 mol/L甲苯溶液)、二氯乙基铝(EADC,0.9 mol/L正庚烷溶液)、三异丁基铝(TIBA,1.4 mol/L甲苯溶液)、二甲醚二溴化镍(Ⅱ)((DME)NiBr2,质量分数98%)、1-己烯(质量分数>99%)、氢化钾(质量分数99%),以上试剂均为美国Aldrich试剂公司产品;苯(分析纯,质量分数≥99%)、甲苯(分析纯,质量分数≥99%)、甲基环己烷(分析纯,质量分数99%)、正己烷(分析纯,质量分数≥99%),以上试剂均为天津市江天化工技术有限公司产品,使用前经分子筛干燥、金属钠回流等脱水处理;乙烯(聚合级,质量分数99.9%)、高纯氮气,天津市赛美特特种气体公司产品。
vario EL Ⅲ型元素分析仪,德国Elementar公司产品;Voyager-DE STR型MALDI-TOF,美国AB SCIEX公司产品;DMX400型核磁共振仪(NMR),美国Bruke公司产品;Agilent GC 7890A 气相色谱仪,美国安捷伦科技有限公司产品。
1.2 镍络合物的合成
1.2.1 双(二苯基膦基)甲基二甲基硅烷(L1)的合成
在-80℃下,将正丁基锂 (41.6 mL,99.84 mmol,2.4 mol/L的己烷溶液)逐滴加入到二苯基膦(18.62 g,0.1 moL)的四氢呋喃溶液中,保持该温度持续搅拌1 h,随后将反应溶液温度缓慢升至室温继续搅拌1 h,减压抽去溶剂,用正己烷洗涤所得固体,过滤、干燥得到锂盐。在-30℃下,向锂盐(2.40 g,12.5 mmoL)的正己烷溶液中缓慢滴加(氯甲基)-二甲基氯硅烷(0.86 g,6.0 mmol),持续搅拌3 h,随后使反应溶液温度缓慢升至室温,减压抽去溶剂,将所得固体用正己烷洗涤、过滤,重结晶得到黄色晶体状的目标产物——双(二苯基膦基)甲基二甲基硅烷(L1),收率45%。
1.2.2 L1/NiBr2(C1)的合成
双膦镍络合物的合成采用的路线如图1所示。在室温下,将(DME)NiBr2(0.154 g, 0.5 mmoL)的二氯甲烷溶液逐滴加入到L1(0.220 g, 0.5 mmoL)的二氯甲烷溶液中,完成滴加后搅拌24 h。减压抽去溶剂,得到棕色固体,用正己烷洗涤、过滤,将棕色固体溶于正己烷/四氢呋喃混合溶剂,在-35℃下重结晶得到目标产物——L1/NiBr2(C1),收率为79%。
1.2.3 双(二苯基膦基)甲基二甲基硅烷(L1)的表征
1H NMR (400 MHz, C6D6)δ7.53 (td, J=7.8, 1.4 Hz, 4H), 7.41~7.29 (m, 4H), 7.10~6.90 (m, 12H), 1.55 (d, J=2.3 Hz, 2H), 0.11 (d, J=4.6 Hz, 6H)。
31P NMR (162 MHz, C6D6)δ-22.97 (d, J=17.6 Hz), -55.86 (d, J=17.5 Hz)。
13C NMR (101 MHz, C6D6)δ143.18 (d, J=16.1 Hz), 138.05 (d, J=16.9 Hz), 136.19 (d, J=17.3 Hz), 134.73 (d, J=19.8 Hz), 130.48 (dd, J=17.3, 6.7 Hz), 15.49 (dd, J=33.5, 11.7 Hz), 0.14 (dd, J=11.8, 4.8 Hz)。
L1:Anal. Calc for C27H28P2Si: C, 73.21; H, 6.33. Found: C, 73.28; H, 6.38. EI-MS:m/z=422.1。
1.2.4 L1/NiBr2(C1)的表征
C1:Anal. Calc for C27H28Br2NiP2Si: C, 49.01; H, 4.24. Found: C, 49.06; H, 4.27。MALDI-TOF-MS:m/z=[M+Na-81Br]+=603.3。
1.3 乙烯高压齐聚反应
所有的乙烯高压齐聚反应均在140 mL的Grest实验室压力反应釜中进行。反应前将反应釜置于105℃的烘箱中干燥2 h,趁热进行3次抽真空、通高纯N2的重复操作,除去反应釜中的氧气和残余的水分,然后用乙烯置换3次。依次将定量的溶剂、助催化剂加入到已预热的高压釜中,搅拌后迅速加入主催化剂,通入乙烯,使釜内压力增加至预定值并保持恒定。乙烯齐聚进行30 min后停止反应,反应结束后用冻乙醇淬灭反应,释放釜压至常压。滤液取样后用气质联用仪(GC-MS)和气相色谱进行定性和定量分析。
2 结果与讨论
2.1 甲基环己烷体系中C1/EADC催化乙烯齐聚
以甲基环己烷为溶剂,C1/EADC可以催化乙烯发生齐聚反应,产物为丁烯和己烯。考察反应温度、nAl/nNi、助催化剂种类对催化体系催化乙烯齐聚性能的影响如表1所示。其中甲基环己烷/C1/EADC体系催化下C4馏分中1-C4的选择性为94.80%~97.80%,催化活性可达4.32×106g/(molNi·h)。用MAO、DEAC代替EADC作为助催化剂,乙烯齐聚表现为催化活性低、线性α-烯烃的选择性低。
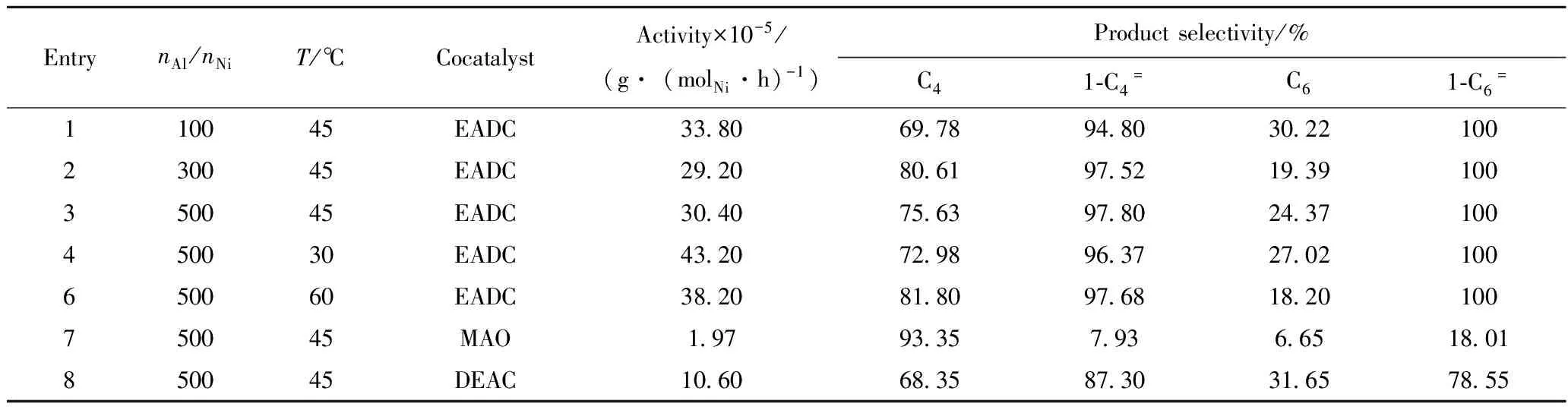
表1 甲基环己烷/C1/EADC体系中反应温度、nAl/nNi和助催化剂种类对乙烯齐聚催化性能的影响Table 1 Effect of reaction temperature,nAl/nNi and cocatalyst on the catalytic property of C1/EADC for ethylene oligomerization in methylcyclohexane
Reaction conditions: Pressure of 1.0 MPa; Time of 30 min;n[Cat]=4.8 μmoL
2.2 甲苯体系中C1/EADC催化乙烯齐聚和Friedel-Crafts烷基化反应
2.2.1 助催化剂及溶剂种类对乙烯齐聚/Friedel-Crafts烷基化串联反应的影响
助催化剂的种类对催化剂活性和选择性的影响见表2。用EADC做助催化剂与MAO、DEAC做助催化剂相比反应活性明显升高,原因可能是成对的氯原子具有两个路易斯酸配位基可供其与金属中心配位,从而对催化剂的催化性能造成影响[17]。TIBA做助催化剂与MAO做助催化剂相比活性大幅降低,这可能是由于不同的烷基取代基形成的不同的金属键对金属活性中心影响的结果,其次助催化剂的空间结构也可能造成这一结果,不同烷基对烷基铝的空间位阻的影响明显不同。用TIBA做助催化剂时,C4馏分的选择性最高,为96.46%。用MAO、DEAC、TIBA做助催化剂时均未出现Friedel-Crafts烷基化反应,仅EADC做助催化剂时出现Friedel-Crafts烷基化反应。文献[14,18-21]指出,强路易斯酸可以催化芳香族化合物与烯烃生成Friedel-Crafts烷基化产物,例如路易斯酸AlCl3在没有金属化合物的参与下可以催化甲苯与乙烯发生Friedel-Crafts烷基化反应,但是EADC在没有金属化合物的参与下却不可以发生此反应。这说明EADC能够活化金属中心形成乙烯齐聚反应和Friedel-Crafts烷基化反应的活性物种,宋磊等[22]指出这种活性物种在生成短链的低聚物以后会在高温下快速分解,并且转化为新的能够催化甲苯发生Friedel-Crafts烷基化反应的路易斯酸。这种路易斯酸的催化原理是,先是酸的质子化作用形成碳正离子聚合物种,然后经过重新排列形成一种更加稳定的化合物,这种亲电子的物种和甲苯反应生成烷基化的产物,如图2所示。

表2 助催化剂种类对催化剂催化活性和产物分布的影响Table 2 Effect of cocatalyst on catalytic activity and product selectivity
Reaction conditions: Pressure of 1.0 MPa; Time of 30 min; Solvent toluene; Temperature of 45℃;n[Cat]=4.8 μmol;nAl/nNi=700
1)Friedel-Crafts alkylation products

图2 EADC在乙烯齐聚与Friedel-Crafts烷基化串联反应中的作用Fig.2 The role of EADC in the tandem reaction of ethylene oligomerization and Friedel-Crafts alkylationA,B,C,D,E,F: Friedel-Crafts alkylation products
溶剂对C1/EADC催化体系的性能有着重要的影响,结果如表3所示。以甲苯为溶剂,EADC为助催化剂时,发生了Friedel-Crafts烷基化反应,产物中有烷基苯化合物存在。所得产物为丁烯、己烯和6种烷基化甲苯:1-丁基甲苯(B)、双-丁基甲苯(D)和三-丁基甲苯(F)是主要的产品,乙基甲苯(A)、己基甲苯(C)、丁基-己基甲苯(E)的含量较少。以苯做溶剂,EADC做助催化剂,Friedel-Crafts烷基化反应的产物与甲苯作溶剂相比较少,这可能是因为甲基取代基的给电子能力较强,能更好地稳定活性阳离子金属或促进其活化,这种影响可能会使活性位的数目增多或者改变催化剂的空间结构使金属中心更易参与反应,从而提高整体的活性,有利于烷基化[17]。
通过气相色谱分析可知烷基化甲苯存在异构体,例如化合物B有3种异构体,分别是邻、对位被直链丁基或非直链丁基所取代[23]。根据结构推测D、E是B、C进一步与α-烯烃烷基化反应所得,由于是在二取代芳香烃的基础上进行Friedel-Crafts烷基化反应,取代基的位阻效应较大,此时烷基化反应比甲苯与烯烃的反应更难发生,因此D、E的含量减少。F则是由D进一步发生烷基化反应的产物,是经3次烷基化的芳香烃产物,由于反应困难,含量较D更低[24]。乙基甲苯(A)的含量较少,说明只有极少量的乙烯与甲苯发生烷基化反应,乙烯与甲苯的烷基化反应困难。笔者做了1组空白实验,即在相同的条件下,不加入镍络合物,仅加入EADC和甲苯与乙烯反应,结果除了极少量的烷基化产物(A)生成以外无其他产物生成,两组实验的结果一致。同时这一结果还证明没有双膦镍络合物参与反应,乙烯齐聚反应与Friedel-Crafts烷基化反应都不会发生。只有在催化体系下通过乙烯齐聚反应先生成α-烯烃,Friedel-Crafts烷基化反应才会发生,因此乙烯齐聚与Friedel-Crafts烷基化反应是串联反应。图3为C1/EADC催化乙烯齐聚与 Friedel-Crafts 烷基化反应的串联反应过程。催化体系先进行乙烯齐聚反应,即乙烯在C1/EADC/甲苯作用下经链增长和β-H链转移,得到C4、C6等短链烯烃,这些短链烯烃进而作为反应物与甲苯溶剂发生烷基化反应,得到多取代芳香烃。
在没有镍络合物的参与下,乙烯与甲苯的烷基化反应困难,因此Friedel-Crafts烷基化反应是在丁烯以及链长更长的烯烃的参与下发生的。相同条件下,甲苯、1-己烯和EADC进行反应,结果是EADC催化1-己烯与甲苯发生Friedel-Crafts烷基化反应,转化为烷基化产物,气质联用仪(GC-MS)分析结果表明:所得产物为C13(1-己基甲苯)、C19(双-己基甲苯)和C25(三-己基甲苯),其中大多数的产物为单取代产物C13(1-己基甲苯)。用丙烯和1-丁烯代替1-己烯进行上述反应,也得到了相应的多取代芳香烃,分别是丙基-甲苯,丁基-甲苯。EADC在该催化体系中起到了双功能的作用,一是齐聚反应的助催化剂,二是烷基化反应的助催化剂。这与Dyer等、Gao等和Omondi等报道的结果一致。
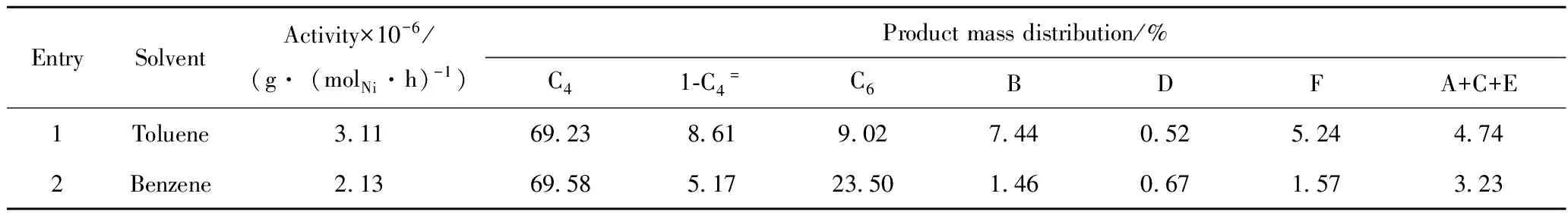
表3 溶剂种类对C1/EADC催化乙烯齐聚与Friedel-Crafts烷基化反应的影响Table 3 Effect of solvent on ethylene oligomerization and Friedel-Crafts alkylation reactions
Reaction conditions: Pressure of 1.0 MPa; Time of 30 min; Temperature of 45℃;n[Cat]=4.8 μmol; Cocatalyst of EtAlCl2;nAl/nNi=300

图3 C1/EADC催化乙烯齐聚与Friedel-Crafts烷基化串联反应的过程Fig.3 Tandem action of ethylene oligomerization and Friedel-Crafts alkylation
2.2.2nAl/nNi对C1/EADC催化乙烯齐聚/Friedel-Crafts烷基化串联反应的影响
不同的nAl/nNi对C1/EADC催化剂的活性和产物的分布有明显影响,其结果如表4所示。由表4可以看出,随着nAl/nNi的增加,催化剂的活性呈现先增加后降低的趋势。当nAl/nNi从100增加到700时,催化剂活性从2.17×106g/(molNi·h)提高到9.22×106g/(molNi·h),此时催化剂活性达到最大值。原因可能是EADC用量较少时,大部分EADC先用于消除体系中残留的氧和水,无法使金属配合物烷基化形成活性位,所以催化活性随nAl/nNi的增加而提高,当nAl/nNi继续增加,过多的EADC会导致金属活性中心过度还原,导致催化剂活性降低[25]。当nAl/nNi为100时,1-丁烯的选择性为88.65%,随着nAl/nNi的增加,1-丁烯的选择性出现明显的下降现象,说明此时乙烯齐聚生成的线性α-烯烃很大程度上与甲苯溶剂反应转化为烷基化产物。当nAl/nNi为700时,烷基化的程度相对较高,继续增加nAl/nNi,烷基化的程度并没有继续增加,反而有所下降,乙烯齐聚的活性也随之降低,原因可能与EADC浓度过高时产生的钝化作用有关,EADC浓度过高时杂质含量增加,从而导致这种钝化作用的产生,影响催化剂的活性以及α-烯烃的选择性。由于该双膦镍络合物/EADC体系下的乙烯齐聚与Friedel-Crafts烷基化的串联反应产物较多,较复杂,所以寻求一种催化剂可减少或消除Friedel-Crafts烷基化反应,从而促进乙烯齐聚的反应,或能够提高Friedel-Crafts烷基化反应仅对一种产物的选择性是今后研究的方向[26]。
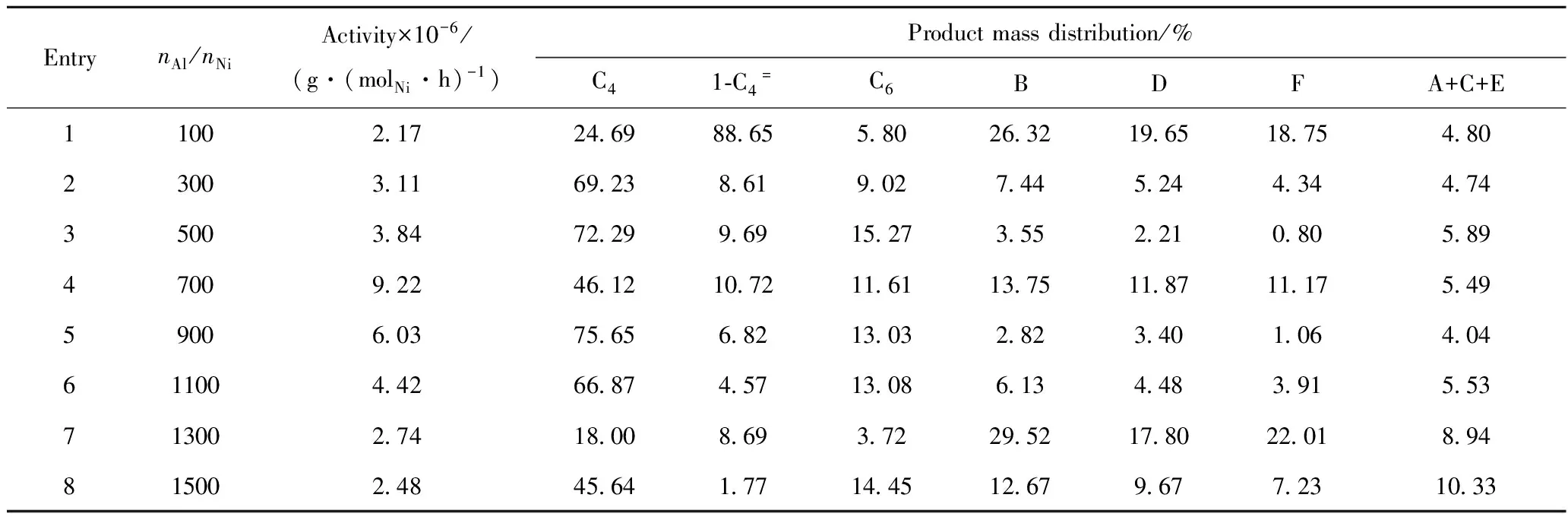
表4 nAl/nNi对乙烯齐聚与Friedel-Crafts烷基化反应的影响Table 4 Effect of nAl/nNi on ethylene oligomerization and Friedel-Crafts alkylation reactions
Reaction conditions: Pressure of 1.0 MPa; Time of 30 min; Temperature of 45℃;n[Cat]=4.8 μmol; Cocatalyst of EtAlCl2
2.2.3 反应温度对C1/EADC催化乙烯齐聚/Friedel-Crafts烷基化串联反应的影响
乙烯齐聚反应和Friedel-Crafts烷基化反应属于放热反应,改变温度会影响催化剂的活性和烷基化产物的选择性。反应温度对C1/EADC催化体系活性及产物选择性的影响见表5。由表5可以看出,随着反应温度的升高,C1/EADC催化剂活性和对C4馏分的选择性均呈先上升后下降的趋势。当温度从15℃升高至45℃,C1/EADC催化剂活性从3.02×106g/(molNi·h) 提高到9.22×106g/(molNi·h),C4馏分的选择性从3.90%提高到46.12%,C6馏分的选择性从1.90%提高到11.61%,可能是由于随着反应温度的升高,分子的平均动能增加,齐聚反应的链增长速率和链转移速率都有加快的趋势,有利于链引发、链增长反应的进行,从而使活性增加,丁烯和己烯的选择性提高。
甲苯与直链烯烃烷基化属于正碳离子反应机理,首先是直链烯烃与酸的质子化作用形成碳正离子聚合物种,然后经过重新排列形成另外一种更加稳定的化合物,这种亲电子的物种和甲苯反应生成烷基化的产物[19],此过程中生成的直链烯烃会异构化生成非直链烯烃,温度较低时可以有效抑制直链烯烃异构化副反应的进行,所以在15℃和30℃时,产物中B、D、F的含量较45℃和60℃时的高,原因可能是温度较低时,异构化程度较弱,大部分直链烯烃直接与甲苯溶剂发生Friedel-Crafts烷基化反应;温度较高时,1位的碳正离子不稳定,直链烯烃会首先异构化为非直链烯烃,然后分别进行烷基化反应,因此烷基化程度会降低[15]。此外温度过高还会导致活性物种的钝化、分解以及链增长的终止,生成的大分子质量的烯烃以及烷基化产物溶解在溶剂中也会影响乙烯向催化剂活性中心的插入反应,从而导致催化剂活性下降[27]。同时,烷基化反应的速率快于乙烯齐聚的速率,使得产物中丁烯的选择性下降,烷基化产物的选择性增加。
3 结 论
合成并表征了双膦镍络合物(C1)并将其用于催化乙烯齐聚的反应。
(1)以EADC为助催化剂,分别在甲基环己烷和甲苯溶剂中进行对比研究,结果显示甲基环己烷为溶剂时,该络合物仅发生乙烯齐聚反应,产物为丁烯和己烯,产物C4馏分中1-丁烯的选择性均在94%以上,说明双膦镍络合物/EADC是高效的乙烯二聚催化体系。
(2)以甲苯为溶剂时,C1能够很好地发生乙烯齐聚反应和Friedel-Crafts烷基化的串联反应,生成丁烯、己烯和6种烷基化产物。对比实验结果说明,该双膦镍络合物仅在甲苯溶剂中发生Friedel-Crafts烷基化反应。
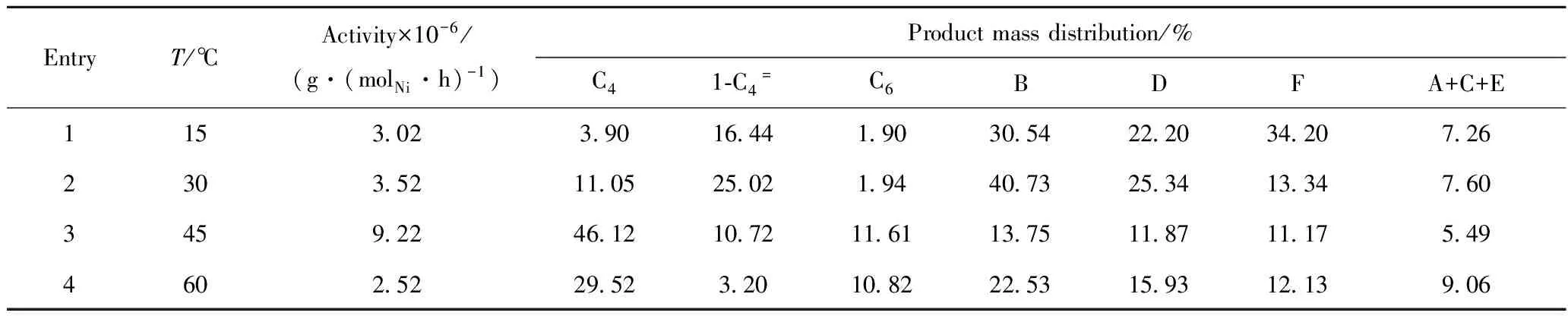
表5 反应温度对C1/EADC催化乙烯齐聚与Friedel-Crafts烷基化反应的影响Table 5 Effect of temperature on ethylene oligomerization and Friedel-Crafts alkylation reactions
Reaction conditions: Pressure of 1.0 MPa; Time of 30 min;n[Cat]=4.8 μmol; Cocatalyst of EtAlCl2;nAl/nNi=700
(3)相同条件下,将甲苯/EADC分别与乙烯、丙烯、丁烯和己烯进行对比实验,结果表明EADC具有双功能作用,一是齐聚反应的助催化剂,二是烷基化反应的催化剂。EADC能够活化金属中心形成乙烯齐聚反应和Friedel-Crafts烷基化反应的活性物种,这种活性物种在生成短链的低聚物以后会在高温下快速分解,并且转化为新的能够催化甲苯发生Friedel-Crafts烷基化反应的路易斯酸。
(4)该乙烯齐聚与Friedel-Crafts烷基化串联反应并不是彼此孤立的反应系统,而是相互联系的有机体。然而烷基化反应产物中,没有显示出明显的选择性,势必会影响该催化剂的有效应用,因此寻求一种催化剂能够提高Friedel-Crafts烷基化反应仅对一种产物的选择性是今后研究的方向。此外研究结果还为齐聚催化方面的研究提供了新思路,并为进一步调控相关因素来增强或消除串联反应提供了方向。
[1] KEIM W, KOWALDT F H, GODDARD R, et al. Novel coordination of (benzoylmethylene) triphenyl-phosphorane in a nickel oligomerization catalyst[J].Angewandte Chemie International Edition in English, 1978, 17(6): 466-467.
[2] KEIM W, BEHR A, LIMBACKER B, et al. Novel nickel-oligomerization catalysts with arsenic-oxygen chelate ligands[J].Angewandte Chemie International Edition in English, 1983, 22(6): 503-503.
[3] 王俊, 梁红姣, 李翠勤, 等. 乙烯齐聚合成α-烯烃镍配合物催化剂研究进展[J].化工进展, 2016, 35(3): 793-800. (WANG Jun, LIANG Hongjiao, LI Cuiqin, et al. Progress of nickel complex catalysts towards ethylene oligomerization forα-olefin[J].Chemical Industry and Engineering Progress, 2016, 35(3): 793-800.)
[4] AJELLAL N, KUHN M C A, BOFF A D G, et al. Nickel complexes based on tridentate pyrazolyl ligands for highly efficient dimerization of ethylene to 1-butene[J].Organometallics, 2006, 25(5): 1213-1216.
[5] GAO Rong, SUN Wenhua, REDSHAW C. Nickel complex pre-catalysts in ethylene polymerization: New approaches to elastomeric materials[J].Catalysis Science & Technology, 2013, 3(5): 1172-1179.
[6] GUAN Zhibin, MARSHALL W J. Synthesis of new phosphine imine ligands and their effects on the thermal stability of late-transition-metal olefin polymerization catalysts[J].Organometallics, 2002, 21(17): 3580-3586.
[7] KEIM W. Nickel: An elementwith wide application in industrial homogeneous catalysis[J].Angewandte Chemie International Edition in English, 1990, 29(3): 235-244.
[8] LIU Weijun, MALINOSKI J M, BROOKHART M. Ethylene polymerization and ethylene/methyl 10-undecenoate copolymerization using nickel (II) and palladium (II) complexes derived from a bulky P ,O chelating ligand[J].Organometallics, 2002, 21(14): 2836-2838.
[9] SPEISER F, BRAUNSTEIN P, SAUSSINE L, et al. Nickel complexes with oxazoline-based P, N-chelate ligands: Synthesis, structures, and catalytic ethylene oligomerization behavior[J].Organometallics, 2004, 23(11): 2613-2624.
[10] SUN Wenhua, LI Zilong, HU Huaiming, et al. Synthesis and characterization of novel nickel (II) complexes bearing N, P ligands and their catalytic activity in ethylene oligomerization[J].New Journal of Chemistry, 2002, 26(10): 1474-1478.
[11] YANG Qingzheng, KERMAGORET A, AGOSTINHO M, et al. Nickel complexes with functional zwitterionic N, O-benzoquinonemonoimine-type ligands: Syntheses, structures, and catalytic oligomerization of ethylene[J].Organometallics, 2006, 25(23): 5518-5527.
[12] DENNETT J N L, GILLON A L, HESLOP K, et al. Diphosphine complexes of nickel (II) are efficient catalysts for the polymerization and oligomerization of ethylene: Steric activation and ligand backbone effects[J].Organometallics, 2004, 23(26): 6077-6079.
[13] COOLEY N A, GREEN S M, WASS D F, et al. Nickel ethylene polymerization catalysts based on phosphorus ligands[J].Organometallics, 2001, 20(23): 4769-4771.
[14] SONG K, GAO Haiyang, LIU Fengshou, et al. Syntheses, structures, and catalytic ethylene oligomerization behaviors of bis (phosphanyl) aminenickel (II) complexes containing N-functionalized pendant groups[J].European Journal of Inorganic Chemistry, 2009, 2009(20): 3016-3024.
[15] DYER P W, FAWCETT J, HANTON M J. Rigidn-phosphino guanidine P, N ligands and their use in nickel-catalyzed ethylene oligomerization[J].Organometallics, 2008, 27(19): 5082-5087.
[16] BUDHAI A, OMONDI B, OJWACH S O, et al. Tandem ethylene oligomerisation and Friedel-Crafts alkylation of toluene catalysed by bis-(3,5-dimethylpyrazol-1-ylmethyl) benzene nickel (II) complexes and ethylaluminium dichloride[J].Catalysis Science & Technology, 2013, 3(12): 3130-3135.
[17] SPALECK W, KUEBER F, WINTER A, et al. The influence of aromatic substituents on the polymerization behavior of bridged zirconocene catalysts[J].Organometallics, 1994, 13(3): 954-963.
[18] CORMA A, GARCIA H. Lewis acids: From conventional homogeneous to green homogeneous and heterogeneous catalysis[J].Chemical Reviews, 2003, 103(11): 4307-4366.
[19] OLECHOWSKI J. Molecular sizing process for preparing low molecular isobutylene-conjugated polyene copolymers: Google Patents, 3720654[P].1973.
[20] OLECHOWSKI J. Catalyzed molecular sizing process: US,3725371[P].1973.
[21] HOMMELTOFT S I, TOPSOE H F A. Alkylation process: US, 5196574[P].1993.
[22] 王俊, 侯爽, 宋磊, 等. 乙烯齐聚催化体系中的 Friedel-Crafts烷基化反应研究进展[J].化工学报, 2016, 67(11): 4541-4551. (WANG Jun, HOU Shuang, SONG Lei, et al. Progress of Friedel-Crafts alkylation reaction in catalyst system of ethylene oligomerization[J].Journal of Chemical Industry and Engineering(China), 2016, 67(11): 4541-4551.)
[23] OBUAH C, OMONDI B, NOZAKI K, et al. Solvent and co-catalyst dependent pyrazolylpyridinamine and pyrazolylpyrroleamine nickel (II) catalyzed oligomerization and polymerization of ethylene[J].Journal of Molecular Catalysis A: Chemical, 2014, 382(2): 31-40.
[24] 秦一超, 叶健, 蒋斌波, 等. 芳氧基锆系催化剂催化乙烯齐聚与Friedel-Crafts烷基化的串联反应[J].高等学校化学学报, 2015, 36(9): 1825-1831. (QIN Yichao, YE Jian, JIANG Binbo, et al. Ethylene oligomerization and Friedel-Crafts alkylation tandem action catalyzed by aryloxy zirconium catalysts[J].Chemical Journal of Chinese Universities, 2015, 36(9): 1825-1831.)
[25] ABBO H S, TITINCHI S J J. A new vanadium (III) complex of 2,6-bis (3,5-diphenylpyrazol-1-ylmethyl) pyridine as a catalyst for ethylene polymerization[J].Molecules, 2013, 18(4): 4728-4738.
[26] NYAMATO G S, ALAM M G, OJWACH S O, et al. (Pyrazolyl)-(phosphinoyl) pyridine iron (II), cobalt (II) and nickel (II) complexes: Synthesis, characterization and ethylene oligomerization studies[J].Journal of Organometallic Chemistry, 2015, 783(5): 64-72.
[27] BLUHM M E, FOLLI C, DORING M. New iron-based bis (imino) pyridine and acetyliminopyridine complexes as single-site catalysts for the oligomerization of ethylene[J].Journal of Molecular Catalysis A: Chemical, 2004, 212(1): 13-18.
Ethylene Oligomerization and Friedel-Crafts Alkylation Tandem ActionCatalyzed by Diphosphine Nickel Complex/EADC
MENG Xuejiao, ZHANG Le, CHEN Yanhui, JIANG Tao
(CollegeofChemicalEngineeringandMaterialScience,TianjinUniversityofScience&Technology,Tianjin300457,China)
In this work, bis(diphenyl phosphine) methyl dimethyl silane(L1) and its nickel(II) halide complexes L1/NiBr2(C1), were synthesized and characterized. The influence of reaction temperature,nAl/nNiand various solvents on ethylene oligomerization were studied.Among these catalytic systems,C1/methyl cyclohexane/EtAlCl2(EADC) was proved to be highly active with the activity up to 4.32×106g/(molNi·h), while the product consisted of mainlyα-olefins(C4,C6) without polymers.The selectivity of 1-butylene in C4fractions was more than 94%. It was also found that oligomerization of ethylene gave C4and C6alkenes, followed by subsequent situ Friedel-Crafts alkylation of the toluene solvent to alkylated toluene products using C1 catalyst, in which the obtainedα-olefins were then converted into the corresponding Friedel-Crafts alkylated-toluene products. EADC in the catalytic systems played an important role to serve double functions, one is the cocatalyst of oligomerization, and the other is the catalyst for alkylation reaction.
nickel complexes; EADC; ethylene oligomerization; Friedel-Crafts alkylated reaction; alkylbenzene
2016-07-18
天津市应用基础与前沿技术研究计划重点资助项目(16JCZDJC31600)和天津市应用基础与前沿技术研究计划一般项目(14JCYBJC20800)基金资助
孟雪姣,女,硕士研究生,从事烯烃齐聚催化剂方面的研究
姜涛,男,教授,博士,从事烯烃齐聚催化剂方面的研究;Tel:022-60602936;E-mail:jiangtao@tust.edu.cn
1001-8719(2017)03-0431-08
0632.12
A
10.3969/j.issn.1001-8719.2017.03.006
