CuO/HZSM-5催化溴甲烷芳构化制备芳烃
2017-06-05陈坦陈皓傅杰陈可泉欧阳平凯
陈坦,陈皓,傅杰,陈可泉,欧阳平凯,
CuO/HZSM-5催化溴甲烷芳构化制备芳烃
陈坦1,陈皓2,傅杰2,陈可泉1,欧阳平凯1,2
(1南京工业大学生物与制药工程学院,江苏南京211800;2浙江大学生物质化工教育部重点实验室,化学工程与生物工程学院,浙江杭州 310027)
采用等体积浸渍法制备了不同负载量(1%~7%)的CuO/HZSM-5催化剂,在固定床反应器中研究了不同反应温度、溴甲烷流量以及CuO负载量对溴甲烷芳构化催化性能的影响。采用SEM、XRD、N2吸附脱附、TEM、XPS、TG、DSC、NH3-TPD等技术对反应前后的催化剂进行表征。XRD 结果显示活性组分CuO 在HZSM-5上具有很好的分散性,并且反应后Cu晶型不变。NH3-TPD 结果显示3%的CuO 负载后,催化剂强酸量增加。在CuO 负载量为3%,温度为360℃,反应空速为240 ml·g-1·h-1条件下得到最高的芳烃收率(22.3%)。XPS 结果显示反应后在催化剂上主要的积炭为石墨碳。催化剂稳定性测试结果表明反应40 h内催化活性没有明显下降。
CuO/HZSM-5;溴甲烷;催化;固定床;芳烃;稳定性
引 言
芳烃是重要的化工基础原料,广泛应用于染料、农药、医药以及高分子材料、纤维材料及树脂和橡胶等化工领域[1]。目前芳烃主要来源于石油资源,由于石油资源的日趋匮乏,研究新的芳烃生产技术逐渐引起重视。预测在未来的20~30年里,世界能源的结构比例中石油将降到20%,而天然气将增加到40%[2],天然气在能源结构中的比重逐渐增加。如何把天然气转化为液体燃料以及化工产品成为天然气研究的主要问题。
天然气中90%以上是甲烷,由于甲烷分子结构对称并且非常稳定,所以甲烷的活化非常困难[3]。目前工业上对甲烷的利用主要有直接法和间接法。直接法有甲烷氧化偶联制乙烷和乙烯[4]、高温裂解制备乙炔[4-5]、选择氧化制甲醇和甲醛[6]等,但是直接法很难获得较高的甲烷转化率和产物收率。甲烷的间接转化是将甲烷先转化成合成气然后用于合成氨、甲醇、液体燃料等。但是生产合成气的工艺复杂,设备投资巨大,操作费用昂贵且经合成气转化路线是一个高耗能的过程[7-9]。因此寻找新的间接转化路线以实现对甲烷的高效利用成为新的研究方向。
近年来,以卤代甲烷为中间产物制备烃类成为一种新的研究方向[10-11],其中主要反应过程为:① 甲烷先转化为卤代甲烷CH3X;② 卤代甲烷直接脱HX转化为烃类物质。该反应路线条件温和、步骤简单、过程也相对经济。卤代甲烷转化反应的催化剂主要有HY、HBeta、HZSM-5、HZSM-11、HZSM-34、SAPO-5、SAPO-34等分子筛,金属组分主要为过渡金属、碱土金属和稀土元素[12-20]。HZSM-5和SAPO-34由于独特的孔道结构和适宜的酸性,表现出很好的催化活性。由于CH3Br中C—Br键能较CH3Cl中C—Cl键能低,反应过程中更加容易脱去Br生成中间体,有利于芳烃的生成,因此以溴甲烷为原料制备芳烃得到更多的关注。虽然近年来对卤代甲烷为中间产物制备烃类的过程已有研究,但是以CuO为活性中心的催化剂研究较少。本文选用HZSM-5为载体,通过等体积浸渍法负载CuO,研究了反应温度、溴甲烷流量以及CuO的负载量对溴甲烷芳构化制备芳烃的影响。
1 实验部分
1.1 实验材料
HZSM-5分子筛购买于南开大学催化剂厂,Cu(NO3)2·3H2O,分析纯,国药集团化学试剂有限公司。溴甲烷,分析纯,郑州星岛化工科技有限公司。
1.2 催化剂的制备
采用等体积浸渍法制备CuO/ZSM-5催化剂。首先测量HZSM-5的饱和吸水量,按照CuO的负载量(质量分数)为1%、3%、5%和7%分别称取一定量的Cu(NO3)2·3H2O配成水溶液,滴加到HZSM-5中。将浸渍好的催化剂在室温下静置12 h,然后在120℃下干燥10 h,最后在550℃焙烧5 h。
1.3 催化剂的表征
SEM表征采用日本日立公司的S-4800型扫描电子显微镜,样品在测试前需进行喷金处理。
N2吸附脱附采用Micromeritics公司的3Flex型物理吸附仪。样品测试前在300℃下氮气吹扫6 h。样品比表面积用BET方法在/0为0.05~0.30计算,微孔孔容、微孔比表面积、外比表面积用t-Plot方法计算,孔径分布用H-K模型计算。
XRD测试用荷兰PANalytical B.V.公司的Empyrean 200895型X射线衍射仪,CuKα射线,管电压40 kV,管电流40 mA,扫描范围为5°~60°,扫描速率为8(°)·min-1。
催化剂的形貌采用JEM-2100F场发射分析型透射电子显微镜进行表征。
TG和DSC表征采用NETZSCH STA 409 PC/PG热分析仪。空气为载气,以5℃·min-1的升温速率从30℃升到750℃。
XPS测试采用VG ESCALAB Mark Ⅱ型XPS光谱分析仪测定。激光源采用MgKα。
NH3-TPD使用仪器为FINESORB-3010,预处理温度120℃,10℃·min-1进行升温。
1.4 溴甲烷芳构化反应
溴甲烷芳构化反应采用固定床反应装置,反应器长58 cm、外径2 cm、内径6 mm,催化剂装填量10 g。溴甲烷通过质量流量计经流量调节后在氮气保护下通入反应器。气相产物经装有NaOH的尾气瓶收集于采气袋中,液相产物经气液分离器分离后收集。气相产物用日本岛津GC-2018型气相色谱仪分析,色谱柱为Agilent GC-GASPRO(30 m),检测器为热导检测器(TCD)。液相产物定性和定量分析使用Agilent 7890N/5977N气相色谱-质谱联用仪,色谱柱为HP-5MS,检测器为氢火焰离子检测器(FID)。溴甲烷的转化率按式(1)计算

式中,a表示溴甲烷的进样总体积;b表示反应后气相产物中溴甲烷总体积。
芳烃总收率的计算方法为

液相产物中芳烃选择性的计算方法为
(3)
式中,n表示由色谱结果根据标准曲线得到的某一芳烃的物质的量;r表示芳烃产物的碳原子数;0表示反应时间内溴甲烷的输入量。
本实验定量方法采用外标法,标准物质选择苯、甲苯、邻二甲苯、对二甲苯、1,3,5-三甲苯、1,2,4-三甲苯、1,2,3-三甲苯、萘和甲基萘,其中C11~14芳烃类物质的定量采用甲基萘作标准物质。
2 结果与讨论
2.1 溴甲烷芳构化结果与讨论
2.1.1 温度对溴甲烷芳构化反应的影响 首先研究了5% CuO/HZSM-5催化剂在不同反应温度对溴甲烷的芳构化的影响,结果如图1所示。在320~400℃温度范围内,随着反应温度的升高,溴甲烷的转化率基本保持在97.0%左右,而芳烃收率呈现先增加后减小的趋势,在360℃时达到最高(19.3%)。升高反应温度可以加快反应速率,但温度过高后,芳烃收率下降可能是由于高温下积炭严重,堵塞了分子筛孔道,380℃下芳烃收率降低至16.0%。得出溴甲烷芳构化得到芳烃最合适的温度为360℃。
2.1.2 空速对溴甲烷芳构化反应的影响 考察了空速对溴甲烷芳构化制备芳烃的影响,在360℃下研究了5% CuO/HZSM-5在不同的溴甲烷空速(180~360 ml·g-1·h-1)下的催化性能,实验结果如图2所示。从图中可以看出,溴甲烷的转化率基本维持在96.5%,随着溴甲烷空速的增加,芳烃收率先增加后降低,在240 ml·g-1·h-1下达到最高为19.3%。这可能是由于溴甲烷空速的提高,减少了反应物以及中间产物如乙烯、丙烯与催化剂的接触时间,导致烯烃聚合成环概率下降,芳烃收率降低。
2.1.3 CuO负载量对溴甲烷芳构化反应的影响
在反应温度为360℃、空速240 ml·g-1·h-1条件下考察了催化剂中CuO负载量对溴甲烷芳构化的影响。如图3所示,随着催化剂中CuO负载量的增加,溴甲烷的转化率始终高于97.0%,而芳烃的收率先增加后减小,在CuO的负载量为3%时达到最高(22.3%)。综合考虑,当CuO负载量为3%时,催化剂催化溴甲烷芳构化性能最好。
表1列出了未负载HZSM-5和3% CuO/ HZSM-5催化溴甲烷芳构化的产物分布。从表中可以看出,3% CuO负载后的HZSM-5芳烃收率比未负载HZSM-5有所提高。3% CuO/HZSM-5所得气态产物分布中主要为C3和C4的烷烃,液态芳烃产物分布中C7和C8芳烃选择性分别为23.2%和35.7%。由此可知,经CuO负载后的HZSM-5可以有效提高溴甲烷芳构化的芳烃收率。
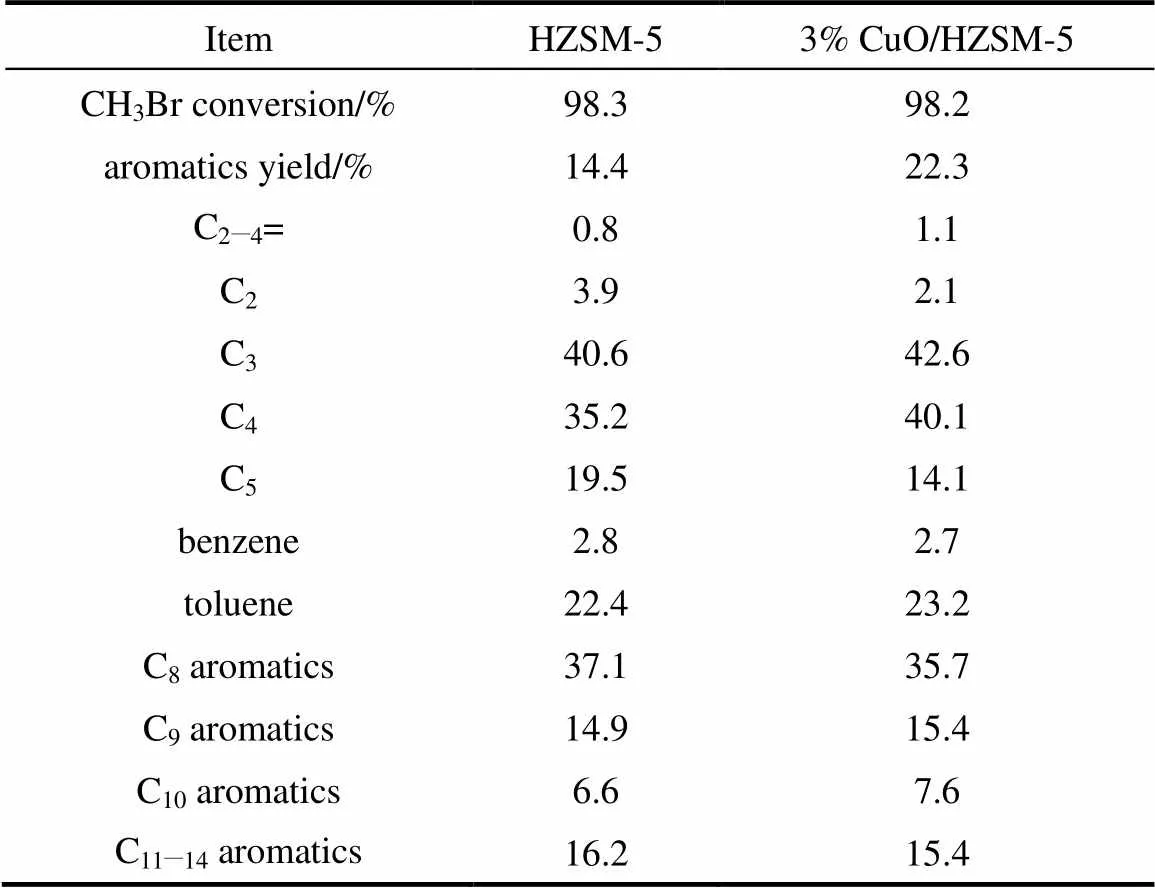
表1 CuO负载后催化剂的催化性能
综上所述,溴甲烷芳构化最佳反应条件为CuO/HZSM-5催化剂中CuO负载量为3%,溴甲烷空速为240 ml·g-1·h-1,温度为360℃。
2.2 催化剂表征
2.2.1 催化剂的SEM表征 图4为3% CuO/ HZSM-5使用前后的SEM谱图,可以直观地观察到反应前后催化剂的形貌变化。从图中可观察到CuO/HZSM-5使用前后分子筛的形貌没有明显的变化。HZSM-5分子筛的粒径范围为3~5 μm。图5是3% CuO/HZSM-5催化剂样品的能谱分析结果,EDS结果检测出Si、Al、O和Cu 4种元素。其中Si、Al和O是载体HZSM-5的组成元素,Cu和O源于CuO,并且从数据结果可以得到,样品中Cu的质量分数为2.49%,可计算出CuO的质量分数为3.11%,与理论负载量相近。
2.2.2 催化剂的N2吸附脱附表征 图6和表2给出了不同负载量CuO/HZSM-5以及3% CuO/HZSM-5使用8 h后的孔道结构数据。从图6得到,CuO负载后,HZSM-5分子筛仍为微孔分子筛,孔径分布在0.6 nm左右。由表中可以看出催化剂的比表面积和孔容随着CuO负载量的增加逐渐下降。原因是由于CuO的引入堵塞了分子筛的孔道,造成比表面积和孔容下降。反应8 h后的3% CuO/HZSM-5的比表面积和孔容相比于使用前的3% CuO/HZSM-5都降低,比表面积和孔容分别从229.3 m2·g-1和0.077 cm³·g-1下降到151.4 m2·g-1和0.054 cm³·g-1。这可能是由于催化剂在反应过程中产生积炭,堵塞了分子筛孔道。

表2 不同负载量CuO/HZSM-5的比表面积和孔容
2.2.3 催化剂的XRD表征 图7为不同负载量CuO/HZSM-5催化剂的XRD谱图。从图中可以看出,随着CuO负载量从1%增加到7%,CuO/HZSM-5催化剂均有CuO特征衍射峰,且随着负载量的增加,特征衍射峰的峰强度明显增强,但当CuO的负载量较低时(1%),催化剂CuO特征衍射峰不明显,这是因为当氧化物含量低于一定值后,氧化物完全进入载体骨架中,呈高度分散状态,其衍射峰不明显甚至不会出现,而当氧化物含量高于一定值后,过多的氧化物就会聚集在催化剂表面,导致出现明显的氧化物晶相衍射峰[21]。3% CuO负载后催化剂使用前后都含有HZSM-5和CuO的特征衍射峰,CuO的特征衍射峰峰位置和类型没有变化,说明催化剂中Cu物种没有明显变化。
a—HZSM-5; b—1% CuO/HZSM-5;c—3% CuO/HZSM-5; d—5% CuO/HZSM-5;e—7% CuO/HZSM-5; f—used 3% CuO/HZSM-5
2.2.4 催化剂的TG和DSC分析 随着反应时间的延长,催化剂的活性逐渐降低,可能是由于积炭的产生堵塞了分子筛孔道,覆盖了催化剂的活性位点。图8为3% CuO/HZSM-5催化剂反应8 h以后的TG-DSC曲线。如图所示,催化剂的TG曲线在150℃左右质量的减少以及DSC曲线中50℃左右放热峰是由于催化剂中吸附的水蒸发造成的。150℃吸附水完全蒸发,质量损失约为5%。TG曲线中300℃出现的失重是由于反应时在催化剂上产生的积炭燃烧分解,对应DSC曲线中300℃下放热峰。700℃下积炭完全燃烧,失重约为5%。根据DSC曲线可以推测反应后的催化剂主要存在一种积炭。
2.2.5 催化剂的XPS表征 对反应8 h后的3% CuO/HZSM-5催化剂进行XPS表征进一步研究催化剂上积炭物种。图9为反应8 h后3% CuO/ HZSM-5催化剂的C 1s谱图。根据C 1s谱图结果可以得到两个峰分别在285.3 eV和287.6 eV,分别对应两种类型的积炭物种,其中285.3 eV为主要积炭,归属于石墨型积炭[7]。结合TG-DSC表征,可以推测反应后催化剂中积炭主要为石墨碳,这种类型的积炭也是导致催化剂活性降低的主要原因。图10为3%CuO/HZSM-5催化剂Cu 2p3/2的XPS谱图。文献报道Cu 2p3/2区域的曲线拟合在933.6、934.8、932.5 eV 3个结合能处分别代表3种不同的铜物种,分别属于CuO、Cu(OH)2和Cu2O/金属Cu[22-23]。图10得到933.2和935.2 eV两个峰,基于文献结果,可以将两个峰分别归因于Cu2+以及与载体有强相互作用的Cu2+(Cu2+—O—Si)[24-25]。
2.2.6 催化剂的TEM表征 TEM可以观察到CuO在催化剂中的微观结构,结果如图11所示。图11(a)为HZSM-5的TEM图,可以明显看到HZSM-5有序的晶格条纹。图11(b)为3% CuO/HZSM-5的TEM图,CuO颗粒粒径大小为10~20 nm,可以发现CuO颗粒在HZSM-5分子筛上呈现较好的分散性,与XRD的表征结果相符合。图11(c)为3% CuO/HZSM-5的EDS图,进一步验证了活性组分CuO负载在HZSM-5分子筛上。
2.2.7 催化剂的NH3-TPD表征 催化剂酸性在溴甲烷芳构化过程中起到非常重要的作用[26],为了探究酸性对溴甲烷芳构化反应的影响,对催化剂进行了NH3-TPD表征,结果如图12所示。从图中可以看出未负载的HZSM-5在180℃左右出现一个脱附峰,经CuO负载后的HZSM-5分别在180和400℃出现两个脱附峰,分别代表弱酸位点和强酸位点[27-29],经CuO负载后的HZSM-5总酸量高于HZSM-5,与文献[30]报道一致。与未负载的HZSM-5相比,CuO负载后的HZSM-5,强酸量明显增加,而弱酸量少量减少,说明CuO的负载改变了分子筛的酸性分布,从而影响溴甲烷芳构化催化性能。
2.3 催化剂的稳定性
考察了3% CuO/HZSM-5催化剂的稳定性,结果如图13所示。从图中可以看出,在反应时间内溴甲烷转化率都维持在95%以上,40 h内芳烃收率基本维持在22%左右,说明催化剂在反应前40 h内都保持在稳定的水平。随着反应时间超过40 h以上,芳烃的收率呈现明显下降的趋势,反应48 h后,芳烃收率小于10%。推测可能原因是由于分子筛孔道的坍塌以及积炭的产生覆盖了催化剂的活性位点。
3 结 论
通过等体积浸渍法在HZSM-5分子筛上负载CuO活性组分得到CuO/HZSM-5催化剂,对溴甲烷芳构化制备芳烃具有较好的催化效果。结果表明,CuO活性组分在HZSM-5载体上具有很好的分散性,并且明显提高了催化剂中强酸量,提高了芳烃收率。结果得到3% CuO负载得到最高的芳烃收率,最佳的反应条件为温度360℃和溴甲烷空速240 ml·g-1·h-1。催化剂在40 h内稳定性能好,没有明显失活。
References
[1] 张大治, 魏迎旭, 沈江汉, 等. 氯甲烷在镁修饰的ZSM-5分子筛催化剂上催化转化研究[J]. 天然气化工, 2006, 31(3): 14-17. ZHANG D Z, WEI Y X, SHEN J H,. Chloromethane conversion over Mg modified ZSM-5 zeolite catalysts[J]. Natural Gas Chemical Industry, 2006, 31(3): 14-17.
[2] 陈庆龄, 钱伯张. 天然气化工发展现状[J]. 现代化工, 2002, 22(5): 1-4. CHEN Q L, QIAN B Z. Current situation of nature gas chemical industry[J]. Modern Chemical Industry, 2002, 22(5): 1-4.
[3] SOUSA-AGUIAR E F,APPEL L G,MOTA C. Natural gas chemical transformations: the path to refining in the future[J]. Catalysis Today, 2005, 101(1): 3-7.
[4] HOLMEN A, OLSVIK O, ROKSTAD O A. Pyrolysis of nature gas: chemistry and process concepts[J]. Fuel Processing Technology, 1995, 42(2/3): 249-267.
[5] HOLMEN A, ROKSTAD O A, SOLBAKKEN A. High-temperature pyrolysis of hydrocarbons(Ⅰ): Methane to acetylene[J]. Industrial & Engineering Chemistry Process Design & Development, 1976, 15(3): 439-444.
[6] LIU R S, IWAMOTO M, LUNSFORD J H. Partial oxidation of methane by nitrous oxide over molybdenum oxide supported on silica[J]. Journal of the Chemical Society, Chemical Communications, 1982, 1(1): 78-79.
[7] 雍瑞生, 谭斌, 王科. 天然气化工的技术进展与发展机遇[J]. 天然气化工, 2009, 34(4): 70-75. YONG R S, TAN B, WANG K. Progress in the technologies for production of chemicals from natural gas and development opportunity[J]. Natural Gas Chemical Industry, 2009, 34(4): 70-75.
[8] 白尔铮. 费托合成燃料的经济性及发展前景[J]. 化工进展, 2004, 23(4): 370-374. BAI E Z. Economics and prospects of FT synfuels[J]. Chemical Industry and Engineering Progress, 2004, 23(4): 370-374.
[9] 陈建钢, 相宏伟, 李永旺, 等. 费托法合成液体燃料关键技术研究进展[J]. 化工学报, 2003, 54(4): 516-523.CHEN J G, XIANG H W, LI Y W,. Advance in key techniques of Fischer-Tropsch synthesis for liquid fuel production[J]. Journal of Chemical Industry and Engineering(China), 2003, 54(4): 516-523.
[10] XIA X R, BI Y L, WU T H,. An infrared spectroscopic study of the mechanism of chloromethane conversion to higher hydrocarbons on HZSM-5 catalyst[J]. Catalysis Letters, 1995, 33(1): 75-90.
[11] NORONHA L A, SOUZA-AGUIAR E F, MOTA C J A. Conversion of chloromethane to light olefins catalyzed by ZSM-5 zeolites[J]. Catalysis Today, 2005, 101(1): 9-13.
[12] JENS K J. Methane conversionmethylchloride: condensation of methylchloride to light hydrocarbons[J]. Studies in Surface Science & Catalysis, 1988, 36: 491-495.
[13] LERSCH P, BALLDERMANN F. Conversion of chloromethane over metal-exchanged ZSM-5 to higher hydrocarbons[J]. Applied Catalysis, 1991, 75(1): 133-152.
[14] SUN Y, CAMPBELL S M, LUNSFORD J H,. The catalytic conversion of methyl chloride to ethylene and propylene over phosphorus-modified Mg-ZSM-5 zeolites[J]. Journal of Catalysis, 1993, 143(1): 32-44.
[15] JAUMAIN D, SU B L. Direct catalytic conversion of chloromethane to higher hydrocarbons over various protonic and cationic zeolite catalysts as studied byFTIR and catalytic testing[J]. Studies in Surface Science and Catalysis, 2000, 130: 1607-1612.
[16] JAUMAIN D, SU B L. Direct catalytic conversion of chloromethane to higher hydrocarbons over a series of ZSM-5 zeolites exchanged with alkali cations[J]. Journal of Molecular Catalysis A: Chemical, 2003, 197(1/2): 263-273.
[17] WEI Y X, ZHANG D Z, XU L,. New route for light olefins production from chloromethane over HSAPO-34 molecular sieve[J]. Catalysis Today, 2005, 106(1): 84-89.
[18] LORKOVIC I M, YILMAZ A, YILMAZ G A,. A novel integrated process for the functionalization of methane and ethane: bromine as mediator[J]. Catalysis Today, 2004, 98(1): 317-322.
[19] LIU Z, HUANG L, LI W S,. Higher hydrocarbons from methane condensation mediated by HBr[J]. Journal of Molecular Catalysis A: Chemical, 2007, 273(1/2): 14-20.
[20] ZHANG D Z, WEI Y X, XU L,. Chloromethane conversion to higher hydrocarbons over zeolites and SAPOs[J]. Catalysis Letters, 2006, 109(1): 97-101.
[21] 史风华, 宋永吉, 罗潇然, 等. 六铝酸盐负载CuO催化还原NO性能[J]. 环境化学, 2012, 31(8): 1222-1226. SHI F H, SONG Y J, LUO X R,. Catalytic reduction of NO over CuO/LaAl12O19catalysts[J]. Environment Chemistry, 2012, 31(8): 1222-1226.
[22] BIESINGER M C, LAU L W M, GERSON A R,. Resolving surface chemical states in XPS analysis of first row transition metals, oxides and hydroxides: Sc, Ti, V, Cu and Zn[J]. Applied Surface Science, 2010, 257(3): 887-898.
[23] POULSTON S, PARLETT P M, STONE P,. Surface oxidation and reduction of CuO and Cu2O studied using XPS and XAES[J]. Surface and Interface Analysis, 1996, 24(12): 811-820.
[24] BENNICI S, GERVASINI A, RAVASIO N,. Optimization of tailoring of CuOspecies of silica alumina supported catalysts for the selective catalytic reduction of NO[J]. Journal of Physical Chemistry B, 2003, 107(22): 5168-5176.
[25] AUROUX A, GERVASINI A, GUIMON C. Acidic character of metal-loaded amorphous and crystalline silica-aluminas determined by XPS and adsorption calorimetry[J]. Journal of Physical Chemistry B, 1999, 103(34): 7195-7205.
[26] SONG Y, ZHU X, XIE S,. The effect of acidity on olefin aromatization over potassium modified ZSM-5 catalysts[J]. Catalysis Letter, 2004, 97(1): 31-36.
[27] LOBREE L J, HWANG I C, REIMER J A,. Investigations of the state of Fe in H-ZSM-5[J]. Journal of Catalysis, 1999, 186(2): 242-253.
[28] MARSCHMEYER S, PAPP H. Surface analysis of a hydrothermally treated H-ZSM-5 zeolite[J]. Surface and Interface Analysis, 1997, 25(9): 660-666.
[29] POST J G, VAN HOOF J H C. Acidity and activity of H-ZSM-5 measured with NH3-t.p.d. and-hexane cracking[J]. Zeolites, 1984, 4(1): 9-14.
[30] TAJBAKHSH M, ALINEZHAD H, NASROLLAHZADEH M,. Preparation, characterization and application of nanosized CuO/HZSM-5 as an efficient and heterogeneous catalyst for the N-formylation of amines at room temperature[J]. Journal of Colloid and Interface Science, 2016, 471(1): 37-47.
Catalytic performance of CuO/HZSM-5 in aromatic synthesis from CH3Br
CHEN Tan1, CHEN Hao2, FU Jie2, CHEN Kequan1, OUYANG Pingkai1,2
(1Biotechnology and Pharmaceutical Engineering, Nanjing Tech University, Nanjing 211800, Jiangsu, China;2Key Laboratory of Biomass Chemical Engineering of Ministry of Education, College of Chemical and Biological Engineering, Zhejiang University, Hangzhou 310027, Zhejiang, China)
CuO/HZSM-5 catalysts with 1%—7% CuO loading, which were prepared by incipient wetness impregnation, were used to study catalytic performance in the conversion of CH3Br to aromatic compounds in a fixed-bed reactor by changing temperature, CH3Br flow rate and CuO loading. Fresh and used catalysts were characterized by SEM, TEM, XRD, XPS, TG, DSC, N2adsorption and desorption, and NH3-TPD. XRD results showed that CuO was highly dispersed on HZSM-5 and structure of CuO crystals did not change during reaction. NH3-TPD results showed that 3% (mass) CuO loading increased strong acidity of catalyst. XPS results showed that coke deposition on used CuO/HZSM-5 catalyst was mainly graphite. The highest aromatic yield of 22.3% was achieved at condition of 3% (mass) CuO loading, 360℃ temperature and 240 ml·g-1·h-1GHSV. The 3% (mass) CuO/HZSM-5 maintained stable catalytic activity within 40 h reaction time.
CuO/HZSM-5; CH3Br; catalysis; fixed-bed; aromatic; stability
10.11949/j.issn.0438-1157.20161659
TQ 032
A
0438—1157(2017)06—2344—08
傅杰。
陈坦(1989—),男,硕士研究生。
国家自然科学基金项目(21436007);浙江省自然科学基金项目(LR17B060002)。
2016-11-24收到初稿,2017-03-20收到修改稿。
2016-11-24.
Prof.FU Jie, jiefu@zju.edu.cn
supported by the National Natural Science Foundation of China (21436007) and the Natural Science Foundation of Zhejiang Province (LR17B060002).
