阿帕替尼治疗晚期非小细胞肺癌1例
2017-06-05秦佳宁
秦佳宁*
(广西柳州市人民医院肿瘤内科,广西 柳州 545000)
阿帕替尼治疗晚期非小细胞肺癌1例
秦佳宁*
(广西柳州市人民医院肿瘤内科,广西 柳州 545000)
阿帕替尼;非小细胞肺癌
1 临床资料
患者女性,49岁,2012年3月以“咳嗽、咳痰2月余”为主诉就诊。一般情况:PS 1分,身高158 cm,体质量48 kg。无高血压、冠心病、糖尿病史,无肿瘤家族史,无吸烟、饮酒史。
辅助检查:胸部CT:右肺下叶周围型肺癌,并两肺多发转移。进一步做纤维支气管镜:(右下肺基底段钳检)低分化鳞状细胞癌。
诊断:右下肺低分化鳞癌T4N3M1 Ⅳa期。
治疗过程:患者肿瘤Ⅳ期,无手术指征。于2012年3月31日至7月23日予TP方案化疗6周期(紫杉醇270 mg,静滴d1,顺铂30 mg,静滴d2~5),过程顺利,期间复查肺部CT肺部肿瘤缩小。此后未特殊治疗,定期复查。
2012年10月复查胸部CT:右肺下叶周围型肺Ca并两肺转移,病灶较前增大。故于10月16日、11月7日、11月29日选择多西他赛联合奈达铂化疗3周期,剂量:多西他赛100 mg d1+奈达铂60 mg d2~3。
2012年12月复查CT提示肺部病灶较前增大,于2012年12月19日改用吉西他滨联合奈达铂化疗,其中吉西他滨1200 mg,静滴d1、d8,奈达铂60 mg,静滴d2~3;后未继续化疗,自服吉非替尼分子靶向治疗,服药1个月后曾复查胸部CT,肺部肿瘤较前稍缩小。后未继续抗肿瘤治疗,此后多次复查病情持续进展,但患者拒绝继续化疗,予生物免疫及中药抗癌治疗。
2013年底因咳嗽、咳痰加重入院。胸部CT:右下肺癌并两肺、右肺门、纵隔淋巴结多发转移瘤较前进展,于12月27日、1月17日、2月15日、3月15日、4月18日、5月27日行吉西他滨联合奈达铂化疗,其中其中吉西他滨1400 mg,静滴d1、d8,奈达铂60 mg,静滴d1~2。共6周期,其后予7月2日、8月12日、10月20日、12月28日继续吉西他滨单药维持化疗:吉西他滨1400 mg,静滴d1、d8,期间最高出现Ⅳ度血小板减少,复查胸部CT肺部病灶较前缩小减少。
2015年5月13日入院复查胸部CT:①右肺下叶肺Ca并两肺、右肺门、及纵隔淋巴结多发转移瘤;进展期。②右肺下叶炎症并右侧胸腔少量积液。(较前进展);于5月19日予长春瑞滨联合顺铂化疗,其中长春瑞滨40 mg,静滴d1、d8,顺铂30 mg d1~4。治疗后病情进展,于6月19日、7月13日、8月17、9月15日改奈达铂联合替吉奥化疗4周期,其中奈达铂60 mg d1~2,替吉奥50 mg d1~14。2015年10月复查提示肿瘤部分进展,建议患者联合恩度、贝伐单抗等抗血管生成药物分子靶向治疗,但患者由于经济原因拒绝,要求继续原方案化疗。于11月6日、12月3日继续奈达铂联合替吉奥化疗2周期。
2016年1月复查肿瘤再次进展,于2016年1月14日选择EP方案化疗,其中奈达铂70 mg,静滴d1~2,依托泊苷50 mg d1~5。复查提示肿瘤进展,予2016年2月19日、3月20日改予紫杉醇联合洛铂化疗2周期,复查肿瘤进展。于4月19日行吉西他滨+卡铂方案进行姑息性化疗,其中:吉西他滨1.2 g,静滴d1,d8,卡铂40 mg,静滴d1~3。但化疗期间患者胸闷、气促加重,急查胸片及胸部B超;示肺部感染及右侧胸腔积液,予抗感染及引流胸水、胸腔灌注化疗等治疗后好转。
考虑患者多线化疗后出现多药耐药且患者化疗耐受性差,2015年5月患者自购阿帕替尼治疗,治疗后复查患者肺部肿瘤明显缩小,胸水消失。患者咳嗽、胸闷、气促症状好转。复查至今仍持续获益,出现Ⅲ度手足反应及高血压,通过指导患者进行局部对症治疗:避免接触水分及化学洗涤剂,保持患处干燥;如出现水泡破溃及渗出可局部使用卤米松软膏或云南白药粉;如无必要尽量避免局部包扎覆盖;使用厄贝沙坦治疗高血压;经治疗后患者手足反应及高血压可控制。见图1~3。
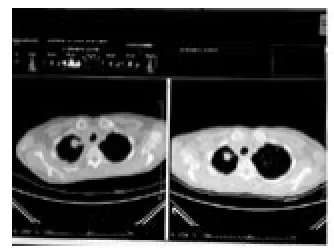
图1
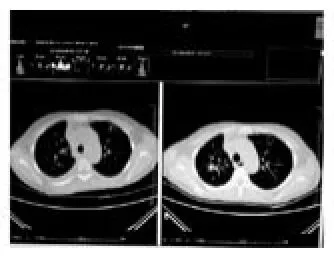
图2
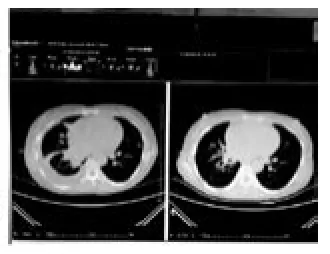
图3
2 讨 论
肺癌是全球最常见的癌症之一,其中非小细胞肺癌约占80%。晚期非小细胞癌的治疗,目前已经从化疗药物占主导地位转变为化疗与新型靶向药物相结合的阶段。相对化疗药物而言,分子靶向药物不良反应较轻微,患者更容易耐受。甲磺酸阿帕替尼片(Apatinib,艾坦)是新一代小分子血管内皮生长因子受体-2(VEGFR-2)酪氨酸激酶抑制剂,曾经获得国家“十一•五”和“十二•五”计划重大新药创制专项基金的支持,其主要作用机制是竞争性结合该受体胞内酪氨酸ATP结合位点,高度选择性地抑制VEGFR-2酪氨酸激酶活性,阻断血管内皮生长因子(VEGF)结合后的信号传导,从而强效抑制肿瘤血管生成[1-2]。国外公司同期研发的雷莫芦单抗,是针对VEGFR-2的大分子肿瘤血管生成抑制剂,以优先审评产品已获得美国食品药品管理局(FDA)的批准上市。在一项阿帕替尼治疗进展期非小细胞肺癌的多中心,随机病例对照II期研究(nct01270386)。入组135例病例按2∶1的比例随机分为阿帕替尼组和安慰剂组,使用阿帕替尼750 mg治疗直至疾病进展或不能耐受的不良反应。入组病例在肿瘤转移后必须经过至少二线以上的方案治疗,ECOG≤1,既往没有使用过VEGF络氨酸激酶抑制剂。结果显示:阿帕替尼组和安慰剂组的中位PFS为4.7个月vs1.9个月(HR=0.278;95%CI:0.170~0.455;P<0.001),阿帕替尼组和安慰剂组的客观反应率和疾病控制率为(12.2%,68.9%) vs(0,24.4%)(P=0.0158,P<0.0001,每组)。不良反应与先前的研究相似,主要为包括血液学毒性(白细胞减少、粒细胞减少和血小板减少等)和非血液学毒性(高血压、蛋白尿、手足皮肤反应、乏力及腹泻等)。多数不良反应均可通过暂停给药、下调剂量及支持对症处理得以控制和逆转[3]。一项双盲,病例对照的阿帕替尼治疗EGFR野生型非小细胞肺癌的Ⅲ期临床研究(nct02332512)正在进行中,结果值得期待。
本病例中,患者被诊断为晚期肺癌后,无手术及局部治疗指征,治疗以全身化疗等综合治疗为主;患者为鳞状细胞癌,缺乏如EGFR基因,ALK基因等分子标志物,治疗难度大,肿瘤恶性程度高。给予一线、二线、三线等多线化疗及试验性使用EGFR-TK类药物治疗后病情呈进行性加重。患者多方案多程化疗后以发生多药耐药且患者化疗耐受性逐期下降,末次出现Ⅲ~Ⅳ度血液毒性,患者已难继续通过化疗获益。通过使用阿帕替尼病情得到控制,无进展生存期达5个月,患者存活至今。本病例表明,阿帕替非小细胞肺癌患者中具有较好的安全性和耐受性,明显延长了患者的无进展生存期,且为口服制剂,方便应用,对于化疗无法控制的进展患者,不失为一种新的优选药物和治疗方法。
阿帕替尼最早在晚期胃癌治疗中被证实安全有效,多个研究显示它作为一个口服的小分子VEGFR-2络氨酸激酶抑制剂可改善包括肺癌,乳腺癌,肝癌其他多种二线以上治疗失败的实体瘤患者的预后并且安全可耐受[4-5]。作为一种抗血管生成的分子靶向药物,其可能对更广泛的肿瘤有效。目前还缺乏关于阿帕替尼联合其他药物的治疗方案,在未来的研究中联合治疗是一个有潜力的研究方向。另外一些关于生物标记的研究已期可作为疗效预测因子。总之,阿帕替尼在多种肿瘤中治疗安全有效,值得进一步临床应用及研究。
[1] Li J,Qin S,Xu J,et al.Apatinib for chemotherapy-refractory advanced metastatic gastric cancer: results from a randomized, placebo-controlled, parallel-arm, phase Ⅱ trial[J].J ClinOncol, 2013,31(26):3219-3225.
[2] Li J,Qin S,Xu J,et al.Randomized, double-blind, placebo-controlled phase Ⅲ trial of apatinibin patients with chemotherapy-refractory advanced or metastatic adenocarcinoma of the stomach or gastroesophageal junction [J].J ClinOncol,2016,34(13):1448-1454.
[3] 秦叔逵,李进.阿帕替尼治疗胃癌的临床应用专家共识[J].临床肿瘤学杂志,2015,20(9):841-847.
[4] Hu X,Zhang J,Xu B,et al.Multicenter phase II study of apatinib, a novel VEGFR inhibitor in heavily pretreated patients with metastatic triple-negative breast cancer[J].Int J Cancer,2014,135(8):1961-1969.
[5] Hu X,Cao J,Hu W,et al.Multicenter phase II study of apatinib in nontriple-negative metastatic breast cancer[J].BMC Cancer,2014,14:820.
R734.2
B
1671-8194(2017)10-0207-02
*通讯作者:E-mail: 360201858@qq.com
