苦参降血糖活性部位分散片剂型研究
2017-06-01刘瑞驹袁经权
刘瑞驹++袁经权
[摘要] 目的 对具有显著降糖活性的苦参乙酸乙酯部位进行分散片处方工艺研究,为工业化生产和临床应用奠定基础。方法 以分散片硬度、崩解度为考察指标,通过正交试验确定最佳处方工艺。采用转篮法测定溶出度,并计算累积溶出度百分率。结果 最佳处方工艺为主药量25%,1.0%阿斯巴甜作为矫味剂,1.4~1.6 mL/100 g浓度的蒸馏水作为润湿剂,0.5%硬脂酸镁作为润滑剂,2.0%PVPP作为崩解剂,MCC-预胶化淀粉(3︰1)作为填充剂。苦参分散片的累積溶出度平均值为82.65%。结论 苦参分散片处方工艺合理可行,可用于苦参分散片的制备及质量控制。
[关键词] 苦参;处方工艺;抗糖尿病;分散片
[中图分类号] R944 [文献标识码] A [文章编号] 1673-7210(2017)04(a)-0017-05
[Abstract] Objective To investigate the dispersible tablets of the ethylacetate extract of Sophora flavescens Ait., which will be laying the basic foundation for its industrial production and clinical study. Methods The orthogonal experiment design was performed to determine the optimized formulation with hardness and disintegration as examine indexes. The rotation basket was applied to determine the dissolution, and the accumulative dissolution percentage was calculated. Results The optimized formulation was shown as follows: the content of extracts in tablets was 25%, 1.0% aspartame was used as sweetener, 1.4-1.6 mL/100 g of distilled water was used as wetting agent, 0.5% magnesium stearate was used as lubricant, 2.0% PVPP was used as disintegrant, and MCC-pregelatinized starch (3︰1) was used as filler. The average value of accumulative dissolution percentage was 82.65%. Conclusion The preparation is reasonable and feasible, which can be used in the preparation and the quality control of Sophora flavescens dispersible tablets.
[Key words] Sophora flavescens; Preparation; Antidiabetic; Dispersible tablets
苦参Sophora flavescens Ait.为豆科槐属植物,味苦,性寒,具清热解毒、祛风杀虫等功效,主治湿热泻痢,肠风便血,黄疽,水肿等症[1]。近年报道苦参用于治疗非典和肿瘤[2]及杀虫剂的开发[3-4]。苦参主要含生物碱和黄酮两类成分,具多种活性[5-6],其中苦参碱、氧化苦参碱为主的苦参碱制剂已经上市,主要用来治疗急、慢性病毒性肝炎,肿瘤等疾病[7-10]。但对于苦参黄酮的研究相对较少,近来发现富含苦参乙酸乙酯部位中黄酮具有良好的降糖活性[11],此外Sato等从苦参乙酸乙酯部位中分离的九种黄酮化合物具有钠-葡萄糖协同转运(SGLT)抑制作用[12]。黄秋云等从苦参乙酸乙酯部位分离的异黄酮苷F对蔗糖酶、异麦芽糖酶、麦芽糖酶活性的IC50分别为 26.7 μmol/L、20 μmol/L、5.34 μmol/L,比儿茶素的活性强37~187倍,对大鼠摄入葡萄糖后血糖值上升的ED50为40 μg/kg,比儿茶素(800 μg/kg)强20倍,还可抑制醛糖还原酶(AR)的活性,IC50为11 μmol/L[13]。以上文献数据表明苦参降血糖活性主要集中在富含黄酮成分的乙酸乙酯部位,故本文重点对具有降血糖作用的苦参乙酸乙酯部位进行剂型研究,鉴于苦参中的黄酮类物质在水中溶解度小[14-15],不利于吸收,为增加黄酮类物质的溶解度,提高其生物利用度,本文将苦参降糖活性部位制成分散片,并进行了处方工艺研究,为进一步促进苦参新的研究和开发提供技术依据。
1 仪器与试药
1.1 仪器
YD-1型片剂硬度测试仪(天津市新天光分析仪器技术有限公司);LB-881B六管崩解仪(无锡科达仪器厂);ZP-7型旋转式压片机(中国泰州市天泰制药机械厂);ZJP型全自动硬胶囊充填机(中国泰州市天泰制药机械厂);ZRC-8C智能溶出仪(天津大学无线电厂);Waters 2515半制备型高效液相:2998二极管阵列检测器,2707自动进样器;Sunfire C18半制备柱(Waters,250 mm × 4.6 mm,5 μm)。
1.2 试药
苦参乙酸乙酯部位提取物(过80目筛);微晶纤维素103型(MCC)、预胶化淀粉、交联聚维酮(PVPP)、蒸馏水、阿斯巴甜、硬脂酸镁(天津市恒兴化学试剂制品有限公司);薄层色谱硅胶和柱色谱硅胶(青岛海洋化工厂);HPLC级乙腈(Merck)。
1.3 药材
苦参Sophora flavescens Ait.于2011年8月购于广西南宁市水街中草药药材市场,经广西药用植物研究所袁经权研究员鉴定,药材标本存放于该所开发中心。
2 方法与结果
2.1 苦参降糖活性部位分散片的制备处方与工艺设计
2.1.1苦参降糖活性部位提取
取5 kg苦参粉碎成粉末,置于中药提取罐中用80%乙醇浸泡1周,隔1~2天搅动一次,将提取液从下口放出,收集。如此反复提取3次,得到总提取液约70 L。将收集得到的提取液减压蒸馏浓缩,除去乙醇,得到浓缩液2.5 L,用等体积的石油醚萃取3次,除去油脂性成分,下层水溶液部分用10%稀硫酸调节pH至3,按等体积比为1︰1用乙酸乙酯萃取4次,减压蒸馏浓缩,除去乙酸乙酯,收集固体物,用烘箱50℃烘干,研磨成粉末,得活性部位784 g,提取率为15.68%,指标性成分苦参酮量约为13.8 g。
2.1.2 苦参降糖活性部位分散片的制备处方设计
苦参降糖活性部位提取物为黄色固体粉末,味苦,其为苦参中的极性较小的黄酮类成分,微溶于水,易溶于乙醇,化学性质稳定,不挥发,常温能稳定存在,高温时会分解。无毒性,可直接口服。依据其化学性质以及相关文献设计处方如下:主药量为25%的苦参乙酸乙酯部位,矫味剂为1%的阿斯巴甜,黏合剂为1.4~1.6 mL/100 g的蒸馏水,润滑剂为1%的硬脂酸镁,崩解剂为2%的交联聚维酮(PVPP),填充剂约占71%。
2.2 苦参降糖活性部位分散片的制备方法
按照处方设计精密称量各组分,主药过80目筛,其他辅料分别过100目筛,湿法制粒,烘干添加润滑剂,混匀,压片即得。
2.3 分散片剂量设计
苦参降糖活性部位在处方中为主药,设计每片片重为200 mg,主药量为50 mg,苦参酮含量约为0.88 mg。依据前期药理实验结果[11],小鼠每日给药量为60 mg/kg可达到较好的降血糖效果,依据人与小鼠剂量换算关系[16],成人每日服用3次,每次2片,可达到较好的降血糖效果。
2.4 分散片处方的单因素考察
分散片中崩解剂常用的有羧甲基纤维素钠、羧甲基淀粉钠、交联聚维酮等,黏合剂常用的有聚乙烯吡咯烷酮、乙醇、水等,填充剂常用的有预胶化淀粉、MCC、淀粉等,润滑剂常用的有硬脂酸镁、微粉硅胶等。预试验比较了上述常用辅料种类和用量对分散片溶出度的影响,最终确定黏合剂为蒸馏水,润滑剂为硬脂酸镁,崩解剂为交联聚维酮,矫味剂为阿斯巴甜。根据预实验结果,以片剂的可压性、硬度、崩解时间及外观光洁度作为评价制剂质量的指标,对片剂的填充剂种类及用量进行筛选。
由于该药物为降糖药,故填充剂筛选实验设计方案为主药量25%,硬脂酸镁1%,阿巴斯甜1%,PVPP2%,三组填充剂分别设为7.10 g的淀粉、微晶纤维素、预胶化淀粉。将实验组中各组分准确称量并混匀,过80目筛后,加适量蒸馏水(约1.5 mL)混合后挤压过30目筛制粒,将颗粒置于干燥箱中烘干,将制得的颗粒用压片机进行压片,片重约为200 mg/片,从3个实验组中各取6片,通过检查制备的分散片的硬度和崩解度来测定其流动性,结果见表1。
从表1可见,实验1制粒得到的颗粒休止角过大,表明其流动性太差,不利于工业生产,且压片得到的分散片硬度太小,轻压即碎,不利于药品的运输,故该填充剂不适合。实验2用MCC作填充剂得到的颗粒流动性良好,但需在较大压力下压片,且得到的分散片硬度过大,崩解时间过长,不合适单独做填充剂。实验3用预胶化淀粉作填充剂得到的颗粒流动性较好,崩解也快,但压片得到的分散片硬度太小,故也不适合单独做填充剂。综合分散片的硬度、崩解度以及颗粒的流动性,选用MCC和预交化淀粉混合使用做填充剂最为合适。
2.5 正交试验设计
由影响分散片的崩解时限和压片操作的因素,设计一个三因素三水平的正交试验来优化相关因素,试验方案见表2~4。
由表4结果可见,填充剂对分散片硬度的影响有统计学意义,各因素影响顺序为A>C>B,填充剂对分散片崩解时间的影响有统计学意义,各因素影响顺序为A>C>B。综合各指标的最佳工艺,选择2个或2个以上指标均较佳的工藝条件[17-19],并结合分散片的成型性及感官评价,优选工艺为A3B2C1,即MCC-预胶化淀粉(3︰1)作为填充剂,2.0%PVPP作为崩解剂,0.5%硬脂酸镁作为润滑剂。最终确定苦参分散片最优处方工艺设计为:主药量为25%的苦参乙酸乙酯部位,矫味剂为1%的阿斯巴甜,黏合剂为1.4~1.6 mL/100 g的蒸馏水,润滑剂为1%的硬脂酸镁,崩解剂为2%的交联聚维酮(PVPP),MCC-预胶化淀粉(3∶1)作为填充剂(71%)。
2.6 苦参分散片的溶出度检测
2.6.1 色谱条件
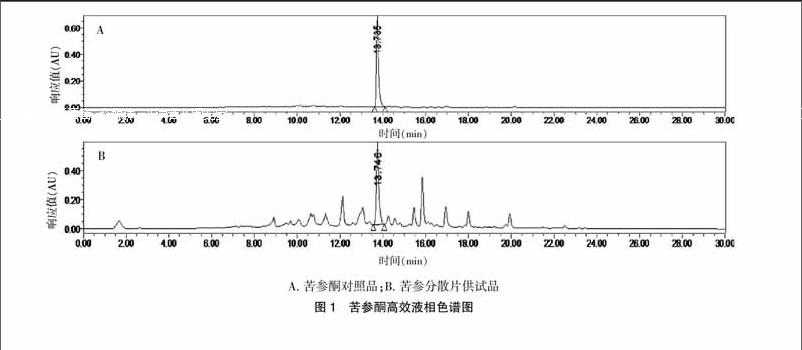
色谱柱Sunfire C18(Waters,250 mm × 4.6 mm,5 μm);流动相:乙腈-水= 80︰20(0.1%甲酸);流速:1.0 mL/min;检测波长:300 nm;进样量:20 μL;柱温:25℃。分别取苦参酮对照品溶液和苦参分散片供试品溶液进样,高效液相色谱图见图1。
2.6.2 对照品溶液的制备
精密称取在105℃干燥至恒重的苦参酮对照品4.21 mg,置10 mL容量瓶中,用甲醇溶解并定容至刻度,制成每1 mL含421 μg的对照品溶液贮备液。
2.6.3 供试品溶液制备
取苦参分散片6片,粉碎,置100 mL具塞锥形瓶中,精密加入甲醇25 mL,加塞,精密称重,超声(功率500 W,频率40 kHz)处理30 min,放冷,再精密称重,用甲醇补足减失的重量,震荡摇匀,滤过(0.45 μm微孔滤膜过滤),取续滤液,即得。
2.6.4 方法学考察
2.6.4.1 线性关系 分别精密量取苦参酮对照品溶液,用甲醇稀释成一系列浓度为0.421、0.211、0.105、0.053、0.027、0.014 mg/mL,注入高效液相色谱仪,按“2.6.1”项下色谱条件测定,以苦参酮浓度(mg/mL)为横坐标(X),峰面积为纵坐标(Y),绘制标准曲线,得回归方程Y=3.92×104X-7527,R2=0.9999,表明苦参酮在0.014~0.421 mg/mL范围内线性关系良好。
2.6.4.2 精密度实验 精密吸取0.421 mg/mL对照品溶液1 mL,置10 mL量瓶中,加甲醇稀释并定容,精密吸取20 μL,连续进样6针,按“2.6.1”项下色谱条件测定。计算苦参酮峰面积的RSD为1.06%,结果表明精密度良好。
2.6.4.3 重现性实验 取苦参片分散片6片,依“2.6.3”项下制备供试品溶液方法处理,平行操作6份,按“2.6.1”项下色谱条件测定。计算苦参酮峰面积的RSD为1.77%,结果表明,该方法的重现性良好。
2.6.4.4 稳定性实验 取苦参分散片6片,精密称定,依“2.6.3”项下制备供试品溶液方法处理,分别于0、4、8、12、24、48 h进样,按“2.6.1”项下色谱条件测定,计算苦参酮峰面积的RSD为1.03%,结果表明供试品溶液在48 h内稳定。
2.6.4.5 回收率试验 精密称取已知含量的苦参分散片约0.2 g,共6份,分别精密加入0.421 mg/mL苦参酮对照品溶液2 mL,依“2.6.3”项下制备供试品溶液方法处理,按“2.6.1”项下色谱条件测定,计算苦参酮回收率为99.83%,RSD为1.25%,结果见表5。
2.6.5 溶出介质的选择
由于苦参降糖活性部位在水中难溶,因此分别用水、4%吐温-80、人工胃液、0.5%十二烷基硫酸钠(SDS)作为溶出介质。取苦参分散片6片,按照溶出度测定法(根据《中国药典》2010版二部附录XC溶出度测定法第一法),加入溶剂500 mL[15],转速为100 r/min,依法操作,45 min时,取溶液5 mL,滤过,测定,结果水、4%吐温-80、人工胃液、0.5%SDS的溶出度分别为35.8%、71.3%、43.6%、81.1%。在0.5%SDS中,苦参酮的溶出度最大,故选定0.5%SDS作为溶出介质。
2.6.6 溶出度的测定
按照《中国药典》2010版二部附录XC溶出度测定法(第一法)进行测定。苦参分散片为难溶性药物,为了增加药物的溶解度,促进药物的释放,往往采用在释放介质中加入表面活性剂的方法[20]。根据表6实验结果,我们选择0.5% SDS溶液作为溶出介质,溶液体积为500 mL,介质温度:(37±0.5)℃。采用转篮法,转速:100 r/min,取样时间:5、10、20、30、45、60 min,在规定时间内分别吸取溶液5 mL,并立即补充5 mL同温度的介质,溶出液用0. 45 μm的微孔滤膜过滤,精密吸取续滤液2 mL,用介质稀释并定容至5 mL作为样品液。另精密称取6份苦参分散片研细,按“2.6.3”项方法配制,作为对照溶液。分别取样品液及对照液采用前述的高效液相色谱法在300 nm波长处测定苦参酮的量,并以此计算累积溶出度,结果见表6。
结果表明,本品的累积溶出度在45 min内随溶出时间增加而上升,45 min后渐渐趋于平稳,溶出度均可达80%以上,片剂间差异小。
3 讨论
糖尿病是一种多病因的代谢性疾病,其特点是慢性高血糖,伴随因胰岛素分泌或作用缺陷所引起的糖、脂肪和蛋白质代谢紊乱,2型糖尿病占患者群体的90%以上,目前我国糖尿病患病率达9.7%,给社会医疗保障体系带来极大负担。传统中医药是我国宝贵的文化遗产,为人类健康事业做出了巨大贡献。我国拥有丰富的中草药资源和几千年利用天然药物防病治病的临床经验,因而从中草药中寻找新颖的抗糖尿病药物蕴含着巨大的潜力。已有文献报道苦参提取物及其化学成分有良好的抗糖尿病活性,但它们以其原型药物应用,不但口感差,稳定性差,而且使用不方便。本研究将其制成现代剂型——中药分散片,可以提高有效成分的溶出度, 促进体内吸收, 使中药得到更有效的应用,它结合片剂和液体制剂的优点并避免了其缺点,不仅稳定性好、便于携带、服用方便,还有生物利用度较高的优点。既可直接吞服或含于口中吮服,也可投入水中迅速崩解形成均匀的混悬液。本课题在中医药理论指导下,结合中药化学、中药药剂学、中药药理学等学科的现代研究成果,根据临床用药的实际要求,考虑处方中与功能主治有关的药物化学成分及其性质,选择分散片剂型,对其制剂工艺方面进行研究,为临床提供一种工艺合理、质量可控、稳定有效的治疗糖尿病药物提供思路。
(志谢:感谢中南民族大学药学院杨新洲教授对本研究给予的指导和帮助!)
[参考文献]
[1] 国家中医药管理局《中华本草》编委会.中华本草(第4卷)[M].上海:上海科学技术出版社,1999:634-643.
[2] 郑艳敏,李轩,赵红艳,等.苦参碱和氧化苦参碱对SMMC-7721细胞增殖及Stat3,Stat5基因表达的影响[J].中国中药杂志,2008,33(19):2234-2237.
[3] 王俊梅,豆衛,杨自芳,等.苦参碱对草地蝗虫种群密度的控制效果[J].草原与草坪,2008(6):66-68.
[4] 张淑红,周宝利,张磊,等.土壤添加蛇床子(Cnidium monnieri)和苦参(Sophora flavescens)对茄子黄萎病及根际微生物的化感影响[J].生态学报,2008,28(10):5194-5199.
[5] 张鸣杰,黄建.苦参碱类抗肿瘤作用机制研究的新进展[J].中国中药杂志,2004, 29(2):115-118.
