雷公藤红素的长期毒性研究
2017-06-01慧海南省药物研究所海南海口570314
王 慧海南省药物研究所,海南 海口 570314
雷公藤红素的长期毒性研究
王 慧
海南省药物研究所,海南 海口 570314
目的:研究雷公藤红素口服给药的长期毒性情况,确定其安全剂量。方法:分别通过设立高、中、低剂量组、空白对照组等组别,研究口服给药3个月后对大鼠的毒性情况,结合给药后大鼠的一般状况、体重、摄食量、血液学检查、尸解结果和组织病理学检查结果进行综合判定,判断动物是否发生毒性反应,确定大鼠无毒性反应剂量、毒性反应剂量或安全剂量范围。结果:对实验数据进行分析发现,3个给药剂量在实验期及恢复期间均不影响大鼠体重、摄食量、脏器系数、血常规指标、血清生化学指标,对高剂量组进行组织病理学检查也尚未发现异常的组织病理学病变。结论:给予大鼠灌胃雷公藤红素3个月,未观察到与受试物本身相关的毒性反应,在剂量470ug/kg下未见有害作用,此剂量可作为安全剂量。
雷公藤红素;长期毒性;毒性研究
雷公藤红素(Celastrol,又名南蛇藤素)主要来源于中药雷公藤的根皮,具有抗炎、抗氧化等活性。近年来发现雷公藤具有很好的抗肿瘤作用,并且市场需求逐年上升,尽管雷公藤红素具有显著的药理活性[1],但其毒性也不容忽视[2],是其临床应用的最大问题。因此,研究对其毒性情况进行全面而深入的认识,在保持或提高其药理活性的同时应该尽可能降低其毒性。
1 仪器与材料
1.1 实验动物 SPF级SD大鼠,体重80~100g,雌雄各半。由长沙市天勤生物技术有限公司(生产许可证号:SCXK(湘)2014-0011)提供。使用屏障级动物房(使用许可证号:SYXK(琼)2014-0025)饲养。A级大、小鼠维持饲料喂养,由长沙市天勤生物技术有限公司(生产许可证号:SCXK(湘)2014-0011)提供。饮水经消毒后由动物自由饮用,符合SPF级动物饮水要求。
1.2 材料 雷公藤红素(海南省药物研究所自提,纯度90.1%);羧甲基纤维素钠(国药集团化学试剂有限公司生产批号:20140406);血液化验分析系统分析试剂(稀释液、溶血剂和清洗剂)由EXIGO公司提供;血生化检测试剂由日本和光,朗道公司提供。
1.3 仪器 DT5-2离心机(时代北利);AUW220D电子天平(岛津);YP30K电子天平(上海良平);TP1020脱水机(莱卡);EG1150H石蜡包埋机(莱卡);RM2245轮转式切片机(莱卡);HI1210摊片机(莱卡);立式显微镜(索尼);血生化测定仪(Echo plus);动物血细胞分析仪(Exigo)。
2 方法
2.1 试验方法[3]将80只SD大鼠随机分为供试品高、中、低剂量组及空白对照组,每组20只,雌雄各半,给药组给予雷公藤470μg/kg、94μg/kg、和47μg/kg,空白对照组给予0.5%羧甲基纤维素钠溶液,各组均按大鼠10 mL/kg体重灌胃给药,每天1次,连续灌胃给药12周,停止给药2周作为恢复期观察,给药期(12周)和恢复期(2周)各组大鼠于第1次给药前及给药后至恢复期结束每周末称体重1次,并观察动物的一般状况及计算每周动物摄食量。给药期和恢复期,各组分别取大鼠14、6只处死,雌雄各半,麻醉后采血,测定血常规、和血清生化学指标,大鼠重要脏器称重后计算脏器系数,病变器官进行主要脏器的组织病理学检查。结合大鼠的状况、组织病理学检查结果及检测数据进行综合判定,判断动物是否发生毒性反应,确定大鼠无毒反应剂量、毒性反应剂量或安全剂量范围。
2.2 统计方法 采用SPSS19.0软件单因素方差分析[4]进行统计处理,数据以(x±SD)表示,采用t检验,P<0.05表示差异有统计学意义。
3 结果
3.1 一般状况 给药期及恢复期间各组大鼠活动灵活,反应敏捷,被毛整洁,目光有神,眼、鼻、口无异常分泌物,进食饮水正常,未见明显毒性反应,各组动物均无死亡。
3.2 对大鼠体重的影响 给药期间,雄性大鼠,低、高剂量组动物体重与对照组比较,差异不具有统计学意义(P>0.05);中剂量组动物体重,在给药第12周,与对照组比较有所下降(P<0.05),恢复期,雄性中剂量组恢复期第1周,与对照组比较降低(P<0.05)。其他组别与对照组比较,差异不具有统计学意义(P>0.05)。结果见表1。
雌性大鼠低剂量组动物体重,在给药第3周,与对照组比较差异具有统计学意义(P<0.05);高剂量组动物体重,在给药第7、8、9周,与对照组比较差异具有统计学意义(P<0.05);中剂量组动物体重与对照组比较,差异不具有统计学意义(P>0.05)。恢复期雌性各组与对照组比较,差异不具有统计学意义(P>0.05)。结果见表2。

表1 给药期及恢复期的雄性大鼠体重 (g,x±SD)
注: 与对照组比较,*P<0.05。

表2 给药期及恢复期的雌性大鼠体重 (g,x±SD)
注:与对照组比较,*P<0.05。
3.3 对大鼠摄食量的影响 给药期间的雄性大鼠摄食量,中剂量组与对照组比较,第12周的动物摄食量明显减少,差异具有统计学意义(P<0.05),高、低剂量组雄性大鼠与对照组比较差异不具有统计学意义(P>0.05)。见表3。
给药期间的雌性大鼠摄食量,高剂量组与对照组比较,第7、8周的动物摄食量明显减少,差异具有统计学意义(P<0.05),其它时间差异不具有统计学意义(P>0.05);低、中剂量组雌性大鼠与对照组比较差异不具有统计学意义(P>0.05),见表4。恢复期,各组之间饲料消耗量差异不具有统计学意义(P>0.05)。

表3 给药期及恢复期的雄性大鼠摄食量 (g,x±SD)
注: 与对照组比较,*P<0.05。

表4 给药期及恢复期的雌性大鼠摄食量 (g,x±SD)
注: 与对照组比较,*P<0.05。
3.4 对大鼠脏器系数的影响 给药期:与对照组比较,雄性大鼠高剂量组肝脏系数及肾脏系数均明显增大(P<0.05),其他各脏器系数及中、低剂量组各脏器系数比较差异不具有统计学意义(P>0.05);与对照组比较,雌性大鼠低剂量组肝脏系数明显增大(P<0.05),中剂量组由于个别大鼠脾脏系数较大,使该项指标均值偏高,标准差较大,但差异不具有统计学意义(P>0.05),其他各脏器系数及低剂量各项脏器系数差异不具有统计学意义(P>0.05)。结果见表5。
恢复期:高、中、低剂量组的各项脏器系数与对照组比较,差异不具有统计学意义(P>0.05)。结果见表6。

表5 给药期大鼠的脏器系数 (x±SD,n=7)
注:与对照组比较*P<0.05。

表6 恢复期大鼠的脏器系数 (x±SD,n=3)
3.5 对大鼠血常规的影响 给药期:与对照组比较,雌性大鼠高剂量血小板指标具有显著意义(P<0.05),同组其它指标及其它各组指标均不具有统计学意义(P>0.05);雄性大鼠各组指标均不具有统计学意义(P>0.05)。结果见表7。
恢复期:与对照组比较,雄性大鼠中剂量红细胞指标具有显著意义(P<0.05),同组其它指标及其它各组指标均不具有统计学意义(P>0.05);雌性大鼠各组指标均不具有统计学意义(P>0.05)。结果见表8。

表7 给药期大鼠血常规检测结果 (x±SD,n=7)
注:与对照组比较*P<0.05。
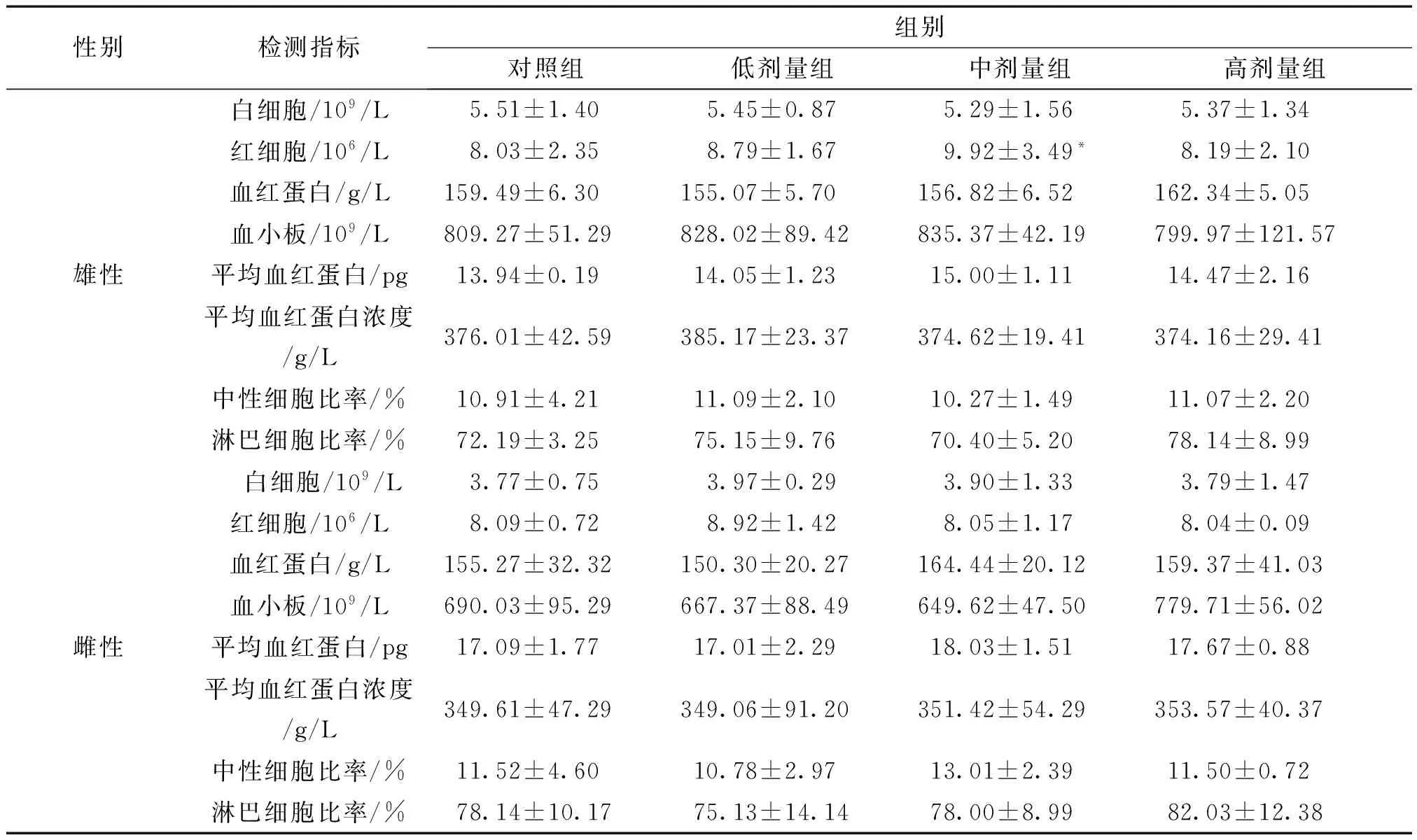
表8 恢复期大鼠血常规检测结果 (x±SD,n=3)
3.6 对大鼠血清生化学指标的影响 给药期:雄性大鼠检测与对照组比较,中剂量组AST明显升高,差异具有统计学意义(P<0.05),其它同组指标及其它各组指标与对照组比较,差异不具有统计学意义(P>0.05);雌性大鼠检测结果与对照组比较,中剂量组AST明显升高,高剂量组ALP明显降低,差异具有统计学意义(P<0.05),其它同组指标及其它各组指标与对照组比较,差异不具有统计学意义(P>0.05)。结果见表9。
恢复期:雄性大鼠检测结果与对照组比较,各剂量组所有指标差异不具有显著性意义(P>0.05);雌性大鼠检测结果与对照组比较,中剂量组及高剂量AST由于个别大鼠测定值较高,标准差较大,但差异不具有统计学意义(P>0.05),其它同组指标及其它各组指标与对照组比较,差异不具有统计学意义(P>0.05)。结果见表10。
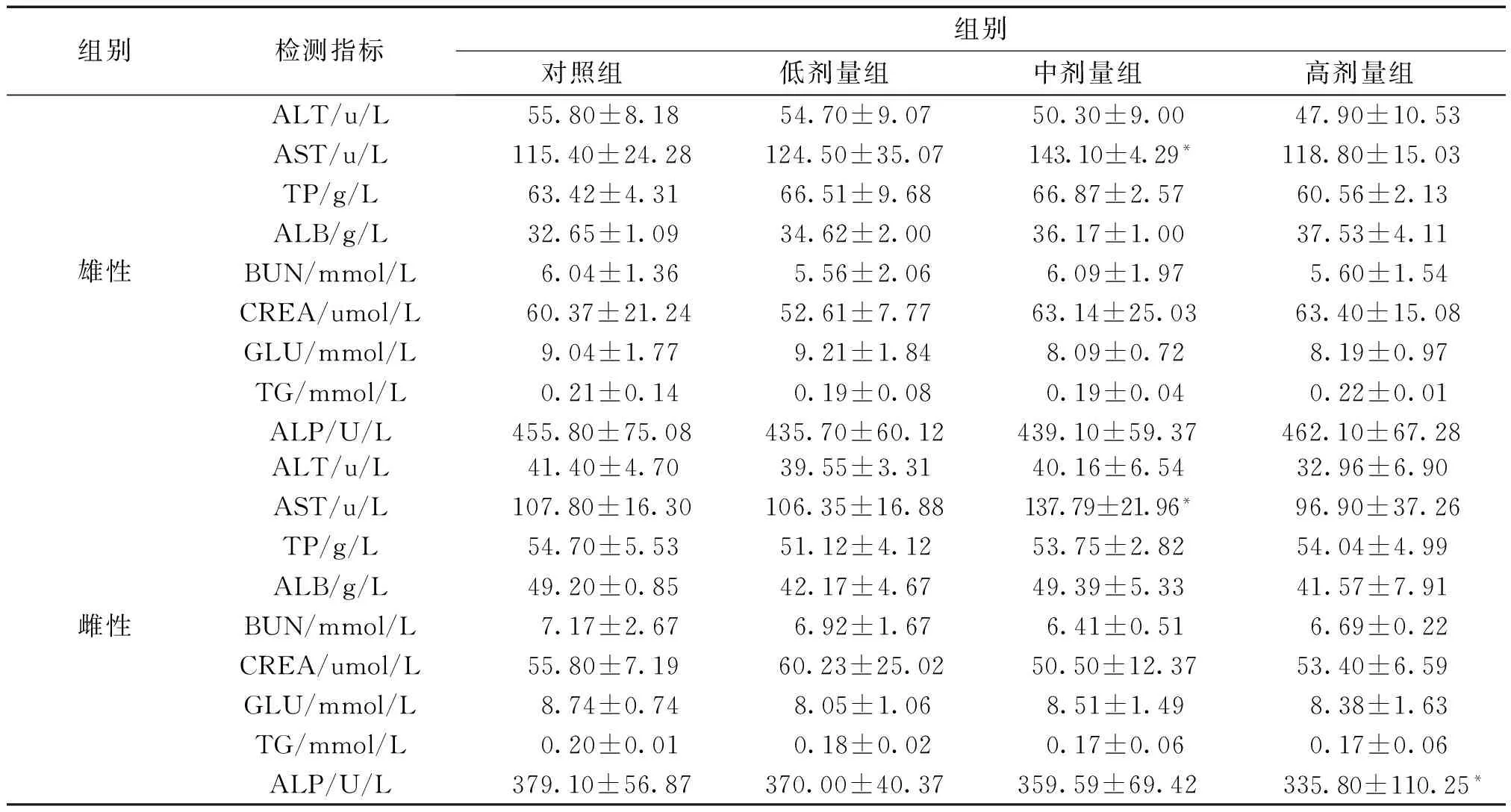
表9 给药期大鼠血清生化学指标检测结果 (x±SD,n=7)
注:与对照组比较,*P<0.05。

表10 恢复期大鼠血清生化学指标检测结果 (x±SD,n=3)
3.7 剖检观察结果及病理组织学检查 实验期及恢复期发现,供试品本身并不引起大鼠组织器官形状、体积大小、色泽、位置、硬度、外膜等的异常改变。取部分高剂量组及对照组动物剖检,未发现与供试品本身相关的病理学检查,因此不进行中、低剂量组检查。
4 讨论
雷公藤红素长期毒性剂量组的剂量设置,是根据本实验室前期研究中得到LD50 4.69mg/kg决定,大鼠3个月长期毒性试验中高、中、低3个剂量可分别采用1/10、1/50、1/100左右的LD50,符合长期毒性试验设计原则[5]。
经3个月给药及恢复期研究发现,雷公藤红素(470μg/kg、94μg/kg和47μg/kg)未引起大鼠一般状况异常、组织器官异常及组织病理学病变,虽然大鼠体重、摄食量及个别脏器系数、血常规指标及血清生化指标在给药期或恢复期出现部分数据的差异性,但从整体研究周期数据来看,均未体现任何规律性,也不存在任何剂量相关性及性别相关性,认为此指标的的差异性不存在实际意义,应并无毒理学意义。
综上所述,在本实验室条件下,大鼠经口灌胃给予雷公藤红素3个月,未观察到与受试物本身相关的毒性反应,在剂量470μg/kg以下未见有害作用,在此剂量以下使用,可作为安全剂量。
[1]胡凯,葛卫红.雷公藤红素药理活性研究进展[J].亚太传统医药,2012,8(11):179-181.
[2]袁菱,陈彦,周蕾,等. 纳米结构脂质载体降低雷公藤红素毒性的实验研究[C].//首届全国方剂组成原理高峰论坛. 2012.
[3]高晓东,李雪萍,徐春茂,等. 扶正逐毒丸制剂大鼠长期毒性实验研究[J]. 中国临床药理学杂志, 2015(7):563-565.
[4]张晓冬,宗英,陆国才,等. 药物长期毒性试验血液和生化指标的统计处理[J].中国新药杂志,2010,19(4):270-272.
[5]国家食品药品监督管理局.药物研究技术指导原则(2005)[M].北京:中国医药科技出版社,2005:217-226.
海南省自然科学基金(NO:814286)。
王慧(1984-),汉族,女,本科,助理研究员,研究方向为药理学研究。E-mail:42321346@qq.com
R285.5
A
1007-8517(2017)06-0039-07
2017-01-13 编辑:梁志庆)
