蜂胶黄酮
——铝锆复合氧化物的制备和缓释性能研究
2017-06-01赵传怡张庆乐许福生张凌霄王福刚王浩
赵传怡 张庆乐 许福生 张凌霄 王福刚 王浩
(泰山医学院药学院,泰安 271016)
蜂胶黄酮
——铝锆复合氧化物的制备和缓释性能研究
赵传怡 张庆乐 许福生 张凌霄 王福刚 王浩
(泰山医学院药学院,泰安 271016)
利用铝锆复合氧化物作为新型药物缓释材料,对蜂胶黄酮进行负载和缓释,为提高其生物利用度提供科学依据。方法:利用植物提取液为软模板合成铝锆复合氧化物,通过单一因素试验评价该材料的制备条件对蜂胶黄酮负载率的影响,并利用体外试验分析了蜂胶黄酮的缓释效果。结果:以冬青提取液作为溶剂、三氯化铝和氯氧化锆的摩尔比为8∶1,添加0.08 g纳米海泡石和400 mg/L环糊精时制备的铝锆复合氧化物对蜂胶黄酮的最大负载率为83.41%。蜂胶黄酮—铝锆复合氧化物在模拟胃液和肠液中最大释放时间为480 min。结论:铝锆复合氧化物适宜作为蜂胶黄酮的缓释载体。
铝锆复合氧化物;蜂胶黄酮;冬青提取液;缓释
黄酮类化合物是一类重要的植物次生代谢物质,广泛分布于植物的根、表皮、叶片和果实中,其在植物体内的含量仅次于纤维素、半纤维素和木质素[1]。许多研究表明,黄酮类化合物具有抗菌、抗病毒、抗癌、抗氧化、降血脂、增强免疫力等多种药理活性,在预防阿尔默茨海默病和心血管疾病等方面具有极为重要的应用价值[2-4]。与大多数天然植物相比,蜂胶中所含有的黄酮种类丰富且含量较高,其提取技术和药物制剂剂型的研究引起了中外学者的广泛关注。乙醇提取法是目前蜂胶黄酮和其他植物黄酮提取中应用最为广泛的提取技术[5],然而由于蜂胶黄酮难溶于水,生物利用度低,其在医学上的应用受到很大限制[6]。开发黄酮制剂的新剂型,提高其生物利用度成为当前的研究热点。
载药纳米粒是一种药物控释和缓释的新剂型,常用的载药材料包括生物可降解聚合物如聚乳酸、聚己内酯等疏水性聚合物[7,8]、壳聚糖、海藻酸钠等亲水性聚合物[9,10]和固体脂质如饱和脂肪酸甘油酰、卵磷脂、甘油三酯等[11,12]。层状双金属氧化物因其具有良好的生物相容性和化学稳定性,层间存在可交换的阴离子,药物分子可插层于层状双金属氧化物的层间而形成药物/层状双金属氧化物杂化物[13,14],从而使其成为一种极具潜力的药物缓释载体材料。许多研究表明,制备方法和条件对层状双金属氧化物的形貌结构具有显著影响[15,16],从而影响其药物负载能力。模板法是目前合成层状双金属氧化物的最常见方法,利用植物提取液作为溶剂和分散剂,通过改变制备条件,可对层状双金属氧化物的颗粒大小和药物负载能力进行有效调控。
本文采用冬青提取液为软模板合成铝锆复合氧化物,利用其作为新型缓释材料,探讨了其制备条件对蜂胶黄酮负载量的影响和缓释效果。
1 材料与仪器
1.1 试验材料
1.2 试验仪器
主要仪器:KQ-100型超声波清洗仪(北京东南仪诚实验室设备有限公司);TDL-5A型台式离心机(金坛市宏华仪器厂);HJ-6型六联磁力搅拌器(江苏省金坛市宏华仪器厂);HY-3型恒温振荡器(江苏省金坛市宏华仪器厂);752S紫外可见分光光度计(上海棱光技术有限公司)。
2 试验方法
2.1.蜂胶黄酮的制备
采用付英娟等人[17]的方法对蜂胶总黄酮进行提取:将0.2 g蜂胶和一定量的质量分数为80%的乙醇溶液加入到锥形瓶中,置于超声波清洗仪中在功率540W下提取20 min,经离心分离后,滤渣重复超声提取若干次,合并滤液,将滤液置于4℃冰箱中冷藏保存。
2.2 铝锆复合氧化物的制备
利用植物提取液为软模板合成铝锆复合氧化物,主要步骤如下:将一定量的三氯化铝、氯氧化锆、纳米海泡石和环糊精加入到盛有100 ml植物提取液的烧杯中,将其置于磁力搅拌器上连续搅拌2h,使溶液混合均匀。然后,利用1.0mol/L的氢氧化钠溶液对其进行逐滴滴定,直至溶液的pH为9.5,继续搅拌2 h后,将混合液置于80℃的烘箱中陈化24 h,过滤后,将滤渣于105℃干燥24 h,得到铝锆复合氧化物。通过改变金属盐种类、铝锆摩尔比、纳米海泡石和环糊精加入量等反应条件制备系列铝锆复合氧化物。
2.3 蜂胶黄酮负载方法
将0.1g的铝锆复合氧化物加入到盛有100 ml浓度为85mg/L蜂胶黄酮的锥形瓶中,置于恒温振荡器上进行震荡反应,待反应达到平衡后,过滤。以芦丁为标准品,在亚硝酸钠-氯化铝-氢氧化钠显色体系中进行显色反应,利用紫外可见分光光度计在510nm处测定滤液的吸光值,利用下式(1)计算蜂胶黄酮负载率:
采用ANSYS三维有限元计算软件进行模拟计算分析。根据实例工程的特性及相关参数,网格选择矩形网格,网格间距设置为5~20m,整个模型共有12856个节点与8266个网格(图3)。

式中:R为蜂胶黄酮负载率;C0为蜂胶黄酮初始浓度;Ce为蜂胶黄酮平衡浓度。
2.4 响应曲面法优化铝锆复合氧化物的制备条件
依据Box-Behnken设计原理,选取铝锆摩尔比、海泡石投加量、环糊精浓度3个影响因素进行响应曲面分析,对铝锆复合氧化物的制备条件进行优化,以蜂胶黄酮负载率为评价指标,确定最优制备条件。实验因素与水平设计见表1。
2.5 蜂胶黄酮释放量的测定

表1 响应面分析因素及水平
首先,配制pH值为4.8的磷酸一柠檬酸缓冲溶液和pH值为7.2的磷酸缓冲溶液作为人工胃液和肠液。然后,将0.3g蜂胶黄酮/铝锆复合氧化物杂化材料加入到100ml的模拟胃液和肠液中,在37℃、100 r/min下进行恒温震荡,按照设定的时间间隔进行取样,经0.45μm的滤膜过滤后,利用紫外——可见分光光度计在510 nm下测定其吸光度,计算蜂胶黄酮释放量。每个实验重复三次,结果取平均值。
3 结果与分析
3.1 制备条件对蜂胶黄酮负载率的影响
3.1.1 不同金属氧化物对蜂胶黄酮负载率的影响
将0.001 mol的氯化铝、氯氧化锆、氯化镁、氯化铁、硫酸锌、氯化锡、硝酸铈分别加入到盛有100 ml冬青提取液的烧杯中,利用类似合成方法,得到氧化铝、氧化锆、氧化镁、氧化铁、氧化锌、氧化锡、氧化铈七种材料。由图1可知,氧化锡对蜂胶黄酮的负载率最低为41.2%,氧化铁、氧化锌、氧化镁和氧化铈对蜂胶黄酮的负载率为50%左右,而氧化铝和氧化锆对蜂胶黄酮的负载率较高,分别为57.6%和60.6%。因此,在后续试验中通过调整铝锆摩尔比来评价铝锆复合氧化物对蜂胶黄酮负载率的影响。

图1 不同金属氧化物对蜂胶黄酮负载率的影响
3.1.2 铝锆摩尔比对蜂胶黄酮负载率的影响

图2 铝锆摩尔比对蜂胶黄酮负载率的影响
将总摩尔质量为0.001mol的氯化铝和氯氧化锆(其摩尔比分别为1∶1、1∶4、1∶8、4∶1、8∶1)依次加入到盛有100 ml冬青提取液的烧杯中,合成铝锆复合氧化物。由图2可知,随着铝锆摩尔比的增加,铝锆复合氧化物对蜂胶黄酮负载率呈现先降低后增加的趋势,当铝锆摩尔比为4∶1时,该复合氧化物对蜂胶黄酮的负载率达到最大值70%,继续增加铝锆摩尔比,蜂胶负载率基本趋于稳定。因此,选择铝锆摩尔比为4∶1时制备该复合氧化物效果较好。
3.1.3 纳米海泡石投加量对蜂胶黄酮负载率的影响

图3 海泡石含量对蜂胶黄酮负载率的影响
将总摩尔质量为0.001mol的氯化铝和氯氧化锆(其摩尔比为4∶1)和不同质量的纳米海泡石(0.02、0.04、0.06、0.08、0.10 g)依次加入到盛有100 ml冬青提取液的烧杯中,采用类似方法合成铝锆复合氧化物。由图3可知,当纳米海泡石的投加量从0.02 g增加到0.08 g时,铝锆复合氧化物对蜂胶黄酮的负载率从48.8%迅速增加到68.8%。超过0.08 g后,继续增加纳米海泡石的用量,铝锆复合氧化物对蜂胶黄酮的负载率基本稳定。因此,选用0.08 g的纳米海泡石进行铝锆复合氧化物的制备为宜。
3.1.4 环糊精浓度对蜂胶黄酮负载率的影响

图4 环糊精含量对蜂胶黄酮负载率的影响
将总摩尔质量为0.001 mol的氯化铝和氯氧化锆(其摩尔比为4∶1)、0.08 g的纳米海泡石和不同质量浓度的环糊精(0、100、200、400、600、800、1000 mg/L)依次加入到盛有100 ml冬青提取液的烧杯中,采用类似方法合成铝锆复合氧化物。由图4可知,当环糊精浓度从0 mg/L增加到200 mg/L时,随着环糊精浓度的增加,蜂胶黄酮的负载率从68.8%增加到80.6%;而当环糊精浓度超过200mg/L时,蜂胶黄酮的负载率增速较为缓慢,基本稳定在82%左右。因此,选取环糊精浓度为200mg/L进行铝锆复合氧化物的制备。
3.2 响应面分析
使用Design-Expert 7.0.0软件对铝锆摩尔比、海泡石投加量、环糊精浓度3个影响因素设计三因素三水平共17个试验响应面分析实验,相应试验数据见表2。
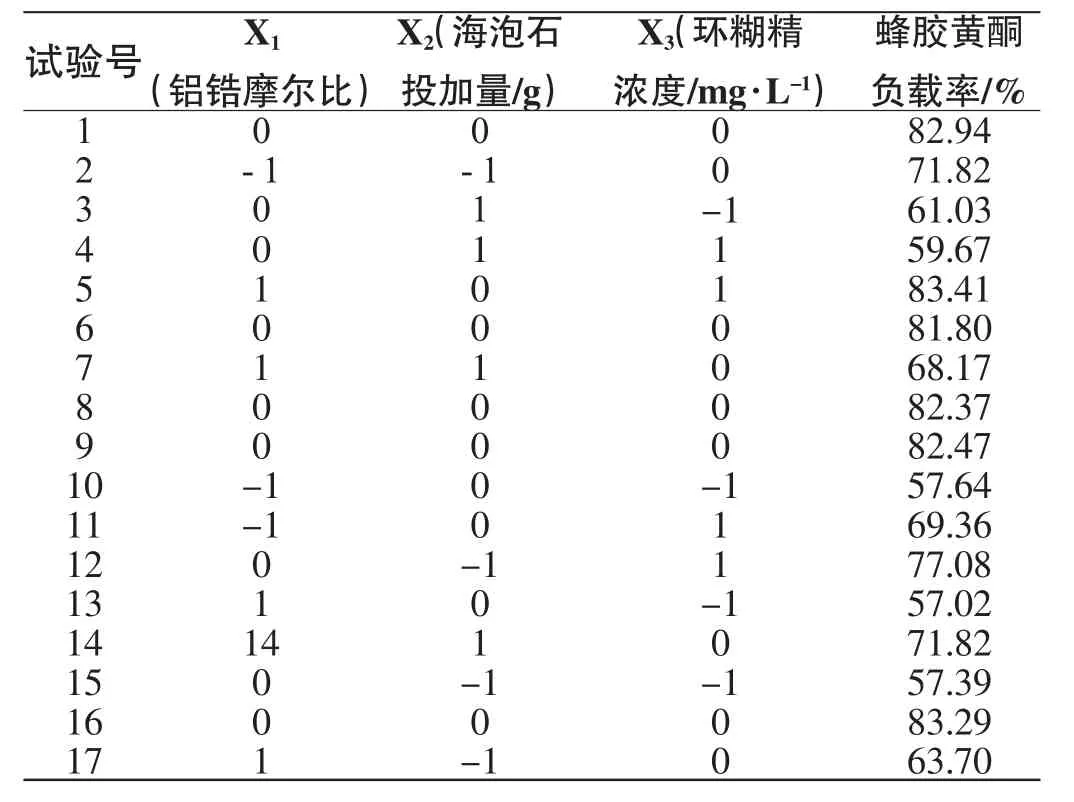
表2 响应中心组合试验设计及结果
数据分析和显著性检验见表3。
试验数据经二次方程式的数学模型拟合后,得到铝锆复合氧化物的最佳制备条件的数学模型为:Y=+ 82.57-0.42X1-1.16X2+6.43X3-5.26X2X3-5.94X12-7.75 X22+11.02X32。由表3中的P<0.01可以看出,其因变量和全体自变量之间的线性关系显著,即这种试验方法是可靠的。从各项方差的进一步检验来看,X3是影响铝锆复合氧化物制备的关键因子。X1和X2对试验结果影响不太明显。另外,方程的失拟项F=93.41,显著,表明方程对试验拟合情况好,实验误差小,因此可用该回归方程代替试验真实点对试验结果进行分析和预测。回归模型预测的最佳去除率的工艺条件是铝锆摩尔比为8∶1、海泡石投加量为0.08 g、环糊精浓度为400 mg/L,此条件下制备的铝锆复合氧化物对蜂胶黄酮的最大负载率为83.41%。
3.3 蜂胶黄酮的释放率的测定
由图5可知,经铝锆复合氧化物负载后,蜂胶黄酮在pH4.8(模拟胃液)和pH 7.2(模拟肠液)下的释放率均随反应时间的延长而逐渐增加,且在模拟胃液下的释放效果更佳。整个释放过程可分为三段:当反应时间小于120 min时,蜂胶黄酮在模拟胃液和肠液下的释放率增幅较大;在120~480 min时,蜂胶黄酮在模拟胃液和肠液下的释放率增幅较为缓慢,逐渐趋于稳定。超过480 min后,蜂胶黄酮释放率基本稳定。因此,该复合氧化物对蜂胶黄酮的最大缓释时间为480 min,在模拟胃液和肠液的最大释放率分别为82.3%和75.7%。
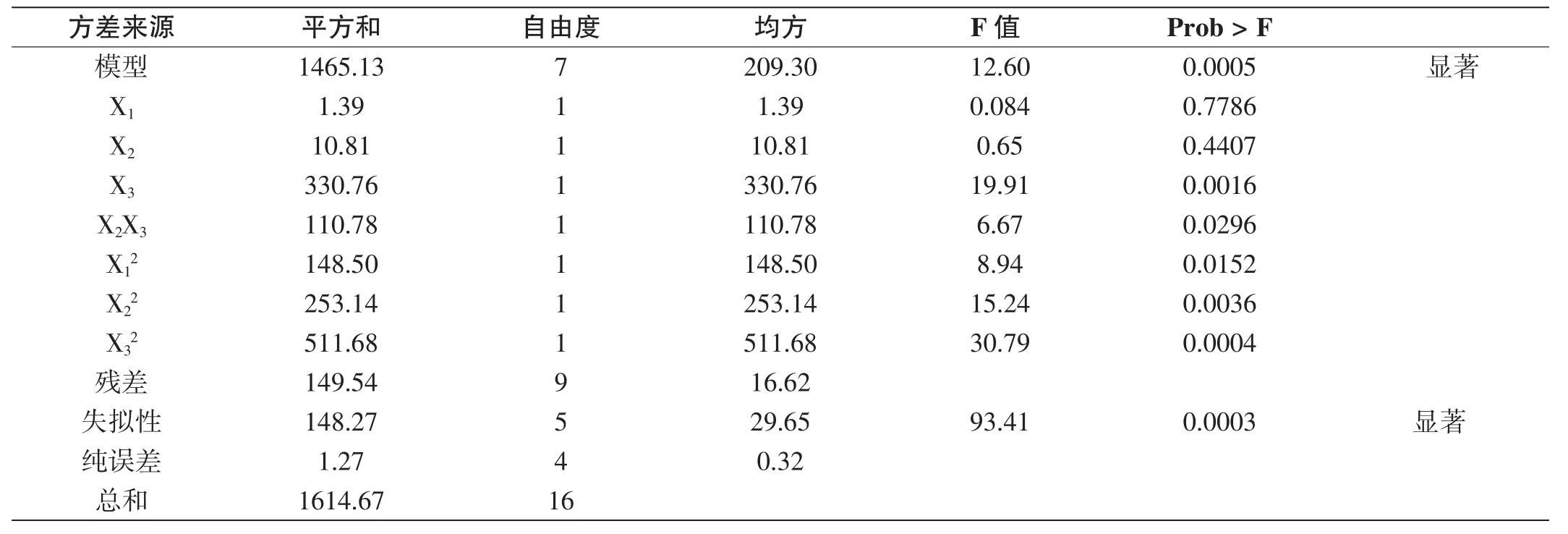
表3 回归方程的方差分析表

图5 蜂胶黄酮在pH为4.8和pH为7.2下的释放率曲线
4 结论
利用冬青提取液为软模板合成的铝锆复合氧化物作为新型缓释材料,对蜂胶黄酮进行负载和缓释,试验结果表明:(1)制备条件对蜂胶黄酮负载量有显著影响,当向100ml冬青提取液中添加总摩尔质量为0.001 mol的氯化铝和氯氧化锆(摩尔比为8∶1)、0.08 g的纳米海泡石、400 mg/L的环糊精时制备的铝锆复合氧化物对蜂胶黄酮的负载率达到最大值83.41%。(2)在模拟胃液和肠液下,该复合氧化物对蜂胶黄酮具有较好的缓释效果,最大释放时间为480 min。
[1]邵芳芳,尹卫平,梁菊.重要的植物多酚及抗氧化性能的研究概况[J].西北药学杂志,2012,225(1):66-68.
[2]曹秦,吴辉,张蓓蓓,等.黄酮类化合物在防治神经退行性疾病中作用的研究进展 [J].中国药理学与毒理学杂志,2015,29(3): 457-463.
[3]李冬生,陈朝银,赵声兰,等.黄酮类化合物改善记忆的机制研究[J].食品工业科技,2014,35(10):360-365.
[4]郭雪微,卢梃,王雪里红.天然黄酮类化合物在心脑血管疾病中应用进展[J].中国老年学杂志,2006,26(4):1001-1003
[5]李帅,赵岩岩,陈晓平.响应面优化微波辅助乙醇提取蜂胶黄酮工艺优化[J].食品科学,2012,33(18):127-132
[6]程智刚.蜂胶提取活性黄酮及酯萜类新工艺和其纳米制剂—蜂胶总黄酮硬脂酸固态脂质纳米粒制备及药理学研究[D].长沙:中南大学,2005,1-116
[7]Wei Zhang,Jing gao,Quangang Zhu,et al.Penetration and diatribution of PLGA nanoparticles in the human skin treated with microneedles[J].International Journal of Pharmaceuties,2010,402(1-2): 205-212
[8]Wean Sin Cheow,Kunn Hadinoto.Enhancing encapsulation efficiency of highly water-soluble antibiotic in poly(lactic-co-glycolic acid)nanoparticles:Modifications of standard nanoparticle preparation methods[J].Colloids and Surfaces A:Physicochemical and Engineering Aspects,2010,370(1-3):79-86
[9]程浩南.羧甲基壳聚糖在药物缓释和组织工程学中的应用新进展[J].材料导报,2015,21:137-144
[10]冯志云,吴敏,朱昌平,等.聚乙二醇共价交联海藻酸钠凝胶制备及其药物缓释性能 [J].材料科学与工程学报,2015,33(3):368-371
[11]管清香,朱昆,林天幕,等.可生物降解固体脂质纳米粒的制备、表征及药物的体外释放 [J].高等学校化学学报,2010,31(11):2298-2302
[12]单良,汤志勇,刘元法,等.蜂胶黄酮萃取物脂质体制备工艺的优化及体外缓释特性[J].食品科学,2008,29(8):232-237
[13]Rives V,Arco M D,Martín C.Layered double hydroxides as drug carriers and for controlled release of non-steroidal antiin ammatorydrugs(NSAIDs):a review[J].Journal ofControlled Release,2013, 169(1/2):28-39.
[14]Rojas R,Palena MC,Jimenez-Kairuz A F,et al.Modeling drug release from a layered double hydroxide-ibuprofen complex[J].Applied ClayScience,2012,62/63:15-20.
[15]李妍.层状双金属氢氧化物作为药物载体及其释放性能研究[J].济南:山东大学,2008.1-56.
[16]Wang Q,O'Hare D.Recent advances in the synthesis and application of layered double hydroxide (LDH)nanosheets[J].Chemical Reviews,2012,112(7):4124-4155.
[17]付英娟,于智峰,张建新.超声波提取蜂胶黄酮的条件优化[J].食品工业科技,2007,28(5):143-146
Preparation of propolis flavonoid/alumina-zirconium oxide composite and controlled-release properties
Zhao Chuanyi,Zhang Qingle,Xu Fusheng,Zhang Lingxiao,Wang Fugang,Wang Hao
(Institute of pharmaceutical,Taishan Medical university,Shan dong Tai'an,271016)
Taking alumina-zirconium composite oxide as a novel material to load propolis flavonoid,providing scientific basis for increasing its bioavailability.Methods:Alumina-zirconium oxide composite was prepared using plant extracts as soft template.Effect of preparation condition of alumina-zirconium oxide composite on propolis flavonoid loading rate was discussed by single factor experiment,and controlled-release properties of propolis flavonoid was analyzed by in vitro test.Results:Using Holly extracts as solvent,when the molar ratio of aluminum chloride and zirconium oxychloride was 8∶1,0.08 g sepiolite and 400mg/L cyclodextrin,the maximum loading ratio of propolis flavonoid on alumina-zirconium composite oxide was got at 83.41%.The maximum release time of propolis flavonoid/alumina-zirconium composite oxide in stimulated gastric juice and intestinal juice was 480 min.Conclusion:Alumina-zirconium oxide composite was suitable for the controlled-release material of propolis flavonoid.
Alumina-zirconium oxide composite;propolis flavonoids;holly extracts;controlled-release
国家大学生创新创业计划项目(201510439076),山东省自然科学基金(ZR2013HL062)
赵传怡(1995-),山东莱芜市人,2013级药学专业本科学生
王浩,副教授,研究方向为中药药理学,E-mail:tywanghao@163.com。
