非小细胞肺癌晚期吉西他滨联合铂类化疗后血清SIL—2R、TNF—α水平的临床意义
2017-05-31刘润华
刘润华
[摘要] 目的 測定非小细胞肺癌患者晚期吉西他滨联合铂类化疗前后血清中SIL-2R、TNF-α水平并分析其临床意义。 方法 方便选取2014年6月—2016年6月于该院就诊的非小细胞肺癌晚期患者160例为观察组,选取同期于该院体检的健康人80名作为对照组,统计化疗前后患者病情缓解情况,采用ELISA方法测定化疗前后血清中的SIL-2R、TNF-α水平,对比分析其临床意义。结果 化疗后病情完全缓解者0例(0.00%);部分缓解者46例(25.56%);疾病稳定者62例(34.44%);疾病进展者72例(40.00%)。疾病控制率为60.00%;观察组患者化疗前血清SIL-2R(698.35± 100.32)U/mL和TNF-α(251.02±25.62)ng/L水平显著高于对照组[SIL-2R(205.34±82.10)U/mL;TNF-α(72.33±15.24)ng/L](P<0.05);观察组患者化疗后[SIL-2R(420.26±115.28)U/mL;TNF-α(125.22±19.03)ng/L]和化疗前[SIL-2R (698.35± 100.32)U/mL;TNF-α(251.02±25.62)ng/L]相比各项指标均显著下降(P<0.05),但仍显著高于对照组(P<0.05);观察组化疗后血清SIL-2R(698.35±100.32)U/mL和TNF-α(251.02±25.62)ng/L水平下降幅度与病情缓解度呈负相关(r=-0.675,r=-0.723;P<0.05)。 结论 非小细胞肺癌患者晚期吉西他滨联合铂类化疗后血清SIL-2R、TNF-α水平显著低于化疗前,下降幅度与病情缓解情况呈负相关,可作为非小细胞肺癌患者晚期化疗疗效的评估指标。
[关键词] 非小细胞肺癌晚期;吉西他滨;铂类;SIL-2R;TNF-α
[中图分类号] R246.1 [文献标识码] A [文章编号] 1674-0742(2016)12(c)-0010-04
[Abstract] Objective To test the levels of SIL-2R and TNF-α in serum of patients with non-small cell lung cancer before and after chemotherapy with gemcitabine and to analyze its clinical significance. Methods Patients with advanced non-small cell lung cancer from June 2014 to June 2016 in our hospital 160 cases of the observation group, healthy people were selected in our hospital physical examination in 80 cases as control group, statistics before and after chemotherapy remission before and after chemotherapy, determination of serum SIL-2R, TNF-α levels by using ELISA method, comparative analysis and its clinical significance. Results After chemotherapy, 0 patients (0.00%) with complete remission (46), partial remission (25.56%), 62 cases (34.44%) with stable disease, 72 cases (40.00%). The disease control rate was 60.00%; the serum SIL-2R(698.35±100.32)U/mL and TNF-α(251.02±25.62)ng/L levels of observation group before chemotherapy were significantly higher than the control group[SIL-2R (205.34±82.10)U/mL;TNF-α(72.33±15.24)ng/L] (P < 0.05);The indexes of patients in the observation group after chemotherapy[SIL-2R(420.26±115.28)U/mL;TNF-α(125.22±19.03)ng/L] compared with before chemotherapy[SIL-2R(698.35±100.32)U/mL;TNF-α(251.02±25.62)ng/L] were significantly decreased (P < 0.05), but still significantly higher than the control group(P<0.05); In the observation group, the level of serum SIL-2R(698.35±100.32)U/mL and TNF-α(251.02±25.62)ng/L decreased after chemotherapy was negatively correlated with the degree of remission(r=-0.675, r=-0.723, P<0.05). Conclusion Patients with advanced non-small cell lung cancer gemcitabine combined with platinum chemotherapy serum SIL-2R, TNF-α levels were significantly lower than that before chemotherapy, decrease and remission were negatively correlated, can be used to evaluate the index of curative effect in patients with advanced non-small cell lung cancer.endprint
[Key words] Advanced stage of non-small cell lung cancer; Gemcitabine; Platinum; Soluble interleukin-2 receptor; Tumor necrosis factor-α
在肺癌患者中临床最常见类型为非小细胞肺癌,早期症状不明显,发现时大多属于中晚期,手术治疗效果不理想,此时临床常采用含铂类两药化疗方案,疗效观察一般采用影像学检查,但不易对早期化疗效果进行观察[1-2]。有研究显示[3],可溶性白细胞介素-2受体(soluble interleukin-2 receptor,SIL-2R)、肿瘤坏死因子α(tumour necrosis factor-α)与肿瘤的发生、发展有密切关系。鉴于此,该文方便选取2014年6月—2016年6月于该院就诊的160例非小细胞肺癌晚期患者作为研究对象,采用酶联免疫吸附法(enzyme linked immunosorbent assay,ELISA)检测非小细胞肺癌患者晚期吉西他滨联合铂类化疗前后血清中SIL-2R、TNF-α水平并分析其临床意义,以期为非小细胞肺癌晚期患者化疗效果提供更多证据,现报道如下。
1 资料与方法
1.1 一般资料
方便选取于该院就诊的非小细胞肺癌晚期患者160例为观察组,其中男性95例,女性65例;年龄33~69岁,平均年龄(55 ± 6.5)岁。病例纳入标准:①经病理组织学、临床检查、影像学检查确诊为Ⅲ~Ⅳ期非小细胞肺癌患者;②确诊后的6个月内无任何抗肿瘤治疗,如化疗、放疗、生物免疫治疗;③可自由活动,活动狀态评分(KPS)≥60分;④签署知情同意书,自愿配合研究。排除标准:①存在严重心、肝、肺、肾等脏器及骨髓功能异常的肺癌患者;②合并有其他心、肝、脾、肾等严重疾病的患者。选取同期于该院体检的健康人80名作为对照组,其中男性49例,女性31例;年龄35~69岁,平均年龄(56 ± 4.5)岁。两组在性别、年龄方面差异无统计学意义(P>0.05),具有可比性。
1.2 方法
1.2.1 药品与试剂 注射用盐酸吉西他滨(国药准字H20030105);注射用顺铂(国药准字H37021358)。人SIL-2R ELISA试剂盒(PK-EL-61216);人TNF-α ELISA试剂盒(Abcam,ab181421)。
1.2.2 化疗方法 观察组患者均采用注射用盐酸吉西他滨联合注射用顺铂进行化疗,其中吉西他滨分别是于第1天和第8天1 000 mg/m2静脉注射30 min;于第1~3天分别静脉注射顺铂25 mg/m2。3周为1个化疗疗程,共2个疗程,2个疗程之间间隔1周。80名健康人不做任何治疗。
1.2.3 指标检测 采用WHO制定的实体瘤疗效评价标准[4]对化疗前后疗效进行评价:所有病灶部位均消失认为完全缓解;所有病灶部位直径总和减小30%及以上认为部分缓解;所有病灶部位直径总和减小30%以下且增大20%以下认为疾病稳定;所有病灶部位直径总和增大20%及以上认为疾病进展。疾病控制率(%)=(完全缓解例数+部分缓解例数+疾病稳定例数)/总例数×100%。分别于清晨空腹情况下采集两组肘静脉处外周血5 mL,离心3 000 rpm,10 min,取上清,作好标记。其中观察组分别于化疗前后分别采集,正常组只采集1次。采用ELISA法测定血清中SIL-2R、TNF-α水平,方法参见试剂盒说明书。正常参考值:SIL-2R<500 U/mL,TNF-α<100 ng/L。
1.3 统计方法
数据采用SPSS 19.0统计学软件包对数据进行处理,计量资料采用均数±标准差(x±s)表示,采用t检验进行分析,计数资料采用χ2检验,血清中SIL-2R、TNF-α水平与化疗疗效的关系采用Spearman相关性分析,P<0.05为差异有统计学意义。
2 结果
2.1 观察组非小细胞肺癌晚期患者化疗疗效
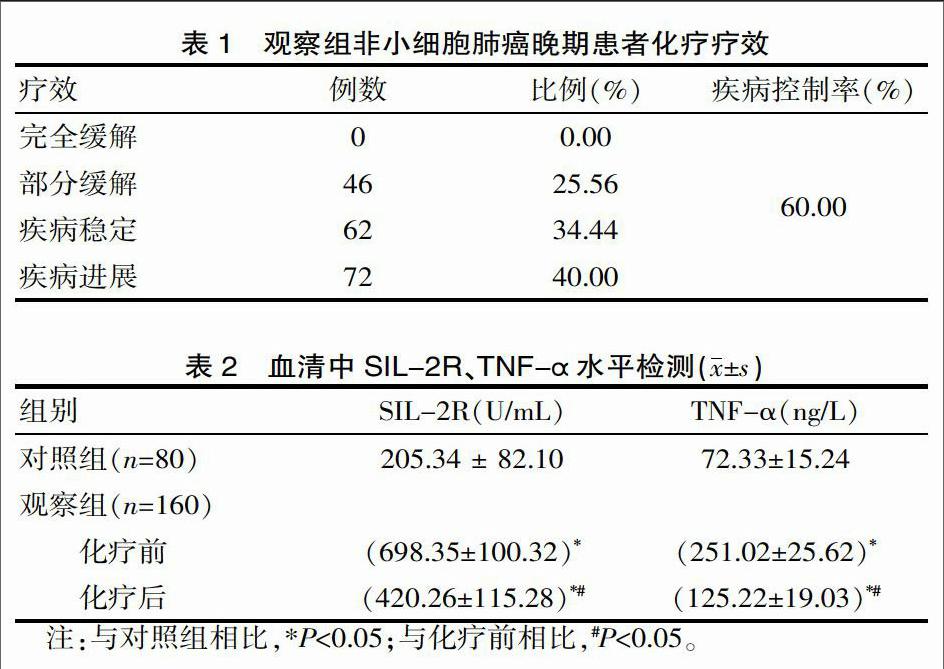
化疗后,观察组完全缓解患者0例(0.00%);部分缓解者46例(25.56%);疾病稳定者62例(34.44%);疾病进展者72例(40.00%)。疾病控制率为60.00%,见表1。
2.2 血清中SIL-2R、TNF-α水平检测
ELISA法检测血清中SIL-2R、TNF-α水平,结果显示,对照组SIL-2R水平显著低于观察组化疗前后,差异有统计学意义(P<0.05);观察组化疗后SIL-2R水平显著低于化疗前,差异有统计学意义(P<0.05)。对照组TNF-α水平显著低于观察组化疗前后(P<0.05);观察组化疗后TNF-α水平显著低于化疗前(P<0.05),见表2。
2.3 血清中SIL-2R、TNF-α水平与化疗疗效的相关性分析
Spearman相关性分析结果显示,观察组SIL-2R、TNF-α水平下降幅度与化疗疗效呈负相关(r=-0.675,r=-0.723;P<0.05)。
3 讨论
肺癌的发病因素主要是环境因素,目前了解得比较多的环境性致肺癌因子有吸烟、电离辐射、大气污染、职业性的致肺癌的化学物质等,但肺癌的确切发病原因和机制尚不完全清楚[5-6]。目前非小细胞肺癌晚期患者标准治疗方案为以铂类为主的联合化疗,对化疗效果正确有效的评价有利于及时调整治疗方案,国内外疗效评价方法主要通过影像手段,但费用高昂且周期长,不能及时有效的反馈结果,耽误最佳调整时期[7-8]。近来有学者发现某些蛋白标记物与肿瘤的发生、发展具有显著相关性[9],因此,该文测定了非小细胞肺癌晚期患者血清中与肿瘤相关的两个重要蛋白标记物SIL-2R、TNF-α,成本低、操作简便、周期短,对恶性肿瘤的诊断、治疗及预后具有重要指导意义。
该研究结果发现,有60%的患者化疗后病情改善;对照组SIL-2R和TNF-α水平显著低于观察组化疗前后;观察组化疗后SIL-2R、TNF-α水平显著低于化疗前,提示,吉西他滨联合顺铂化疗可以显著改善非小细胞肺癌晚期患者病情,抑制肿瘤标志物SIL-2R、TNF-α的分泌,且化疗疗效与SIL-2R、TNF-α水平呈负相关。姜世涛等[10]对吉西他滨联合铂类化疗的58例晚期非小细胞肺癌患者血清SIL-2R、CYFRA21-1及TNF-α水平进行探讨,结果显示,化疗后患者客观缓解率、疾病控制率、无进展生存期均得到改善,且SIL-2R、CYFRA21-1及TNF-α水平下降幅度与疾病控制率呈显著相关,与该文研究结果一致。
综上所述,吉西他滨联合顺铂治疗非小细胞肺癌晚期患者具有显著疗效且与肿瘤标志物SIL-2R、TNF-α具有相关性,但该文中数据为单中心数据,代表性差,尚需多中心样本进一步研究。
[参考文献]
[1] 杨新妹, 徐玉芬, 宋斌斌, 等. 益气化痰方联合化疗对晚期非小细胞肺癌患者临床疗效、不良反应以及生存质量的影响[J]. 中华中医药学刊,2016,34(5):1037-1039.
[2] 李清林. 消癌平注射液联合GP化疗方案治疗晚期非小细胞肺癌临床疗效研究[J]. 中华中医药学刊, 2016, 34(4): 785-787.
[3] 张蕾, 任中海, 薛永飞. 非小细胞肺癌组织中miR-219和环氧合酶-2表达水平联合预测新辅助化疗患者预后的价值分析[J]. 中国地方病防治杂志,2016(3):300-301.
[4] 冯卫能,张良运,石海燕.NRP1表达与晚期非小细胞肺癌一线含铂方案化疗敏感性及预后的相关性分析[J].中国癌症杂志,2016,26(6):514-520.
[5] 李达, 吴素琼,马明越.中药注射液抗肺癌机制及其分子生物标志物[J].中华中医药杂志, 2015,30(7):2437-2440.
[6] 范贤坤,黄永慧.伊立替康加卡铂治疗晚期非小细胞癌临床研究[J].中国卫生产业,2012(6):5-6.
[7] 何海浪, 王谦, 赵阳. 参附注射液联合含铂一线化疗方案endprint
