杂质离子对共晶冷冻结晶过程中冰晶结晶特性的影响*
2017-05-25胡超群沙作良王彦飞杨立斌赵楠楠
胡超群,朱 亮,2,沙作良,王彦飞,杨立斌,赵楠楠
(1.天津科技大学化工与材料学院,天津300457;2.迈安德集团有限公司)
杂质离子对共晶冷冻结晶过程中冰晶结晶特性的影响*
胡超群1,朱 亮1,2,沙作良1,王彦飞1,杨立斌1,赵楠楠1
(1.天津科技大学化工与材料学院,天津300457;2.迈安德集团有限公司)
以硝酸钾水溶液为研究对象,考察了杂质离子对共晶冷冻结晶过程中冰晶结晶特性的影响。首先,建立并验证了共晶冷冻结晶过程冰点的测定方法,并基于Extend-UNIQUAN模型对硝酸钾体系的冰点进行模拟计算。同时考察了不同种类杂质离子对硝酸钾水溶液冰点、结晶点、以及冷冻介稳区宽度的影响,实验研究结果表明:硝酸钾水溶液中离子杂质浓度越高,冰点、结晶点的温度越低,介稳区宽度越宽;杂质离子浓度相同的硝酸钾水溶液其冰点温度随着杂质离子半径减小而减小,结晶点温度和介稳区宽度与阳离子杂质价态成反比,与阴离子杂质价态成正比。并利用基于经典成核理论所推导的介稳区宽度模型方程对实验数据进行模拟计算,模拟结果与实验值符合较好,计算得到硝酸钾水溶液的冰晶成核级数为1.46。
冰晶;介稳区;硝酸钾;共晶冷冻结晶
共晶冷冻结晶是利用冰与水溶液之间的固液相平衡原理,将水以冰晶的形式析出并将其从液相中分离出去,从而获得纯净的冰晶和盐的一种结晶技术。相较于其他的结晶手段,该技术可在低温下操作,气液界面小,此外还具有微生物繁殖、溶质的劣化及挥发性芳香成分损失可控制在极低水平等优点。特别适用于浓缩热敏性液态食品、生物制药、要求保留天然色香味的高档饮品及中药汤剂等。水冻结所需要热量为355 kJ/kg,100℃和0℃时水蒸发所需的热量为2 248 kJ/kg和2 495 kJ/kg,由此可见冷冻结晶消耗的能量约为蒸发法的0.15倍。因此,从理论上讲冷冻结晶是一种节省能量的结晶手段[1-2]。
共晶冷冻结晶已成功应用于废水处理工艺并取得许多进展,其中废水中的杂质离子对体系的冰点、介稳区宽度均有很大影响。冰点是溶液的一个重要属性,对处理废水工艺具有指导意义,介稳区是结晶过程控制的重要环节。在工业结晶的实际操作中,过饱和度通常被控制在介稳区范围内进行,这样能使得到的产品晶形好且粒度均匀。体系介稳区的宽度是选择合适的过饱和度操作条件的重要依据,还是结晶器的设计的关键要素[3]。因此,探究杂质离子对冰点、介稳区宽度的影响具有重要的意义。
笔者以硝酸钾为原料,考察了共晶冷冻结晶过程冰点的测定方法及不同种类的杂质离子对冰点、结晶点、介稳区宽度的影响,从而确定共晶冷冻结晶过程中的一些热力学及动力学参数,该参数可用于共晶冷冻结晶过程中的控制。在实际生产中,可用于改善操作条件、减低成本、提高产品质量。
1 实验部分
1.1 原料和仪器
原料与试剂:硝酸钾、硝酸镁、硝酸铝、氯化钾、硫酸钾,均为分析纯,博欧特(天津)化工贸易有限公司提供;实验用水:去离子水(天津盛腾达化学试剂公司)。
仪器:500 mL结晶器、78-1型数显搅拌器、LAUDA-RP845型循环水浴。冷冻结晶的实验装置见图1。

图1 共晶冷冻结晶的实验装置
1.2 理论分析
1.2.1 硝酸钾水溶液冰点测定原理
冰点是水和冰平衡共存时的温度,在硝酸钾水溶液的冷冻过程中,当温度达到或低于冰点温度时溶液却不结冰的现象称之为过冷现象。处于过冷现象的溶液极不稳定,任一扰动便可触发其结晶。过冷的硝酸钾水溶液突然爆发成核生成冰晶,体系由于发生相变而释放潜热,使溶液的温度回升。回升至某一点时,温度有短暂的平衡,此后溶液温度将继续下降,这段较平稳的温度即为溶液的冰点。
1.2.2 硝酸钾水溶液冰点的计算
根据物理化学的基本原理,溶液的冰点与溶液中溶剂的活度[4]有关:
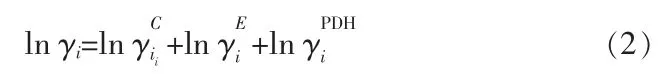
在Extend-UNIQUAC模型中,组分i的活度系数γi由组合项、剩余项及德拜-休克尔项3部分组成,分别反映分子大小和形状、分子间的交互作用及静电作用对γ的贡献。
其中,对于离子态的静电长程作用项[6]为:
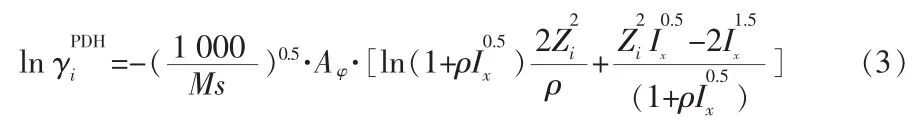
运用Gibbs-Duhem方程,得到溶剂的活度系数:
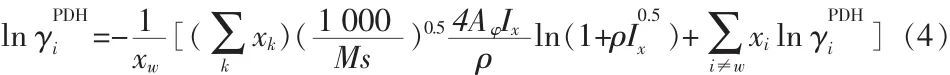
式中,Ms为溶剂的相对分子质量;Aφ为 Debye-Hückel常数;ρ为方法参数;是以物质的量分数为标度的离子强度;Zi为溶质离子的电荷数。其中Aφ、ρ可查文献[7]。
组合项和剩余项分别为:

其中:
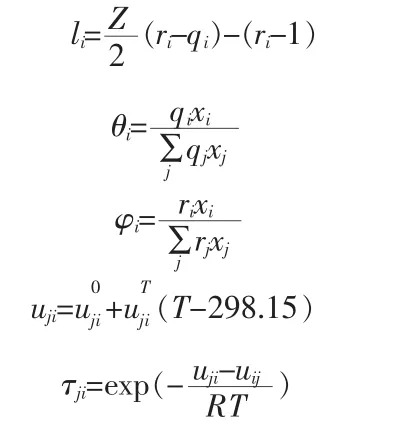
式中,θi和φi是物质i的平均面积分数和体积分数;ri和qi的数值根据分子的vanderWalls体积和表面积算出[8];Z为晶格配位数,其值取10;uij是分子i-j的相互作用能,uij=uji。 由式(2)得出水的活度系数,可由式αi=γixi计算出水的活度,再代入式(1)中即可计算出溶液的冰点。
1.3 实验步骤
1.3.1 硝酸钾水溶液冰点测定过程
开启恒温装置,调至预定温度恒温。向结晶器中加入200.00 g蒸馏水,再加入10.53 g的硝酸钾,在400 r/min的速率下充分搅拌以确保硝酸钾完全溶解,随后先快速将温度降至0℃,再以0.05℃/min的降温速率将溶液从0℃开始冷冻。当溶液开始析出冰时,记录因冰析出释放热量而使溶液温度回升至最高点时的温度,此后用带有滤嘴的注射器抽取上清液,用烘干法计算溶液回升至最高点时硝酸钾的浓度,进而得到在此浓度下硝酸钾溶液的冰点。
1.3.2 硝酸钾水溶液介稳区测定过程
开启恒温装置,调至预定温度恒温。向结晶器中加入200.00 g蒸馏水,再加入10.53 g的硝酸钾,在400 r/min的速率下充分搅拌以确保硝酸钾完全溶解,随后先快速将温度降至0℃,再以0.05℃/min的降温速率将溶液从0℃开始冷冻。当溶液开始析出冰晶时,记录结晶点的温度,重复实验3次,记录实验数据。
2 结果与讨论
2.1 硝酸钾水溶液冰点的测定结果与分析
实验考察了硝酸钾水溶液冰点的测定方法,将实验测定的冰点数据与文献提出的数据通过Extend-UNIQUAN模型对比,以确定测定冰点的方法是否可行。
图2为质量分数为5%的硝酸钾溶液冷冻结晶过程中温度随时间变化的曲线。由图2可见,当温度降至结晶点温度-5.61℃时,溶液中开始有冰晶析出,由于冰析出释放热量使溶液的温度回升至-1.45℃,在此温度下维持短暂的恒定后继续下降,得到平衡点时硝酸钾的质量分数为5.44%(表1);配制质量分数为5.44%的硝酸钾溶液,将温度恒定至-1.45℃时,水和冰平衡共存,溶液浓度恒定不变,通过验证得出5.44%硝酸钾溶液的冰点为-1.45℃,与文献[9]中5.0%的硝酸钾溶液的冰点-1.4℃几乎一致(见表2),由此可认为该冰点测定方法是可行的。
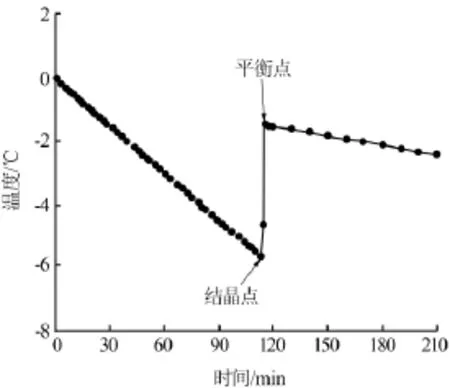
图2 5.0%的硝酸钾水溶液共晶冷冻结晶过程中温度随时间变化曲线

表1 KNO3-H2O体系相平衡和介稳区数据
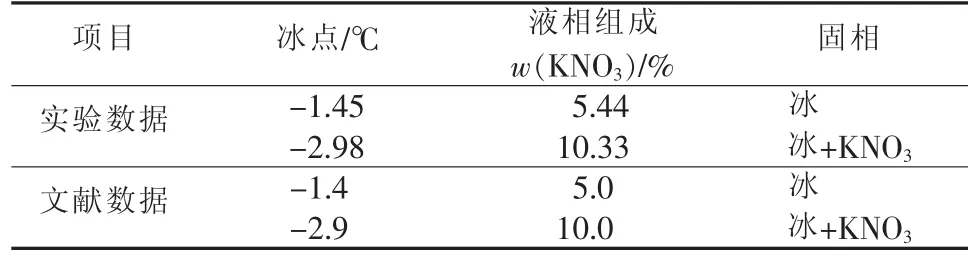
表2 KNO3-H2O体系冰点的实验值与文献值的对比
运用上述测定冰点的方法,得到不同质量分数(w)的硝酸钾水溶液的冰点(T),并将其与Extend-UNIQUAN模型计算出硝酸钾溶液的冰点对比,结果见图3。由图3可见,运用Extend-UNIQUAN模型计算得到的冰点值与本研究提出的测定冰点方法得到的冰点值基本一致,进一步验证了测定方法的可行性。将冰点温度与浓度数据经二次多项式拟合得到T=-209.376 4w2+0.808 0w-0.801 1,R2=0.991 5。
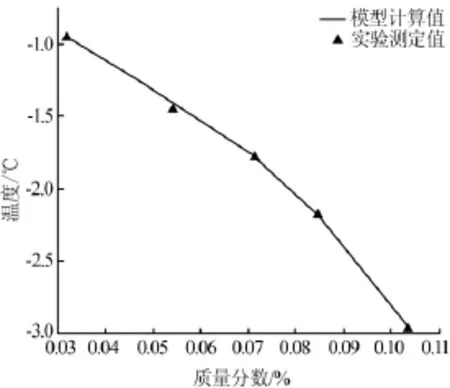
图3 硝酸钾水溶液冰点模型计算值与实验值对比
2.2 含不同杂质离子的硝酸钾水溶液冰点的测定结果与分析
为考察不同杂质离子对硝酸钾水溶液的冰点温度的影响,先配制质量分数为5.44%的硝酸钾溶液,向溶液中添加不同浓度的Na+、Mg2+、Al3+等作为阳离子杂质和不同浓度的Cl-、SO42-等作为阴离子杂质,设定搅拌速率为400 r/min,确定溶液充分混合后,以0.05℃/min的降温速率将溶液从0℃开始冷冻,在冷冻结晶过程中记录冰点温度,同时利用Extend-UNIQUAN模型对体系的冰点进行计算预测,结果见图4。由图4结果可知,运用Extend-UNIQUAN模型计算的冰点值的平均相对偏差为5%左右,在低浓度时其计算值与实验值更符合,高浓度时偏差略大。从图4还可见,同种离子的浓度越高,溶液的冰点温度越低;离子半径越小,冰点温度越低。因为水合效应对离子半径较小、电荷较高的溶液体系影响更大,因离子半径r(Al3+)<r(Mg2+)<r(Na+)<r(Cl-)<r(SO42-),所以在掺杂的离子杂质中,掺加Al3+的硝酸钾水溶液的冰点值最低。
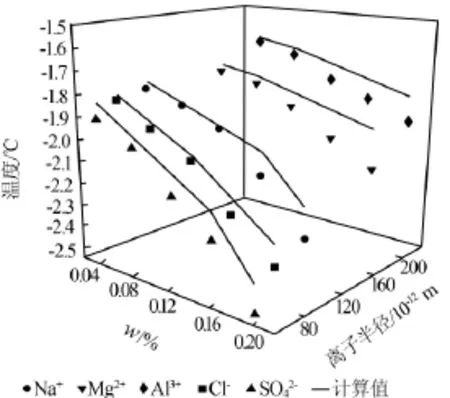
图4 含不同离子杂质的5.44%硝酸钾水溶液冰点模型计算值与实验值对比曲线
将硝酸钾水溶液的冰点温度分别与杂质离子的浓度数据经二次多项式拟合得到通式:
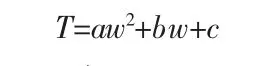
式中,参数a、b和c见表3。
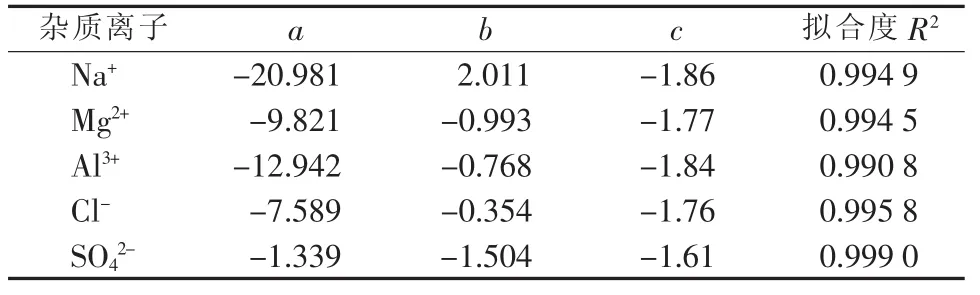
表3 含不同离子杂质的5.44%硝酸钾溶液冰点方程参数表
2.3 含不同杂质离子的硝酸钾水溶液结晶点的测定结果与分析
为考察不同杂质离子对硝酸钾水溶液结晶点温度的影响,先配制质量分数为5.44%的硝酸钾溶液,向溶液中添加不同浓度的杂质离子(Na+、Mg2+、Al3+、Cl-、SO42-),设定搅拌速率为400 r/min,待溶液充分混合后,以0.05℃/min的降温速率将溶液从0℃开始冷冻,在冷冻结晶过程中记录冰点温度,结果见图5。
将硝酸钾水溶液的结晶点温度分别与杂质离子的浓度数据经二次多项式拟合得到通式:
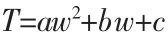
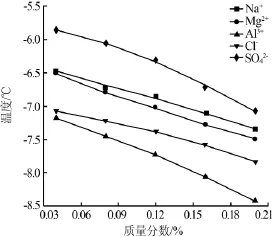
图5 不同离子杂质对5.44%硝酸钾水溶液结晶点温度的影响
式中,参数a、b和c见表4。
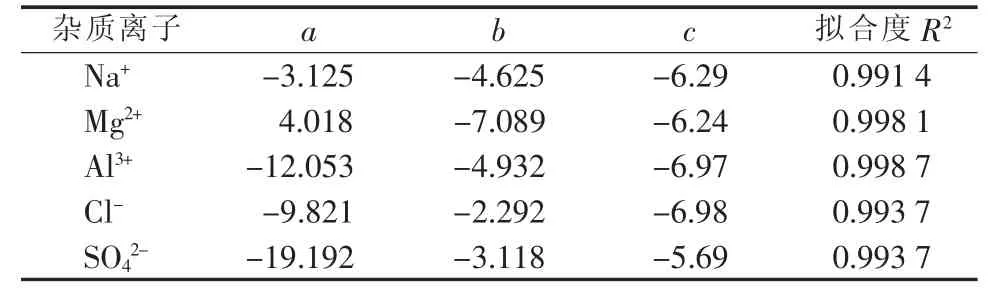
表4 含不同离子杂质的5.44%硝酸钾溶液结晶点方程参数表
从图5和表4可以看出,同种离子浓度越高,溶液的结晶点温度越低;阳离子杂质价态越高,溶液的结晶点温度越低,阴离子杂质价态越低,溶液的结晶点温度越低。
2.4 硝酸钾水溶液的介稳区测定结果与分析
2.4.1 降温速率对硝酸钾水溶液介稳区宽度的影响
为考察不同降温速率对硝酸钾水溶液介稳区宽度的影响,实验在测量介稳区时保持一定的浓度、降温速率(0.05℃/min)等条件,实验结果见图6。
根据经典成核理论和J.Nyvlt[10]的实验结果,当搅拌速率一定时:

式中:b为降温速率,℃/h;m为成核级数;k为成核速率常数;ΔTmax为介稳区宽度,℃。
将ln b与ln(ΔTmax)作图可得一条直线,直线的斜率为成核级数m的倒数。采用式(7)对不同降温速率下硝酸钾水溶液的介稳区宽度进行关联,得到不同冰点下的模型方程,结果见表5。
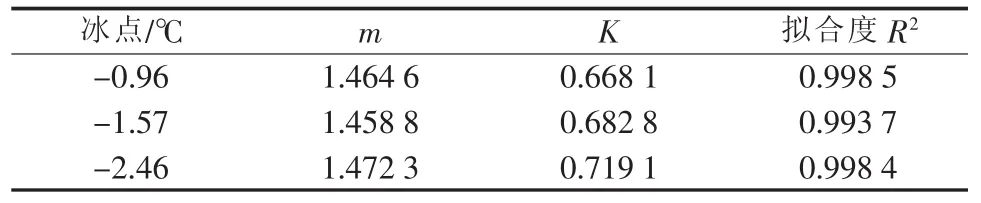
表5 不同冰点的介稳区宽度模型参数
由表5可见,成核级数m值变化不大,说明硝酸钾水溶液结晶与冰点温度基本无关,取平均值m= 1.46。选择上述3组模型方程的计算数据与实验值作对比,结果见图6。从图6可见,模型方程的计算值与实验值十分接近,符合经典成核理论,即随着降温速率的增大,介稳区宽度增大。
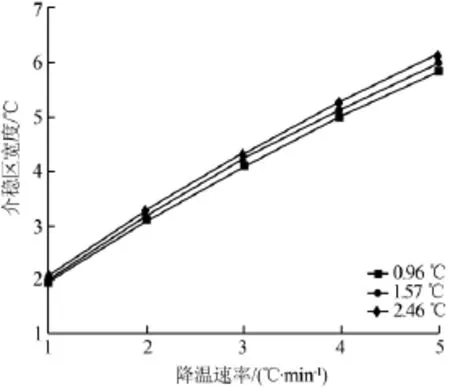
图6 不同降温速率下介稳区宽度模型方程计算值与实验值对比曲线
2.4.2 不同杂质离子对硝酸钾水溶液介稳区宽度的影响
介稳区宽度与搅拌速率、降温速率、温度及测定方法等因素息息相关。实验在测量介稳区时,选择质量分数为5.44%、搅拌速率为400 r/min、降温速率为0.05℃/min。在此条件下,考察了含有不同杂质离子的硝酸钾溶液的介稳区宽度(ΔT),为工艺实验提供了热力学数据,实验结果见图7。
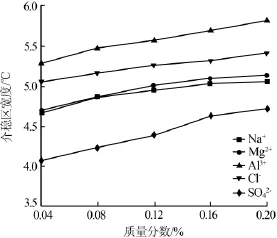
图7 不同离子杂质对5.44%硝酸钾溶液介稳区宽度的影响
从图7可以看出,若硝酸钾溶液中掺杂杂质则溶液的介稳区宽度会增大,同时从图7中可以看出离子杂质浓度越高,溶液的介稳宽度越宽;阳离子价态越高,溶液介稳区宽度越宽,阴离子杂质价态越低,溶液介稳区宽度越宽。
3 结论
通过对硝酸钾溶液冷冻结晶过程进行较为系统的研究,得到结论:1)将通过实验建立的测定冰点的方法测得的冰点值,分别与文献值和 Extend-UNIQUAC模型计算值作对比,结果表明测定冰点方法是可行的。2)溶液中同种离子杂质的浓度越高,其冰点温度越低,不同离子杂质条件下,离子半径越小,冰点温度越低。3)溶液中阳离子杂质的价态越高,其结冰点温度越低,介稳区宽度越宽;反之阴离子杂质价态越低,冰点和结冰点温度越低,介稳区宽度越宽。4)用经典成核理论推导了介稳区宽度的模型方程,结果与实验值符合较好,成核级数m为1.46。
[1] 李亚,孙潇,孙卫东.冷冻浓缩技术的应用及研究进展[J].食品与生物,2008(3):9-10,16.
[2] 谢绍雷,张超,纪律,等.硫酸镁亚型盐田卤水低温冷冻结晶规律的研究[J]无机盐工业,2015,47(2):35-38.
[3] Reddy ST,LewisAE,Witkamp GJ,etal.RecoveryofNa2SO4·10H2O from a reverse osmosis retentate by eutectic freeze crystallisation technology[J].Chemical Engineering Research and Design,2010,88(9):1153-1157.
[4] Lee LS,Sun SL,Lin C L.Predictionsof thermodynamic properties ofaqueous single-electrolyte solutionswith the two-ionic-parameter activity coefficientmodel[J].Fluid Phase Equilibria,2008,264(1/ 2):45-54.
[5] AliHaghtalab,Kiana Peyvandi.Generalized electrolyte-UNIQUACNRFmodel for calculation ofsolubility and vapor pressureofmulticomponent electrolytes solutions[J].Journal of Molecular Liquids,2012,165:101-112.
[6] AliHaghtalab,Kiana Peyvandi.Electrolyte-UNIQUAC-NRFmodel for the correlation of the mean activity coefficient of electrolyte solutions[J].Fluid Phase Equilibria,2009,281(2):163-171.
[7] Zhao E S,Yu M,SauvéR E,et al.Extension of theWilsonmodel to electrolyte solutions[J].Fluid Phase Equilibria,2000,173(2):161-175.
[8] Garcia A V,Thomsen K,Stenby E H.Prediction ofmineral scale formation in geothermaland oilfield operationsusing the Extended UNIQUACmodel.PartⅡ.Carbonate-scalingminerals[J].Geothermics,2006,35(3):239-284.
[9] 邓天龙,周桓,陈侠.水盐体系相图原理及其应用[M].北京:化学工业出版社,2013.
[10] Nyvlt J.Kinetics of nucleation in solutions[J].Journal of Crystal Growth,1968,3/4:377-383.
Effectof impurity ionson crystallization propertiesof ice crystals in eutectic freeze crystallization process
Hu Chaoqun1,Zhu Liang1,2,Sha Zuoliang1,Wang Yanfei1,Yang Libin1,Zhao Nannan1
(1.College ofChemical Engineering and MaterialsScience,Tianjin University of Science&Technology,Tianjin 300457,China;2.Myande Group Limited)
The effectof impurity ions in potassium nitrate solution on the crystallization properties of ice crystals during the eutectic freeze crystallization was investigated.At first,the determination method of freezing point was developed and verified,and the freezing point predicted modelwas developed based on Extend-UNIQUANmodel.With the determination method of freezing point,the influence of impurities ionson the freezing point,crystallization point,andmetastablewidth was investigated.Results showed that the higher concentrations of impurities in potassium nitrate aqueous solution,the lower temperatureof freezingpointand crystallization pointand thewiderofmetastable zone.However,given the same concentrations of different impurity ions in potassium nitrate aqueous solutions,the temperature of freezing pointwas inversely proportional to the radius of ions.In addition,the temperature of crystallization point decreased with increase in valence of cations and decreased in valence of anions,aswell as the width ofmetastable zone.The simulationmodel ofmetastable zone width was derived by means of the classical nucleation theory.The calculated results were in good agreement with the experimental data,and the nucleation orderof ice crystal in potassium nitrate aqueous solutionswasestimated to be 1.46.
ice crystal;metastable zone;potassium nitrate;eutectic freeze crystallization
TQ131.13
A
1006-4990(2017)05-0025-05
2016-11-22
胡超群(1993— ),女,硕士研究生,主要研究方向为工业结晶。
朱亮
天津市应用基础与前沿技术研究计划(重点项目)(14JCZDJC40900)。
联系方式:zhuliang@tust.edu.cn
