定性和定量分析磺胺氯吡嗪钠可溶性粉中的未知添加物
2017-05-11包爱情陈慧华陆春波陈晓林林仙军
包爱情, 陈慧华, 陆春波, 周 炜, 王 彬, 陈晓林, 林仙军
(浙江省兽药饲料监察所, 浙江 杭州 311101)
研究论文
定性和定量分析磺胺氯吡嗪钠可溶性粉中的未知添加物
包爱情*, 陈慧华, 陆春波, 周 炜, 王 彬, 陈晓林, 林仙军
(浙江省兽药饲料监察所, 浙江 杭州 311101)
定性和定量分析了一批兽药磺胺氯吡嗪钠可溶性粉中的未知添加物。使用电位滴定法对该批磺胺氯吡嗪钠可溶性粉进行含量测定,发现滴定异常,根据标准进行的两项鉴别有一项不合格,因此怀疑添加了其他化合物。采用超高效液相色谱-四极杆-飞行时间质谱(UHPLC-Q/TOF MS)对该批样品进行筛查,发现疑似添加物,并使用高效液相色谱-二极管阵列检测(HPLC-DAD)法进行了双重确证和含量测定。该批样品中非法添加物为乙酰甲喹和磺胺二甲嘧啶,添加量分别为40.3和16.4 mg/g。通过总结该批样品非法添加物的发现、确证和含量测定的整个过程,得出一种较好的筛查未知物的模式,为兽药处方外非法添加筛查提供可借鉴的思路。
超高效液相色谱-四极杆-飞行时间质谱;液相色谱-二极管阵列检测;磺胺氯吡嗪钠;乙酰甲喹;磺胺二甲嘧啶;兽药;非法添加
近年来,随着国家对食品安全越来越重视,对食品中非法添加化合物的打击力度也逐年加大,畜产品作为人类饮食中重要的组成,其安全至关重要,打击兽用药品处方外非法添加是保证畜产品安全的重要手段。当前药品食品类非法添加的筛查方法主要为液相色谱-二极管阵列检测(HPLC-DAD)法[1-3]、气相色谱(GC)法[4]和高效液相色谱-质谱(HPLC-MS)法[5-9]。HPLC-DAD法简便快速、成本相对较低、应用范围较广,农业部颁布的兽药非法添加化学药物检查方法的公告中涉及的大多为该法。但HPLC-DAD法依赖于化学药物光谱图库,而对于库外的化合物缺少有效的指引,对没有紫外吸收的化合物缺少定性分析的能力,对复杂样品也难以避免本底干扰。HPLC-MS法具有灵敏度高、提供信息量更为丰富等特点,是打击兽药非法添加的重要工具。但由于其成本昂贵,对操作人员要求较高,且因灵敏度较高导致处理复杂样品如中兽药制剂时易发生交叉污染,目前应用相对较少。相对于低分辨质谱,高分辨质谱在未知物筛查和确证中的应用更为广阔[10-17]。当前兽药非法添加物的定量检测主要依赖HPLC-DAD法[2,4,18]和高效液相色谱-三重四极杆质谱(HPLC-QqQ-MS)法[19,20]。
高分辨质谱对非法添加化合物的筛查确证能力往往取决于化合物质谱库的大小,质谱库中包含的化合物越全面,未知物筛查工作就越高效。多种手段结合使用,如高分辨质谱结合HPLC-DAD共同确证未知化合物可以大大提高定性检测未知物的能力[12,13,21]。
近日,在一批抽检兽药样品磺胺氯吡嗪钠可溶性粉中的处方外非法添加物筛查中,发现未知添加物。通过超高效液相色谱-四极杆-飞行时间质谱(UHPLC-Q/TOF MS)对该批样品进行筛查,发现疑似添加物,使用HPLC-DAD法进行了双重确证和含量测定。本文通过实际样品检测中发现的异常,提出存在未知添加物的怀疑,推断确证添加物,最后定量测定添加物,总结出一种兽药中未知物筛查较好的模式,为兽药处方外非法添加筛查提供可以借鉴的思路,针对当前相对不够规范的兽药行业,本文的研究具有较好的实际应用价值。
1 实验部分
1.1 仪器、试剂与材料
Agilent 1290-6550 UHPLC-Q/TOF MS配安捷伦双喷射流电喷雾离子(Dual AJS ESI)源,MassHunter工作站、定性分析软件和MassHunter Workstation Personal Compound Database and Library (PCDL)个人谱图数据库软件(美国Agilent公司);十八烷基键合硅胶色谱柱(150 mm×3.0 mm,3 μm,美国Waters公司);十八烷基键合硅胶色谱柱(250 mm×4.6 mm, 5 μm,美国Agilent公司);超纯水机(美国Millipore公司); XS205电子天平、T50滴定仪(瑞士Mettler Toledo公司); KQ-500E超声仪(昆山市超声仪有限公司)。
乙酰甲喹对照品(纯度99.6%,批号H011108)、磺胺二甲嘧啶(纯度99.8%,批号H0371008)购于中国兽医药品监察所;磺胺氯吡嗪钠对照品(纯度99.0%,批号21024)购于德国Dr. Ehrenstorfer公司。磺胺氯吡嗪钠可溶性粉(规格30 g∶100 g;批号20151201)及其他合格兽药样品为浙江省内抽检及委托样品。
甲醇(色谱纯,美国Merck公司);甲酸(色谱纯,美国ACS恩科化学公司);乙酸铵(分析纯,西陇化工股份有限公司);磷酸(分析纯,上海凌峰化学试剂有限公司)。其他试剂均为国产分析纯。
1.2 实验条件
1.2.1 UHPLC-Q/TOF MS条件
采用十八烷基键合硅胶色谱柱(150 mm×3.0 mm, 3 μm);柱温为25 ℃;进样量为2 μL。流动相A为含5 mmol/L乙酸铵的0.1%(体积分数)甲酸水溶液,流动相B为含5 mmol/L乙酸铵的0.1%(体积分数)甲酸甲醇溶液;流速为0.5 mL/min。梯度洗脱程序:0~1 min, 5%B; 1~4 min, 5%B~60%B; 4~14 min, 60%B~100%B; 14~18 min, 100%B,后运行3 min。质谱采用Dual AJS ESI源;扫描方式为电喷雾正离子(ESI+)全扫描;毛细管电压为4.0 kV;碰撞电压(Fragmentor)为350 V;干燥气流速为15 L/min,温度为350 ℃;鞘气流速为12 L/min,温度为350 ℃。一级质谱数据采集为单级质谱全扫描模式,扫描范围为m/z100~1 000;采集速率为1.5 spectra/s。二级质谱数据采集为targeted MS/MS模式,扫描范围为m/z50~1 000;采集速率为2.5 spectra/s;碰撞能量为10、20和40 eV。采集数据时连续导入参比溶液,对仪器质量轴进行实时校正,参比离子为m/z121.050 9和922.009 8。
1.2.2 HPLC-DAD条件
采用十八烷基键合硅胶色谱柱(250 mm×4.6 mm, 5 μm);进样量为20 μL;流动相A为0.2%(体积分数)磷酸溶液,流动相B为甲醇,流速为1.0 mL/min。梯度洗脱程序:0~2.0 min, 2%B; 2.0~25.0 min, 2%B~100%B; 25.0~28.0 min, 100%B; 28.0~28.1 min, 100%B~2%B; 28.1~31.0 min, 2%B。扫描波长为210~400 nm,记录250 nm波长处的谱图。
1.3 溶液的制备
1.3.1 供试品溶液的制备
精密称取1 g磺胺氯吡嗪钠可溶性粉,加入80 mL 50%(体积分数,下同)甲醇,超声5 min,冷却至室温,置于100 mL量瓶中,用50%甲醇稀释至100 mL,摇匀。精密量取5 mL上述溶液置于50 mL容量瓶中,用50%甲醇定容,作为HPLC-DAD确证溶液。精密量取上述溶液5 mL置于50 mL容量瓶中,用50%甲醇定容,作为UHPLC-Q/TOF MS筛查和确证溶液。
1.3.2 对照品溶液的制备
分别取适量磺胺二甲嘧啶、乙酰甲喹、磺胺氯吡嗪钠对照品,用50%甲醇溶解并稀释成10 mg/L的溶液,供HPLC-DAD验证用。用50%甲醇稀释成100 μg/L的溶液,供UHPLC-Q/TOF MS确证用。

图 1 (a)某实际样品和(b)合格样品的滴定曲线Fig. 1 Titration curves of (a) a real sample and (b) a qualified sample
2 结果与讨论
2.1 未知物的发现和初步分析
参照《中国兽药典》[22]用电位滴定法对该批磺胺氯吡嗪钠可溶性粉样品进行含量检测时,无法滴定至终点,且与合格样品的滴定曲线差异甚大(见图1)。进行两项鉴别时,芳香第一胺类试验鉴别合格,但薄层色谱鉴别中对照品溶液与供试品溶液的斑点位置和颜色有极微小差别,鉴别不合格。推测样品中含其他磺胺类药物,也可能含有其他非法添加物。
2.2 未知物的推断
使用UHPLC-Q/TOF MS对该批样品进行一级质谱数据采集,图2a为总离子流色谱图(TIC),在5.366和5.668 min有2个明显的峰,对峰1和峰2分别进行质谱提取,检测到在m/z279.090 7和219.076 5两处响应明显更强(见图2b和图2c)。因鉴别试验中有芳香第一胺类反应,样品中含有磺胺类药物的概率较大。首先在磺胺类药物PCDL库中进行匹配;发现磺胺二甲嘧啶和磺胺二甲异嘧啶的[M+H]+与m/z279.090 7匹配,两者的分子式均为C12H14N4O2S,但磺胺二甲异嘧啶的出峰时间为4.771 min,与供试品不匹配,而磺胺二甲嘧啶出峰时间为5.334 min,与供试品匹配,推测该化合物为磺胺二甲嘧啶。另一个离子在已经建立的一级数据库中进行匹配,发现乙酰甲喹的[M+H]+与m/z219.076 5匹配,且保留时间一致,匹配分数为98.26,推测该化合物为乙酰甲喹。
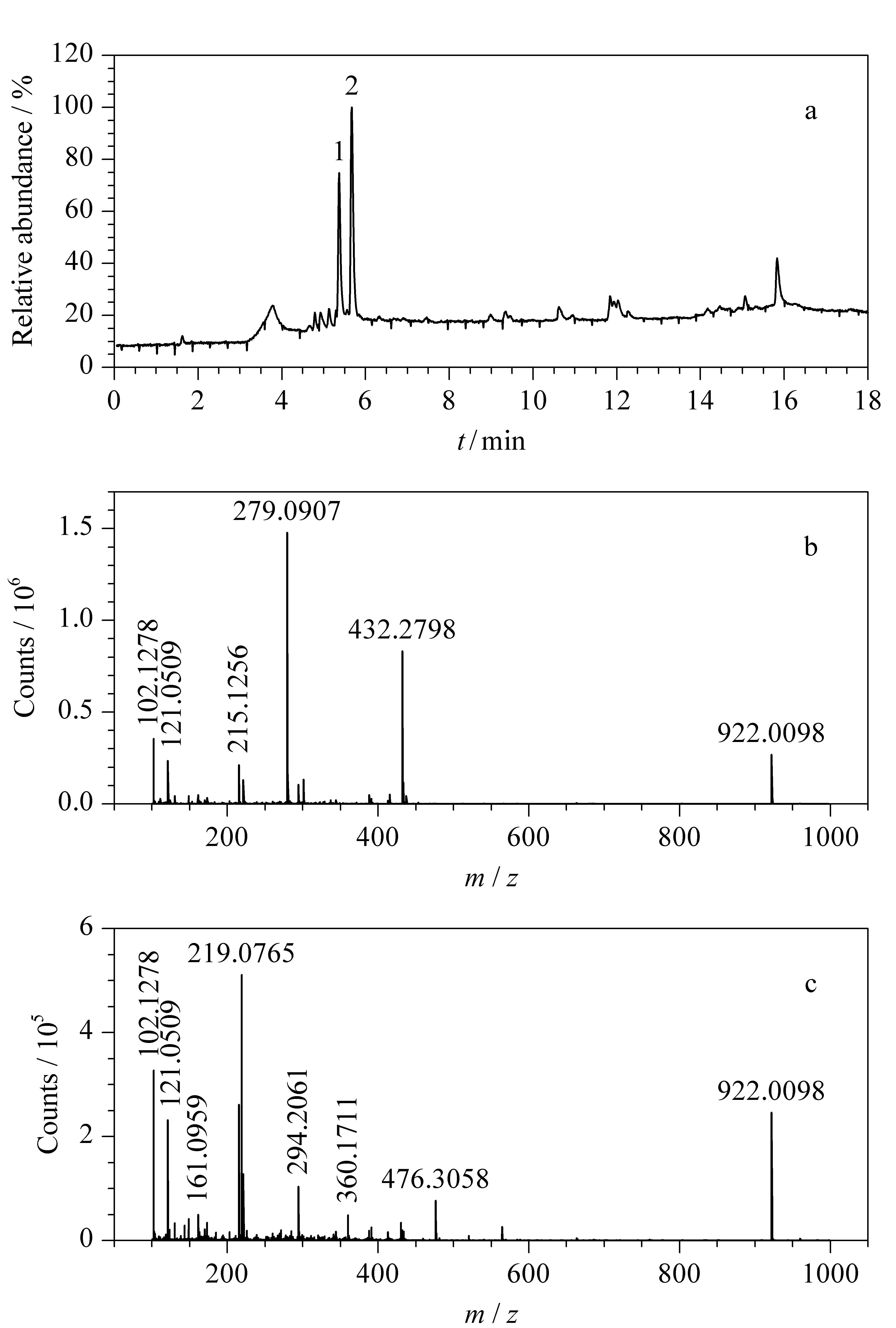
图 2 (a)样品总离子流色谱图及(b)峰1和(c)峰2的质谱提取图Fig. 2 (a) Total ion chromatogram of the sample and mass spectra extracted from (b) peak 1 and (c) peak 2

图 3 磺胺氯吡嗪钠可溶性粉中疑似化合物的二级质谱图Fig. 3 MS/MS spectra of the suspected compounds in sulfachlorpyrazine sodium soluble powder
2.3 未知物的确证
2.3.1 UHPLC-Q/TOF MS确证
图3为将供试品溶液按照1.2.1节条件分别以m/z279.091 0和219.076 4(磺胺二甲嘧啶和乙酰甲喹的精确[M+H]+)为母离子进行二级质谱采集的谱图。另取磺胺二甲嘧啶和乙酰甲喹对照品溶液(100 μg/L)在相同的条件下采集二级质谱。对照品图谱与供试品图谱几乎完全一致,匹配值高达99.26和99.58,表明非法添加的化合物为磺胺二甲嘧啶和乙酰甲喹。
2.3.2 HPLC-DAD确证
在液相保留时间和紫外光谱两方面将样品与对照品进行比对。通过不同浓度本底添加峰纯度检查和光谱相似度检查对样品中的未知物进行确证。
样品在该试验条件下检出2个较大的未知色谱峰,与该条件下乙酰甲喹和磺胺二甲嘧啶对照品的保留时间一致,紫外光谱相似;同时发现该批样品中未检出标示的磺胺氯吡嗪钠(见图4)。不同浓度(取与供试品溶液峰面积相当的对照品溶液与之混合,对照品溶液与供试品溶液按体积比1∶4、1∶1和4∶1混合)的本底添加试验峰纯度检查结果显示:添加前后,样品色谱图相应位置上的色谱峰纯度值大于纯度阈值,为单一物质峰。光谱相似度检查结果显示:添加前后,样品色谱图相应位置上色谱峰的光谱匹配度高于匹配阈值,与对照品的光谱相似。验证结果及峰纯度检查、光谱相似度检查结果见表1。
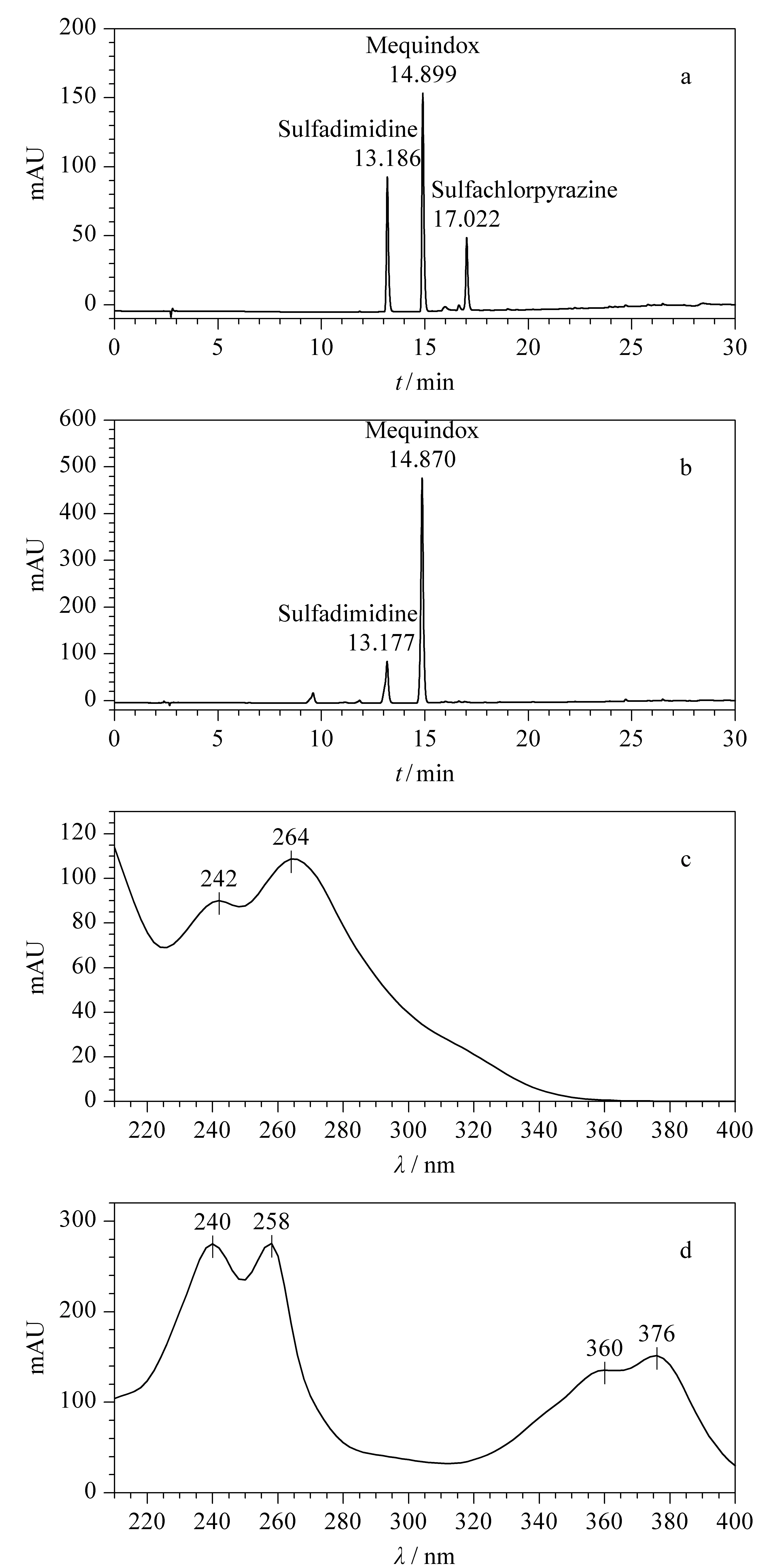
图 4 (a)混合对照品溶液(10 mg/L)和(b)样品色谱图及(c)磺胺二甲嘧啶和(d)乙酰甲喹光谱图Fig. 4 Chromatograms of (a) the mixed reference substances (10 mg/L) and (b) the sample, and spectrograms of (c) sulfadimidine and (d) mequindox
2.4 含量测定
经上述UHPLC-Q/TOF MS和HPLC-DAD双重验证,确证供试品中含有乙酰甲喹和磺胺二甲嘧啶,这两种非法添加物在农业部2448号公告[23]中均已涉及。公告中氟喹诺酮类制剂中非法添加乙酰甲喹、喹乙醇等化学药物的检查方法和氟苯尼考制剂中非法添加磺胺二甲嘧啶、磺胺间甲氧嘧啶的检查方法用于其他制剂检查时,需进行空白试验。按照此公告方法进行试验,供试品中乙酰甲喹和磺胺二甲嘧啶含量分别为40.3和16.4 mg/g。
2.5 电位滴定异常的分析
样品中虽未检出磺胺氯吡嗪钠,但检出了磺胺二甲嘧啶,且含量达16.4 mg/g,应有突跃,调看自动滴定方法发现设置了5 mL的预滴定(合格样品滴定终点一般都在12~20 mL之间,为了更加高效地完成滴定大批量检测工作,设置预滴定有其合理性)。将预滴定取消后,按照标准取样1.60 g,滴定终点出现在0.88 mL。为了避免误判,取样15.00 g,按同法操作,滴定终点出现在8.20 mL,线性良好,表明之前无法滴定至终点实际上是由于预滴定已经过了滴定终点。

表 1 峰纯度检查与光谱相似度检查的结果
DAD: diode array detection.
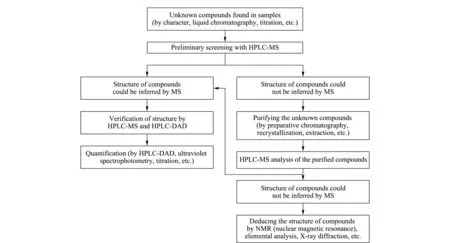
图 5 兽药中未知化合物检测的模式化路线图Fig. 5 Model route of inspection of unknown compounds adulterated in veterinary drugs
2.6 对非法添加物的思考
经UHPLC-Q/TOF MS和HPLC-DAD双重验证,发现样品中未检出磺胺氯吡嗪钠而检出处方外的磺胺二甲嘧啶和乙酰甲喹。添加乙酰甲喹可以为不法企业“增强”药物效果,从而达到“多病同治”的效果,但标示为磺胺氯吡嗪钠可溶性粉,却未检出磺胺氯吡嗪钠,反而检出磺胺二甲嘧啶,令人深思。经深入调研,发现磺胺二甲嘧啶原料粉的价格在50到70元/kg而其他磺胺类药物普遍在100元/kg以上,但磺胺二甲嘧啶的疗效却不比其他磺胺类药物差,因此不法企业用磺胺二甲嘧啶来替代其他磺胺类药物来降低成本。而《中国兽药典》[24]中收载的磺胺类药物,除复方磺胺甲噁唑、复方磺胺氯达嗪粉和磺胺嘧啶片使用液相色谱方法定量外,其余均使用滴定作为定量检测的方法,这就为企业造假提供了一定的法律漏洞。按照现行标准检测,磺胺二甲嘧啶可以在鉴别中显芳香第一胺类鉴别,电位滴定时无法与其他磺胺类药物区分,且薄层色谱区别非常微小,因此企业使用磺胺二甲嘧啶替代其他磺胺类药物,有较大概率蒙混过关。目前本单位在磺胺类药物非法添加筛查中亦发现其他磺胺制剂添加磺胺二甲嘧啶的情况,推断应为相同的目的。
2.7 非法添加物的筛查模式
图5为总结上述推导与验证过程,参照文献[12],将兽药中添加未知化合物检测模式化的路线图。可疑样品先通过HPLC-MS初筛,若能顺利发现并确证未知物,则使用HPLC-MS和HPLC-DAD进行双重验证,并开发定量方法进行定量。若HPLC-MS初筛未能确定化合物,则对样品进行净化减少基质干扰,净化后的样品若可被HPLC-MS确证则同上操作,反之则需要借助其他手段共同确证。
3 结论
当前兽药行业不够规范,处方外非法添加的现象时有发生,因此要大力加强对处方外非法添加的打击才能保证兽用药的安全。标准的滞后也让不法分子有了更多的可乘之机,本文发现使用磺胺二甲嘧啶替代磺胺氯吡嗪钠时,除薄层鉴别有极微小区别,其余项目均可符合要求,因此在磺胺类药物标准中很有必要增加紫外光谱扫描和液相色谱方法测定含量和有关物质。本文发现了一批样品的非法添加物,建立了UHPLC-Q/TOF MS筛查确证和HPLC-DAD双重确证,进行了含量测定,最后总结出一种较好的模式化筛查流程,为未来兽药处方外非法添加提供了思路,对打击兽药处方外添加有较好的实际应用价值。
[1] Enríquez-Gabeiras L, Gallego A, Garcinuo R M, et al. Food Chem, 2012, 135: 193
[2] Dong L L, Fan Q. Chinese Journal of Veterinary Drug, 2016, 50(8): 19
董玲玲, 范强. 中国兽药杂志, 2016, 50(8): 19
[3] Han D Q, Lu Y, Yin G, et al. Chinese Traditional Patent Medicine, 2015, 37(10): 2197
韩东岐, 鲁艺, 殷果, 等. 中成药, 2015, 37(10): 2197
[4] Zhang L H, Zhou J, Wang M. Chemical Reagents, 2015, 37(5): 433
张立华, 周剑, 王敏. 化学试剂, 2015, 37(5): 433
[5] Wang Z, Wu C S, Wang G L, et al. J Sep Sci, 2015, 38(6): 925
[7] Pang W S, Yang H W, Wu Z S, et al. Chromatographia, 2009, 70(10): 1353
[8] Kim J Y, Choi J Y, Yoon C Y, et al. J Korean Soc Appl Biol Chem, 2015, 58(1): 137
[9] Hu J L, Zeng L, He L, et al. J Chromatogr Sci, 2016, 54(5): 847
[10] Zhang Q T, Tu Z C, Wang H, et al. Food Chem, 2015, 170: 160
[11] Li Y B, Zhang Z Z, Hou Z G, et al. RSC Adv, 2015, 5: 202
[12] Han N N, Bi Y F, Liu S W, et al. Chinese Journal of Pharmaceutical Analysis, 2016, 36(2): 306
韩宁宁, 毕言锋, 刘少伟, 等. 药物分析杂志, 2016, 36(2): 306
[13] Li S Y, Wang Y, Zhou F, et al. Chinese Journal of Chromatography, 2015, 33(12): 1251
李诗言, 王扬, 周凡, 等, 色谱, 2015, 33(12): 1251
[14] Sivagnanam K, Komatsu E, Rampitsch C, et al. J Sci Food Agric, 2016, 97(1): 357
[15] Shan S M, Luo J G, Pan K, et al. Biomed Chromatogr, 2016, 30(11): 1861
[16] Zhang M M, Zhao H Q, Zhao Z G, et al. J Sep Sci, 2016, 39(11): 2097
[17] Li Y, Zhou G S, Peng Y, et al. J Pharm Biomed Anal, 2016, 118: 167
[18] Luo C J, Lu C B, Lin X J, et al. Chinese Journal of Veterinary Drug, 2015, 49(4): 24
罗成江, 陆春波, 林仙军, 等. 中国兽药杂志, 2015, 49(4): 24
[19] Liu X H, Zhang X Q, Qiao Y, et al. Chinese Journal of Veterinary Drug, 2015, 49(1): 41
刘雪红, 张秀芹, 乔颖, 等. 中国兽药杂志, 2015, 49(1): 41
[20] Wang X L, Guo T, Wang S S, et al. Journal of Instrumental Analysis, 2015, 34(1): 119
王晓利, 郭涛, 王珊珊, 等. 分析测试学报, 2015, 34(1): 119
[21] Dong L L, Cao Y, Yu X H, et al. Chinese Journal of Veterinary Drug, 2016, 50(8): 15
董玲玲, 曹莹, 于晓辉, 等. 中国兽药杂志, 2016, 50(8): 15
[22] Commission of Chinese Veterinary Pharmacopoeia. Pharmacopoeia of People’s Republic of China, Part 1. Beijing: China Agriculture Press, 2010: 394
中国兽药典委员会. 中华人民共和国兽药典, 一部. 北京: 中国农业出版社, 2010: 394
[23] Ministry of Agriculture. No. 2448 Bulletin of the Ministry of Agriculture of the People’s Republic of China. (2016-09-19) [2016-12-01]. http://www.moa.gov.cn/govpublic/SYJ/201609/t20160922_5282118.htm
农业部. 中华人民共和国农业部公告2448号. (2016-09-19) [2016-12-01]. http://www.moa.gov.cn/govpublic/SYJ/201609/t20160922_5282118.htm
[24] Commission of Chinese Veterinary Pharmacopoeia. Pharmacopoeia of People’s Republic of China, Part 1. Beijing: China Agriculture Press, 2010: 378
中国兽药典委员会. 中华人民共和国兽药典, 一部. 北京: 中国农业出版社, 2010: 378
Qualitative and quantitative analysis of unknown additives in sulfachlorpyrazine sodium soluble powder
BAO Aiqing*, CHEN Huihua, LU Chunbo, ZHOU Wei,WANG Bin, CHEN Xiaolin, LIN Xianjun
(ZhejiangProvinceInstituteofVeterinaryDrugandFeedstuff,Hangzhou311101,China)
A qualitative and quantitative analysis of unknown additives in a batch of veterinary soluble sulfachlorpyrazine sodium powder had been implemented. The content of soluble sulfachlorpyrazine sodium powder was determined by potentiometric titration. The result showed that the titration was aberrant. According to the standard method, one of the two identifications was unqualified. It revealed that some unknown compounds may be doped in the sample. Then the screening of the sample through ultra high performance liquid chromatography coupled with quadrupole time-of-flight tandem mass pectrometry (UHPLC-Q/TOF MS) showed that the suspicious additives were found in the sample. Furthermore, double confirmation and content determination were accomplished by high performance liquid chromatography-diode array detection (HPLC-DAD). Mequindox and sulfadimidine as the illegal additives were detected at 40.3 and 16.4 mg/g respectively. By summarizing the above progress of deduction, validation and content determination, a good pattern was developed for screening illegal additives in veterinary drugs which provided a reference for the inspection of illegal adulterations in veterinary drugs.
ultra high performance liquid chromatography coupled with quadrupole time-of-flight tandem mass spectrometry (UHPLC-Q/TOF MS); high performance liquid chromatography-diode array detection (HPLC-DAD); sulfachlorpyrazine sodium; mequindox; sulfadimidine; veterinary drug; illegal adulteration
10.3724/SP.J.1123.2016.12004
2016-12-04
公益性农业行业专项(201203023-4).
Foundation item: Special Fund for Agro-Scientific Research in the Public Interest (No. 201203023-4).
O658
A
1000-8713(2017)05-0520-06
* 通讯联系人.Tel:(0571)56269752,E-mail:baoaiqing@126.com.
