醇分子作为牺牲剂对Pt/TiO2光催化水解产氢效率的影响
2017-04-24李福颖王仁章王绪绪
李福颖,牛 玉,王仁章,王绪绪
(1.三明学院资源与化工学院,福建 三明 365004;2.福州大学光催化研究所,福建 福州 350002; 3.福州大学石油化工学院,福建 福州 350116)
醇分子作为牺牲剂对Pt/TiO2光催化水解产氢效率的影响
李福颖1,2,牛 玉1,3,王仁章1,王绪绪2
(1.三明学院资源与化工学院,福建 三明 365004;2.福州大学光催化研究所,福建 福州 350002; 3.福州大学石油化工学院,福建 福州 350116)
鉴于太阳光催化分解水获取氢能源反应中,产氢效率受到牺牲剂组成和结构的影响,以Pt/TiO2为模型催化剂,125 W高压汞灯为光源,在常压环境下,比较不同一元醇(甲醇、乙醇、正丙醇、正丁醇)和多元醇(乙二醇、丙三醇、丁四醇、聚乙二醇)的反应性能.实验结果发现,乙二醇作为牺牲剂时产氢效率最高,可达到17.62 mmol·(g·h)-1.研究还发现,反应不仅生成了H2和CO2,还生成了CO、CH4、C2H6、C2H4等产物.基于产物分布,进一步对醇分子作为牺牲剂时,光解水的产氢机理进行了探讨.
光催化作用; 水解离; 醇分子牺牲剂; 乙二醇;氢能源
0 引言
光催化技术由于能将水还原成氢气、将二氧化碳还原为有机物和将有机污染物降解,一直吸引着人们的高度关注.对于光催化分解水(光解水)反应,目前为止,以TiO2及其改性修饰材料为基础研发的光催化材料已达两百多种[1-2].令人欣喜的是一批非二氧化钛类光催化材料,如金属盐类(NiO/NaTaO3、SrNb2O7、SrTa2O6、In1-xNixTaO4及PbBi2Nb2O9等)、掺杂氢氧化物和固溶体氧化物类(Ga1-xZnxO1-xNx、In(OH)ySz、Sm2Ti2O5S2、LaTiO2N及TaON 等)、多元金属硫化物类(Zn1-xCuxS、AglnZn7S9及Pt-PdS/CdS等)等被证实有比TiO2类材料更优良的光解水产氢活性.少数一些材料,如NiO/La/KTaO3、Cr/Rh/GaN/ZnO、RhO2/Mo-BiVO4等具有非常高的光量子效率[3-5].光解水产氢技术研究发展前景光明.
虽然这些研究进展令人振奋,但详细的综合分析发现,在所报道的光催化材料中,仅有个别材料能在紫外光下使水完全分解,许多被声称能光解水成氧气和氢气的材料,实际上只能分别在电子给予体牺牲剂或电子接受体牺牲剂存在的条件下光解水产生氢气或者氧气,并不能单独使纯水完全分解.外加的电子给予体牺牲剂,因具有比催化剂价带电位负的多的氧化还原电势,当体系受光照激发时易于俘获价带的光生空穴,以其“氧化牺牲”为代价换取光催化剂导带电子对于H+到氢气的还原和保证催化剂自身被氧化失活.同理,外加的电子接受体牺牲剂,因具有比催化剂导带电位正的多的氧化还原电势,当体系受光照激发时易于俘获导带的光生电子,以其“还原牺牲”为代价换取光催化剂价导带空穴对于水到氢气的氧化和保证催化剂自身不被还原失活.在可见光分解水研究中,几乎所有的催化剂只能在牺牲剂存在的条件下,才能获得氧气或氢气.所以,研究添加牺牲剂对光解水的影响,探究其作用规律,通过选择优良的牺牲剂提高产氢或产氧效率,具有重要的科学和实际意义[6-11].
常使用的电子给予体牺牲剂包括甲醇、乙醇、丙三醇[12]、三乙胺、三乙醇胺[13]、乙二胺四乙酸[14]、硫化钠/亚硫酸钠[15]、葡萄糖[16]等,电子接受体牺牲剂包括硝酸银[17]、碘酸盐[18]、过硫酸盐[19]等.其中,在评价光解水产氢活性时,甲醇牺牲剂的使用最为广泛.由于复杂的中间体,多样的牺牲剂,加之很难将表面分析技术应用到悬浮液体系中等因素,至今未能建立一个清晰的解释牺牲剂在光解水反应中的作用机制.为此,在常压条件下,以Pt/TiO2为模型催化剂,考察了几种醇分子牺牲剂紫外光解水的产物分布,以探讨牺牲剂的作用机理[20-21].
1 实验部分
1.1 光催化剂制备
采用原位光还原沉积法,制备Pt负载TiO2型光催化剂:在水溶液中,加入适量TiO2锐钛矿纳米粒子(纯度99.9 %,粒径15 nm,Alfa Aesar)和H2PtC16溶液,超声分散5 min后,在磁力搅拌的条件下,以300 W氙灯为光源,在含乙醇10%(体积分数)的水溶液中,原位光沉积反应5 h;再经抽滤、洗涤、干燥、研磨,得到含Pt 1%(质量分数)的Pt/TiO2催化剂.
1.2 光催化剂表征
样品的晶相结构采用 Bruker D8 Advance型X射线粉末衍射仪分析;光吸收性能在 Varian Cary 500型UV-Vis-NIR紫外可见漫反射吸收光谱仪上测定;表面形貌和粒径大小采用JEM 2010型透射电子显微镜观测TEM和高分辨TEM谱图;光电子能谱采用ESCALAB 250型X射线光电子能谱仪测定;表面积和孔结构采用Micromeritics ASAP 2020型全自动物理化学吸附仪测定.
1.3 光催化性能评价
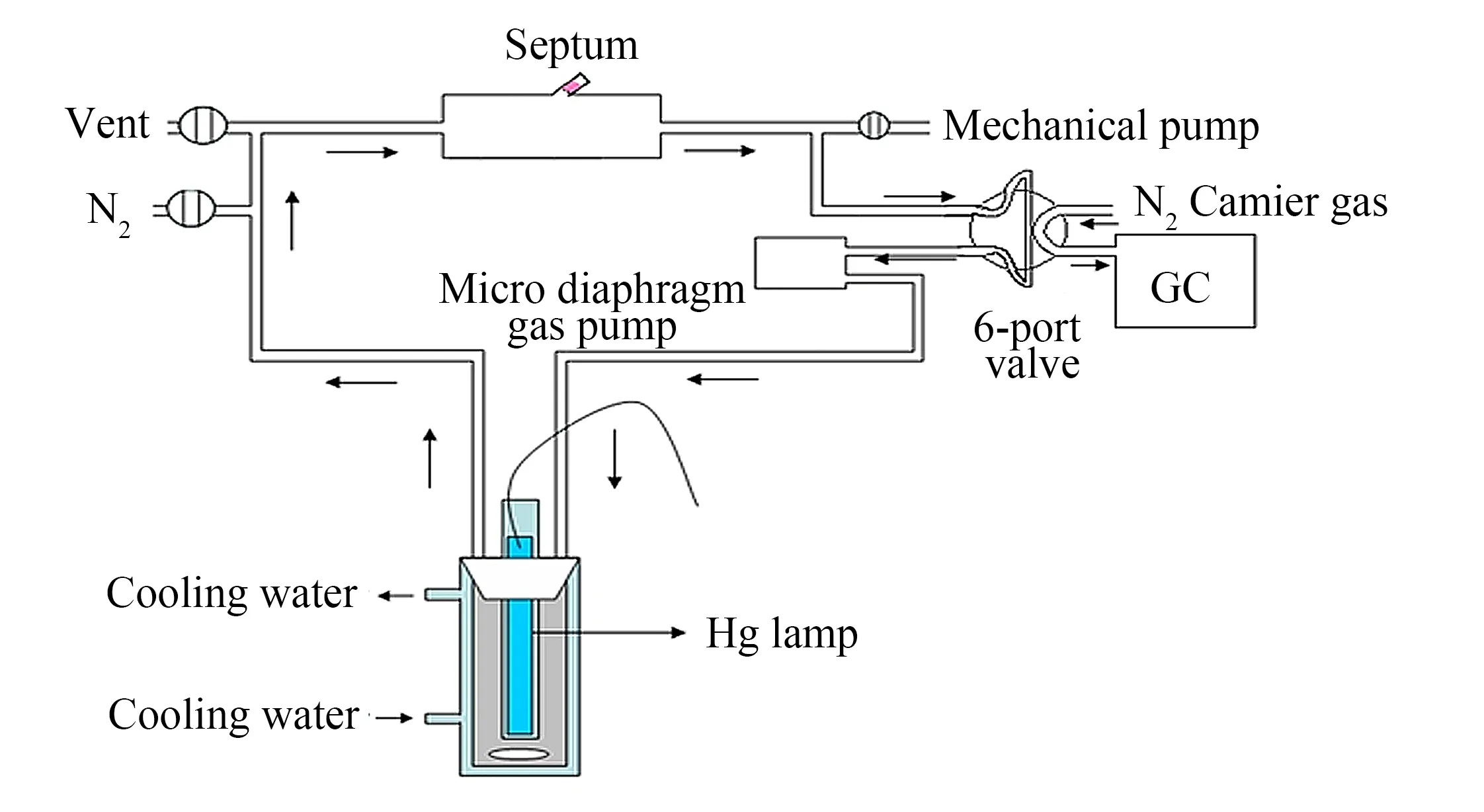
图1 光解水反应装置Fig.1 Schematic diagram of water splitting system
反应在如图1所示的密闭玻璃循环体系中进行,在圆柱形夹套玻璃反应器中加入165 mL去离子水、50 mg Pt/TiO2和5 mL醇分子牺牲剂,通过磁力搅拌器搅拌均匀,并使用冷凝水将反应液温度始终控制在10 ℃左右.反应前,使用机械泵将整个体系抽真空,然后充入高纯氮气,此过程重复3次,以便将体系内的空气除尽.反应液吸脱附30 min后,开启内插式光源(125 W高压汞灯)和气体循环泵,每小时通过气相色谱分析气相产物.
2 结果和讨论
2.1 样品的晶相
图2为TiO2锐钛矿和Pt/TiO2样品的XRD谱图.谱图中2θ= 25.1°、37.6°、48.0°、53.8°、55.0°和 62.7°(JCPDS 21-1272)处的峰均为TiO2锐钛矿特征衍射[22].可能由于Pt含量低或分散度高,未能发现任何与Pt有关的衍射峰.根据25.3°处衍射峰的半峰宽,用Scherrer方程估算出锐钛矿TiO2的平均颗粒大小为(13±2)nm.表明负载Pt没有改变TiO2基底的晶相结构和晶体大小.
2.2 样品的光吸收
图3为锐钛矿TiO2和Pt/TiO2样品的紫外-可见漫反射光谱.以标准BaSO4粉末为参比,发现在TiO2表面负载Pt后,与纯TiO2样品的光吸收阈值380 nm 相比,Pt/TiO2的紫外吸收带边发生红移,说明负载Pt使得光吸收能力略有增强[23].

图2 样品的XRD光谱 Fig.2 XRD of the samples
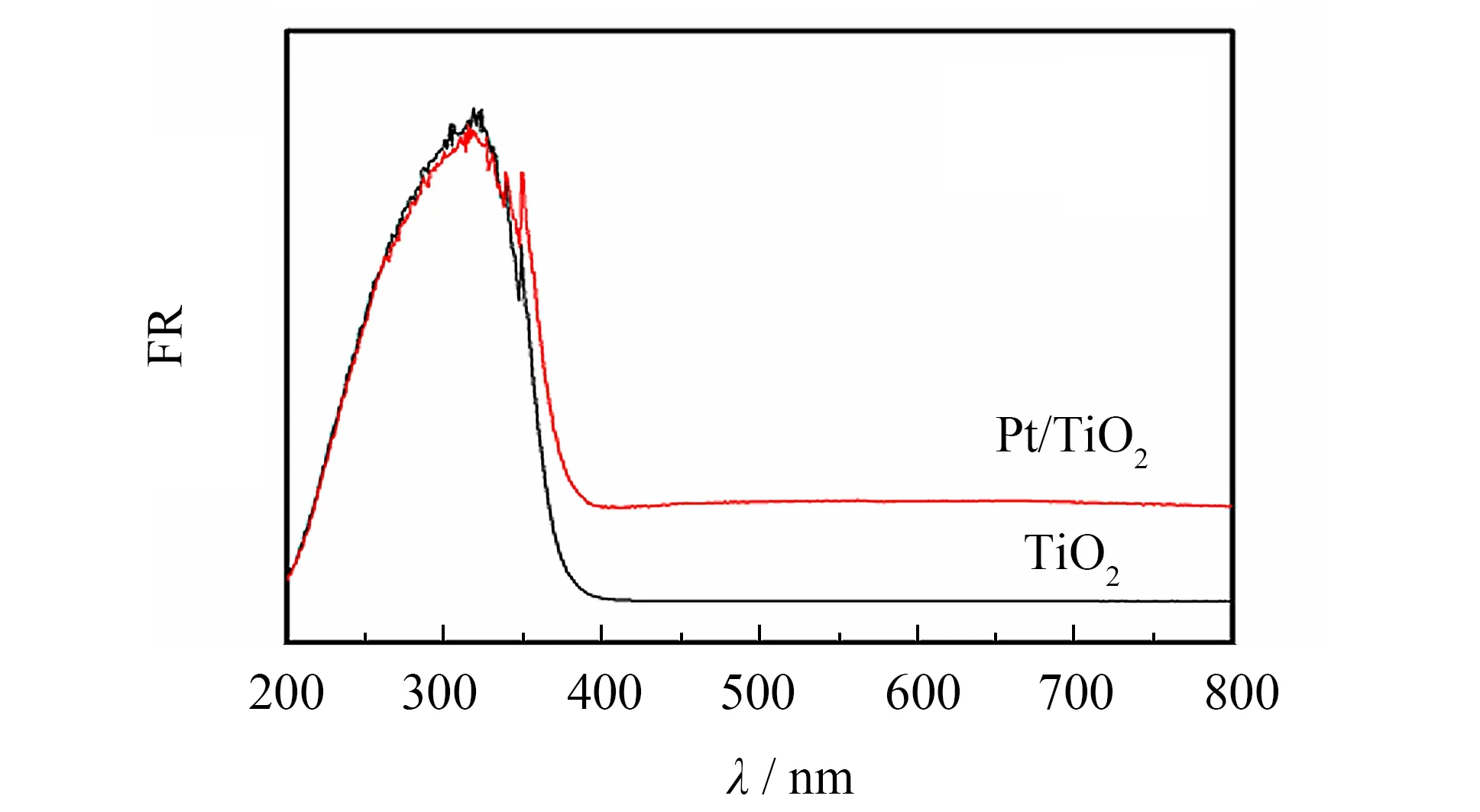
图3 样品的紫外可见漫反射光谱Fig.3 UV-Vis DRS of the samples
2.3 样品的形貌
图4、5分别是Pt/TiO2样品的TEM图和HTEM图.可以看出,Pt修饰TiO2表面后其晶体结构没有发生变化,颗粒尺寸都约为15 nm,与XRD计算的结果一致.在 HTEM 图上,观察到晶格间距为 0.35和0.209 nm的晶格条纹,与锐钛矿TiO2的d101和Pt的d200一致.另外还发现,采用光沉积法负载的Pt在TiO2表面不同区域的分布有明显差别,存在团簇现象.

图4 Pt/TiO2样品的TEM图Fig.4 TEM of the Pt/TiO2 sample

图5 Pt/TiO2样品的HTEM图Fig.5 HTEM of the Pt/TiO2 sample
2.4 元素的化学状态
图6、7分别为Pt/TiO2样品的全扫描和精细扫描谱图.从图6可以看出,样品除了 C 1s吸收峰外,没有发现其它杂质峰.图7表明,Ti 2P1/2和Ti 2P3/2的结合能分别为 464.35和458.55 eV,O 1s 的结合能为529.87 eV,与文献报道的数值几乎相同[24].在74.08 和70.78 eV观察到两个峰,分别属于Pt 4f7/2和Pt 4f5/2的结合能,很好地与Pt0相匹配,说明负载的Pt主要以零价态存在.
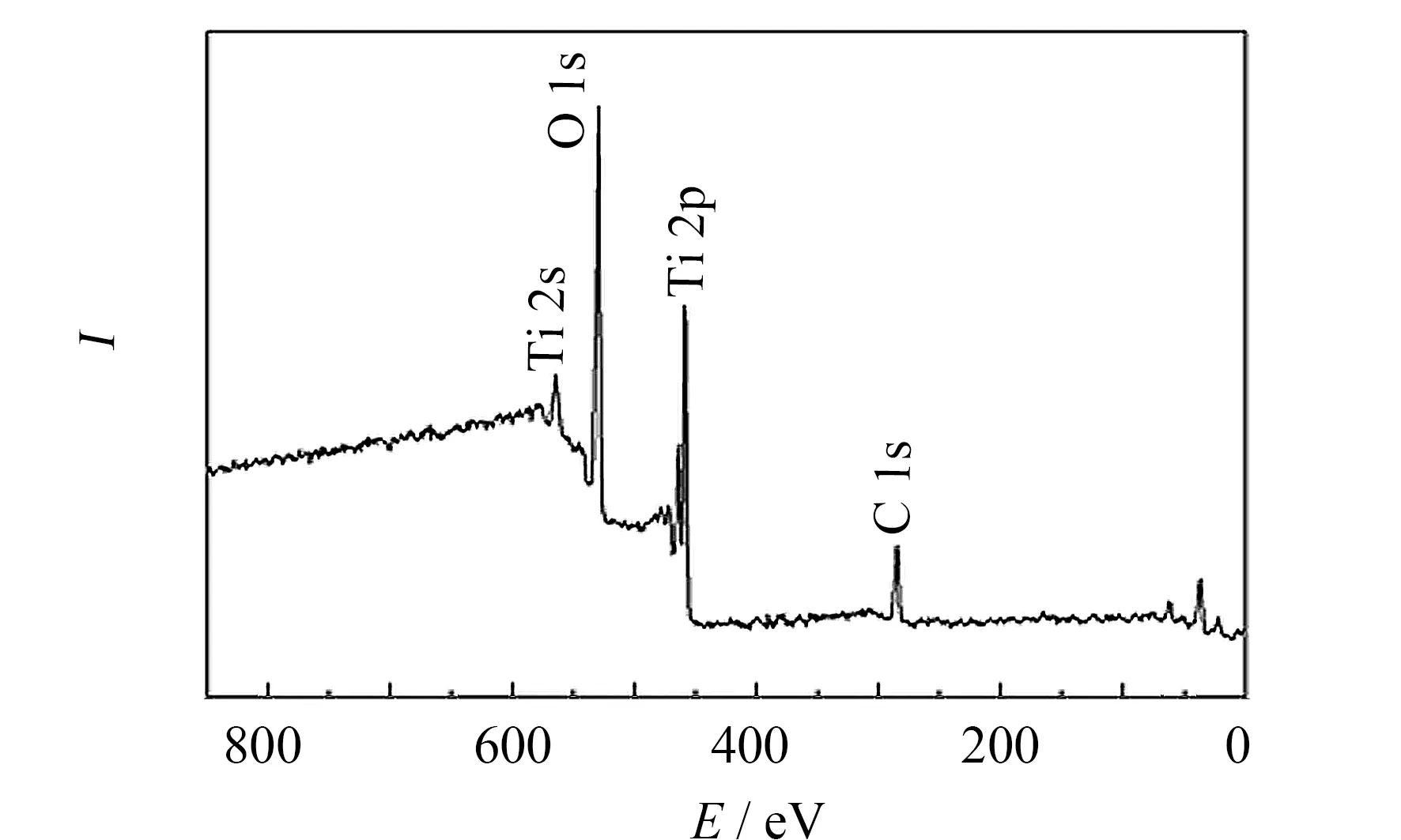
图6 Pt/TiO2样品的宽扫描XPS谱图Fig.6 Wide scan XPS spectra of the Pt/TiO2 sample
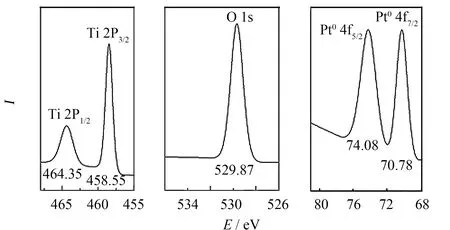
图7 Pt/TiO2样品的Ti 2P,O 1s 和 Pt 4f 窄扫描XPS谱图Fig.7 High-resolution XPS spectra of Ti 2P,O 1s and Pt 4f regions of the Pt/TiO2 sample
2.5 样品的织构

表1 样品的物理化学参数Tab.1 Physicochemical characteristics of as-prepared samples
图8、9分别为锐钛矿TiO2和Pt/TiO2样品的低温(77 K)N2吸脱附和孔径分布曲线.样品的物理化学参数列于表1.由图8、9和表1可知,Pt/TiO2样品的吸附等温线、比表面积、孔体积和孔径几乎与纯TiO2样品的一致.表明负载Pt没有明显改变TiO2的结构性质,同时也表明Pt纳米颗粒高度分散在TiO2表面.
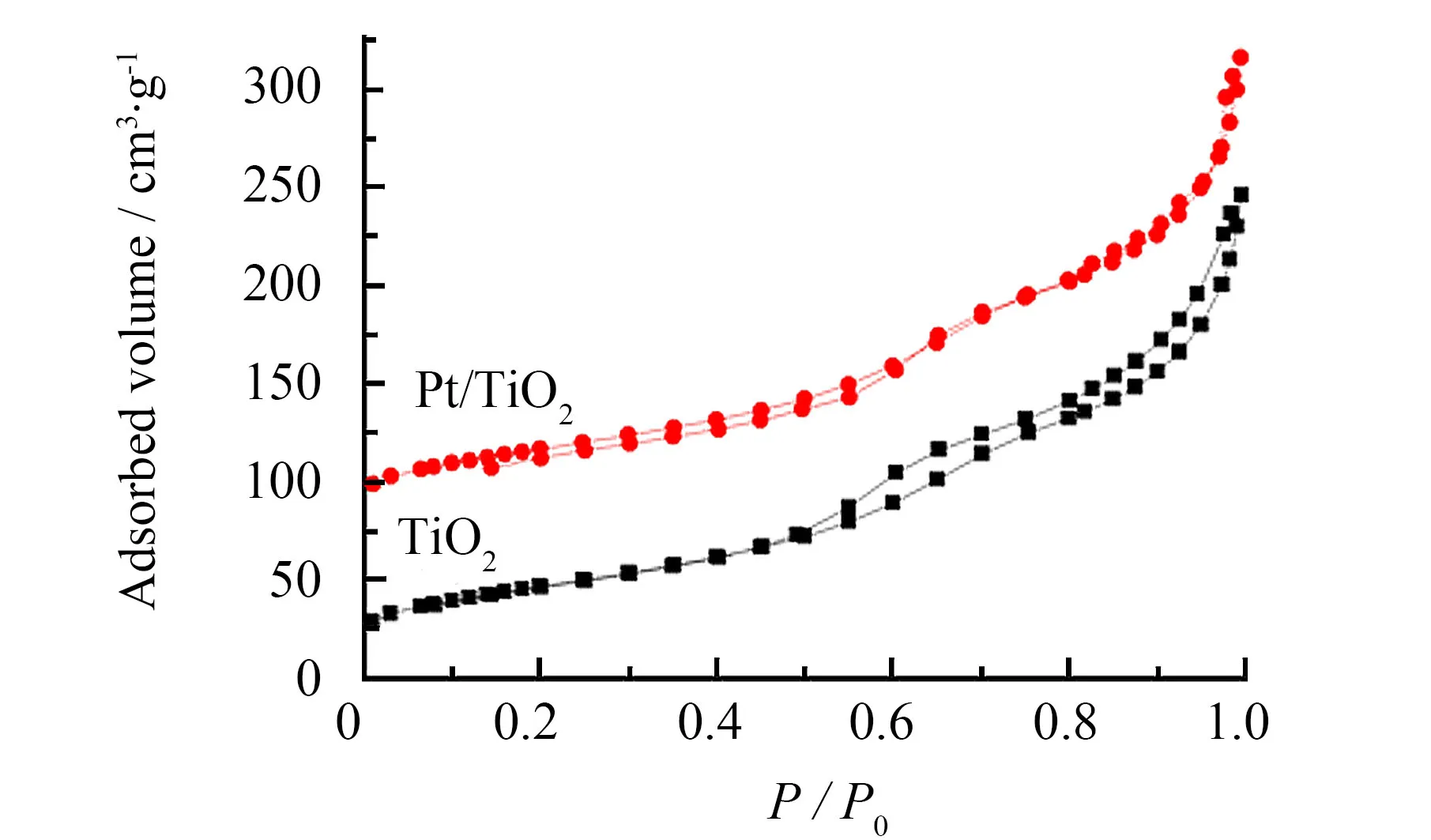
图8 样品的低温氮气吸附—脱附曲线Fig.8 N2-sorption isotherms of the samples
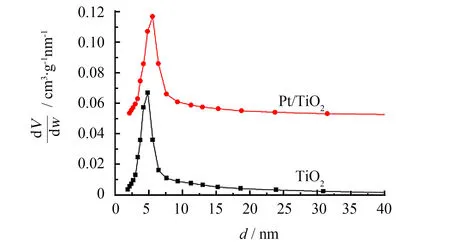
图9 样品的孔径分布曲线Fig.9 BJH pore-size distributions of the samples
2.6 醇分子牺牲剂对Pt/TiO2光催化产氢活性的影响
以50 mg Pt/TiO2为催化剂,以5 mL甲醇、乙醇、正丙醇、正丁醇、乙二醇、丙三醇,或5 mg丁四醇、聚乙二醇为牺牲剂,探讨光催化醇分子牺牲剂的产物生成规律,结果如图10所示.其中,乙二醇表现出最好的光解水产氢活性.
2.6.1 光催化一元醇牺牲剂的产物分析
以50 mg Pt/TiO2催化剂和5 mL甲醇、乙醇、正丙醇、正丁醇等一元醇,探讨光催化一元醇牺牲剂的产物生成规律,结果如图11所示.由图11可知,产氢活性顺序为:甲醇>乙醇>正丙醇>正丁醇.显然,一元醇的产氢活性随着碳链的增长逐渐降低.可能是由于一元醇的溶剂极性差异所致,碳链越短极性越强,在催化剂表面吸附能力越强,也说明吸附作用是光化学反应的决速步[26].
以一元醇为牺牲剂的光催化反应中,除了CO、CO2还检测到CH4、C2H6和C2H4等气相产物,这些气相产物随反应时间线性增加.以不同一元醇为牺牲剂时Pt/TiO2光解水反应10 h后,各气相产物分布列在表2中.从实验结果可以看出,以不同一元醇为牺牲剂时Pt/TiO2光解水的烃类气相产物比例存在很大差异,乙醇、正丙醇、正丁醇为牺牲剂时分别大量生成了CH4、C2H6、C2H4.
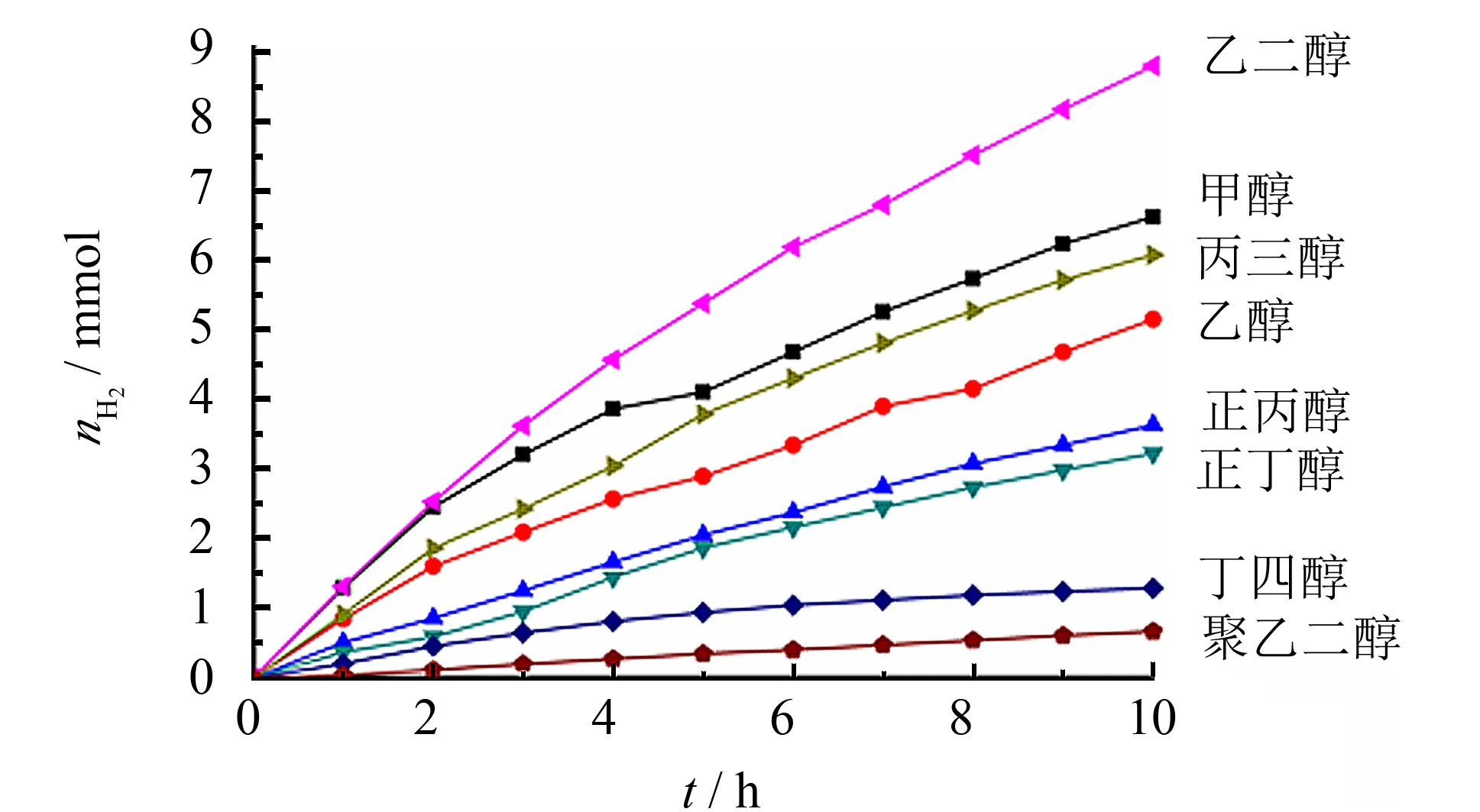
图10 醇类光解水产氢的对比实验Fig.10 Photolysis aquatic hydrogen contrast experiment of alcohols
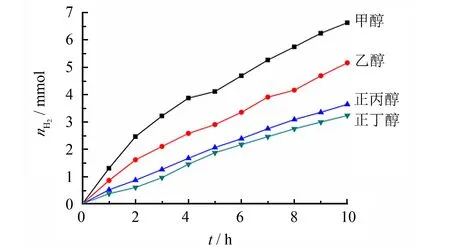
图11 一元醇光解水产氢的对比实验Fig.11 Photolysis aquatic hydrogen contrast experiment of monobasic alcohol

表2 不同一元醇牺牲剂时Pt/TiO2光解水反应气相产物分布Tab.2 Gasous product distributions of the photocatalytic descomposirion of water on Pt/TiO2 with different monohydric alcohols as sacrificial agents (mmol)
2.6.2 光催化多元醇牺牲剂的产物分析
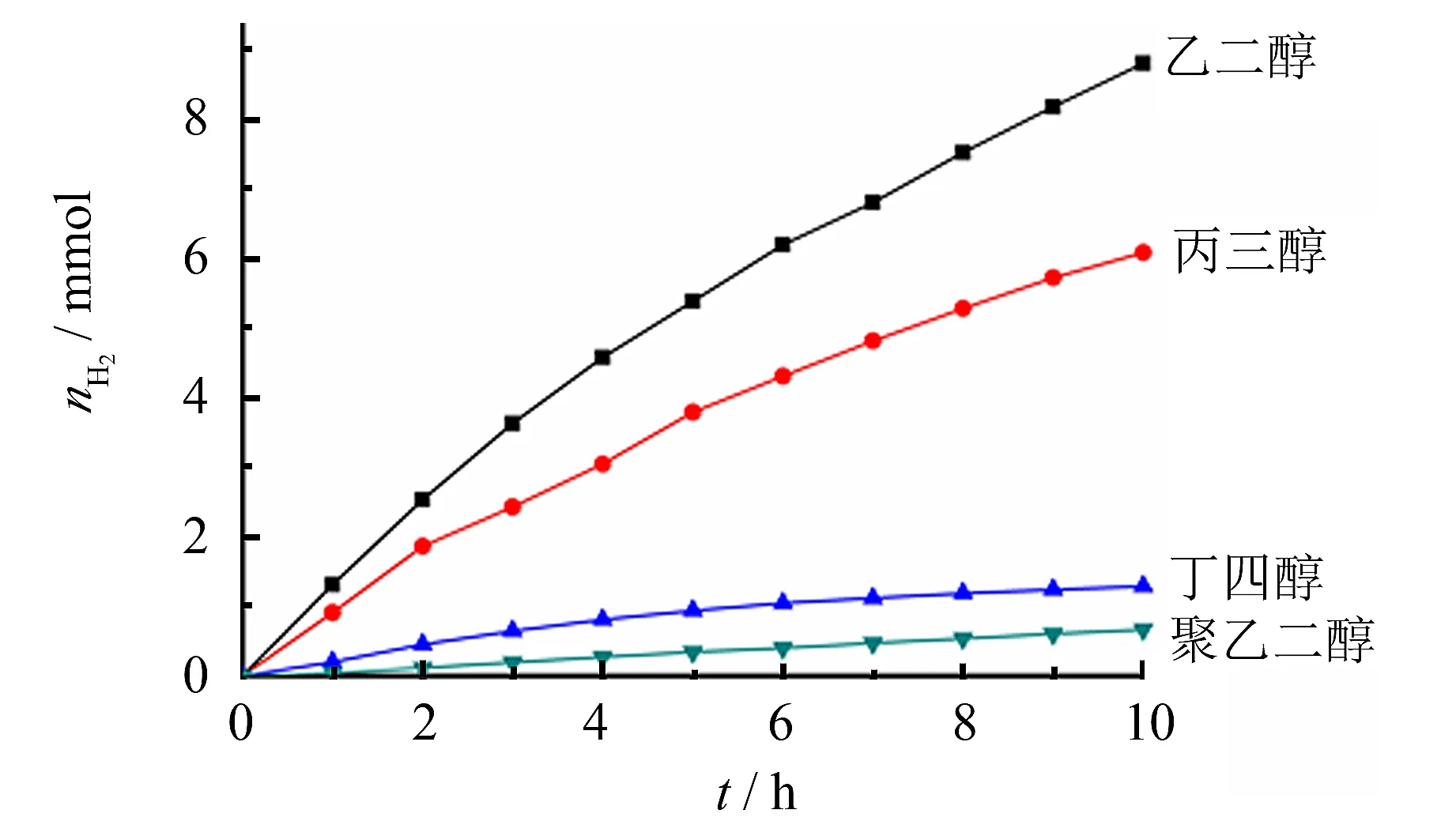
图12 多元醇光解水产氢的对比实验Fig.12 Photolysis aquatic hydrogen contrast experiment of polyhydric alcohol
以50 mg Pt/TiO2催化剂和5 mL乙二醇、丙三醇(或50 mg丁四醇、聚乙二醇)等多元醇,探讨光催化多元醇牺牲剂的产物生成规律,结果如图12所示.由图12可知,产氢活性顺序为:乙二醇>丙三醇>丁四醇>聚乙二醇.分析得出,多元醇牺牲剂的产氢活性随着羟基数目的增多和碳链的增长而逐渐降低.由此得出,多元醇的羟基并没能全部参与羟基解离,反而由于碳链的增长发生了光催化重整,产氢速率逐渐降低.
同样,在以多元醇为牺牲剂的光催化反应中,也检测到了CO、CO2、CH4、C2H6和C2H4等气相产物,这些气相产物随反应时间线性递增.从采用不同多元醇牺牲剂,Pt/TiO2光催化水分解反应10 h的实验数据,可以看出烃类气相产物比例没有明显差异.各气相产物分布列在表3中.
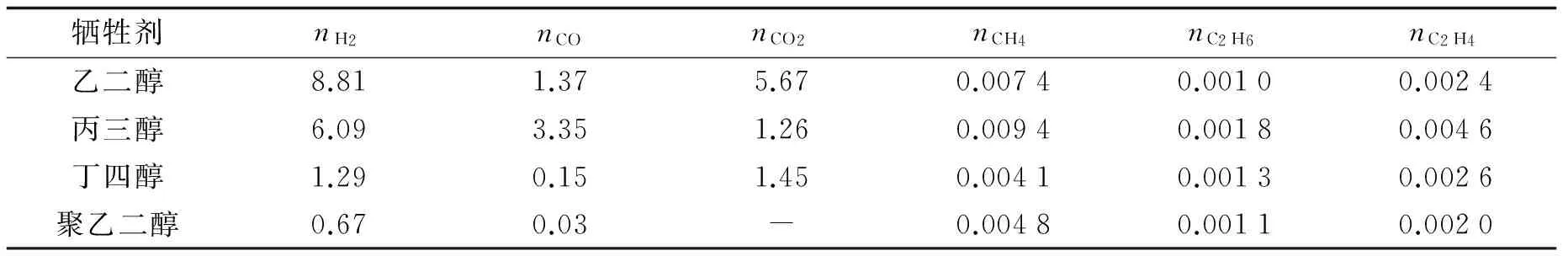
表3 不同多元醇牺牲剂时Pt/TiO2光解水反应气相产物分布Tab.3 Gasous product distributions of the photocatalytic descomposirion of water on Pt/TiO2 with different polyhydric alcohols as sacrificial agents (mmol)
3 醇类牺牲剂存在下Pt/TiO2光催化水分解机理探讨
基于无氧气氛下的光催化反应中,空穴和·OH为主要氧化物种,对一元醇为牺牲剂的光催化反应历程做如下推测[27-28]:首先一元醇在Pt/TiO2表面通过其羟基氧与TiO2表面5配位的Ti原子配位吸附,随后羟基上的氢解离,生成H+和RCH2O-,解离的质子迁移到Pt颗粒表面,与光生电子反应生成H2,而RCH2O-则被空穴氧化,生成·RCHOH自由基;该自由基发生羟基解离从而生成RCHO;RCHO进一步被·OH氧化脱氢,生成RCOOH,或被H2还原生成RCH2OH;RCOOH经photo-Kolbe反应脱羧生成CO2(CO2还可被H2还原成CO)及CxHy.
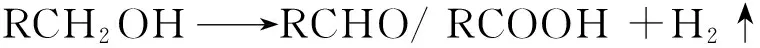
副产物醛和酸可进一步被氧化:
在化学反应中,多元醇一般先只有一个羟基发生反应,在高温、强酸等条件下,才可使多个羟基参与反应.所以,在光催化反应中,多元醇为牺牲剂时的反应历程非常复杂,不仅发生光生空穴猝灭,而且存在光催化重整,至今未见详细报道其参与反应的历程.
在常压、惰性气氛条件下,以Pt/TiO2为模型光催化剂,比较醇分子牺牲剂的紫外光解水产氢活性时,发现乙二醇最佳.可能是由于乙二醇的相对介电常数高于一元醇,且短碳链的二元醇能够较多的参与羟基解离,其真实的反应历程较为复杂,需借助原位分析检测等手段做进一步的深入研究.
4 结语
1)醇分子牺牲剂的作用.氢源作为光致电子-空穴复合抑制剂[29],其氧化产生的羟基自由基连续不断地抑制光生电子-空穴复合,提高催化剂表面的氧化能力,同时捐助额外的电子,增加表面量子产率,促进光解水产氢速率.
2)Pt/TiO2下醇分子牺牲剂的光解水产氢活性规律.产氢活性与醇分子牺牲剂的碳链长度和羟基数目有关,等长度碳链时羟基越多产氢效率越高,生成烃类气体的概率越小.常压、惰性气氛条件下对比发现,乙二醇为牺牲剂时,Pt/TiO2光解水产氢活性最高.
3)光还原的影响.醇分子作为牺牲剂时,生成的CO2和H2可能会发生光还原反应,一方面消耗了H2,另一方面阻碍了催化剂表面电子传递,致使光解水产氢效率降低.因此,抑制CO2在催化剂表面的光还原显得十分必要.
[1] 李涛海,吴季怀,陈秀琴.需要牺牲剂可见光下分解水的光催化材料[J].化工新型材料,2004,32 (4):1-4.
[2] 刘恢.可见光响应光催化剂及其分解水的研究[D].上海:上海交通大学,2008:31-35.
[3] LIANOS P.Production of electricity and hydrogen by photocatalytic degradation of organic wastes in a photoelectrochemical cell:the concept of the Photofuelcell:a review of a re-emerging research fiel[J].Journal of Hazardous Materials,2011,185(2/3):575-590.
[4] ESSWEIN A J,NOCERA D G.Hydrogen production by molecular photocatalysis[J].Chemical Reviews,2007,107(10):4 022-4 047.
[5] YOSHIDA H,HIRAO K,NISHIMOTO J I,etal.Hydrogen production from methane and water on platinum loaded titanium oxide photocatalysts[J].Journal of Physical Chemistry C,2008,112(14):5 542-5 551.
[6] MILLS A,ILUNTE S L.An overview of semiconductor photocatalysis[J].Journal of Photochemistry and Photobiology A:Chemistry,1997,108(1):1-35.
[7] YANG J H,WANG D,HAN H X,etal.Roles of cocatalysts in photocatalysis and photoelectrocatalysis[J].Accounts of Chemical Research,2013,46(8):1 900-1 909.
[8] KHO Y K,IWASE A,TEOH W Y,etal.Photocatalytic H2evolution over TiO2nanoparticles.The synergistic effect of anatase and rutile[J].Journal of Physical Chemistry C,2010,114(6):2 821-2 829.
[9] BARRECA D,FOMASIERO P,GASPAROTTO A,etal.The potential of supported Cu2O and CuO nanosystems in photocatalytic H2production[J].Chemistry and Sustainable Chemistry,2009,2(3):230-233.
[10] LI Y B,WU J H,HUANG Y F,etal.Photocatalytic water splitting on new layered perovskite A2.33Sr0.67Nb5O14.335(A=K,H)[J].International Journal of Hydrogen Energy,2009,34(19):7 927-7 933.
[11] GENTILIA P L,PENCONI M,ORTICA F,etal.Synergistic effects in hydrogen production through water sonophotolysis catalyzed by new La2xGa2yIn2(1LxLy)O3solid solutions[J].International Journal of Hydrogen Energy,2009,34(22):9 042-9 049.
[12] GOMBAC V,SORDELLI L,MONTINI T,etal.CuOx-TiO2photocatalysts for H2production from ethanol and glycerol solutions[J].Journal of Physical Chemistry A ,2010,114(11):3 916-3 925.
[13] ZHANG P,JACQUES P A,MURIELLE C K,etal.Phosphine coordination to a cobalt diimine-dioxime catalyst increases stability during light-driven H2production[J].Inorganic Chemistry,2012,51(4):2 115-2 120.
[14] KOBAYASHI M,MASAOKA S,SAKAI K.Photoinduced hydrogen evolution from water by a simple platinum(II)terpyridine derivative:a Z-scheme photosynthesis[J].Angewandte Chemie International Edition,2012,51(30):7 431-7 434.
[15] ZHANG J,YU J G,JARONIEC M,etal.Noble metal-free reduced graphene oxide-ZnxCd1-xS nanocomposite with enhanced solar photocatalytic H2- production performanc[J].Nano Letters,2012,12(9):4 584-4 589.
[16] FU X L,LONG J L,WANG X X,etal.Photocatalytic reforming of biomass:a systematic study of hydrogen evolution from glucose solution[J].International Journal of Hydrogen Energy,2008,33(22):6 484-6 491.
[17] AMEY D,WATKINS T,MAGGARD P A.Effects of particle surface areas and microstructures on photocatalytic H2and O2production over PbTiO3[J].Journal of the American Ceramic Society,2011,94(5):1 483-1 489.
[18] HARA S,YOSHIMIZU M,TANIGAWA S,etal.Hydrogen and oxygen evolution photocatalysts synthesized from strontium titanate by controlled doping and their performance in two-step overall water splitting under visible light[J].Journal of Physical Chemistry C,2012,116(33):17 458-17 463.
[19] PUNTORIERO F,SARTOREL A,ORLANDI M,etal.Photoinduced water oxidation using dendrimeric Ru(II)complexes as photosensitizers[J].Coordination Chemistry Reviews,2011,255(21/22):2 594-2 601.
[20] CHO H W,WU J J.Photoreduction of graphene oxide enhanced by sacrificial agents[J].Journal of Colloid and Interface Science,2015,438(15):291-295.
[21]KEFAYAT U,ASGHAR A,SHU Y,etal.Microwave-assisted synthesis of Pt-graphene/TiO2nanocomposites and their efficiency in assisting hydrogen evolution from water in the presence of sacrificial agents[J].Science of Advanced Materials,2015,7(4):606-614.
[22] FU X L,WANG X X,DENNI Y C,etal.Photocatalytic reforming of C3-polyols for H2production:Part (I).Role of their OH groups[J].Applied Catalysis B:Environmental,2011,106(supp 3/4):681-688.
[23] ZHANG F X,CHEN J X,ZHANG X,etal.Synthesis of titania-supported platinum catalyst:the effect of pH on morphology control and valence state during photodeposition[J].Langmuir,2004,20(21):9 329-9 334.
[24] BOND G C,FLAMERZ S.Structure and reactivity of titania-supported oxides:IV Characterisation of dried vanadia/titania catalyst precursor[J].Applied Catalysis,1989,46(1):89-102.
[25] LO C C,HUNG C H,YUAN C S,etal.Photoreduction of carbon dioxide with H2and H2O over TiO2and ZrO2in a circulated photocatalytic reactor[J].Solar Energy Materials and Solar Cells,2007,91(19):1 765-1 774.
[26] SUN W,ZHANG S Q,LIU Z X,etal.Studies on the enhanced photocatalytic hydrogen evolution over Pt/PEG-modified TiO2photocatalysts[J].International Journal of Hydrogen Energy,2008,33(4):1 112-1 117.
[27] WEI Y L,LI J,HUANG Y F,etal.Photocatalytic water splitting with in-doped H2LaNb2O7composite oxide semiconductors[J].Solar Energy Materials and Solar Cells,2009,93(8):1 176-1 181.
[28] MAENAKA Y,SUENOBU T,FUKUZUMI S.Hydrogen evolution from aliphatic alcohols and 1,4-selective hydrogenation of NAD+catalyzed by a [C,N] and a [C,C] cyclometalated organoiridium complex at room temperature in water[J].Journal of the American Chemical Society,2012,134 (22):9 417-9 427.
[29] BARRECA D,FOMASIERO P,GASPAROTTO A,etal.The potential of supported nanosystems in photocatalytic H2production[J].Chemistry and Sustainable Chemistry,2009,2(3):230-233.
(责任编辑:洪江星)
Effect of different alcohols as sacrificial agents on efficiency of the photocatalytic decomposition of water to hydrogen over Pt/TiO2
LI Fuying1,2,NIU Yu1,3,WANG Renzhang1,WANG Xuxu2
(1.College of Resources and Chemical Engineering,Sanming University,Sanming,Fujian 365004,China;2.Research Institute of Photocatalysis,Fuzhou University,Fuzhou,Fujian 350002,China;3.School of Chemical Engineering,Fuzhou University,Fuzhou,Fujian 350116,China)
In the process of photocatalytic water splitting,some alcoholic compounds are frequently used as the sacrificial agents capturing photogenerated holes to facilitate reduction of water molecules by the conduction band electron.In previous studies,more attention has been paired to development of novel and highly efficient photocatalysts,few researches involve the effect of composition and structure of the sacrificial agents on the production efficiency of hydrogen.Pt/TiO2was used as the model photocatalyst,a 125 W high pressure mercury lamp was used as the light source irradiation.When methanol,ethanol,propanol,n-butyl alcohol,glycol,glycerin,erythritol and polyethylene glycol were used as the sacrificial agents,the water splitting results show that the rates of hydrogen production was the highest when glycol was used as the sacrificial agent,attained 17.62 mmol·(g·h)-1.The experiment results not only generated H2and CO2,but also had the production of CO,CH4,C2H6and C2H4.The mechanism of hydrogen production was discussed based on the distribution of photocatalytic reaction products.
photocatalysis; water splitting; alcohols sacrificial agents; glycol;hydrogen energy
10.7631/issn.1000-2243.2017.02.0268
1000-2243(2017)02-0268-07
2015-12-15
王绪绪 (1955- ),教授,主要从事环境光催化方面的研究,xwang@fzu.edu.cn
福建省自然科学基金资助项目(2015J01601); 福建省2011洁净煤气化技术协同创新中心资助项目(XK1401,XK1403);福建省教育厅青年基金资助项目(JA15475)
TQ426.1
A
