超声-弱碱协同作用下巨龙竹木质素的分离及表征
2017-04-24邓嘉雯杨海艳史正军邓佳杨静郑志锋辉朝茂
邓嘉雯,杨海艳△,史正军*,邓佳,杨静,郑志锋,辉朝茂
(1.西南林业大学云南省高校生物质化学炼制与合成重点实验室;2.西南林业大学教育部省部共建西南山地森林资源保育与利用重点实验室,昆明650224)
超声-弱碱协同作用下巨龙竹木质素的分离及表征
邓嘉雯1,杨海艳1△,史正军1*,邓佳2,杨静1,郑志锋1,辉朝茂2
(1.西南林业大学云南省高校生物质化学炼制与合成重点实验室;2.西南林业大学教育部省部共建西南山地森林资源保育与利用重点实验室,昆明650224)
巨龙竹是一种具有极高研究和开发价值的大型经济用材竹种,其基础理化性质有待进一步解析研究。为表征巨龙竹木质素的化学结构,在超声-弱碱协同作用下处理竹材原料,脱蜡竹粉在2%NaOH溶液中分别经超声处理5,20,40,60和90 min,并设置仅在2% NaOH溶液中抽提90 min的对照组,最后得到6个木质素样品L1~L6。采用红外光谱(FTIR)、核磁共振碳谱(13C NMR)和二维核磁共振(2D HSQC)分别对分离得到的巨龙竹木质素进行结构分析。结果表明:超声-弱碱协同处理对竹材木质素具有良好的促溶效果,随着超声作用时间的增加,木质素得率从6.6%提高到22.9%;巨龙竹木质素大分子主要由愈创木基(G)、紫丁香基(S)和对羟基苯基(H)结构单元构成,属于禾草类木质素(GSH型);巨龙竹木质素大分子的主要联接键为β-O-4′醚键,其次是β-β′和β-5′结构;但随着超声处理时间的增加,巨龙竹木质素中一定量的β-O-4′联接键会被打断。
巨龙竹;木质素;超声-弱碱协同作用;结构表征
木质素是竹材细胞壁主要组成物质中结构最复杂的组分,人们至今依然没有完全掌握其内在结构规律。早在1952年,Leopold等[1]就发现竹子木质素与木材不同, 它由紫丁香基(S)、愈创木基(G)和对羟基苯基(H)3种基本单元构成。Lu等[2]用AcBr衍生、Zn粉还原使其β位醚键断裂的方法(DFRC)证明了撑蒿竹(Bambusapervariabilis)木质素中存在β-芳基醚和γ-对香豆酸酯构型。Li等[3]研究发现琴丝竹(Neosinocalamusaffinis)木质素结构中存在其他竹子木质素鲜有的α-O-α′连接键(占6.1%)。Yang等[4]发现金竹(Phyllostachyssulphurea)离子液体可溶性木质素大分子基本单元间化学连接键中β-O-4′、β-β′和β-5′联接分别占43.2%,4.3%和5.1%。最近,Wen等[5]研究发现硬头黄竹(Bambusarigida)木质素结构中,以β-O-4′连接的苯丙烷单元侧链γ位碳比其他方式连接的γ位碳具有更多的对香豆酸和阿魏酸酯结构。黄曹兴等[6]发现竹黄在稀硫酸预处理过程中发生解聚反应,木质素侧链区域螺旋二烯酮联接键发生断裂,同时,木质素在稀硫酸预处理过程中的缩合反应主要发生在愈创木基单元上。对比分析现有研究可发现,虽然人们对竹材木质素化学结构的研究已经取得一定进展,但有关竹子木质素中苯丙烷单元间碳-碳键和醚键连接方式、结合位置、结合强度等化学结构特征还有待深入解析。
巨龙竹(Dendrocalamussinicus)因其具有秆型高大、单株产量高、生长速度快等优良特性,而被视为是一种具有极高研究和开发价值的大型经济用材竹种。但由于其分布地经济文化相对落后,人们对其认识较晚,目前对其基本理化性质的研究还远远不够,其高值化开发利用缺乏可靠的科学理论指导,潜在的开发利用价值一直未能得以真正实现。鉴于此,笔者拟通过超声波与化学处理相结合的方法分离巨龙竹木质素,并对其进行结构表征,解析竹材木质素化学结构特征,以期为巨龙竹资源的化学转化利用提供理论依据。
1 材料与方法
1.1 试验材料
选择3年生巨龙竹为原料,采自云南省普洱市孟连县景信乡。将采伐的竹子去除梢和侧枝,并将竹秆按基部、中部、梢部进行三等分,风干后切成小块,粉碎并筛选出粒径0.25~0.42 mm(60~40目)的竹粉。粉碎后的竹粉经体积比2∶1的甲苯-乙醇溶液在索氏抽提器中抽提10 h,去除抽提物,脱蜡竹粉在60℃条件下烘干,保存备用。
1.2 试验方法
将60 g脱蜡的竹粉平均分成6份,每份10 g,在温度为30℃、功率400 W、频率35 Hz、NaOH质量分数2.0%、固液比1∶10(g/mL)的条件下,将前5份竹粉分别经超声结合碱处理(含2.0%NaOH)5,20,40,60和90 min,第6份竹粉作为对照,仅在2.0% NaOH碱溶液中抽提90 min。将每一步抽提出来的样品分别进行残渣和滤液的分离,调节滤液pH至5.5,中和后的液体用旋转蒸发仪减压浓缩到约30 mL,后缓慢倒入3倍体积质量分数95%乙醇进行沉淀,并用磁力搅拌器搅拌,静置0.5 h后析出半纤维素沉淀。通过离心机将固液分离,去掉多糖组分,将滤液继续减压浓缩到15 mL并调pH至2.0,静置后析出木质素,经离心分离和冷冻干燥分别得到竹材木质素样品L1~L6,备用。
1.3 木质素分析与表征
1.3.1 红外光谱分析
木质素样品的红外光谱分析在Nicolet 6700傅里叶红外光谱仪上进行。采用KBr压片法,样品均匀分散于KBr中,质量分数为1%。扫描波长范围4 000~400 cm-1,扫描次数设为32次,分辨率1.928 cm-1,在透射模式下获得红外光谱数据。
1.3.2 核磁共振分析
核磁共振碳谱(13C NMR)和二维核磁共振(2D HSQC)均采用布鲁克400 M超导核磁共振仪进行测定。13C NMR以氘代 DMSO为溶剂,将80 mg木质素溶于0.5 mL DMSO-d6中。采用30°脉冲序列,采样时间1.36 s,弛豫时间1.89 s,累计扫描30 000次。2D HSQC分析时,把60 mg样品溶于1 mL的 DMSO-d6中,采样时间0.17 s,弛豫时间1.5 s,采样128次,256增加量。
2 结果与分析
2.1 得率分析
本试验在相同浓度的碱溶液、依次增加超声时间条件下对脱蜡竹粉进行抽提,并得到6个木质素样品。木质素得率按照产物占总木质素(酸溶木质素和酸不溶木质素)的百分比进行计算。巨龙竹原料木质素含量为26.12%,酸溶木素和酸不溶木素的含量分别参照国家标准GB/T 10337—2008、GB/T 2677.8—1994 测量。超声弱碱协同作用下抽提巨龙竹木质素样品的得率如表1所示。由表1可知,在超声-弱碱协同作用5,20,40,60和90 min后,竹材木质素样品L1~L5的得率随作用时间而逐步提高,而对照组L6在无超声作用条件下抽提90 min,其得率仅为3.9%,表明超声作用可显著提升竹材木质素的溶出效率。

表1 巨龙竹木质素样品的得率
2.2 红外光谱分析
木质素L1~L6红外光谱结果如图1所示,红外光谱中各个信号峰参照相关文献进行标识[7-9]。从图1可见,6个木质素样品的红外光谱吸收峰都极为相似,只在吸收强度上略有不同。L6作为对照组没有进行超声处理,但其与其他5个样品在超声-弱碱协同作用下抽提得到的竹材木质素的红外吸收峰并没有太大差异,这也间接说明了超声处理除对木质素组分起促溶作用外,并未显著改变木质素的化学结构。

图2 木质素L2、L5的13C NMR谱Fig. 2 13C NMR spectra of L2 and L5


图1 巨龙竹木质素组分的红外光谱图Fig. 1 FTIR spectra of lignin fractions isolated from Dendrocalamus sinicus
2.3 核磁共振碳谱分析
为了进一步研究木质素大分子的整体结构信息,对巨龙竹木质素样品L2和L5进行了核磁共振碳谱分析,测定结果如图2。木质素13C NMR图中相关信号峰对照文献进行了相关归属[10-13]。从巨龙竹木质素样品L2和L5的核磁共振碳谱图可看出,化学位移(δ)172.1处的信号峰是由脂肪酸中的—COOH形成的,可能源自提取过程中部分水解的乙酰基。δ104~168为木质素特征峰区,δ168.1,159.7,144.1,130.1,125.2,115.8和115.5处分别代表对香豆酸酯(pCA)的 C-γ、C-4、C-α、C-2/C-6、C-1、C-β和C-β,从13C NMR图谱中也能看出对香豆酸脂的信号峰很强,说明巨龙竹木质素中对香豆酸酯的含量较高。木质素L2和L5的13C NMR图谱中均出现明显的愈创木基单元(G)、紫丁香基单元(S)以及对羟基苯基单元(H)信号峰。其中,S型结构单元对应的信号峰有δ152.1 (C-3/C-5,醚化),132.2 (C-1,非醚化)和104.2 (C-2/C-6,醚化),G型结构单元对应的信号峰有δ149.1(C-3,醚化和非醚化),145.4 (C-4,非醚化的)和111.1 (C-2),H型结构单元C-2/C-6信号峰在δ128.3,C-3/C-5结构的相关信号峰出现在δ114.7处,相对较弱的信号说明其在木质素大分子中含量较低。上述信号进一步证实了巨龙竹木质素属于GSH型木质素。
在侧链信号区,β-O-4′结构信号位于δ72.2 (C-α)和δ60.0 (C-γ);β-β′联接结构的信号位于δ71.3(C-γ)。而愈创木基(G)或紫丁香基(S)的甲氧基出现在δ56.0强信号处。此外,δ90~102处无无任何信号峰,表明该木质素糖含量极少。
2.4 二维碳氢相关核磁共振谱图分析
为了深入解析木质素化学结构特征,在一维核磁基础上,本研究利用二维核磁共振(HSQC)样品进行分析。需要说明的是,在一般情况下,木质素样品进行核磁表征时,会将木质素样品进行乙酰化处理,以提高木质素在溶剂中的溶解度。但经该预处理后,木质素样品中一些本身的酰化结构会因乙酰化处理而被掩盖,从而导致天然木质素的固有酰化结构无法被检测和区分出来。故本实验对所得样品并没有进行乙酰化处理,而是直接将其溶于氘代试剂进行测试。巨龙竹木质素样品L2、L5的二维核磁共振(HSQC)图谱如图3。各相关信号峰的归属参照文献[12-16]进行,结果见表2。
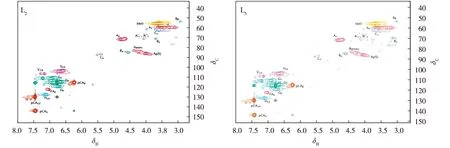
图3 L2、L5的HSQC谱图Fig. 3 HSQC-NMR spectra of lignin sample L2 andL5

信号δC/δH归属Bβ536/303Cβ⁃Hβinβ⁃β′(resinol)substructures(B)MeO556/370C⁃HinmethoxylsAγ597/322Cγ⁃Hγinβ⁃O⁃4′substructures(A)Cγ622/367Cγ⁃Hγinphenylcoumaransubstructures(C)Bγ709/379Cγ⁃Hγinβ⁃β′resinolsubstructures(B)A′γ(A″γ)711/416Cγ⁃Hγinγ⁃acylatedβ⁃O⁃4′substructures(A′andA″)Aα716/485Cα⁃Hαinβ⁃O⁃4′substructureslinkedtoaSunit(A,A′)Aβ(G/H)836/424Cβ⁃Hβinβ⁃O⁃4′substructureslinkedtoaGunitandHunit(A)Bα849/464Cα⁃Hαinβ⁃β′(resinol)substructures(B)Aβ(S)859/409Cβ⁃Hβinβ⁃O⁃4′substructureslinkedtoaSunit(A)Cα868/549Cα⁃Hαinphenylcoumaransubstructures(C)S2,61038/668C2,6⁃H2,6inetherifiedsyringylunits(S)S′2,61066/718C2,6⁃H2,6inoxidized(CαO)phenolicsyringylunits(S′)G21109/700C2⁃H2inguaiacylunits(G)G51157/681C5⁃H5inguaiacylunits(G)pCAβ1154/628Cβ⁃Hβ,p⁃coumaroylatedsubstructures(pCA)G61191/672C6⁃H6,Gunits(G)FA61225/705C6⁃H6inFAH2,61277/716C2,6⁃H2,6inHunits(H)pCA2,61299/747C2,6⁃H2,6,p⁃coumaroylatedsubstructures(pCA)pCAα1440/746Cα⁃Hα,p⁃coumaroylatedsubstructures(pCA)
注:(A)β-O-4′醚键结构,γ位为羟基;(A′)β-O-4′醚键结构,γ位为乙酰基;(A″)β-O-4'醚键结构,γ位为酯化对羟基苯甲酸酯;(B)树脂醇结构,由β-β′、α-O-γ′和γ-O-α′联接而成;(C)苯基香豆满结构,由β-5′和α-O-4′联接而成;(G)愈创木基结构;(S)紫丁香基结构;(S′)氧化紫丁香基结构,α位为酮基;(H)对羟苯基结构;(pCA)酯化的对香豆酸单元;(FA)阿魏酸酯结构。下同。
木质素基本单元之间联接方式的重要特征信号主要集中在二维HSQC谱图的侧链区(化学位移δC/δH40~100/2.5~6.0),其中,以β-O-4′芳基醚键结构和甲氧基(δC/δH55.6/3.70)的信号最强。β-O-4′结构(A、A′和A″)中α、γ位相关信号出现在化学位移δC/δH71.6/4.85和71.1/4.15,S型β-O-4′结构β位信号在δC/δH85.9/4.09,G/H型β位的信号出现在δC/δH83.6/4.24,γ位信号出现在δC/δH59.7/3.2。β-β′结构(树脂醇B)的α位信号出现在化学位移δC/δH84.9/4.65,γ信号出现在δC/δH70.9/3.79,β位信号出现在δC/δH53.6/3.03。β-5′结构(C,苯基香豆满)α、γ位的相关信号分别出现在δC/δH86.8/5.49和62.2/3.67。结合L2和L5的二维HSQC谱图可知,巨龙竹木质素β-O-4′和β-β′结构的信号较强,而β-5′结构信号较弱,说明巨龙竹木质素中的主要联接键为β-O-4′和β-β′结构,另外还含有少量的β-5′结构。
从二维HSQC图谱中的芳环区(化学位移δC/δH100~160/6.0~8.5)可检测到巨龙竹木质素大分子基本机构单元紫丁香基结构(S)、愈创木基结构(G)、对羟基苯基结构(H)的相关信号以及对香豆酸(pCA)和少量阿魏酸(FA)的信号。其中,紫丁香基(S)结构单元C2,6-H2,6信号位于δC/δH103.8/6.68,α位氧化的紫丁香基结构(S′)C2,6-H2,6信号位于δC/δH106.6/7.18;愈创木基(G)结构单元的C2-H2、C5-H5、C6-H6信号分别位于δC/δH110.9/7.00、115.7/6.81、119.1/6.72;对羟基苯基(H)结构单元的C2, 6-H2, 6信号位于δC/δH127.7/7.16。此外,酯化的对香豆酸酯信号在HSQC图谱中也较明显,其C2,6-H2,6信号位于129.9/7.47,侧链Cα和Cβ的信号分别位于144.0/7.46、115.4/6.28。
由图3比较可知,L2和 L5中各结构单元的相关信号强弱程度基本一致,再次表明超声处理不会明显打断巨龙竹木质素大分子中的各种联接键。
综合红外光谱和核磁共振谱图综合分析结果可以看出,巨龙竹木质素属于禾草类木质素(GSH型),其大分子中可能存在的基本结构单元及主要联接结构如图4所示。
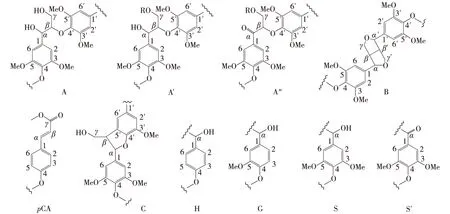
图4 巨龙竹木质素结构单元及主要联接结构Fig. 4 Main substructures presented in lignin fractions isolated from Dendrocalamus sinicus
3 结 论
1)弱碱条件下,超声处理能有效促进竹材木质素溶出。在2.0% NaOH 水溶液中从竹材中提取木质素,超声协同处理5,20,40,60和90 min以及对照组仅抽提90 min时,竹材木质素的溶出率分别为6.6%,14.9%,16.0%,20.7%,22.9%和3.9%,木质素得率随超声处理时间延长而增加。
2)巨龙竹木质素大分子主要由愈创木基(G)、紫丁香基(S)和对羟基苯基(H)结构单元构成,属于典型的禾草类木质素(GSH型)。
3)巨龙竹竹材木质素大分子的主要联接键为β-O-4′醚键,其次是β-β′和β-5′结构,超声处理对木质素结构破坏较小,所得的木质素样品较完整的保存了竹材木质素的天然结构特征。
[1]LEOPOLD B, MALMSTROM I L. Studies on lignin. IV. Investigation on the nitrobenzene oxidation products of lignin from different woods by paper partition chromatography[J]. Acta Chemica Scandinavica, 1952, 6(1):49-54.
[2]LU F, RALPH J. Non-degradative dissolution and acetylation of ball-milled plant cell walls:high-resolution solution-state NMR [J]. The Plant Journal, 2003, 35(4):535-544.
[3]LI M F, SUN S N, XU F, et al. Ultrasound-enhanced extraction of lignin from bamboo (Neosinocalamusaffinis):characterization of the ethanol-soluble fractions[J]. Ultrasonics Sonochemistry, 2012, 19(2):243-249.
[4]YANG D, ZHONG L X, YUAN T Q, et al. Studies on the structural characterization of lignin, hemicelluloses and cellulose fractionated by ionic liquid followed by alkaline extraction from bamboo[J]. Industrial Crops and Products, 2013, 43:141-149.
[5]WEN J L, XUE B L, XU F, et al. Unmasking the structural features and property of lignin from bamboo[J]. Industrial Crops and Products, 2013, 42:332-343.
[6]黄曹兴, 何娟, 闵斗勇,等. 稀硫酸预处理对毛竹竹黄木质素结构的影响[J]. 林业工程学报, 2016, 1(1):55-60. HUANG C X, HE J, MIN D Y et al. Effect of dilute acid pretreatment on the lignin structure of Moso bamboo inner skin[J]. Journal of Forestry Engineering, 2016, 1(1):55-60.
[7]MARQUES A V, PEREIRAL H, RODRIGUES J, et al. Isolation and comparative characterization of Björkman lignin from the saponified cork of Douglas-fir bark[J]. Journal of Analytical and Applied Pyrolysis, 2006, 77(2):169-176.
[8]XU F, SUN R C, SUN J X , et al. Determination of cell wall ferulic andp-coumaric acids in surgarcane bagasse[J]. Analytia Chimica Acta, 2005, 552(2):207-217.
[9]孙勇, 张金平, 杨刚,等. 二氧化氯氧化云杉木质素的光谱研究[J]. 光谱学与光谱分析, 2007, 8(27):1551-1554. SUN Y,ZHANG J P, YANG G,et al. Study on the spectra of spruce lignin with chlorine dioxide qxidation[J]. Spectroscopy and Spectral Analysis, 2007, 8(27):1551-1554.
[10]XU F, GENG C Z, LIU C F, et al. Structural characterization of residual lignins isolated with cyanamide-activated hydrogen peroxide from various organosolvs pretreated wheat straw[J]. Journal of Applied Polymer Science, 2008, 552(2):555-564.
[11]CAPANEMAL E A, BALASKSHIN M Y, KADLA J F. Quantitative characterization of a hardwood milled wood lignin by nuclear magnetic resonance spectroscopy [J]. Journal of Agricultural and Food Chemistry, 2005, 53(25):9639-9649.
[12]SUN X F, XU F, SUN R C, et al. Characteristics of degraded lignins obtained from steam exploded wheat straw[J]. Polymer Degradation and Stability, 2004, 86(2):245-256.
[13]史正军. 甜龙竹及巨龙竹半纤维素、木质素结构诠释及相互间化学键合机制解析[D]. 北京:北京林业大学, 2013. SHI Z J. Structural characterization of hemicelluloses and lignin, and their inter-linkages inDendrocalamusbrandisiiandDendrocalamussinicus[D]. Beijing:Beijing Forestry University, 2013.
[14]MARTINEZ A T, RENCORET J, MATQUES G, et al. Monolignol acylation and lignin structure in some nonwoody plants:a 2D NMR study[J]. Phytochemistry, 2008, 69(16):2831-2843.
[16]RENCORET J, MATQUES G, GUTIERREZ A, et al. HSQC-NMR analysis of lignin in woody (EucalyplusglobulusandPiceaabies) and non-woody (Agavesisalana) ball-milled plant materials at the gel state [J]. Holzforschung, 2009, 63(6):691-698.
Isolation and structural characterization of lignin isolated fromDendrocalamussinicusby ultrasonic-alkaline treatment
DENG Jiawen1, YANG Haiyan1△, SHI Zhengjun1*, DENG Jia2,YANG Jing1, ZHENG Zhifeng1, HUI Chaomao2
(1. University Key Laboratory of Biomass Chemical Refinery & Synthesis, Southwest Forestry University, Kunming 650224, China; 2. Key Laboratory for Forest Resources Conservation and Use in the Southwest Mountains of China, Southwest Forestry University, Kunming 650224, China)
In response to the severe challenges of resource scarcity and energy shortage, the preparation of biobased materials, energy and chemicals has attracted increasing attention. Fractionation of lignocelluloses based on the concept of biorefinery is of vital importance for their effective utilization.Dendrocalamussinicus, belonging to Bambusoideae of Gramineae, has strong and woody stems (maximum diameter of 30 cm, maximum height of 33 m). It is the largest bamboo species in the world and widely distribute in the southwest of China. According to whether the bottom ofD.sinicusbends or not, it can be divided into two subspecies, straight-barD.sinicusand askewD.sinicus. Due to its easy propagation, fast growth and high productivity, the bamboo species is considered as a potential renewable non-woody forestry feedstock for the production of biofuel and biomaterials. However, the detailed physicochemical properties of the largest bamboo species have not been clarified so far. In this study, five soluble lignin fractions (L1, L2, L3, L4and L5) were isolated under the ultrasonic-alkaline (2% NaOH) combined treatment for 20, 40, 60 and 90 min, respectively. In addition, another bamboo lignin fraction (L6) was isolated by 2% NaOH without ultrasonic treatment as control. Isolated lignin samples were characterized by FTIR,13C NMR and 2D HSQC NMR. The results showed that the ultrasonic-alkaline combined treatment could promote bamboo lignin dissolution. The obtained bamboo lignin belongs to GSH-type lignin, consisting syringl (S), guaiacyl (G) and p-hydroxylphengl (H) units. The major inter-unit linkages presented in the obtained bamboo lignin wereβ-O-4′ aryl ether linkages,β-β′, andβ-5′ linkages. With the increased of ultrasonic treatment time, the yield of lignin increased from 6.6% to 22.9%, and a certain amount ofβ-O-4′ linkages were degraded. The results of present study provided useful information for the selection and evaluation to superior germplasm resources.
Dendrocalamussinicus; lignin; ultrasonic-alkaline treatment; structural characterization
2016-06-15
2016-09-30
国家自然科学基金(31260165,31560195);云南省科技计划项目(2015FD023)。
邓嘉雯,女,研究方向为竹类资源的开发利用。杨海艳为共同第一作者。通信作者:史正军,男,博士,副教授。E-mail:shizhengjun1979@163.com
TQ35
A
2096-1359(2017)02-0064-06
