注射用替加环素无菌方法适用性实验的研究
2017-04-21陈伟娜王燕清陈嘉璐
陈伟娜 王燕清 陈嘉璐
[摘要]目的建立注射用替加环素无菌的方法适用性。方法用100mL 0.1%的MgCh溶液冲洗后,再用700mL pH 7.0含0.1%吐温-80的0.1%无菌蛋白胨溶液冲洗,以消除替加环素样品的抑菌活性,进行注射用替加环素的细菌及真菌的无菌验证。结果采用上述方法进行验证,6种菌的供试品与阳性对照生长状况一致。结论注射用替加环素的无菌检验,需要用100mL 0.1%的MgCl2溶液冲洗后,再用700mL pH7.0含0.1%吐温-80的0.1%无菌蛋白胨溶液冲洗。
[关键词]注射用替加环素;无菌检查;方法适用性;MgCh;吐温-80
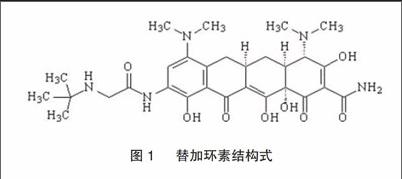
替加环素由惠氏(Wyeth)公司研发,美国FDA于2005年6月和2006年7月批准惠氏的替加环素(Tigecycline,商品名Tygacil注射用替加环素)为治疗复杂腹腔内感染和复杂皮肤感染的一线药物,其化学结构式见图1。该品种是甘氨酰四环素类抗生素中获得批准的第一个产品。替加环素对G+菌、G-菌、厌氧菌有广谱抗菌活性,包括多重耐药性的G+菌,如MRSA、MRSE、抗青霉素的肺炎链球菌、VRE。对不同耐药机制的耐四环素致病菌同样有效,但对铜绿假单胞菌无抗菌活性。替加环素是新型甘胺酰环素类抗生素,主要与细菌核糖体30S亚基结合,阻碍氨基酸肽延长,从而抑制细菌蛋白质合成来发挥抗菌活性。他克服或限制了很多抗菌药物产生的两种主要耐药机制:外排泵和核糖体保护。避免了四环素类抗生素耐药机制对其产生作用。
为消除本品的抑菌活性,在无菌方法学验证中,本研究采用了多种样品处理办法,包括添加高锰酸钾溶液、硫酸铜溶液、柠檬酸钠溶液、氯化镁溶液、0.1%吐温-80等,结果表明:以高锰酸钾溶液、硫酸铜溶液、柠檬酸钠溶液处理样品,均不能有效消除本品的抑菌活性;注射用替加环素进口注册标准中采用的氯化镁溶液及0.1M的HCl溶液处理样品能消除样品抑菌活性,但验证表明,该操作中用到0.1M盐酸,对试验菌有灭活作用;0.1%吐温-80处理样品,能有效消除本品的抑菌活性,而且对试验菌无灭活作用。因而最终采用薄膜过滤法,用100mL 0.1%的MgCl.溶液冲洗后,再用700mLpH 7.0含0.1%吐温-80的0.1%无菌蛋白胨溶液冲洗。
1.材料
1.1实验器材
HTY-SPA型无菌隔离仓(杭州泰林生物技术设备有限公司),BKF330型全封闭集菌培养器(杭州泰林生物技术设备有限公司),LRH-250A型生化培养箱(广东医疗器械厂)。
1.2样品
注射用替加环素(规格为40mg/瓶),由丽珠医药集团研究所提供。
1.3培养基及冲洗液
培养基:硫乙醇酸盐流体培养基、胰酪大豆胨培养基、胰酪大豆胨琼脂培养基、沙氏葡萄糖培养基、沙氏葡萄糖琼脂培养基,均购自广东环凯微生物有限公司。培养基适用性符合《中国药典》2015版,四部(通则1101)规定。
冲洗液:pH7.0含0.1%吐温80的0.1%蛋白胨水溶液。
1.4试验用菌种
金黄色葡萄球菌(staphvlococcus aureus)[CMCC(B)26003];枯草芽孢杆菌(bacillus subtilis)[CMCC(B)63501];铜绿假单胞菌(pseudomonas aeruginosa)[CMCC(B)10104];生孢梭菌(clostridium sporogenes)[CMCC(B)64941];白念珠菌(candida albicans)[CMCC(F)98001];黑曲霉菌(aspergillus niger)[CMCC(F)98003]。菌种均来自中国食品药品检定研究院医学菌种保藏中心。
2.方法与结果
参照2015版《中国药典》方法及注射用替加环素进口注册标准。
2.1菌液制备
参照《中国药典》2015版四部通则1101无菌检查法操作,取30~35℃培养24h的铜绿假单胞菌、金黄色葡萄球菌、枯草芽孢杆菌的胰酪大豆胨培养物和生孢梭菌的硫乙醇酸盐流体培养物,用0.9%无菌氯化钠溶液稀释得到10~100CFU/mL的菌悬液,备用。取20~25℃培养48h的白色念珠菌的沙氏葡萄糖培养物,用0.9%无菌氯化钠溶液稀释得到10~100CFU/mL的菌悬液,备用。取20~25℃培养6d黑曲霉的新鲜培养物,加入0.05%聚山梨酯80的0.9%无菌氯化钠溶液4mL洗下孢子,吸出转移至空试管作为原液,用含有0.05%聚山梨酯80的0.9%无菌氯化钠溶液稀释,得到10~100CFU/mL的孢子悬液,备用。
2.2试验步骤
因为替加环素对真菌没有抑菌活性,所以在方法學摸索的过程中只选取细菌及厌氧菌进行验证,而且,为了降低工作量,细菌先用枯草芽孢杆菌做代表,待方法确定后,再进行6种菌的验证,具体步骤如下。
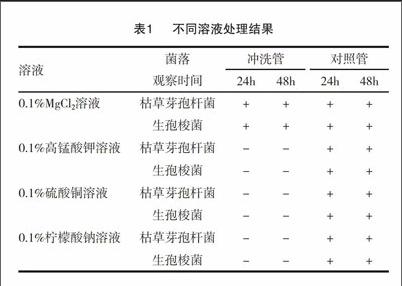
2.2.10.1%MgCI2溶液消除抑菌能力的考察参考注射用替加环素进口注册标准,同时为了保证滤膜的冲洗体积不超过800mL,将0.1%MgCL2溶液的体积由750mL改为100mL,0.1M的HCL溶液的体积由750mL改为400mL,具体方法如下:取供试品10瓶/菌,以约50mL无菌氯化钠溶液溶解并转移至全封闭集菌培养器中,每菌用0.1%MgCL,溶液lOOmL冲洗后,用0.1M的HCL溶液400mL冲洗,最后用300mL的0.1%无菌蛋白胨溶液冲洗,冲洗后在滤膜上加lmL 10~100CFU/mL的菌悬液,过滤后取出滤膜,于胰酪大豆胨琼脂培养基中30~35℃培养。同时,分别用0.1%高锰酸钾溶液、0.1%硫酸铜溶液、0.1%柠檬酸钠溶液代替0.1%MgCL2溶液,方法同上,考察其他中和剂抑菌作用,见表1。
结果可见,唯有0.1%MgCl溶液能够消除注射用替加环素的抑菌作用。
为了考察处理用溶液对菌液的影响,我们用10~IOOCFU的菌液代替供试品溶液,方法同上,由表2结果可知,0.1M的HCl溶液对细菌的生长有抑制作用。
2.2.2冲洗液的确定 参考我们在做该产品原料微生物限度验证时的经验,并结合以上试验结果,拟对试验进行调整:取供试品10瓶/菌,以约50mL无菌氯化钠溶液溶解并转移至全封闭集菌培养器中,每菌分别用700mLpH 7.0含0.1%及0.3%的吐温80的0.1%无菌蛋白胨溶液冲洗后,在滤膜上加1mL 10~100CFU/mL的菌悬液,过滤后取出滤膜,于胰酪大豆胨琼脂培养基中30~35℃培养。同时为了考察处理用溶液对菌液的抑菌作用,用10~100CFU的菌液代替供试品,同法操作(注:最后过滤后不再加菌液),由表3可知,用700mL的0.1%及0.3%的吐温80的0.1%无菌蛋白胨溶液替代400mL 0.1MHCL溶液和300mL 0.1%无菌蛋白胨溶液组合作为冲洗液,能够符合无菌验证的要求,而且,为了试验方便,最终选择0.1%的吐温80的0.1%无菌蛋白胨溶液。
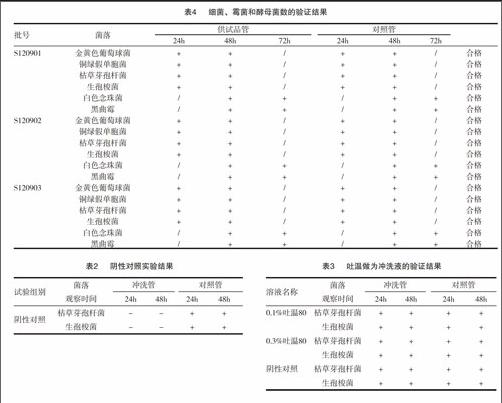
2.2.3方法适用性实验的确定 用以上确定的方法,进行细菌、真菌的验证。细菌验证采用薄膜过滤法,取供试品10瓶/菌,以约50mL无菌氯化钠溶液溶解并转移至全封闭集菌培养器中,每菌用100mL 0.1%的MgCL2溶液冲洗后,再用700mL pH7.0含0.1%吐温-80的0.1%无菌蛋白胨溶液冲洗,冲洗后注入100mL硫乙醇酸盐流体培养基,并加入1mL试验菌菌液,摇匀;另取一装有同样体积培养基的滤筒,加入等量的试验菌,摇匀,作为对照菌液。置30~35℃生化培养箱中培养48h,结果见表4。霉菌、酵母菌验证采用薄膜过滤法,按上述同法操作,冲洗后注入100mL沙氏葡萄糖培养基,并加入1mL试验菌菌液,摇匀;另取一装有同样体积培养基的滤筒,加入等量的试验菌,摇匀作为对照菌液。置23-28℃生化培养箱中培养72h。见表4。
2.3试验结果
验证结果表明:与阳性对照比较,含供试品各容器中的试验菌均生长良好。以该法操作,能够消除替加环素样品的抑菌活性,方法可行。
即采用薄膜过滤法,取供试品10瓶/菌,以约50mL无菌氯化钠溶液溶解并转移至全封闭集菌培养器中,每菌用lOOmL 0.1%的MgCl.溶液冲洗后,再用700mL pH 7.0含0.1%吐温-80的0.1%无菌蛋白胨溶液冲洗,冲洗后注入100mL硫乙醇酸盐流体培养基或沙氏葡萄糖培养基,并加入lmL试验菌菌液,分别培养。
3.讨论
因替加环素对G+菌、G-菌、厌氧菌有广谱抗菌活性,包括多重耐药性的G+菌,如MRSA、MRSE、抗青霉素的肺炎链球菌、VRE,所以不能使用常规方法进行无菌的方法适用性实验。注射用替加环素的进口注册标准JX20100227已有无菌验证方法,但其存在一定的问题:(1)冲洗液体积过多,其采用750mL 0.1%的MgCL.溶液冲洗后再用750mL的0.1M的HCL溶液,最后再用300mL的0.1%无菌蛋白胨溶液冲洗,总冲洗体积达到1800mL;(2)0.1M的HCL溶液对试验菌有抑菌活性,阴性对照实验中,菌液不生长。
在药品无菌、微生物限度检查等实验中,对于抑菌性供试品可以使用适宜的中和剂消除抑菌成分,使用的中和剂不应与培养基发生反应,不应改变培养基原有性状,不应对结果判断产生影响。MgCl.溶液作为无菌验证中的中和剂,在有抑菌作用的药物应用广泛。在稀释液、冲洗液添加Mg2+作為中和剂,与培养基中的添加应用不同。稀释液、冲洗液为一过性使用,即样品制备、作用一定时间后,可以采用适宜的方法去除,从而消除其可能对实验带来的影响。实验结果显示,Mg2+作为小分子的无机化合物,极易通过滤膜,稍加冲洗,即可去除。
当药品本身具有抗菌活性时,应当首先消除其抗菌活性,才能保证检验结果的真实性和有效性。对于一些抑菌活性较强的抗生素,要消除其抑菌活性,可在冲洗液中加入一定浓度的吐温80。本研究参考了原料微生物限度验证时的经验,对吐温80的浓度进行了摸索,确定了该产品验证时的吐温浓度为0.1%。
本方法结合了进口注册标准中的MgCl2溶液的中和作用,同时增加了pH 7.0含0.1%吐温-80的0.1%无菌蛋白胨溶液作为冲洗液,该方法验证6种菌均符合规定,方法可行。
