碱液处理对荞麦淀粉物理性能和结构的影响
2017-04-14许杨杨朱轶群曹晓虹韩立宏
王 琳,许杨杨,朱轶群,焦 芮,曹晓虹,韩立宏,*
(1.北方民族大学生物科学与工程学院,宁夏银川 750021;2.合肥工业大学食品科学与工程学院,安徽合肥 230009)
碱液处理对荞麦淀粉物理性能和结构的影响
王 琳1,许杨杨1,朱轶群1,焦 芮2,曹晓虹1,韩立宏1,*
(1.北方民族大学生物科学与工程学院,宁夏银川 750021;2.合肥工业大学食品科学与工程学院,安徽合肥 230009)
通过考察荞麦淀粉的表观直链淀粉含量、膨胀度和溶解度,借助快速粘度仪、差示量热扫描仪、X-射线衍射仪、扫描电子显微镜分析荞麦淀粉的糊化特性、热特性、晶型结构和颗粒表面形态,研究了不同质量分数碱液提取对荞麦淀粉物理性能和结构的影响。结果表明,当碱液质量分数达到0.18%左右时,提取荞麦淀粉的表观直链淀粉含量最大;当碱液质量分数小于0.24%时,碱处理不会对荞麦淀粉糊化焓产生显著影响,也不会造成淀粉颗粒形态及内部结构的显著破坏。碱液提取法可用于荞麦淀粉的制备,但应控制碱液质量分数不能超过0.24%。
荞麦淀粉,碱液,糊化特性,热特性,颗粒结构
荞麦(Fagopyrum)又名三角麦,属于双子叶廖科(Polygonaceae)禾谷类作物,主要有甜荞(FagopyrumescμLentum Moench)和苦荞(Fagopyrumtataricum(Linn)Gaench)两个栽培品种,具有优异的营养及药用价值[1-3]。荞麦富含60%~70%淀粉,荞麦淀粉具有较高的峰值粘度、水合能力和较低的溶解性,与其他谷物不同的是荞麦中含有7.5%~35%的具有生理功能和食品加工性能的抗性淀粉[4]。荞麦淀粉的开发利用将不断受到消费者和食品加工业的高度关注。
碱液提取法是目前最常用的淀粉制备方法,但是碱处理可以不同程度改变淀粉颗粒的片晶结构[5-6]、物理特性[5-7]和消化性能[6,8]等,淀粉的碱敏感性与其来源和品种直接相关[9]。目前还没有关于碱液提取法制备荞麦淀粉的公开研究报道,本研究采用不同浓度的NaOH溶液浸泡荞麦粉提取荞麦淀粉,通过测定与分析荞麦淀粉的表观直链淀粉的含量、膨胀度、溶解度、热特性、糊化特性、颗粒形态结构等,探索荞麦淀粉的碱敏感性,进而判断碱提取法是否适用于荞麦淀粉的制备,为荞麦的精深加工及荞麦淀粉的工业化提供理论依据。
1 材料与方法
1.1 材料与仪器
荞麦米 山逗子荞麦,购自银川新华百货连锁超市;氢氧化钠、戊二醛、磷酸、乙醇、叔丁醇 均为分析纯,购自Sigma-Aldrich公司。
GL-20B高速冷冻离心机 中国上海安亭科学仪器厂;RVA3-D快速粘度分析仪 澳大利亚Newport科学仪器公司;TA.XTplus物性仪 英国Stable Micro System公司;S-3000N扫描电子显微镜 日本日立公司;D/max-2550 PC型X射线衍射仪 日本Rigku公司;PL203电子天平 梅特勒-托利多仪器(上海)有限公司。
1.2 实验方法
1.2.1 荞麦淀粉的提取 荞麦米去离子水室温浸泡6 h,料液质量比(1∶2)胶体磨粉碎,过100目筛除皮,筛下物4000×g离心10 min,沉淀物真空冷冻干燥,得荞麦粉。取18 g干燥荞麦粉在不同质量分数(0.00%、0.06%、0.12%、0.18%、0.24%、0.30%)的NaOH溶液中浸泡24 h(4 ℃),每隔30 min搅拌一次。然后,将混合物在1800×g条件下离心10 min,弃去上清液,刮掉沉淀上层的深色物质,剩余物用去离子水反复洗涤离心至其显中性(用酚酞作指示剂),冷冻干燥即得荞麦淀粉。
1.2.2 表观直链淀粉含量测定 表观直链淀粉的测定参照McGrance等的方法[10]。1 g(干基)荞麦淀粉样品加入2 mL DMSO(二甲基亚砜),85 ℃水浴中振荡15 min,取出冷却,去离子定容至25 mL。然后,取1 mL淀粉溶液用去离子水定容至25 mL,加入2.5 mL碘液,在600 nm处使用紫外可见分光光度计测定其吸光度。每个样品重复3次。
1.2.3 膨胀度和溶解度测定 精确称量淀粉样品0.100 g(干基)置于15 mL容积的离心管中,加入10 mL去离子水,80 ℃水浴振荡30 min,冰水浴冷却至室温,4000×g条件下离心10 min,沉淀(湿淀粉,质量为M)和上清液分别在110 ℃条件下干燥至恒重,即得干燥淀粉沉淀的质量(M1)和溶解淀粉的质量(M2)。每个样品重复3次。淀粉的膨胀度和溶解度分别表示为:


1.2.4 糊化特性分析 荞麦淀粉糊化特性分析参照顾娟等[11]的方法,采用快速粘度分析(RVA)法进行测定。将25.5 g 去离子加入到干淀粉样品中,使粘度仪铝盒中样品总重量为28 g。测定程序为:以12 ℃/min的速度从50 ℃升温到95 ℃,在95 ℃条件下保持2.5 min后,再以12 ℃/min的速度从95 ℃冷却到50 ℃,记录整个过程中淀粉糊的RVA特征曲线变化。每个样品重复3次。记录整个过程中淀粉糊的RVA特征曲线变化。每个样品重复3次。
1.2.5 热特性测定 荞麦淀粉热特性测定参考于颖等[12]的方法,采用差示扫描量热仪评价淀粉热特性变化。含75%去离子水的淀粉浆测试前20 ℃条件下平衡48 h。加热速率10 ℃/min,温度范围为20 ℃至120 ℃,计算淀粉糊化初始温度、峰值温度、终止温度以及焓值。每个样品重复3次。
1.2.6 X射线衍射 样品的X射线衍射采用Rigku-D/max-2550/PC X射线衍射仪测定。测定条件:采用铜Kα辐射,电压40 kV,电流30 mA,2θ区域扫描的范围4.00°~40.00°,步长0.02°,积分时间2.00 s。淀粉结晶度由仪器按下式计算:
结晶度(%)=晶体衍射峰面积(kcps·deg)/[无定形峰面积(kcps·deg)+晶体衍射峰面积(kcps·deg)]×100
1.2.7 颗粒形态结构 取2 mg(干基)淀粉样品均匀涂抹在粘合金属胶带表面,喷金。然后使用扫描电子显微镜在15 kV加速电压下观察淀粉颗粒形态结构。
1.2.8 数据统计分析 所有实验数据结果均以3次平行实验的平均值表示,采用Origin Pro 7.5软件进行数据分析与作图。
2 结果与讨论
2.1 不同质量分数碱液处理对荞麦淀粉表观直链淀粉含量的影响
不同质量分数碱液处理对荞麦淀粉表观直链淀粉含量的影响如图1所示。从图1中可以看出,当碱液质量分数小于0.18%时,随着碱液质量分数增大,荞麦淀粉表观直链淀粉含量增大(p<0.05);当碱液质量分数大于0.18%时,荞麦淀粉表观直链淀粉含量随着碱液质量分数的增大而下降(p<0.05)。

图1 不同质量分数碱液处理对荞麦淀粉表观直链淀粉含量的影响Fig.1 Effects of sodium hydroxide solutions with different mass percentage on apparent amylose content of buckwheat starch注:不同字母表示差异显著(p<0.05),图2、图3同。
淀粉颗粒表面紧密连接着一些贮藏蛋白和结合蛋白,随着碱液浓度的增加,淀粉颗粒表面结合的蛋白质的去除率增大,可导致淀粉表观直链淀粉含量增大[13];但是,如果碱液浓度过大,则可引起淀粉颗粒在常温条件下发生糊化行为,使得淀粉颗粒内部的一些直链淀粉溶出到碱液中,而导致淀粉颗粒表观直链淀粉含量下降。
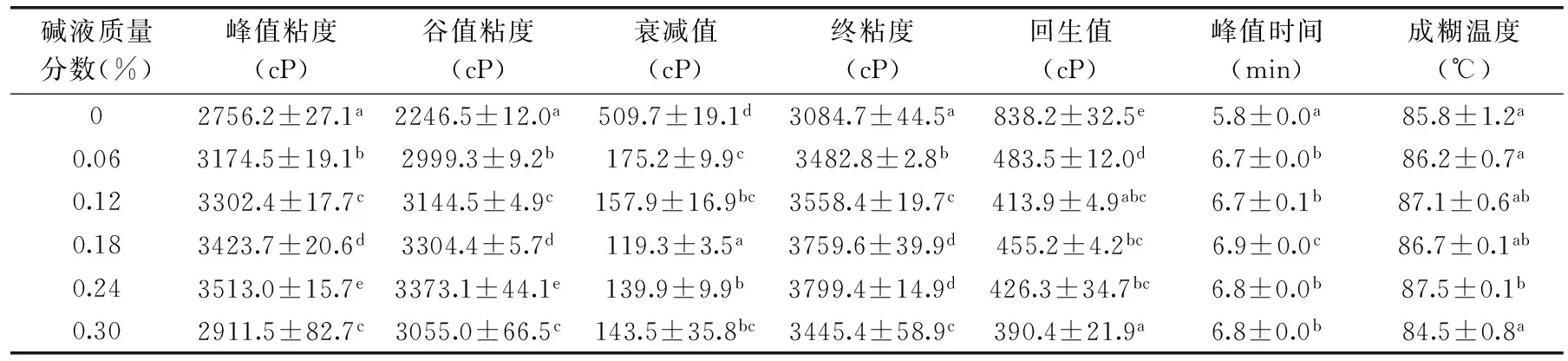
表1 不同质量分数碱液对荞麦淀粉糊特征值的影响
注:平均值±标准差(n=3),同列不同字母代表差异显著(p<0.05),表2同。
2.2 不同质量分数碱液处理对荞麦淀粉膨胀度和溶解度的影响
不同质量分数碱液对荞麦淀粉颗粒膨胀度和溶解度的影响分别如图2、图3所示。

图2 不同质量分数碱液处理对荞麦淀粉膨胀度的影响Fig.2 Effects of sodium hydroxide solutions with different mass percentage on the swelling power of buckwheat starch
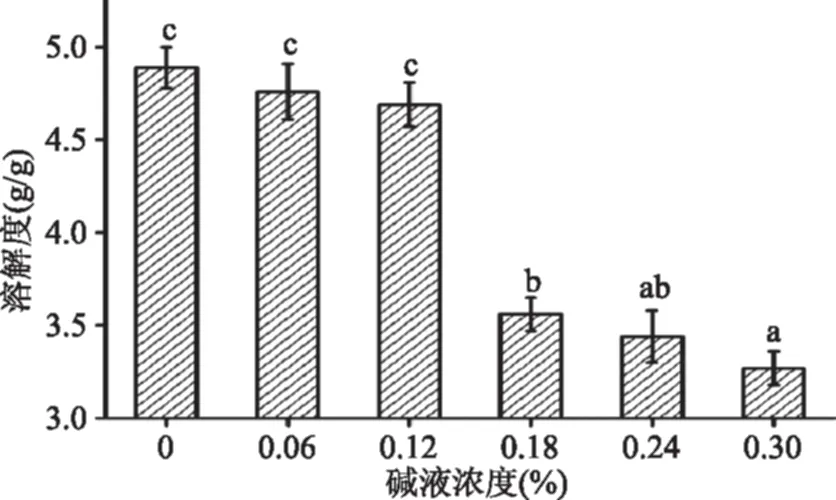
图3 不同质量分数碱液处理对荞麦淀粉溶解度的影响Fig.3 Effects of sodium hydroxide solutions with different mass percentage on the solubility of buckwheat starch
从图2、图3可以看出,碱液质量分数较低时,随着碱液质量分数增大,荞麦淀粉的膨胀度也随之增大;当碱液质量分数达到0.18%时,淀粉颗粒膨胀度随着碱液质量分数增大呈现下降趋势。碱液质量分数增大对淀粉颗粒溶解度的影响在碱液质量分数低时不显著,但当碱液质量分数达到0.18%时,淀粉颗粒溶解度显著减小(p<0.05)。
当淀粉颗粒在足量水中被加热时,颗粒晶体内起到稳定淀粉分子双螺旋结构作用的淀粉链段间氢键就会逐渐被破坏[14],淀粉颗粒的体积随着温度升高不断增大。大量研究表明,在淀粉颗粒内部直链淀粉没有充分溶出之前,谷物淀粉颗粒不会完全膨胀漰解,即直链淀粉对于抑制淀粉颗粒膨胀和维持膨胀淀粉颗粒的完整性至关重要[15]。其次,淀粉颗粒表面结合的蛋白质及脂类物质对淀粉颗粒的膨胀度也有一定程度的抑制作用。随着碱液浓度增大,一方面淀粉颗粒表面的蛋白质和脂类物质去除率增大[13],从而导致淀粉颗粒的膨胀度起初呈现显著增大(p<0.05)趋势;另一方面,较高浓度的碱液破坏淀粉颗粒的无定形区程度增大,会进一步促进淀粉颗粒中直链淀粉的溶出量增大,从而导致所提取的淀粉颗粒膨胀过程中的溶解度下降。
2.3 不同质量分数碱液处理对荞麦淀粉糊化特性的影响
淀粉的糊化特性参数是衡量淀粉加工使用性能的关键指标。淀粉一般在冷水中不溶,但当在水分存在条件下加热时,水分子逐渐进入到淀粉颗粒的内部,进而颗粒开始膨胀,直链淀粉不断溶出,淀粉分子与水分子之间形成氢键,淀粉悬浮液的粘度不断升高。不同质量分数碱液对荞麦淀粉糊化特征值的影响如表1所示。
从表1中可以看出,与对照相比(碱液质量分数为0),碱液提取处理使得荞麦淀粉糊化峰值粘度、谷值粘度和终粘度增大,但是当碱液质量分数达到0.30%时,荞麦淀粉峰值粘度、谷值粘度和终粘度均呈现显著下降趋势(p<0.05)。不同质量分数碱液处理使得荞麦淀粉的糊化衰减值和回生值显著降低(p<0.05)。碱处理使得荞麦淀粉的糊化峰值粘度升高的研究结果跟Lai等[16]报道的关于NaOH对谷物淀粉的糊化特性的影响的结果一致,这是因为淀粉的膨胀度在低于质量分数为0.18%碱液的处理下显著增大,而淀粉的膨胀度和糊化峰值粘度之间是呈显著正相关的[17]。
2.4 不同质量分数碱液处理对荞麦淀粉热特性的影响
不同质量分数的碱液对荞麦淀粉的糊化初始温度、峰值温度、终止温度及糊化焓的影响如表2所示。从表2可以看出,随着碱液质量分数增大,所得淀粉的糊化初始温度呈现显著增大的趋势,而峰值温度和终温度没有显著的规律性变化。荞麦淀粉的糊化焓随着处理碱液质量分数的增大呈现下降的趋势。
糊化焓是淀粉糊化之前淀粉颗粒内部分子链段有序性的衡量指标,它是反映淀粉颗粒结晶度的重要参数,淀粉颗粒有序结果破坏会导致糊化焓值下降[18]。当碱液质量分数达到0.24%时,荞麦淀粉的糊化焓相比对照显著降低,说明这个浓度的碱液已经对淀粉颗粒的结晶结构造成了破坏。
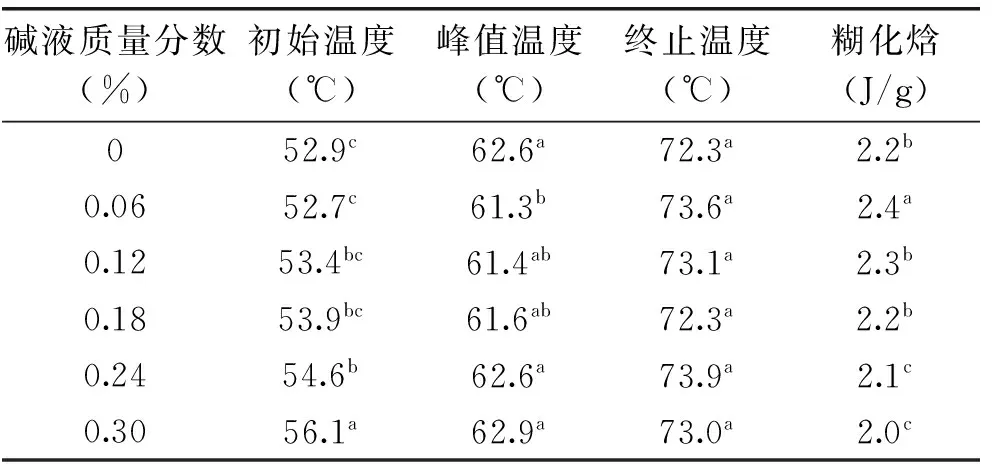
表2 不同质量分数碱液对荞麦淀粉热特性的影响
2.5 不同质量分数碱液处理对荞麦淀粉结晶结构的影响
不同质量分数碱液对荞麦淀粉结晶结构的影响如图5所示。从图5可以看出,碱处理不会改变荞麦淀粉的晶型结构。随着碱液质量分数增大,淀粉结晶度呈现出下降的趋势。当碱液质量分数达到0.24%左右时,淀粉结晶度相比其他低质量分数碱液处理及对照显著下降,说明质量分数为0.24%的NaOH溶液处理对淀粉颗粒的结晶结构造成了一定程度的破坏,这与不同质量分数碱液对荞麦淀粉热特性影响结果一致。

图5 不同质量分数碱液对荞麦淀粉X-射线衍射的影响Fig.5 Effects of sodium hydroxide solutions with different mass percentage on X-ray diffraction patterns of buckwheat starch
2.6 不同质量分数碱液处理对荞麦淀粉颗粒形态的影响
不同质量分数碱液对荞麦淀粉颗粒形态的影响如图6所示。从图6可以看出,未经过碱液处理的淀粉颗粒(A1、A2)有些黏连在一起,淀粉颗粒形状不规则。这可能是因为未经过碱液处理的淀粉颗粒表面黏附着大量蛋白质及脂类等物质,而使淀粉颗粒黏在一起。随着碱液质量分数不断增大(按B、C、E、F、G的顺序,碱液质量分数依次为0.06%、0.12%、0.18%、0.24%、0.30%),淀粉颗粒之间黏连的现象明显消失,淀粉颗粒形状呈多角形,而且淀粉颗粒表面的黏附物显著减少。当碱液质量分数达到0.24%及以上时,淀粉颗粒表面出现了明显的小洞,说明高质量分数碱液对淀粉颗粒的表面结构造成了破坏,这也再次充分证明上述关于淀粉热特性和结晶度随着碱液质量分数的升高而发生的变化。

图6 不同质量分数碱液对荞麦淀粉颗粒形态的影响Fig.6 Effects of sodium hydroxide solutions with different concentration on the surface microstructure of buckwheat starch注:A1未经碱液处理淀粉(×3000);A2未经碱液处理淀粉(×8000);B1 0.06%碱液处理淀粉(×3000);B2 0.06%碱液处理淀粉(×8000);C1 0.12%碱液处理淀粉(×3000);C2 0.12%碱液处理淀粉(×8000);E1 0.18%碱液处理淀粉(×3000);E20.18%碱液处理淀粉(×8000);F1 0.24%碱液处理淀粉(×3000);F2 0.24%碱液处理淀粉(×8000);G1 0.30%碱液处理淀粉(×3000);E2 0.30%碱液处理淀粉(×8000)。
3 结论
不同质量分数碱液处理会对荞麦淀粉物理特性造成显著影响。当碱液质量分数低于0.18%时,提取淀粉的直链淀粉含量随碱液质量分数的增大显著增大;质量分数小于0.24%的碱液,不会对淀粉糊化焓产生显著影响。X-射线衍射和扫描电子显微镜分析结果证明:质量分数小于0.24%的碱液不会对淀粉颗粒形态及内部结构产生显著破坏。碱液提取法可用于荞麦淀粉的制备,但应控制碱液质量分数不能超过0.24%。
[1]李晶,骆丽君,郭晓娜,等. 蒸制对冷冻荞麦熟面品质的影响研究[J]. 中国粮油学报,2016,31(2):9-12.
[2]郭春锋,李婧妍,张守文. 抗性淀粉生理功能研究进展[J]. 食品科技,2006(2):1-3.
[3]Levrat M A. Effectiveness of resistant starch,compared to guar gum,in depressing plasma cholesterol and enhancing fecal steroid excretion[J]. Lipids,1996,31:1069-1075.
[4]周一鸣,李保国,崔琳琳,等. 荞麦淀粉及其抗性淀粉的颗粒结构[J]. 食品科学,2013,34(23):25-27.
[5]Cai J,Yang Y,Man J,et al. Structural and functional properties of alkali-treated high-amylose rice starch[J]. Food Chemistry,2014,145(15):245-253.
[6]Wang S,Copeland L. Effect of alkali treatment on structure and function of pea starch granules[J]. Food Chemistry,2012,135(3):1635-1642.
[7]Paredes-Lópezb O,Bello-Péreza L A. Physicochemical and morphological characteristics of nixtamalized maize starch[J]. Starch/Stärke,2007,59(6):277-283.
[8]Wang S,Luo H,Zhang J,et al. Alkali-induced changes in functional properties andinvitrodigestibility of wheat starch:the role of surface proteins and lipids[J]. Journal of Agricultural and Food Chemistry,2014,62(16):3636-3643.
[9]Qiao D L,Yu L,Liu H SH,et al. Insights into the hierarchical structure and digestion rate of alkali-modulated starches with different amylose contents[J],Carbohydrate Polymers,2016,144(25):271-281.
[10]McGrance S J,Cornell H J,Rix C J A. simple and rapid colorimetric method for the determination of amylose in starch products[J]. StarchStarke,1998,50(4):158-163.
[11]顾娟,洪雁,顾正彪. 荞麦淀粉理化性质的研究[J]. 食品与发酵工业,2008,34(4):36-39.
[12]于颖,冯佳,徐桂花. 热处理对荞麦淀粉糊化特性的影响研究[J]. 粮食与食品工业,2010(2):32-35.
[13]罗明昌. 淀粉颗粒结合蛋白质研究进展[J]. 粮油加工,2007(2):111-114.
[14]Tester R F,Karkalas J. Swelling and gelatinization of oat starches[J]. Cereal Chemistry,1996,73(2):271-277.
[15]Karim A A,Nadiha M Z,Chen F K,et al. Pasting and retrogradation properties of alkali-treated sago(Metroxylon sagu)starch. Food Hydrocolloids,2008,22(6):1044-1053.
[16]Lai L N,Karim A A,Norziah M H,et al. Effects of Na2CO3and NaOH on pasting properties of selected native cereal starches[J]. Journal of Food Science,2004,69(4):249-256.
[17]Vandeputte G E,Vermeylen R,Geeroms J,et al. Rice starches. III. Structural aspects provide insight in amylopectin retrogradation properties and gel texture[J]. Journal of Cereal Science,2003,38(1):61-68.
[18]Thirathumthavorn D,Charoenrein S. Thermal and pasting properties of native and acid-treated starches derivatized by 1-octenyl succinic anhydride[J]. Carbohydrate Polymers,2006,66(2):258-265.
Effects of sodium hydroxide solutions physical on properties and structure of buckwheat starch
WANG Lin1,XU Yang-yang1,ZHU Yi-qun1,JIAO Rui2,CAO Xiao-hong1,HAN Li-hong1,*
(1.College of Biological and Engineering,Beifang University of Nationalities,Yinchuan 750021,China;2.School of Biotechnology and Food Engineering,Hefei University of Technology,Hefei 230009,China)
The pasting property,thermal property characteristics,crystal structure and particle morphology of buckwheat starch were analyzed,and the effects of sodium hydroxide solutions with different mass percentage on physical properties and structure of buckwheat starch were further studied by means of the rapid visco analyzer,differential scanning calorimeter,X-ray diffractometer and scanning electron microscope through investigating the apparent amylose content,solubility and swelling of buckwheat starch. The results showed that the apparent amylose content of buckwheat starch was highest when the mass percentage of sodium hydroxide solutions was about 0.18%. The alkali treatment did not obviously influence the gelatinization enthalpy of buckwheat starch,and not also significantly destroyed the particle morphology and its inner structure when the mass percentage of sodium hydroxide solutions was about 0.24%. The alkali extraction method was able to be used for extracting buckwheat starch,but the mass percentage of sodium hydroxide solutions had to be less than 0.24%.
buckwheat starch;alkali solution;pasting properties;thermal characteristics;granule structure
2016-08-09
王琳(1996-),女,大学本科,研究方向:食品工程技术,E-mail:1405494704@qq.com。
*通讯作者:韩立宏(1979-),女,副教授,研究方向:谷物深加工理论及应用,E-mail:hanlihong_0317@126.com。
宁夏回族自治区自然科学基金(NZ13081);国家自然科学基金(31460406)。
TS201.2
A
1002-0306(2017)06-0079-05
10.13386/j.issn1002-0306.2017.06.006
