胆翘注射液急性和亚慢性毒性试验
2017-04-13吴建华黄宏业杨善忠何家康胡庭俊廖玲玲
吴建华 ,黄宏业 ,杨善忠 , 何家康 ,胡庭俊*,廖玲玲
(1.广西大学动物科学技术学院,广西南宁 530005;2.广西北斗星动物保健品有限公司,广西南宁 530003;3.广西壮族自治区畜牧研究所,广西南宁 530001;4.广西柯新源原种猪有限责任公司,广西南宁 530001)
胆翘注射液急性和亚慢性毒性试验
吴建华1,黄宏业2,杨善忠2, 何家康1,胡庭俊1*,廖玲玲3,4*
(1.广西大学动物科学技术学院,广西南宁 530005;2.广西北斗星动物保健品有限公司,广西南宁 530003;3.广西壮族自治区畜牧研究所,广西南宁 530001;4.广西柯新源原种猪有限责任公司,广西南宁 530001)
旨在评价胆翘注射液的毒性,为临床安全用药提供理论依据。以昆明小鼠为研究对象,进行急性和亚慢性毒性试验。在急性毒性试验中, 给予小鼠不同浓度的胆翘注射液来测定胆翘注射液的半数致死量和最大耐受量;在亚慢性毒性试验中,小鼠以(10、5、2.5 g/kg)不同剂量连续腹腔注射给药28 d,在给药第28天观察小鼠的临床体征、体重及饲料利用率、血常规、血液生化指标和病理组织学变化。结果显示,急性毒性试验各剂量组小鼠均无死亡,无法测出LD50,最大耐受量为20 g/kg。亚慢性毒性试验中用药组小鼠的临床体征、体重及饲料利用率、血常规、血液生化指标与空白组小鼠相比,无显著差异(P>0.05),组织病理学观察,实质器官无异常病变。表明胆翘注射液实际无毒,安全性好。
胆翘注射液;毒性试验;小鼠
黄芩具有清热燥湿,泻火解毒等功效。主要用于治疗呼吸系统感染、肝胆性疾病、变态反应性疾病等,临床应用已有千年之久,是中医常用药之一[1];黄芩苷为草本植物黄芩的主要有效成分,属于黄酮类化合物;现代药学研究表明,黄芩苷在清除自由基、抗氧化、减轻组织的缺血再灌注损伤、调节免疫、促进细胞凋亡,以及抗肿瘤等多方面均有作用;在抗菌消炎、抗病毒、保护肝肾、抗肿瘤、改善微循环等多方面均有显著作用[2-3]。 猪胆酸味苦性寒,具有清热燥湿的作用。临床用于化脓性感染、肠梗阻、便秘,以及急性肠胃炎、菌痢、急性传染性肝炎和单纯的消化不良等疾病[4]。胆翘注射液是广西北斗星动物保健品有限公司研发的中兽药产品,含有黄芩苷、猪胆酸等有效成分。本研究旨在考察胆翘注射液的毒性作用,为胆翘注射液的临床用药提供依据。
1 材料与方法
1.1 材料
1.1.1 实验动物 昆明种小鼠,雌雄各半,购自广西医科大学实验动物中心,动物合格证号为:SCXK桂2014-0002。于购买后新环境下适应饲养7 d,每天人工照明12 h。灌胃前禁食8 h~12 h,不限制饮水。
1.1.2 受试药品 胆翘注射液,广西北斗星动物保健品有限公司中试产品;规格:0.5 g/mL,即每1 mL胆翘注射液相当于原生药0.5 g,10 mL/支。
1.2 方法
1.2.1 急性毒性预试验 选用8周龄、体重为20 g~25 g昆明系小鼠20只,随机分为5组,每组4只,分笼饲养。胆翘注射液设A(20 g/kg)、B(10 g/kg)、C(5 g/kg)、D(2.5 g/kg)、E(1.25 g/kg)5个剂量组。于试验开始24 h内一次性对小鼠进行灌胃给药。此后观察7 d,记录小鼠的饮食、饮水量变化及是否有中毒或死亡症状出现。若无死亡小鼠,则于用药第8天,将所有供试鼠断颈处死,剖检,观察小鼠的心脏、肝脏、脾脏、肺脏、肾脏、胸腺、胃﹑肠道等脏器有无异常。若无异常,进行急性毒性最大耐受量试验 。
1.2.2 最大耐受量试验 ①选用8周龄、体重为20 g~25 g昆明系小鼠20 只,于试验开始24 h内给每只小鼠腹腔注射胆翘注射液0.2 mL,剂量为20 g/kg。②给药后24 h内注意观察小鼠是否出现中毒反应,随后每天观察2次,观察小鼠的饮食、精神状态、自主活动、排粪等,并及时做好记录。连续观察7 d,观察期保证饲喂条件不变。于用药第8天,将所有供试鼠断颈处死,剖检,检查小鼠的心脏、肝脏、脾脏、肺脏、肾脏、胸腺、胃﹑肠道等脏器有无异常。
1.2.3 亚慢性毒性试验 80只昆明种小鼠随机分为4组,即第1组为空白对照组,第2、3、4组分别为胆翘注射液2.5 g/kg剂量组、5 g/kg剂量组和10 g/kg剂量组,每组20只,雌雄各10只,分笼饲养,空白对照组腹腔注射生理盐水,给药组给予胆翘注射液,其中第2组2.5 g/kg,第3组5 g/kg,第4组10 g/kg,每只小鼠注射溶液体积为0.2 mL/10 g,连续28 d。
1.2.4 观察指标
1.2.4.1 临床体征 试验期间观察小鼠是否出现与药物相关的不良反应,如精神状态、呼吸、行为及排粪等情况变化。给药后观察28 d。记录小鼠不良反应出现的时间、程度、持续时间。观测的不良反应包括过敏反应、局部刺激,消化系统表现如流涎等。不良反应观察时间:对试验中出现不良反应者,应观察至症状恢复正常。
1.2.4.2 体重及饲料利用率 试验前、试验结束时对小鼠称体重。每7 d于喂料前称重1次,而后计算小鼠的增重、增重率及饲料利用率。
增重率(%)=增重(g)/试验前体重(g)×100%
饲料利用率(%)=增重(g)/饲料消耗量(g)×100%
1.2.4.3 样品采集及处理 在给药28 d时,每组小鼠眼眶采血,所采血液分两管放置,其中1管置于带抗凝剂的离心管中,用于血常规分析;另1管不加抗凝剂,血液样品于室温下静置2 h,然后2 500 r/min离心5 min,取上层血清,置-80℃保存,用于血液生化指标分析。采血后颈椎脱臼处死,采集肝脏、脾脏和肾脏称重,计算肝脏、脾脏和肾脏的脏器指数。脏器指数=脏器重(mg)/体重(g)。
1.2.4.4 血常规分析 加抗凝剂的全血进行白细胞总数计数、白细胞分类计数。
1.2.4.5 血液生化指标分析 血清按试剂盒操作测定谷草转氨酶(AST)、谷丙转氨酶(ALT)、肌酐(Cr)、尿素氮(BUN)水平。
1.2.4.6 病理组织学观察 给药28 d采血后处死小鼠,取肝、脾、肾固定于100 g/L中性福尔马林1周,流水冲洗过夜,梯度乙醇脱水,二甲苯透明,常规石蜡包埋,切片,HE染色。光学显微镜下观察。
1.2.5 统计学分析 本试验所得数据均采用SPSS22.0软件中的比较均值-单因素方差分析法分析,并采用多重比较法进行试验组间的显著性检验。结果以平均值±标准差表示。
2 结果
2.1 急性毒性试验预试验结果
经过7 d的观察,胆翘注射液急性毒性试验预试验的5个组共20只小鼠,除在给药后30 min内精神略显沉郁、活动量减少,之后均表现正常,饮水、采食及排便无较大变化,全部存活。在试验第8天将全部小鼠脱颈处死,剖检其内脏。其心脏、肝脏、脾脏、肺脏、肾脏、胸腺、胃﹑肠道等脏器未见异常变化。结果表明,无法测得胆翘注射液的半数致死量(LD50),故仅进行最大耐受量试验。
预试验详细分组及小鼠死亡情况如表1。
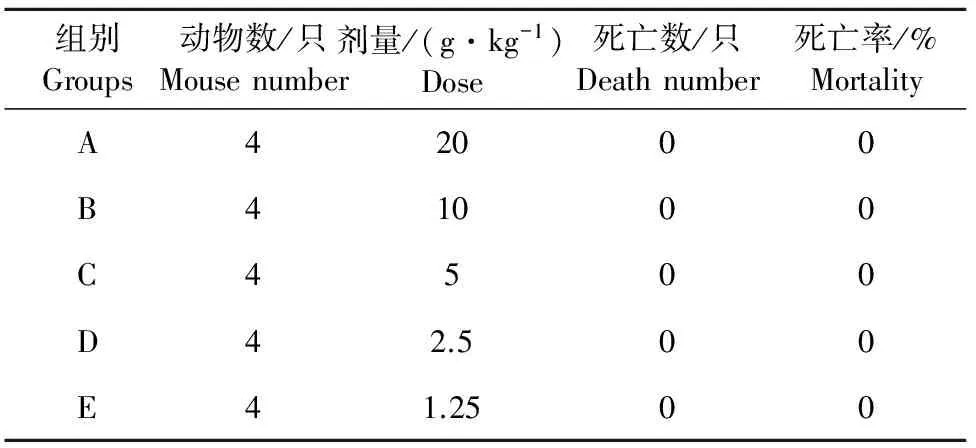
表1 预试验小鼠死亡情况统计表
2.2 最大耐受量试验结果
2.2.1 临床表现 腹腔注射后,30 min内小鼠精神状态正常,采食饮水正常;24 h内小鼠未出现中毒症状。观察7 d,无中毒症状出现,所有小鼠食欲、精神状态均正常,采食、饮水、排便等活动正常,无小鼠死亡。
2.2.2 剖检 于用药第8天对处死的小鼠进行大体解剖,观察心脏、肝脏、脾脏、肺脏、肾脏、胸腺、胃、肠道等脏器,肉眼均未见任何明显的病理变化。
2.3 亚慢性毒性试验结果
2.3.1 临床表现 各组小鼠在腹腔注射给药后,由于注射时刺激出现轻度不适,精神略显沉郁、活动量减少,之后均恢复正常,反应灵敏、皮毛光泽,饮水采食及排便无较大变化,试验过程中未出现死亡小鼠。
2.3.2 胆翘注射液对小鼠体重及饲料利用率的影响 表2和表3结果显示,腹腔注射一定剂量的胆翘注射液对小鼠增重率和饲料利用率无影响。
2.3.3 胆翘注射液对小鼠脏器指数的影响 表4结果显示,用药28 d给药组肝脏指数、肾脏指数、脾脏指数与空白对照组相比差异均不显著(P>0.05)。结果表明,胆翘注射液腹腔注射对小鼠的肝、肾脏及脾脏无显著影响。
2.3.4 血液常规检测结果 如表5所示,用药28 d小鼠血常规检测结果表明,给药组小鼠的白细胞总数与空白对照组比较,差异不显著(P>0.05)。各白细胞百分比的比较中,10 g/kg、2.5 g/kg剂量组小鼠的淋巴细胞数降低,但小鼠淋巴细胞正常范围为48%~92%,试验结果在正常范围内波动[5];10 g/kg剂量组小鼠的中性粒细胞数升高,但未超出正常范围(7%~51%)[5];2.5 g/kg剂量组单核细胞比例上升,但是都在正常范围波动(0~0.3%)[5];说明胆翘注射液对血液常规指标无显著影响。

表2 小鼠的增重情况
注:*表示与空白对照组进行比较,差异显著(P<0.05)。
Note:*indicates significant difference compared with blank control group(P<0.5).

表3 小鼠的饲料利用率
注:*表示与空白对照组进行比较,差异显著(P<0.05)。
Note:*indicates significant difference compared with blank control group(P<0.5).

表4 用药28 d后小鼠的脏器指数测定结果

表5 用药28 d小鼠血液中白细胞分类计数结果
注:*表示与空白对照组进行比较,差异显著(P<0.05)。
Note:*indicates significant difference compared with blank control group(P<0.5).
2.3.5 血液生化指标检测结果 表6结果显示,用药28 d时小鼠血液生化结果显示,给药组小鼠的血清谷丙转氨酶活性、尿素氮和肌酐水平与空白对照组比较差异不显著(P>0.05),谷草转氨酶与空白对照组比较差异显著(P<0.05)。
2.3.6 病理组织学观察 用药第28天时,将各试验组小鼠颈椎脱臼处死,剖检,10 g/kg剂量组有部分小鼠的肝脏边缘发黑,肾脏稍微肿大,被膜紧张,容易剥离,肾表面及切面均呈红色,切面皮质略显增厚,肾小球呈灰白色半透明小颗粒状隆起。高剂量组其他组织无肉眼可见变化。空白对照组、2.5 g/kg剂量组、5 g/kg剂量组的小鼠内脏器官均未见明显病理变化。
用药后28 d小鼠眼眶采血后,每组随机抽样20只小鼠剖检,发现内脏器官无眼观病理变化。各组取肝、脾、肾做病理组织切片,未发现颗粒变性、水泡变性和坏死点等变化。结果表明,各组小鼠肝、脾、肾组织未出现明显的病理变化(图1)。

表6 用药28 d时小鼠血液生化指标检测结果
注:*表示与空白对照组进行比较,差异显著(P<0.05)。
Note:*indicates significant difference compared with blank control group(P<0.5).
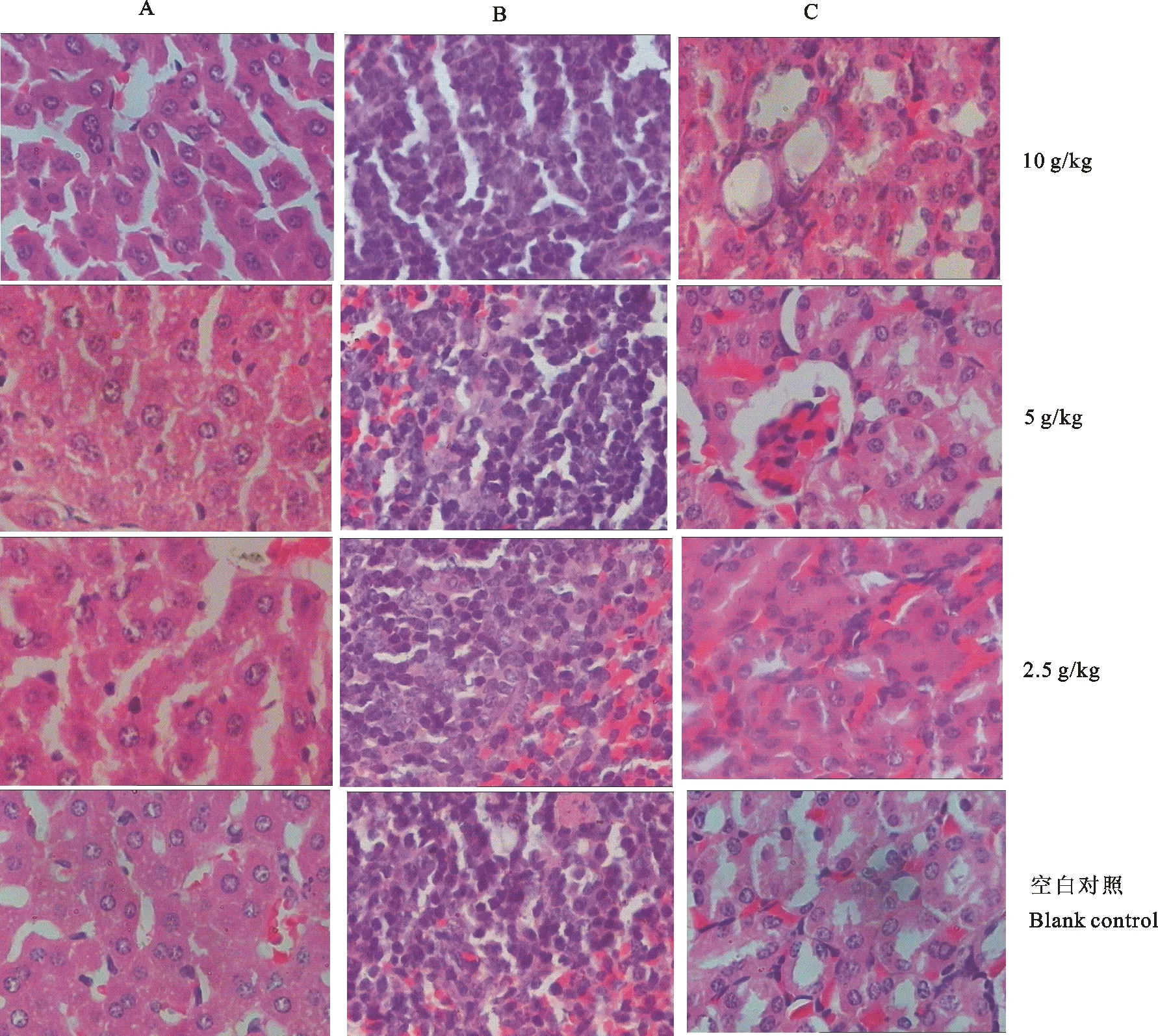
A.肝脏;B.脾脏;C.肾脏
3 讨论
临床上黄芩药理作用广泛。其主要有抗氧化、清除自由基、抗炎、抗肿瘤、阻止钙离子通道、抑制醛糖还原酶、抗病毒、抗过敏等作用;并对免疫系统、心脑血管系统、消化系统和神经系统等具有保护作用[6]。近年来有关黄芩不良反应的报道时有出现[7-9],现代药理研究证明,黄芩不良反应与黄芩苷有密切关系[10],本试验通过对小鼠进行腹腔注射胆翘注射液,观察小鼠的临床症状以及生理生化指标,结果显示,小鼠无明显的不良反应,按照毒理学评价标准[11],当药物的LD50>5 g/kg时,该药物属于实际无毒性物质。本试验中胆翘注射液高剂量达到20 g/kg,未见毒性反应,表明胆翘注射液对小鼠实际无毒。根据急性毒性试验预试验的结果,无法测出胆翘注射液的LD50,因此可做最大耐受量试验以反映药物的安全性。
最大耐受量试验中,胆翘注射液剂量为20 g/kg,小鼠健康存活,未见毒性反应,测得胆翘注射液的最大耐受量为20 g/kg。
胆翘注射液分别以10、5、2.5 g/kg剂量,连续用药28 d,在观察期内未见小鼠有不良反应,精神状态良好、饮食正常。各试验组小鼠血液常规指标和血液生化指标均在正常范围内变动,表明胆翘注射液分别按10、5、2.5 g/kg剂量应用时对小鼠生理生化功能无不良影响。胆翘注射液按10、5、2.5 g/kg剂量应用后,试验小鼠肝、脾、肾未见肉眼及组织学病理变化,未见明显的毒副作用。
综合分析各项检测指标,表明胆翘注射液实际无毒,在临床上应用是安全的。
[1] 朱 伟,孙红光,朱 迅.黄芩苷元对炎症反应的影响[J].中国药理学通报,2009,25(2):194-197.
[2] 李 敬,刘云海,陈 新,等.黄芩中黄芩苷的抗内毒素作用[J].医药导报,2006(12):1237-1240.
[3] 张喜平,程琪辉,张 宇.黄芩苷胶囊小鼠急性毒性试验[J].医学研究杂志,2006,35(9):16-19.
[4] 刘 直.猪胆汁的临床应用和实验研究[J].生化药物杂志,1993(1):3-5.
[5] 王冬平.实验动物血液生理生化参考手册[M].北京:科学出版社,2011.
[6] 张喜平,程琪辉,沈培红,等.黄芩苷类注射剂安全性与急性毒性实验研究[C]//全国中药注射剂安全性及产业发展交流研讨会论文集,浙江杭州:2009.
[7] 何慧晶,付 娟.中药黄芩致过敏1例报告并文献复述[J].湖北中医杂志,2016,38(2):56-58.
[8] 冯艳霜.187例中药致过敏反应文献分析[J].药物不良反应杂志,2002,4(2):81-83.
[9] 李铁军,李朝阳.黄芩汤致过敏反应1例[J].中国现代应用药学,1999,16(5):11.
[10] 田锋齐,乔海灵,郜 娜.黄芩苷的致过敏作用机制[J].中国药理通讯,2009(2):63.
[11] 袁伯俊.药物毒理学实验方法与技术[M].北京:化学工业出版社,2007.
Study on Acute and Subchronic Toxicity of Danqiao Injection
WU Jian-hua1,HUANG Hong-ye2,YANG Shan-zhong2,HE Jia-kang1,HU Ting-jun1,LIAO Ling-ling3,4
(1.CollegeofAnimalScienceandTechnology,GuangxiUniversity,Nanning,Guangxi,530005,China; 2.GuangxiBeidouxingAnimalHealthProductsLimitedCompany,Nanning,Guangxi,530003,China; 3.GuangxiInstituteofAnimalHusbandry,Nanning,Guangxi,530001,China; 4.GuangxiKeXinyuanLimitedLiabilityCompanyofOriginalBreeding,Nanning,Guangxi,530001,China)
In order to evaluate the toxicity of Danqiao injection for the guidance of clinical treatment,the acute and subchronic toxicity test were assessed in KM mice respectively.To determine the acute toxicity,the median lethal dose and the maximum tolerated dose of Danqiao injection were determined.In the subchronic toxicity test,the mice were given with(10,5,2.5 g/kg)for 28 d with peritoneal injection.The clinical signs,body weight and feed utilization rate,blood routine,blood biochemical indexes and histopathological lesions in mice were observed on 28 d after challenge.The results showed that there was no any poisoning and death cases in each group and the maximum tolerated dose was 20 g/kg body weight.There was no significant difference in clinical signs,body weights and feed utilization rates,blood routines,blood biochemical indexes among three treatment groups and control group.The histopathological result reveled no lesion in mice.In conclusion,Danqiao injection was safty for its clinical application.
Danqiao injection;toxicity test;mouse
2016-08-17
南宁市科学研究与技术开发计划项目(20143328)
吴建华(1986-),男,河南辉县人,硕士研究生,主要从事中药免疫药理学研究。
S853.74
A
1007-5038(2017)04-0088-05
*通讯作者
