血清Cystain C、尿NGAL及尿损份分子1联合检测对儿童过敏性紫癜早期肾损伤的诊断效能
2017-04-04徐莲刘健胜于艳辉张慧刘雅婷房亚菲卢思广
徐莲,刘健胜,于艳辉,张慧,刘雅婷,房亚菲,卢思广
(徐州医学院附属连云港医院,江苏连云港222002)
血清Cystain C、尿NGAL及尿损份分子1联合检测对儿童过敏性紫癜早期肾损伤的诊断效能
徐莲,刘健胜,于艳辉,张慧,刘雅婷,房亚菲,卢思广
(徐州医学院附属连云港医院,江苏连云港222002)
目的观察血清半胱氨酸蛋白酶抑制剂C(Cystatin C)和尿中性粒细胞明胶酶相关脂质运载蛋白(NGAL)、尿肾损伤分子-1(KIM-1)联合检测对儿童过敏性紫癜(HSP)早期肾损伤(HSPN)的诊断效能。方法选择36例HSPN患儿为HSPN组,36例无肾炎的HSP患儿为HSP组,22例健康儿童为对照组。采用胶乳增强免疫比浊法检测各组患儿血清Cystatin C,采用ELISA法检测各组患儿尿NGAL、KIM-1,采用化学发光法检测各组患儿尿肌酐(uCr)。比较各组血清Cystatin C、尿NGAL/uCr、KIM-1/uCr。绘制血清Cystatin C、尿NGAL/uCr、KIM-1/uCr及三者联合检测诊断HSPN的受试者工作曲线(ROC曲线),计算曲线下面积、截断值及灵敏度、特异度。结果HSPN、HSP组患儿血清Cystatin C均高于对照组(P均<0.05),但是HSPN组患儿血清Cystatin C与HSP组相比P>0.05。HSPN组患儿尿NGAL/uCr、KIM-1/uCr均高于HSP组和对照组(P均<0.05),但是HSP组患儿尿NGAL/uCr、KIM-1/uCr与对照组相比P均>0.05。血清Cystatin C、尿NGAL/uCr、尿KIM-1/uCr诊断HSPN的ROC曲线的曲线下面积(AUC)分别为0.679(95%CI:0.543~0.815,P=0.023)、0.716(95%CI:0.586~0.846,P=0.006)和0.681(95%CI:0.539~0.822,P=0.022)。选取的截断点分别为0.575 mg/L、2.695×10-2ng/mg和0.615×10-2ng/mg,相应的敏感度分别为58.3%、61.1%和66.7%,特异度分别为68.2%、77.3%和72.7%。三者联合检测诊断HSPN的AUC为0.814,敏感性、特异性分别为88.9%、63.6%。结论血清Cystatin C、尿NGAL、尿KIM-1联合检测诊断HSPN的效能优于单独检测。
半胱氨酸蛋白酶抑制剂C;中性粒细胞明胶酶相关脂质运载蛋白;肾损伤分子-1;过敏性紫癜;肾功能损伤
过敏性紫癜(HSP)是经典的白细胞碎裂性小血管炎,是儿童期常见的系统性血管炎,其发病机制可能是外界各种刺激因素作用于具有遗传背景的个体导致的IgA免疫复合物型疾病[1, 2]。临床特点为血小板不减少性紫癜,常伴有关节肿痛、腹痛、便血、血尿和蛋白尿。HSP累及肾脏出现血尿、蛋白尿等临床表现时,称为紫癜性肾炎(HSPN),绝大多数肾损伤患儿能完全恢复,少数进展为慢性肾炎,死于肾衰竭。传统肾损伤指标有血肌酐(sCr)、尿素氮(BUN)、β2微球蛋白(β2-MG)等,但大多易受肾外因素如年龄、性别、肌肉量、炎症等的影响,诊断HSPN的效能并不好。半胱氨酸蛋白酶抑制剂C(Cystatin C)能自由滤过肾小球,几乎全部在近端肾小管重吸收后降解[3],被认为与肾小球滤过率(GFR)相关。中性粒细胞明胶酶相关脂质运载蛋白(NGAL)、肾损伤分子-1(KIM-1)主要表达于受损的近端肾小管上皮细胞[4, 5],是肾小管损伤的敏感标志物。本研究观察了三者联合检测在HSPN中的诊断效能。现报告如下。
1 资料与方法
1.1 临床资料 选取2015年2~10月收治的36例HSPN患儿为HSPN组,其中男17例、女19例。年龄7~9岁,平均8岁。身高121.5~137.0 cm,平均126.5 cm。体质量22.3~32.8 kg,平均26.5 kg。病程2~10 d,平均4.5 d。无肾炎的HSP患儿36例为HSP组,其中男17例、女19例。年龄6~9岁,平均7.5岁。身高121.3~140.8 cm,平均126.0 cm。体质量22.1~33.6 kg,平均26.0 kg。病程1~7 d,平均4.5 d。另选22例同期门诊健康查体儿童为对照组,其中男10例、女22例。年龄6~10岁,平均8岁。身高116.0~145.0 cm,平均130.0 cm。体质量20.0~38.5 kg,平均25.0 kg。入选标准:①年龄为3~13岁;②HSP符合《诸福棠实用儿科学》第7版HSP的诊断标准[6],HSPN符合2009年中华医学会儿科分会肾脏病学组制定的HSPN诊断标准[7];③近期均未使用任何糖皮质激素或细胞毒性药物;④排除其他免疫性疾病、风湿性疾病、急性感染、肿瘤等。三组儿童性别、年龄、身高、体质量相比,P均<0.05。本研究已经医院伦理委员会批准,所有入组儿童的家长均签署知情同意书。
1.2 血清Cystatin C检测方法 用促凝管采集各组受检者静脉血3 mL,室温下静置30 min,置于离心管中3 500 r/min离心5 min,取上清液用EP管分装并冻存在-80 ℃冰箱保存待测。采用胶乳增强免疫比浊法检测血清Cystatin C,严格按照试剂盒(购自宁波天康生物科技有限公司)说明书操作。
1.3 尿NGAL、KIM-1、肌酐(uCr)检测方法 用尿杯留取各组受检儿童新鲜中段晨尿10 mL,用ELISA法检测尿NGAL、KIM-1,按照试剂盒(购自武汉博士德生物工程有限公司)说明书操作。在用全自动生化分析仪检测尿肌酐uCr,用其计算尿NGAL/uCr、KIM-1/uCr。
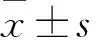
2 结果
2.1 三组血清Cystatin C、尿NGAL/uCr、尿KIM-1/uCr比较 HSPN组、HSP组、对照组患儿血清Cystatin C分别为(0.62±0.14)、(0.60±0.12)、(0.53±0.11)mgL,HSPN、HSP组患儿血清Cystatin C均高于对照组(P均<0.05),但HSPN组患儿血清Cystatin C与HSP组相比P>0.05。HSPN组、HSP组、对照组患儿尿NGAL/uCr分别为3.9(1.1~10.3)×10-2ng/mg、1.6(0.9~2.9)×10-2ng/mg、1.6(0.7~2.6)×10-2ng/mg,尿KIM-1/uCr分别为0.8(0.5~1.3)×10-2ng/mg、0.5(0.3~0.9)×10-2ng/mg、0.5(0.3~0.8)×10-2ng/mg。HSPN组患儿尿NGAL/uCr、KIM-1/uCr均高于HSP组和对照组(P均<0.05),但是HSP组患儿尿NGAL/uCr、KIM-1/uCr与对照组相比P均>0.05。
2.2 血清Cystatin C、尿NGAL/uCr、尿KIM-1/uCr诊断HSPN的效能 血清Cystatin C、尿NGAL/uCr、尿KIM-1/uCr诊断HSPN的ROC曲线的曲线下面积(AUC)分别为0.679(95%CI:0.543~0.815,P=0.023)、0.716(95%CI:0.586~0.846,P=0.006)和0.681(95%CI:0.539~0.822,P=0.022)。选取的截断点分别为0.575 mg/L、2.695×10-2ng/mg和0.615×10-2ng/mg,相应的敏感性分别为58.3%、61.1%和66.7%,特异度分别为68.2%、77.3%和72.7%。三者联合检测诊断HSPN的AUC为0.814,敏感度、特异度分别为88.9%、63.6%。
3 讨论
HSP是免疫复合物介导的全身性小血管炎,大约50%的患儿在发病4~6周内发展为HSPN,大约1%~7%的HSPN患儿进展为慢性肾脏病或终末期肾病[8],故HSPN是影响HSP长期预后最为关键的因素。HSPN肾脏病理主要为IgA沉积所致的不同程度的系膜增生性肾小球肾炎[9],常伴有随着疾病的严重程度而加重的肾小管间质病变,且肾小管间质损害在HSPN的预后方面占有重要地位[10]。Cystatin C是一种分子量为13 kD的非糖基化碱性蛋白质,属于半胱氨酸蛋白酶抑制剂超家族,参与细胞内外蛋白质的水解代谢[11]。Cystatin C的编码基因为管家基因,故在人体所有有核细胞中生成速率恒定,其惟一代谢器官是肾脏,低分子量联合带正电荷等生化特性使血清Cystatin C可以自由滤过肾小球进入原尿,几乎全部在近曲小管上皮细胞重吸收后降解且不被肾小管分泌[12], 所以血清Cystatin C的浓度主要由肾小球滤过能力决定。血清Cystatin C在2岁以上的儿童中趋于稳定,相较于sCr更不易受性别、年龄、身高和肌肉量的影响[13, 14]。 研究表明在各种急、慢性肾损伤中血清Cystatin C能更敏感的反映GFR情况[15, 16]。
NGAL是脂质运载蛋白家族中的一员[17]。NGAL在肾小管上皮细胞的形成与修复中发挥重要作用[18]。生理条件下,NGAL促进肾间充质祖细胞转化为肾小管上皮细胞,促进肾脏生长发育[19, 20];病理情况下,NGAL诱导肾小管上皮细胞修复再生、促进肾脏功能恢复[21]。血浆NGAL能通过肾小球自由滤过,大部分在近端小管被重吸收,尿中浓度较低[22]。多项研究[23, 24]表明尿NGAL的增加可能是由于近端肾小管受损阻碍了NGAL 的重吸收或 NGAL 合成增加,所以NGAL主要反映肾小管损伤。研究表明无论是急性肾损伤[25]还是慢性肾损伤[26],与传统指标相较尿NGAL能更敏感的反应肾损伤的发生。
KIM-1是分子量约104 kD的I型跨膜糖蛋白[27],是T细胞膜蛋白家族(TIM)成员之一。KIM-1低表达于Th2细胞,影响相关细胞因子的分泌,参与多种免疫紊乱性疾病的调节[28]。KIM在正常的肾脏几乎不表达,在受损的近端肾小管上皮细胞表达明显增高,其胞外段可在基质金属蛋白酶的作用下迅速裂解并释放到尿液中[29]。研究表明尿KIM-1在各种急、慢性肾脏疾病中均显著增高,且与肾小管KIM-1的表达水平相关[30, 31],因而尿KIM-1可以作为近端肾小管损伤的标志物。
HSPN与IgA肾病在肾脏病理上难以区分,均可见IgA为主的系膜沉积。目前共识认为HSPN和IgA肾病存在共同的发病机制即IgA1分子铰链区糖基化异常[32]。研究表明,IgA肾病患者的尿NGAL和尿KIM-1水平明显高于健康对照组,且与肾小管表达水平和肾小管损伤程度密切相关[33~35],IgA肾病患者血清Cystatin C水平与肾小球损伤程度也密切相关[36]。本研究中,为了消除尿液浓缩的影响,所有尿指标经uCr校正,HSPN组尿NGAL/uCr和KIM-1/uCr显著高于HSP组和对照组, HSPN组血清Cystatin C高于对照组,说明HSPN患儿同时存在肾小球和肾小管间质损害。本研究结果显示,血清Cystatin C、尿NGAL/uCr和KIM-1/uCr诊断HSPN的AUC分别0.679、0.716和0.681,说明三者在HSPN的诊断中具有良好的诊断效能,以尿NGAL/uCr最佳。三者联合检测的AUC大于各标志物单项检测的AUC,说明联合检测各指标能提高HSPN的诊断率。
本研究初步探讨了血清Cystatin C、尿NGAL和KIM-1在HSP早期肾损伤中的诊断价值,为进一步研究HSPN的病理机制及临床评估提供了依据。但是本研究样本量相对较少且未进行长期的随访研究,所以后续的研究中需注意加大样本量并进行随访研究以进一步明确指标与治疗效果间的相关性。
[1] Park SJ, Suh JS, Lee JH, et al. Advances in our understanding of the pathogenesis of Henoch-Schonlein purpura and the implications for improving its diagnosis[J]. Expert Rev Clin Immunol, 2013,9(12):1223-1238.
[2] Saulsbury FT. Henoch-Schonlein purpura[J]. Curr Opin Rheumatol, 2010,22(5):598-602.
[3] Mussap M, Plebani M. Biochemistry and clinical role of human cystatin C[J]. Crit Rev Clin Lab Sci, 2004,41(5-6):467-550.
[4] van Timmeren MM, van den Heuvel MC, Bailly V, et al. Tubular kidney injury molecule-1 (KIM-1) in human renal disease[J]. J Pathol, 2007,212(2):209-217.
[5] Mishra J, Ma Q, Prada A, et al. Identification of neutrophil gelatinase-associated lipocalin as a novel early urinary biomarker for ischemic renal injury[J]. J Am Soc Nephrol, 2003,14(10):2534-2543.
[6] 胡亚美,江载芳.诸福棠实用儿科学[M]. 7版.北京:人民卫生出版社,2009:288-290.
[7] 中华医学会儿科学分会肾脏病学组.儿童常见肾脏疾病诊治循证指南(二):紫癜性肾炎的诊治循证指南(试行)[J].中华儿科杂志,2009,47(12):911-913.
[8] Chen JY, Mao JH. Henoch-Schonlein purpura nephritis in children: incidence, pathogenesis and management[J]. World J Pediatr, 2015,11(1):29-34.
[9] 刘玲, 张东风, 李春珍, 等. 儿童过敏性紫癜肾炎的临床及病理分析[J]. 临床儿科杂志, 2015,33(2):151-154.
[10] 沈茜, 徐虹,宋善路, 等. 肾小管间质损害对儿童过敏性紫癜肾炎预后影响的探讨[J]. 中国实用儿科杂志, 2003,18(6):356-358.
[11] Randers E, Erlandsen EJ. Serum cystatin C as an endogenous marker of the renal function--a review[J]. Clin Chem Lab Med, 1999,37(4):389-395.
[12] Onopiuk A, Tokarzewicz A, Gorodkiewicz E. Cystatin C: a kidney function biomarker[J]. Adv Clin Chem, 2015,68(7):57-69.
[13] 陈学军, 沈月芳, 钟小薇, 等. 儿童透射比浊法血清半胱氨酸蛋白酶抑制剂C参考区间的建立及其与年龄、性别的相关性[J]. 中华检验医学杂志, 2011,25(9):785-790.
[14] Bokenkamp A, Domanetzki M, Zinck R, et al. Cystatin C--a new marker of glomerular filtration rate in children independent of age and height[J]. Pediatrics, 1998,101(5):875-881.
[15] Wei L, Ye X, Pei X, et al. Diagnostic accuracy of serum cystatin C in chronic kidney disease: a meta-analysis[J]. Clin Nephrol, 2015,84(2):86-94.
[16] Odutayo A, Cherney D. Cystatin C and acute changes in glomerular filtration rate [J]. Clin Nephrol, 2012,78(1):64-75.
[17] Kjeldsen L, Johnsen AH, Sengelov H, et al. Isolation and primary structure of NGAL, a novel protein associated with human neutrophil gelatinase[J]. J Biol Chem, 1993,268(14):10425-1032.
[18] Mori K, Nakao K. Neutrophil gelatinase-associated lipocalin as the real-time indicator of active kidney damage[J]. Kidney Int, 2007,71(10):967-970.
[19] Yang J, Goetz D, Li JY, et al. An iron delivery pathway mediated by a lipocalin[J]. Mol Cell, 2002,10(5):1045-1056.
[20] Challen GA, Martinez G, Davis MJ, et al. Identifying the molecular phenotype of renal progenitor cells[J]. J Am Soc Nephrol, 2004,15(9):2344-2357.
[21] Schmidt-Ott KM, Mori K, Li JY, et al. Dual action of neutrophil gelatinase-associated lipocalin[J]. J Am Soc Nephrol, 2007,18(2):407-413.
[22] Flo TH, Smith KD, Sato S, et al. Lipocalin 2 mediates an innate immune response to bacterial infection by sequestrating iron[J]. Nature, 2004,432(7019):917-921.
[23] Supavekin S, Zhang W, Kucherlapati R, et al. Differential gene expression following early renal ischemia/reperfusion[J]. Kidney Int, 2003,63(5):1714-1724.
[24] Kuwabara T, Mori K, Mukoyama M, et al. Urinary neutrophil gelatinase-associated lipocalin levels reflect damage to glomeruli, proximal tubules, and distal nephrons[J]. Kidney Int, 2009,75(3):285-294.
[25] Haase M, Bellomo R, Devarajan P, et al. Accuracy of neutrophil gelatinase-associated lipocalin (NGAL) in diagnosis and prognosis in acute kidney injury: a systematic review and meta-analysis[J]. Am J Kidney Dis, 2009,54(6):1012-1024.
[26] Nishida M, Kawakatsu H, Okumura Y, et al. Serum and urinary neutrophil gelatinase-associated lipocalin levels in children with chronic renal diseases[J]. Pediatr Int, 2010,52(4):563-568.
[27] Ichimura T, Bonventre JV, Bailly V, et al. Kidney injury molecule-1 (KIM-1), a putative epithelial cell adhesion molecule containing a novel immunoglobulin domain, is up-regulated in renal cells after injury[J]. J Biol Chem, 1998,273(7):4135-4142.
[28] Su EW, Lin JY, Kane LP. TIM-1 and TIM-3 proteins in immune regulation[J]. Cytokine, 2008,44(1):9-13.
[29] Waanders F, van Timmeren MM, Stegeman CA, et al. Kidney injury molecule-1 in renal disease[J]. J Pathol, 2010,220(1):7-16.
[30] Shao X, Tian L, Xu W, et al. Diagnostic value of urinary kidney injury molecule 1 for acute kidney injury: a meta-analysis[J]. PLoS One, 2014,9(1):84131.
[31] van Timmeren MM, van den Heuvel MC, Bailly V, et al. Tubular kidney injury molecule-1 (KIM-1) in human renal disease[J]. J Pathol, 2007,212(2):209-217.
[32] Kiryluk K, Moldoveanu Z, Sanders JT, et al. Aberrant glycosylation of IgA1 is inherited in both pediatric IgA nephropathy and Henoch-Schonlein purpura nephritis[J]. Kidney Int, 2011,80(1):79-87.
[33] Xu PC, Zhang JJ, Chen M, et al. Urinary kidney injury molecule-1 in patients with IgA nephropathy is closely associated with disease severity[J]. Nephrol Dial Transplant, 2011,26(10):3229-3236.
[34] Ding H, He Y, Li K, et al. Urinary neutrophil gelatinase-associated lipocalin (NGAL) is an early biomarker for renal tubulointerstitial injury in IgA nephropathy[J]. Clin Immunol, 2007,123(2):227-234.
[35] Peters HP, Waanders F, Meijer E, et al. High urinary excretion of kidney injury molecule-1 is an independent predictor of end-stage renal disease in patients with IgA nephropathy[J]. Nephrol Dial Transplant, 2011,26(11):3581-3588.
[36] 钟正霞, 李正付, 裘志成, 等. IgA肾病患者血清胱抑素C与肾脏病理变化的关系探讨[J]. 现代医药卫生, 2015,31(3):398-399.
10.3969/j.issn.1002-266X.2017.35.027
R725.9
B
1002-266X(2017)35-0079-04
2017-01-02)
连云港市科技局社会发展计划项目(QN121001)。
