例谈解析晶体结构的几个问题
2017-04-04魏香三
魏香三
摘要:晶体结构是高考化学的重要考点之一。针对晶体结构中的晶胞计算和晶胞粒子坐标等难点,分别通过典型题例对晶胞中粒子的个数、晶体的密度、粒子所占晶胞体积的百分率、粒子坐标等进行了分析,并提出了相关的教学建议。
关键词:晶体结构;晶胞计算;晶体密度;晶胞粒子坐标分析;教学建议
文章编号:1005–6629(2017)2–0081–04 中图分类号:G633.8 文献标识码:B
2017年普通高等学校招生全国统一考试大纲已正式公布,“物质结构与性质”作为化学选考模块之一。“物质结构与性质”中的“晶体结构”既是重点,又是难点,学生往往对“晶胞结构的计算、晶胞中粒子的坐标分析”感觉束手无策。针对这个问题,下面以高考常见的题型为例进行分析,并提出相关的教学建议。
1 晶胞结构的计算
1.1 晶胞结构中的微粒个数
以立方晶胞为例,常见有简单立方晶胞、体心立方晶胞和面心立方晶胞,根据均摊法来计算[1]。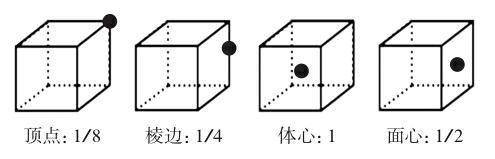
简单立方晶胞中粒子个数:8×1/8=1
体心立方晶胞中粒子个数:8×1/8+1=2
面心立方晶胞中粒子个数:8×1/8+6×1/2=4
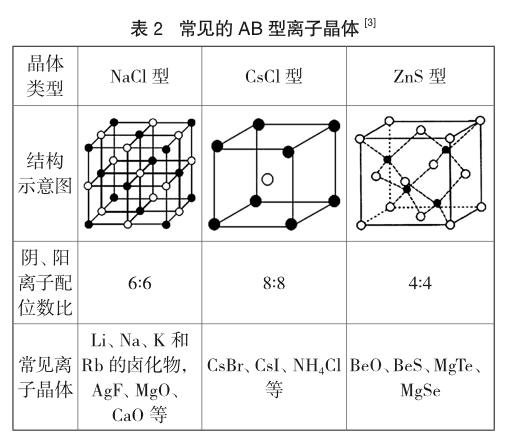
1.2 常见晶胞中粒子的配位数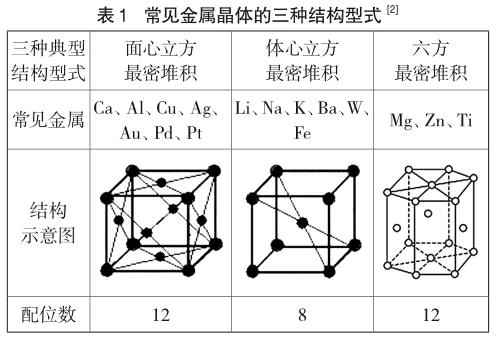
1.3 晶体密度的计算
①计算出1个晶胞中粒子个数:n
②推算出1mol晶胞中含粒子的物质的量:n mol
(M:晶體的摩尔质量,V:1个晶胞的体积)
例1 (2014年全国新课标Ⅰ卷第37题)[化学-选修3:物质结构与性质]早期发现的一种天然准晶颗粒由Al、Cu、Fe三种元素组成。回答下列问题:
(3)新制备的Cu(OH)2可将乙醛氧化为乙酸,而自身还原成Cu2O。Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有 个铜原子。
(4)铝单质为面心立方晶体,其晶胞参数a=0.405nm,晶胞中铝原子的配位数为 。列式表示铝单质的密度 g/cm3(不必计算出结果)
[分析]
本题从知识层面上考查了学生的计算能力,如晶胞中原子的数目、粒子的配位数、晶体的密度等计算。
从晶胞的类型上既考查了面心立方晶胞,又考查了体心立方晶胞。
[解题步骤]
(3)在氧化亚铜立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中含有的氧原子:8×1/8+6×1/2+4=8。
根据氧化亚铜的化学式:Cu2O,铜和氧的原子个数比为2:1,得出该晶胞中含有的铜原子为16个。
(4)根据常见晶胞中金属原子的配位数,铝单质为面心立方晶体,则晶胞中铝原子的配位数为12。
铝单质为面心立方晶体,其原子个数:
1.4 晶体原子空间利用率的计算[4]
(1)计算晶胞中的微粒数,然后求晶胞中原子的体积(球体积)之和。
(2)计算晶胞的体积:V=a3(a:晶胞参数),如:简单立方 体心立方 面心立方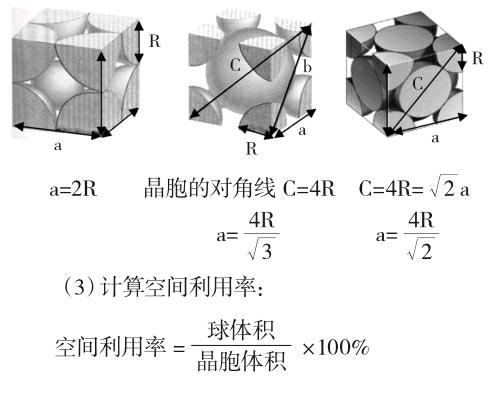
简单立方:
晶胞所含微粒数为:8×1/8=1

[分析]
本题从知识层面上考查了学生的计算能力,如晶胞原子数目、晶体物质密度、晶胞中原子的体积占晶胞体积的百分率等。
从晶胞的类型上既考查了面心立方晶胞,又考查了体心立方晶胞。
[解题步骤]
①从晶胞的结构上看,As是面心立方结构,该晶胞中含As的个数:8×1/8+6×1/2=4;Ga在该晶胞内部,该晶胞中含Ga的个数:4
根据晶胞可知晶胞中Ga和As的个数均是4个,所以晶胞的体积是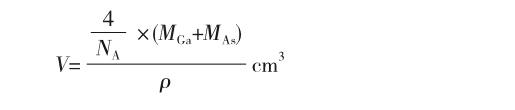
③已知二者的原子半径分别为rGa pm和rAs pm,阿伏伽德罗常数值为NA,则GaAs晶胞中原子的体积占晶胞体积的百分率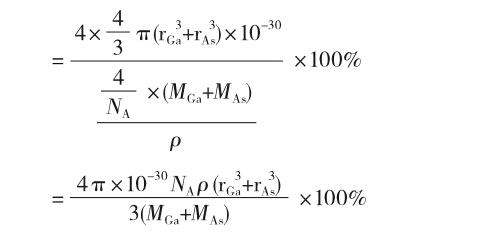
2 晶胞中粒子的坐标分析
2.1 晶胞的特征(大小、形状)
常用六个常数描述,它们是a、b、c、α、β、γ,叫晶胞参数。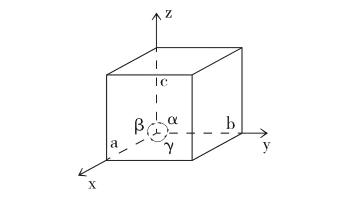
2.2 晶胞有两个基本要素
(1)晶胞参数:晶胞参数和点阵参数一致,由a、b、c、α、β、γ规定,即平行六面体的边长和各边之间的夹角。
(2)坐标参数:若从原点指向原子的向量可表示为r=xa+yb+zc,则原子的坐标参数为(x,y,z)[5]。
如离子晶体:CsCl晶胞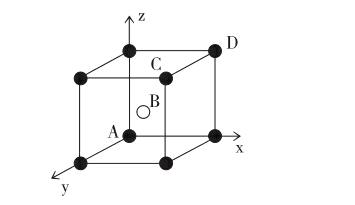
白色球为Cs+、黑色球为Cl-;坐标参数为:A(0,0,0);B(1/2,1/2,1/2);C(1,1,1);D(1,0,1)。
又如金属晶体:Cu晶体结构
晶胞中5个等径球的坐标参数:A(0,0,0);B(1/2,1/2,0);C(1/2,0,1/2);D(0,1/2,1/2);E(1,1,1)。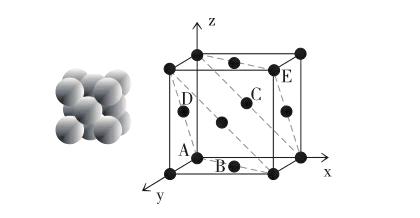
例3 2016新课标I卷37[化学-选修3:物质结构与性质]锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(6)晶胞有两个基本要素:
②晶胞參数,描述晶胞的大小和形状。已知Ge单晶的晶胞参数a=565.76pm,其密度为g·cm-3(列出计算式即可)。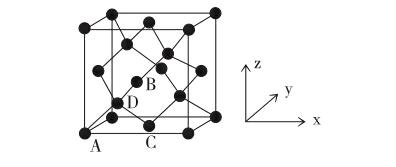
[分析]
Ge单晶的晶胞具有金刚石型结构,如金刚石晶胞结构。
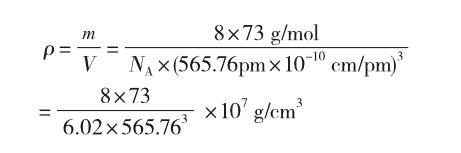
3 教学建议
(1)在教学中,通过氯化钠、氯化铯、金刚石、石墨、干冰、二氧化硅等典型晶体结构模型,分析晶体结构,把晶体结构中的结构微粒抽象为“点”,微粒之间的空间位置关系抽象为“线”和“面”,让学生建立立体几何空间模型,然后用数学知识解决晶体结构的问题。
(2)在高考备考中,要围绕“晶体结构-晶胞(晶体微粒)-典型晶体(金刚石、石墨的原子晶体、冰、CO2的分子晶体、NaCl、CsCl、CaF2的离子晶体、钾、镁、铜、简单立方的金属晶体)结构”这条主线,通过分析常见高考的题型,归纳出常考的知识点,让学生牢固掌握:典型原子晶体(金刚石、单晶硅、二氧化硅)结构特征及其与性质的关系;晶胞原子数目计算、晶体组成(化学式、中心原子配位体、配位数)判断、(晶体)物质密度、微粒间距的计算。
(3)由于晶体结构知识能全面考查学生的观察能力、思维能力和空间想象能力,因而是高考选做题之一。在分析这类题目时,让学生通过对晶体结构的观察,找出晶胞是属于简单立方晶胞、面心立方晶胞还是体心立方晶胞,然后利用分摊法,来解决晶体中所含的微粒数、晶体的化学式等。
(4)晶体结构虽枯燥乏味、死板僵化,但具有对称之美、简单之美、和谐之美。教学中可以通过视频展示晶体对称之美,克服学生对晶体结构知识的畏惧,激发学生对晶体研究的兴趣。
(5)在分析晶体结构时,可以利用现代技术手段,通过微课或者视频,展示晶体结构,从而使抽象的知识具体化、形象化,使复杂的问题简单化。
参考文献:
[1]教育部考试中心. 2016年普通高等学校招生全国统一考试大纲(理科)[M].北京:高等教育出版社,2016:329.
[2][3]陈光巨,王磊,王明召.普通高中课程标准实验教科书·物质结构与性质(选修)[M].济南:山东科学技术出版社,2007:75~76,78~81.
[4][5]王磊.普通高中课程标准实验教科书·物质结构与性质(选修)(教师用书)[M].济南:山东科学技术出版社,2007:137.
