微波降解果胶对其流变性质的影响及动力学
2017-03-31梁瑞红王淑洁贺小红李鹏林郭小娟
梁瑞红,王淑洁,贺小红,陈 军,李鹏林,郭小娟
(南昌大学 食品科学与技术国家重点实验室,江西 南昌 330047)
微波降解果胶对其流变性质的影响及动力学
梁瑞红,王淑洁,贺小红,陈 军*,李鹏林,郭小娟
(南昌大学 食品科学与技术国家重点实验室,江西 南昌 330047)
对不同质量浓度(0.5、1.0、1.5、2.0 g/100 mL)的果胶溶液微波处理不同时间(0、1、3、5、8、15、20、30 min)后的流变性质及动力学进行考察。结果表明,随着果胶溶液质量浓度降低、微波处理时间延长、剪切速率增大,样品的表观黏度和特性黏度[η]均降低。用牛顿幂律方程描述溶液的流体行为,果胶溶液是剪切稀化的假塑性非牛顿流体,在低质量浓度时,微波处理对溶液的流体行为影响最大。根据特性黏度对样品进行反应动力学拟合,发现果胶的微波降解遵循反应一级动力学,在质量浓度0.5 g/100 mL时降解速率最快,质量浓度1.5 g/100 mL时降解速率最慢。经与沸水浴无微波的空白组对比,发现微波降解果胶的过程还存在非热效应。
果胶;微波;降解;流变性质;特性黏度;动力学;非热效应
梁瑞红, 王淑洁, 贺小红, 等. 微波降解果胶对其流变性质的影响及动力学研究[J]. 食品科学, 2016, 38(5): 1-6. DOI:10.7506/spkx1002-6630-201705001. http://www.spkx.net.cn
LIANG Ruihong, WANG Shujie, HE Xiaohong, et al. Effect of microwave treatment on rheological properties and degradation kinetics of pectin[J]. Food Science, 2016, 38(5): 1-6. (in Chinese with English abstract) DOI:10.7506/spkx1002-6630-201705001. http://www.spkx.net.cn
微波是一种电磁波,其热效应是由分子通过自身的运动引起的,相对于传统加热反应受热不均、升温缓慢,其具有受热均匀、环保等优点。近年来关于微波对大分子多糖的降解已有较多报道,如微波对香菇多糖[1]、壳聚糖[2-3]、纤维素[4]和λ-卡拉胶[5]的降解。通常认为其原理是,多糖分子一般均含有羟基等极性基团,使其分子内电荷分布不均匀,在微波场中能迅速吸收电磁波的能量,通过分子偶极作用和分子的高速振动产生热效应,使糖苷键断裂,大分子多糖降解[6]。
但是还有研究认为微波降解多糖的过程中不只存在热效应,同时还存在微波非热效应。Bednarz等[7]研究发现在微波和传统两种加热方法下有不同的有机合成反应速率。Wasikiewicz等[2]通过在相同温度下比较微波处理和传统热处理对壳聚糖降解的影响时发现,传统热处理的分子质量降解速率明显低于微波处理的分子质量降解速率,表明导致壳聚糖降解的不仅有微波辐照的热效应,还有分子之间振动所产生的机械剪切作用。
果胶是一种存在于植物细胞的初生壁和中间层,主要由α-1,4-糖苷键连接的D-半乳糖醛酸组成的酸性杂多糖。其结构通常认为含有均聚半乳糖醛酸(homogalacturonan,HG)、鼠李半乳糖醛酸Ⅰ型(rhamnogalacturonan Ⅰ,RG Ⅰ)和鼠李半乳糖醛酸Ⅱ型(rhamnogalacturonan Ⅱ,RGⅡ)3 种形式。果胶具有许多重要功能,在食品工业中可用作增稠剂、乳化剂、稳定剂等,是联合国粮农组织/世界卫生组织(United Nations Food Agriculture Organization/World Health Organization,FAO/WHO)食品添加剂联合委员会推荐的安全无毒的天然食品添加剂,无每日添加量限制;在医药行业中可抑制透明质酸酶和组胺的释放、内毒素诱导的炎症反应和预防癌症发生与转移[8],还可单独或与其他赋形剂一起配制软膏、膜剂、栓剂及微囊等药物制剂[9];在化妆品和个人护理产品中,果胶除了使油、霜等质地自然,还被用作洗发水、乳液等的有效稳定剂和增稠剂[10],以及抗皮肤衰老剂[11]。但果胶在加工过程中无可避免的会受到各种物理化学作用而导致果胶发生降解,功能性质发生变化,严重制约了果胶的大量工业化应用,此外,研究果胶的降解对了解果胶复杂的分子结构和功能作用有重大意义[12]。因此果胶的降解现象和规律备受国内外学者关注。
关于果胶的物理降解已有大量研究,如研磨和均质[13-16]、超声波[17-18]、物理射线[19-20]、脱水作用[21]等均对果胶有一定的降解作用,吴双双[22]研究了不同pH值下微波对柑橘果胶的降解,但微波降解动力学及微波单独作用时溶液质量浓度对果胶降解的影响尚鲜有报道。本研究主要以苹果果胶为研究对象,通过对不同质量浓度的样品微波处理不同时间,研究微波对果胶的流变性质及特性黏度的影响,特性黏度对微波降解果胶的动力学进行拟合,为苹果果胶的微波降解规律和应用提供理论依据和指导。有限公司;MCR302流变仪 奥地利Anton Paar公司;ALPHA1-2冷冻干燥机 德国Martin Christ公司;玻璃恒温水浴缸 金坛市城东新瑞仪器厂。
1.3 方法
1.3.1 样品的制备
称取果胶溶于100 mL的蒸馏水中,配制质量浓度分别为0.5、1.0、1.5、2.0 g/100 mL的果胶溶液,完全溶解后,移入三口烧瓶中,接通冷凝水,在680 W、100 ℃微波条件下,分别处理1、3、5、8、15、20、30 min,冻干。设置沸水浴无微波,其他条件相同的果胶溶液为空白对照组。
1.3.2 剪切速率扫描
微波处理后的样品用MCR302流变仪进行剪切速率扫描,转子选用有1°夹角的锥板CP50-1,缝间隙为0.102 mm,在25 ℃剪切速率0.01~100 s-1的范围内进行扫描。然后用牛顿幂律方程进行拟合。
τ=Kγn(1)
式中:τ为剪切应力/Pa;K为稠度系数;γ为剪切速率/s-1;n为流体行为指数,其大小表示液体偏离牛顿指数的程度,n<1时样品溶液为剪切变稀的假塑性流体,n=1时,溶液为牛顿流体,n>1时,为胀塑性流体。
1.3.3 特性黏度的测定
特性黏度[η]采用乌氏黏度计方法进行测定。将以上所得样品和原果胶溶于0.1 mol/L的NaCl溶液中,样品质量浓度为0.2 g/100 mL。先测定溶剂NaCl溶液流出毛细管的时间,再取10 mL样品加入乌氏黏度计中,记录溶液从毛细管中流出的时间,用5 mL 0.1 mol/L的NaCl溶液稀释4 次得果胶溶液质量浓度为0.13、0.10、0.08、0.07 g/100 mL,分别记录其流出毛细管的时间,用哈金斯(Huggins)公式[23](公式(2))建立曲线外推至0,得样品特性黏度(公式(2)~(5))。进行测定前样品和溶剂均需过0.45 μm的水系滤膜,测试在25 ℃的恒温条件下进行。

1 材料与方法
1.1 材料与试剂
苹果果胶 美国Sigma Aldrich公司;氯化钠(分析纯)。
1.2 仪器与设备
XH-200A电脑微波固液相合成/萃取工作站 北京祥鹄科技发展有限公司;乌式黏度计 上海正慧工贸
式中:ηsp为增比黏度;[η]为特性黏度/(dL/g);k为Huggins常数;c为果胶质量浓度/(g/mL);η为果胶溶液黏度/(Pa•s);ηs为溶剂黏度/(Pa•s);ηr为相对黏度;t1为样品流出时间/s;t2为溶剂流出时间/s。
1.3.4 反应动力学模型
任瑞[1]和Zhou Gefei[5]等通过研究微波对香菇多糖和λ-卡拉胶的降解,建立了微波降解后香菇多糖和λ-卡拉胶的特性黏度[η]变化的反应动力学方程,结果显示微波降解多糖的过程和酸水解[24]与热降解[25]多糖一样遵循一级反应动力学,因此可以假设微波降解果胶的过程同样遵循一级动力学。
由公式(6)和(7):


得[η]与时间t的关系方程式:

式中:Mt为果胶在时间t时的分子质量/D;M0为果胶在时间0时的分子质量/D;k为一级反应动力学降解速率常数/min-1;t为微波反应时间/min;kMH和α是系统常数,分别为0.017 4和0.84[26];m是单糖单位的平均分子质量,为190 D[27](假设果胶溶液中所有的糖苷键对微波处理时的敏感性相同);[η]t和[η]0分别果胶在时间t和0时的特性黏度。
2 结果与分析
2.1 剪切速率扫描及牛顿幂律方程拟合


图 1 不同质量浓度果胶溶液微波处理不同时间后表观黏度随剪切速率的变化Fig. 1 Apparent viscosity versus shear rate plots of pectin at different concentrations after microwave treatment for various times
由图1可看出,不同质量浓度微波处理不同时间的果胶溶液表观黏度均随剪切速率的增加而降低,表现出经典的非牛顿假塑性流体行为。这与Chen Jun等[13]用动态高压微射流处理苹果果胶有相似的行为。剪切力可能破坏了果胶的有序结构,剪切速率由0.01 s-1升高至1.00 s-1时,外部强加的运动速率逐渐增加至大于分子内构建新交互作用的速率时,网络结构的交联密度降低导致果胶的黏度降低[28]。当剪切速率大于1.00 s-1时,样品的表观黏度基本保持不变,表现为牛顿流体行为,这可能是因为此时果胶分子间的缠结和分子内的交互作用已遭到大部分的破坏,流动曲线较为平缓[17]。由图1还可看出随着微波处理时间的延长,样品的表观黏度降低,这可能是因为微波打断了果胶链,分子质量降低,果胶分子间的缠结和分子内的交互作用减少,导致果胶的表观黏度降低。

表 1 0.5 g/100 mL的果胶溶液流变曲线牛顿幂律拟合参数Table 1 Power law fi tting parameters of pectin solution at 0.5 g/100 mL
对流变数据进行牛顿幂律拟合,以溶液质量浓度0.5 g/100 mL为例,由表1可看出,随着微波处理时间的延长,稠度系数K从0.018降低至0.006(30 min),果胶溶液变得越来越稀。随着处理时间延长,n值表现出增加的趋势,在微波处理30 min后流体行为指数n增至0.993,流体行为向理想型牛顿流体转化。
一般情况下,聚合物的黏度随质量浓度的升高而增加,根据聚合物的结构不同,黏度随着质量浓度的增加趋势有着不同斜率的线性关系[29]。图2为微波处理0 min和30 min后不同质量浓度的果胶溶液的流变曲线。如图2所示,微波处理相同时间时,溶液的表观黏度随质量浓度的升高而增加。溶液质量浓度越高,溶液中分子间发生缠结现象的可能性越高,表观黏度越大。

图 2 微波处理0 min(A)和30 min(B)后不同质量浓度的果胶溶液表观黏度随剪切速率的变化Fig. 2 Apparent viscosity versus shear rate plots of pectin at different concentrations after microwave treatment for 0 (A) and 30 min (B)

表 2 微波处理0 min和30 min后不同质量浓度的果胶溶液稳态流变曲线牛顿幂律拟合参数Table 2 Power law fi tting parameters of pectin solutions at different concentrations after microwave treatment for 0 and 30 min
对图2的流变数据进行牛顿幂律方程拟合所得参数如表2所示,随着果胶溶液质量浓度的增加,稠度指数K增加,溶液变黏稠。微波处理0 min,在质量浓度1.5 g/100 mL时,n值最大为0.925,其流体行为最接近理想状态下的牛顿流体,这可能是因为在质量浓度1.5 g/100 mL时,溶液中果胶分子的网络结构最稳定,在剪切速率0.01~100 s-1范围内分子结构被破坏得较慢,或分子间和分子内新的交互作用的建立速率最快,表观黏度变化较小。微波处理30 min后,n值在质量浓度0.5 g/100 mL时最大,达到0.993;样品溶液的稠度指数K在0.5、1.0、1.5、2.0 g/100 mL时分别降低至微波处理0 min时的35.35%、37.69%、37.04%、48.13%。流体行为指数n在质量浓度为0.5、1.0、2.0 g/100 mL时均增加,这说明微波处理30 min后果胶溶液更接近理想型牛顿流体。其中质量浓度0.5 g/100 mL时n值增加最大,从0.779增加至0.993,表明此质量浓度下微波处理果胶对其流体行为影响最大。在质量浓度1.5 g/100 mL时,n值从0.925降低至0.903,溶液流体行为偏离理想型牛顿流体,这可能是因为微波处理30 min后,溶液中分子稳定的网络结构被破坏,外部强加的剪切运动对分子结构的破坏力加大,使溶液的表观黏度更大幅度地降低。
2.2 特性黏度与微波处理时间的关系

图 3 微波处理对不同质量浓度的果胶特性黏度的影响Fig. 3 Effect of microwave treatment on the intrinsic viscosity of pectin at different concentrations
由图3可看出,随着微波处理时间的延长,特性黏度降低,且随着样品质量浓度的增加,特性黏度的降低量减少,如在微波处理30 min后,果胶质量浓度为0.5、
1.0 、1.5、2.0 g/100 mL时,样品特性黏度从4.257 dL/g分别降低至2.856、2.940、3.571、3.651 dL/g。在微波处理
1 min后特性黏度降低幅度最大,这可能是因为果胶分子突然吸收电磁波,发生分子偶极作用和分子的强烈振动,使分子间的热能突然增加,糖苷键断裂,分子质量减少,特性黏度降低。微波处理果胶的时间越长,分子间热能越高,使果胶降解的程度越大,分子质量越小,其特性黏度越低。果胶质量浓度越高,分子间的接触及交联程度越大,黏度越高,微波处理后溶液中分子间交联转变的机会更大,其特性黏度减少量更小。果胶质量浓度低,单位分子接收到的能量大,所以容易降解。
2.3 反应动力学研究

图 4 不同质量浓度下-(随微波处理时间的变化Fig. 4 Change inof pectin at different concentrations as a function of microwave processing time
表 3 不同浓度果胶溶液微波处理后与微波处理时间的线性关系Table 3 Linear relationship betweenof pectin at different concentrations and microwave processing time

表 3 不同浓度果胶溶液微波处理后与微波处理时间的线性关系Table 3 Linear relationship betweenof pectin at different concentrations and microwave processing time
果胶质量浓度/(g/100 mL) 斜率截距R20.50.002 0.0490.986 1.00.0020.0400.993 1.50.0010.0150.958 2.00.0010.0050.954

表 4 不同质量浓度果胶微波处理过程中降解速率常数Table 4 First-order rate constants for the microwave-induceddegradation of pectin at different concentrations
0.5 g/100 mL时果胶降解速率最快,1.5 g/100 mL时果胶降解速率最慢,这和牛顿幂律拟合所得的流动行为指数的变化规律是一致的,这可能与果胶溶液的松弛程度和空间位阻有关。
2.4 微波非热效应研究

图 5 微波和沸水浴对果胶特性黏度的影响Fig. 5 Effects of microwave treatment and boiling water bath on the intrinsic viscosity of pectin
2.4.1 特性黏度由图5可知,沸水浴处理后果胶溶液的特性黏度降低,但高于微波处理后果胶溶液的特性黏度,且在较高质量浓度下,沸水浴处理后样品的特性黏度与微波处理后样品的特性黏度的差异较小。
2.4.2 表观黏度
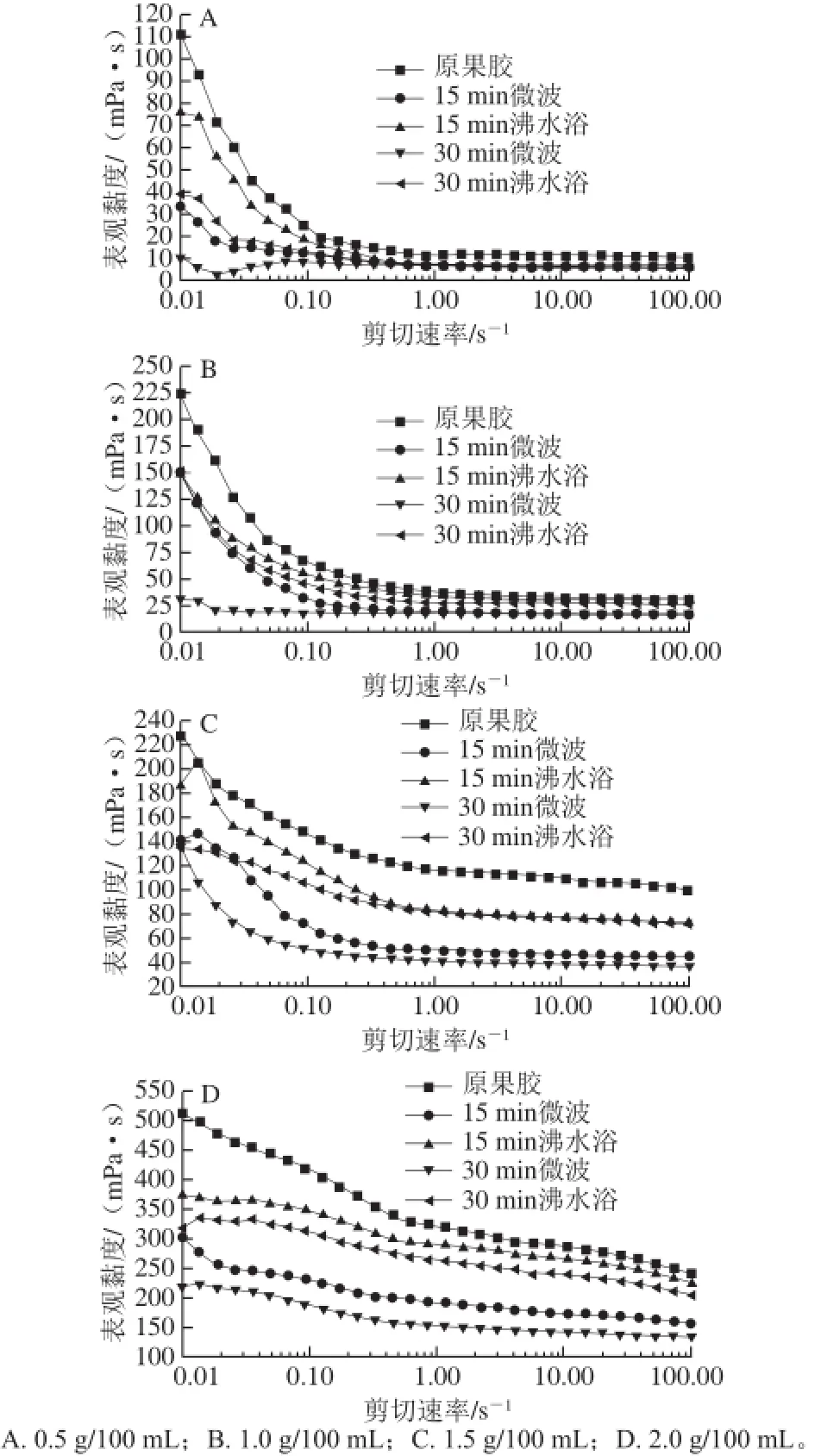
图 6 不同质量浓度果胶溶液微波和沸水浴处理后表观黏度随剪切速率的变化Fig. 6 Apparent viscosity versus shear rate plots of pectin after microwave and boiling water bath treatments
从图6可以看出,不同质量浓度的果胶溶液沸水浴处理一段时间后,表观黏度的变化规律与微波处理相似,均随剪切速率的增加、处理时间的延长而降低。但表观黏度的降低量要低于微波处理时表观黏度的降低量。
由图5、6可知,沸水浴无微波条件下处理果胶溶液,样品的降解程度要低于相同温度条件下微波处理后样品的降解程度,由此可以证明微波降解果胶的过程中除了热效应外可能还存在微波非热效应使果胶链断裂,导致果胶降解。
3 结 论
剪切速率扫描图表明果胶溶液的表观黏度随剪切速率的增加、质量浓度的降低、微波处理时间的延长而降低,通过牛顿幂律拟合可知,在低质量浓度(0.5 g/100 mL)条件下微波处理果胶对溶液的流体行为影响最大,在较高质量浓度(1.5 g/100 mL)条件下,微波处理果胶反而使溶液的流体行为更偏离理想型牛顿流体。
果胶溶液的特性黏度也随着质量浓度的降低、微波处理时间的延长而降低,根据特性黏度进行动力学拟合可知在微波功率680 W、处理时间30 min内,样品的与时间有良好的线性关系,与酸水解多糖相似,说明在此功率下,30 min内,微波降解果胶遵循一级动力学。在0.5 g/100 mL下降解速率最快,1.5 g/100 mL时降解速率最慢。
与沸水浴无微波处理的样品比较可知,微波条件下果胶的降解不只是因为热效应,同时还有微波非热效应的存在。具体是哪种非热效应导致果胶发生了降解,降解机理如何,还有待进一步探索研究。
[1] 任瑞, 马海乐, 朱春梅, 等. 香菇多糖微波降解反应动力学研究[J]. 化学工程, 2009, 37(4): 38-40. DOI:10.3969/j.issn.1005-9954.2009.04.011.
[2] WASIKIEWICZ J M, YEATES S G. “Green” molecular weight degradation of chitosan using microwave irradiation[J]. Polymer Degradation and Stability, 2013, 98(4): 863-867. DOI:10.1016/ j.polymdegradstab.2012.12.028.
[3] 周苗苗. 微波辅助降解壳聚糖的研究[D]. 北京: 中国科学院, 2015: 23-45.
[4] 牟莉. 微波辅助下木质纤维素降解与溶解过程的研究[D]. 长春: 东北师范大学, 2012: 33-49
[5] ZHOU G F, YAO W H, WANG C H. Kinetics of microwave degradation of λ-carrageenan from Chondrus ocellatus[J]. Carbohydrate Polymers, 2006, 64(1): 73-77. DOI:10.1016/ j.carbpol.2005.10.023.
[6] 来水利, 潘志友, 李晓峰. 微波辐射下壳聚糖降解性能的研究[J]. 陕西科技大学学报(自然科学版), 2005, 23(1): 38-40. DOI:10.3969/ j.issn.1000-5811.2005.01.010.
[7] BEDNARZ S, BOGDAL D. The comparative study of the kinetics of knoevenagel condensation under microwave and conventional conditions[C]//The Fifth International Electronic Conference on Synthetic Organic Chemistry. 2001.
[8] TAMAKI Y, KONISHI T, FUKUTA M, et al. Isolation and structural characterisation of pectin from endocarp of Citrus depressa[J]. Food Chemistry, 2008, 107(1): 352-361. DOI:10.1016/ j.foodchem.2007.08.027.
[9] 涂国云, 王正武, 王仲妮. 果胶的制备与应用[J]. 食品与药品, 2007, 9(6): 50-55. DOI:10.3969/j.issn.1672-979X.2007.06.018.
[10] CIRIMINNA R, CHAVARRíA-HERNÁNDEZ N, HERNÁNDEZ A I R, et al. Pectin: a new perspective from the bioref i nery standpoint[J]. Biofuels, Bioproducts and Biorefining, 2015, 9(4): 368-377. DOI:10.1002/bbb.1551.
[11] LEBRETON-DECOSTER C, ROUSSELLE P, LAPERDRIX C, et al. Oligogalacturonides improve tissue organization of in vitro reconstructed skin[J]. International Journal of Cosmetic Science, 2011, 33(5): 455-461. DOI:10.1111/j.1468-2494.2011.00655.x.
[12] COENEN G J, KABEL M A, SCHOLS H A. CE-MSn of complex pectin-derived oligomers[J]. Electrophoresis, 2008, 29(10): 2101-2111.
[13] CHEN J, LIANG R H, LIU W, et al. Degradation of highmethoxyl pectin by dynamic high pressure microfluidization and its mechanism[J]. Food Hydrocolloids, 2012, 28(1): 121-129. DOI:10.1016/j.foodhyd.2011.12.018.
[14] SHPIGELMAN A, KYOMUGASHO C, CHRISTIAENS S, et al. The effect of high pressure homogenization on pectin: importance of pectin source and pH[J]. Food Hydrocolloids, 2015, 43: 189-198. DOI:10.1016/j.foodhyd.2014.05.019.
[15] RALET M C, THIBAULT J F. Effect of extrusion-cooking on plant cell-walls from lemon. Part I. characterization of the water-soluble pectins and comparison with acid-extracted pectins[J]. Carbohydrate Research, 1994, 260: 283-296.
[16] CORREDIG M, WICKER L. Changes in the molecular weight distribution of three commercial pectins after valve homogenization[J]. Food Hydrocolloids, 2001, 15(1): 17-23. DOI:10.1016/S0268-005X(00)00044-8.
[17] 张丽芬. 果胶多糖超声波定向降解途径及机理研究[D]. 杭州: 浙江大学, 2013: 37-52.
[18] SESHADRI R, WEISS J, HULBERT G J, et al. Ultrasonic processing influences rheological and optical properties of high-methoxyl pectin dispersions[J]. Food Hydrocolloids, 2003, 17(2): 191-197. DOI:10.1016/S0268-005X(02)00051-6.
[19] GLEGG R E, KERTESZ Z I. Aftereffect in the degradation of cellulose and pectin by gamma rays[J]. Science, 1956, 124: 893-894. DOI:10.1126/science.124.3227.893.
[20] DOGAN M, KAYACIER A, IC E. Rheological characteristics of some food hydrocolloids processed with gamma irradiation[J]. Food Hydrocolloids, 2007, 21(3): 392-396. DOI:10.1016/ j.foodhyd.2006.04.010.
[21] BEN-SHALOM N, PLAT D, LEVI A, et al. Changes in molecular weight of water-soluble and EDTA-soluble pectin fractions from carrot after heat treatments[J]. Food Chemistry, 1992, 45(4): 243-245. DOI:10.1016/0308-8146(92)90154-T.
[22] 吴双双. 微波和高速剪切诱导果胶降解的研究[D]. 南昌: 南昌大学, 2014: 67-69.
[23] HUGGINS M L. The viscosity of dilute solutions of long-chain molecules. IV. dependence on concentration[J]. Journal of the American Chemical Society, 1942, 64(11): 2716-2718. DOI:10.1021/ ja01263a056.
[24] KARLSSON A, SINGH S K. Acid hydrolysis of sulphated polysaccharides. desulphation and the effect on molecular mass[J]. Carbohydrate Polymers, 1999, 38(1): 7-15. DOI:10.1016/S0144-8617(98)00085-X.
[25] BRADLEY T D, MITCHELL J R. The determination of the kinetics of polysaccharide thermal degradation using high temperature viscosity measurements[J]. Carbohydrate Polymers, 1988, 9(4): 257-267. DOI:10.1016/0144-8617(88)90044-6.
[26] MORRIS G A, CASTILE J, SMITH A, et al. The effect of different storage temperatures on the physical properties of pectin solutions and gels[J]. Polymer Degradation and Stability, 2010, 95(12): 2670-2673. DOI:10.1016/j.polymdegradstab.2010.07.013.
[27] MORRIS G A, de al TORRE J G, ORTEGA A, et al. Molecular fl exibility of citrus pectins by combined sedimentation and viscosity analysis[J]. Food Hydrocolloids, 2008, 2(8): 1435-1442. DOI:10.1016/ j.foodhyd.2007.09.005.
[28] MORRIS E R, CUTLER A N, ROSS-MURPHY S B, et al. Concentration and shear rate dependence of viscosity in random coil polysaccharide solutions[J]. Carbohydrate Polymers, 1981, 1(1): 5-21. DOI:10.1016/0144-8617(81)90011-4.
[29] KALE M S, YADAV M P, HICKS K B, et al. Concentration and shear rate dependence of solution viscosity for arabinoxylans from different sources[J]. Food Hydrocolloids, 2015, 47: 178-183. DOI:10.1016/ j.foodhyd.2015.01.012.
[30] LII C, CHEN C H, YEH A I, et al. Preliminary study on the degradation kinetics of agarose and carrageenans by ultrasound[J]. Food Hydrocolloids, 1999, 13(6): 477-481. DOI:10.1016/S0268-005X(99)00031-4.
Effect of Microwave Treatment on Rheological Properties and Degradation Kinetics of Pectin
LIANG Ruihong, WANG Shujie, HE Xiaohong, CHEN Jun*, LI Penglin, GUO Xiaojuan
(State Key Laboratory of Food Science and Technology, Nanchang University, Nanchang 330047, China)
The rheological properties and degradation kinetics of pectin at various concentrations (0.5, 1.0, 1.5 and 2.0 g/100 mL) subjected to microwave treatments for different time periods (0, 1, 3, 5, 8, 15, 20 and 30 min) were assayed. The results showed that both the apparent viscosity and intrinsic viscosity [η] of the samples decreased with the reduction of pectin concentration, and with the increase of microwave processing time and shear rate. Using power law equation to describe their rheological behaviors, the pectin solutions were a share-thinning non-Newtonian fl uid. Microwave treatment had the greatest impact on fl uid behavior at low concentrations of pectin. The microwave-induced degradation of pectin was fi tted based on [η] to a fi rst-order kinetic model, and pectin at 0.5 g/100 mL was degraded fastest and at 1.5 g/100 mL slowest. Compared with the samples subjected to boiling without microwave treatment, microwave treatment also had non-thermal effects in pectin degradation.
pectin; microwave; degradation; rheological properties; intrinsic viscosity; kinetics; non-thermal effect
10.7506/spkx1002-6630-201705001
TS207.1
A
2016-06-29
国家自然科学基金青年科学基金项目(31401655);国家重点实验室重点青年基金项目(SKLF-QN-201503)
梁瑞红(1966—),女,研究员,博士,研究方向为食品(含生物质)资源的开发利用。E-mail:liangruihong@ncu.edu.cn
*通信作者:陈军(1986—),男,副研究员,博士,研究方向为食品(含生物质)资源的开发利用。E-mail:chen-jun1986@hotmail.com
