清肺抑火片质量标准研究
2017-03-30邵维在段治尚万德生阙玉玲周永斌
邵维在,段治尚,万德生,阙玉玲,周永斌
(云南腾药制药股份有限公司研发部,云南腾冲679100)
清肺抑火片质量标准研究
邵维在,段治尚,万德生,阙玉玲,周永斌
(云南腾药制药股份有限公司研发部,云南腾冲679100)
目的:修订提高清肺抑火片的质量标准。方法:采用显微鉴别法、薄层色谱(TLC)法对制剂中的大黄、桔梗、黄柏、苦参进行定性鉴别;采用HPLC法对黄芩中的黄芩苷进行定量分析,色谱柱:Agilent TC-C18(250 mm×4.6 mm,5 m);流动相:甲醇-0.4%磷酸溶液(53:47);流速:0.6 mL/min;检测波长:280 nm;柱温:30℃。结果:在显微鉴别中检出草酸钙簇晶大,直径60~ 140 μm(大黄)、菊糖扇形或类圆形(桔梗);在TLC色谱中检出大黄、黄柏、苦参;黄芩苷进样量在0.025~4.000 μg/mL范围内线性关系良好,r=0.999 8;平均加样回收率99.8%,RSD=0.34%(n=9)。结论:所建立的方法可靠、准确、专属性强,可控制该制剂的质量。
清肺抑火片;显微;薄层色谱;高效液相色谱;黄芩苷
清肺抑火片为云南腾药制药股份有限公司的普药大品种,源于1963年版《中国药典》“清肺抑火丸”〔1〕处方增加片剂规格申报生产,由黄芩、栀子、黄柏、大黄、苦参、天花粉、知母、桔梗、前胡共9味药组成,现行版标准收载于《部颁标准》第二册〔2〕。具有清肺止嗽,降火生津。用于治疗肺热咳嗽,痰延壅盛,口鼻生疮,牙根出血,牙齿疼痛,咽喉肿痛,小便赤黄,大便干燥等症状。现在执行的“清肺抑火片”质量标准偏低,为控制其产品质量,笔者采用显微鉴别、薄层鉴别对方中大黄、桔梗、黄柏、苦参进行鉴别;采用高效液相色谱(HPLC)法对黄芩所含主要成分黄芩苷的含量进行定量测定。现报告如下。
1 仪器与试药
双目生物显微镜XSP-18B(南京江南光电股份有限公司);三用紫外仪ZF-2型(上海市安亭电子仪器厂);美国Agilent-1100液相色谱仪(安捷伦科技有限公司);UV1700紫外分光光度计(岛津苏州有限公司);用十八烷基硅烷键合硅胶为填充剂Agilent TC-C18(250 mm×4.6 mm,5 μm)色谱柱;SK5200H型超声仪(上海科导超声仪器有限公司);电子分析天平AE240(梅特勒托利多仪器上海有限公司);数显恒温水浴锅DRHH-S4(上海双捷实验设备有限公司);大黄对照药材(批号:120902-201010);盐酸小檗碱对照品(批号:110713-201212);苦参碱对照品(批号:110805-200508);黄芩苷对照品(批号:110715-201117,供含量测定用);上述所用的对照品均购买于中国食品药品检定研究院〔3〕。清肺抑火片(批号:120437、120438、120439)由云南腾药制药股份有限公司生产;HPLC用甲醇为色谱纯,水为娃哈哈饮用纯净水(大理娃哈哈食品有限公司制造),其他试剂均为分析纯。
2 方法与结果
2.1大黄、桔梗显微鉴别取本品,置显微镜下观察:草酸钙簇晶大,直径60~140 μm(大黄),菊糖扇形或类圆形(桔梗)〔4〕。见图1。

图1 大黄、桔梗显微图
2.2大黄的薄层鉴别取本品适量于乳钵中研细,称取0.6 g置150 mL平底烧瓶中,加甲醇20 mL,超声处理20 min,放冷,滤过,滤液置蒸发皿中蒸干,残渣加水10 mL使溶解,再加盐酸1 mL,转移至三角烧瓶中,于水浴上加热回流30 min,立即冷却,转移至分液漏斗中加乙醚震摇提取2次,每次20 mL,合并乙醚液,挥干,残渣加甲醇2 mL使溶解,即得供试品溶液。另取不含大黄的阴性对照品,同法制备阴性对照品溶液。再取大黄对照药材0.5 g,按照上述方法制备对照药材溶液〔4〕。照薄层色谱法(《中国药典》附录ⅥB)试验,吸取供试品溶液、阴性对照品溶液、对照药材溶液各4 μL,分别点于同一硅胶G薄层板(羧甲基纤维素钠为黏合剂)上,以石油醚(30~60℃)-甲酸乙酯-甲酸(15:5:1)的上层溶液为展开剂,展开,取出,晾干,置紫外光灯(365 nm)下检视。供试品色谱中,在与对照药材色谱相应的位置上,显相同的橙黄色荧光主斑点,置氨蒸气中熏后,斑点变为红色。阴性对照品无干扰,具有专属性,见图2~3。

图2 大黄紫外光灯(365 nm)TLC图
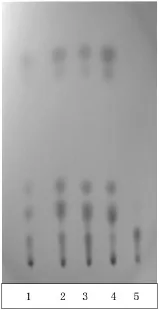
图3 大黄氨蒸气熏TLC图
2.3黄柏薄层鉴别取本品适量于乳钵中研细,称取1.2 g置150 mL平底烧瓶中,滴加氨溶液5 mL充分湿润,加二氯甲烷30 mL,超声处理15 min,滤过,滤液置蒸发皿中蒸干,残渣加甲醇1 mL使溶解,即得供试品溶液。另取不含黄柏的阴性对照品,同法制备阴性对照品溶液。再取盐酸小檗碱对照品,加甲醇制成1 mL含0.5 mg的溶液,作为对照品溶液〔4〕。照薄层色谱法(《中国药典》附录VI B)试验,吸取供试品溶液、阴性对照品溶液、对照品溶液各2 μL,分别点于同一硅胶G薄层板上(以羧甲基纤维素钠溶液为黏合剂),以正丁醇-冰乙酸-水(7:1:2)为展开剂,展开,取出,晾干,置紫外光灯(365 nm)下检视。供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的荧光斑点。阴性对照品无干扰,具有专属性,见图4。
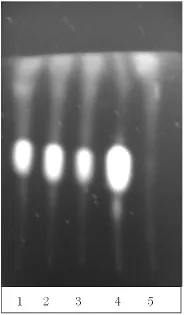
图4 黄柏紫外光灯(365 nm)TLC图
2.4苦参薄层鉴别供试品溶液的制备:取“2.3”项下的供试品溶液,作为苦参薄层鉴别项的供试品溶液。另取不含苦参的阴性供试品,按上述“2.3”项方法,同法制备阴性对照品溶液。再取苦参碱对照品,加乙醇制成每1 mL含0.5 mg的溶液,作为对照品溶液。照薄层色谱法(《中国药典》附录VI B)试验,吸取供试品溶液、阴性对照品溶液、对照品溶液各4 μL,分别点于同一硅胶G板薄层板上(以2%的氢氧化钠溶液制备),以甲苯-丙酮-甲醇(8:3:0.5)为展开剂,展开,取出,晾干,喷以碘化铋钾试液〔4-5〕。供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的斑点。阴性对照品无干扰,具有专属性,见图5。
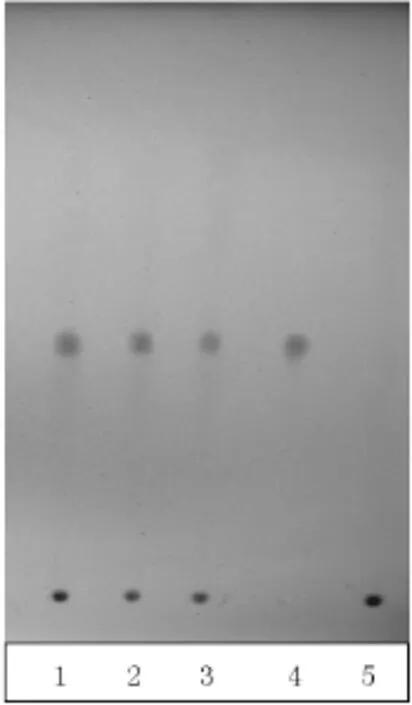
图5 苦参TLC图
2.5黄芩苷的含量测定方法与结果
2.5.1 色谱条件及系统适应性色谱柱:Agilent TC-C18(250 mm×4.6 mm,5 μm);甲醇-0.4%磷酸溶液(53:47)为流动相;流速:0.6 mL/min;检测波长:280 nm;柱温:30℃。进样量:10 μL;理论板数按黄芩苷峰计算应不低于4 000〔4,6-7〕。
色谱条件选择:以流动相为溶剂配制的对照品溶液,测定其紫外吸收光谱,从图6中看出,黄芩苷有两个最大吸收峰,第一个吸收峰与溶剂的最大吸收峰比较接近,第二个最大吸收峰波长为277.7 nm,参照中国药典“黄芩”项下的条件,确定280 nm波长为检测波长。见图6。

图6 黄芩甘紫外光谱吸收图
2.5.2 对照品溶液的制备精密称取黄芩苷对照品适量,置50 mL容量瓶中,加甲醇使溶解并稀释至刻度,制成每1 mL含25 μg的对照品溶液,摇匀,即得。
2.5.3 供试品溶液的制备取本品20片,研细,取粉末约0.5g,精密称定,置50 mL容量瓶中,加甲醇约30 mL,超声处理30 min,加甲醇至刻度,摇匀,滤过,取续滤液5 mL,置50 mL量瓶中,加甲醇至刻度,作为供试品溶液,即得〔4〕。
2.5.4 缺黄芩阴性样品的制备按处方比例,称取除黄芩外的其余药材,制备缺黄芩阴性对照品,按“2.5.3”项下方法制备缺黄芩的阴性对照溶液。其在与黄芩苷对照品色谱图中相同的保留时间处无吸收峰,表明阴性对照品无干扰,见图7。

图7 清肺抑火片HPLC图
2.5.5 线性关系考察精密称取对照品适量,加甲醇制成每1 mL含黄芩苷2.5、5、10、25、50、100、150、200、400 μg的溶液,测定,以进样量为横坐标,峰面积为纵坐标,绘制标准曲线,回归方程:Y=77.088 321 4X-38.857 937(r=0.999 8),理论板数平均为9 360。结果表明黄芩苷在0.025~4.000 μg之间与峰面积呈良好线性关系。
2.5.6 精密度试验精密吸取清肺抑火片(批号:120437)的供试品溶液10 μL,按“2.5.1”项下色谱条件分别进行6次,测定峰面积。结果,RSD=0.33%(n=6),表明本方法精密度较好。
2.5.7 稳定性试验取同一供试品溶液(批号:120437),分别于0、2、4、6、8、12、24 h按“2.5.1”项下色谱条件进样1次,测定峰面积。结果,RSD=1.34%,表明供试品溶液在24 h内峰面积基本稳定。
2.5.8 重复性试验取同一批样品,分别精密称取0.5、0.6、0.7 g各3份,按“2.5.3”项下方法制成供试品溶液,并按“2.5.1”项下色谱条件进样,测定其黄芩苷含量。结果,RSD=0.02%(n=9),结果表明本方法重复性良好。
2.5.9 加样回收率试验取已测定含量的同一批(批号:120437,含黄芩苷约10.4 mg/份)样品9份,每份约0.5 g,精密称定,精密加入一定量的对照品(含黄芩苷:1.00 mg/mL)8、10、12 mL,按供试品溶液的制备方法处理,依法测定,计算加样回收率,见表1。
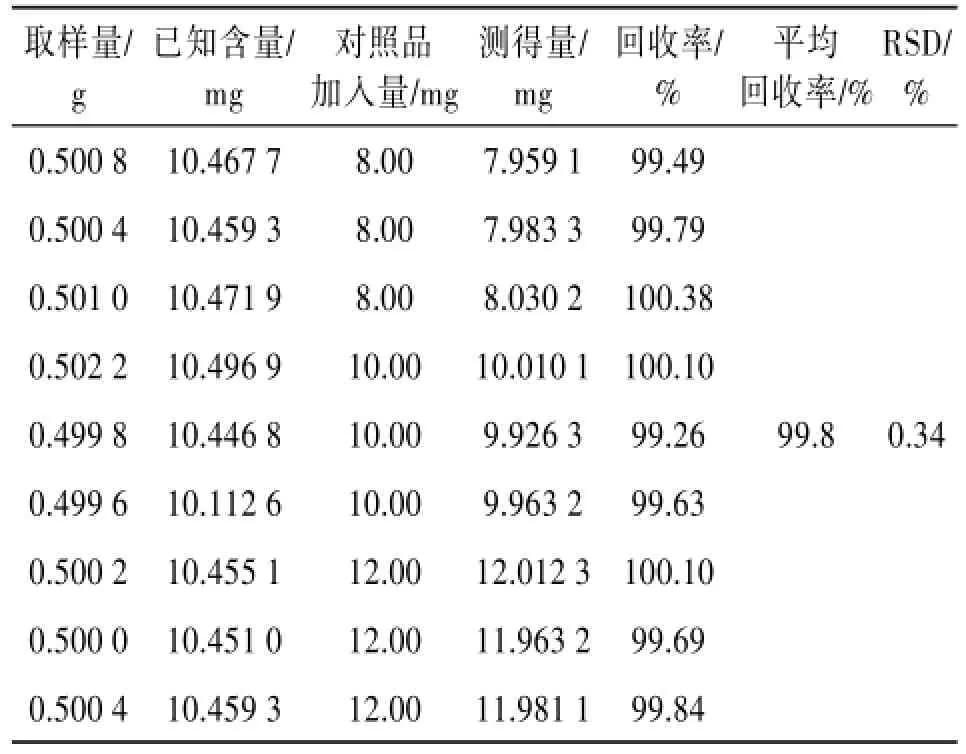
表1加样回收测定结果
2.5.10 样品含量测定依法对3批样品(120437、120438、120439)进行含量测定,见表2。

表2 3批样品含量测定
3 结论
清肺抑火片是我企业常年生产的品种,原质量标准较低,没有鉴别项及含量测定项。为了能更全面的控制清肺抑火片的质量,我们增加黄芩苷含量测定,大黄、黄柏、苦参薄层鉴别,及大黄、桔梗显微鉴别。黄芩是本品君药,清热燥湿,泻火解毒,其黄芩苷含量是评价药材质量的一个重要指标,故选作含量测定指标。大黄、桔梗是药品中以药粉投料的两味药材,故建立显微鉴别项。其次是大黄、黄柏、苦参定性鉴别方法成熟,专属性强,故建立薄层鉴别项。
〔1〕国家药典委员会.中华人民共和国临床用药须知(2010年版):化学药和生物制品卷〔M〕.北京:中国医药科技出版社,2011.
〔2〕卫生部.中华人民共和国卫生部药品标准〔M〕.北京:人民卫生出版社,1964.
〔3〕苗明三,李振国.现代实用中药质量控制技术〔M〕.北京:人民卫生出版社,2000:89.
〔4〕国家药典委员会.中华人民共和国药典:一部〔S〕.北京:中国医药科技出版社,2010:22-287.
〔5〕韩颂,于喜水,赵敏.苦参药材质量标准的研究〔J〕.中医药学报,2009,37(2):40-42.
〔6〕李晓梅,赵琪钟,卫舒帆.HPLC法测定清肺抑火片中黄芩苷的含量〔J〕.中国药师,2007,10(4):358-359.
〔7〕李应芬,李照宏,朱正华.清肺抑火片质量标准的研究〔J〕.中成药,2008,30(2):301-302.
Study on the Quality Standard of Qingfei Yihuo Tablet
Shao Weizai,Duan Zhishang,Wan Desheng,Que Yuling,Zhou Yongbin
(The Research and Development Department,Yunnan Tengyao Pharmaceutical Co.,Ltd.,Tengchong,Yunnan 679100,China)
Objective:To develop a method for revising and improving the quality standards of the Qingfei Yihuo Tablet.Methods:Microscopic identification and TLC method were adopted to identify the quality of the Dahuang,Jugeng,Huangbo and Kusheng in preparation and analyzing the Huangqigan in Huangqi by the method of HPLC.The analysis was performed on an Agilent TC-C18column with the mobile phase consisting of methanol(A)−0.4%phosphate acid(53:47)by gradient elution at a flow rate of 0.6 mL/min.The detection wavelength was set at 280 nm and the column temperature was 30℃.Results:Calcium oxalate crystal clusters were checked out by the method of microscopic identification,the diameter of Dahuang was 60-140 microns and the shape of Jugeng was inulin fan or quasi-circular.Additional,Dahuang,Huangbo and Kusheng were detected out by the methods of TLC and the HPLC results showed that the linear ranges were 0.025-4.000 μg/mL(r=0.999 8)for Huangqigan.The average recoveries(n=9)were 99.8%,RSD=0.34%.Conclusion:The developed method is accurate,reproducible and specific and the quality of the preparation can be controlled.
Qingfei Yihuo Tablet;microscopic identification;TLC;HPLC;Huangqigan
R284.1
A
2096-2266(2017)02-0020-04
10.3969/j.issn.2096-2266.2017.02.004
(责任编辑 李杨)
2015-06-16
2015-10-10
邵维在,工程师,主要从事中药新产品研发、产品工艺优化、中药治疗标准研究.
