非心脏手术患者围术期心肌梗死的特点及危险因素
2017-03-27崔军凯余阳周文君柳梅
崔军凯 余阳 周文君 柳梅
·临床研究·
非心脏手术患者围术期心肌梗死的特点及危险因素
崔军凯 余阳 周文君 柳梅
目的 研究非心脏手术患者围术期心肌梗死的高危因素及预后。方法 选取562例非心脏手术患者,收集患者的围术期病例资料,统计患者心肌梗死危险因素,围术期心肌梗死的发生率及特点。结果 在562例患者中共有19例发生围术期心肌梗死,发生率为3.4%,发生时间为术后(43.5±12.7)h。其中非ST段抬高心肌梗死11例,ST段抬高心肌梗死8例;左冠状动脉梗死14例,右冠状动脉梗死5例。年龄、既往有心肌梗死病史、术前有不稳定型心绞痛、术前心电图ST-T段改变、术前冠状动脉病变、术前糖尿病、术前高血压病、非心脏手术的级别均是围术期心肌梗死的高危因素,且与围术期心肌梗死的发生相关。19例心肌梗死的患者中,有16例行急诊经皮冠状动脉介入治疗,3例行药物保守治疗,处置后2例仍有不稳定型心绞痛, 1年内出现心功能下降1级及1级以上的患者有2例,心律失常1例,未再发生心肌梗死病例,无死亡病例。结论 多种因素会导致围术期心肌梗死的发生,加强术前评估,对存在高危因素的患者给予预防措施,一旦发生心肌梗死,及时处理,绝大部分患者预后尚可。
非心脏手术; 围术期; 心肌梗死
随着生活水平的提高及生活习惯的改变,冠状动脉粥样硬化性心脏病(冠心病)的发病率逐年升高。冠心病患者接受非心脏手术的比例也越来越高。冠心病、心律失常、糖尿病等多种因素可能会导致非心脏手术围术期心肌梗死的发生[1]。本研究纳入562例非心脏手术患者,分析多种危险因素与发生围术期心肌梗死的关系,心肌梗死的处理以及患者的预后。
1 对象与方法
1.1 研究对象
纳入2014年1月至2015年1月在江汉大学附属医院接受中、大型外科手术的非心脏手术患者562例。入选标准:(1)年龄18~80岁;(2)接受中、大型非心脏手术;(3)患者或委托人已签署知情同意书。排除标准:(1)终末期心功能衰竭;(2)合并严重的凝血功能障碍;(3)严重的其他器官功能衰竭。562例患者中男性321例(57.1%),平均年龄(56.2±13.5)岁。接受的手术包括呼吸系统手术81例(14.4%)、消化系统手术204例(36.3%)、泌尿系统手术110例(19.6%)及骨科手术167例(29.7%)。术前患者合并的内科疾病包括高血压病63例(11.2%)、糖尿病31例(5.5%)、冠心病53例(9.4%,既往有心肌梗死病史者12例)、慢性阻塞性肺疾病(COPD)32例(5.7%)、支气管炎35例(6.2%)、肾功能不全23例(4.1%)、慢性胃炎52例(9.3%)、胃溃疡25例(4.4%)、慢性肠炎12例(2.1%)。术前实验室检查示:肝功能异常47例(8.4%),肾功能异常23例(4.1%),贫血12例(2.1%),低蛋白血症49例(8.7%),N末端B型脑钠肽前体(NT-pro BNP)升高37例(6.6%)。术前辅助检查示:心电图检查提示节律异常21例(3.7%),束支传导阻滞36例(6.4%),ST-T段改变45例(8.0%),陈旧性Q波10例(1.8%),心室高电压28例(5.0%),肺型P波3例(0.5%),QT间期延长9例(1.6%),电轴偏移34例(6.0%);彩色多普勒超声心动图提示心脏扩大29例(5.2%),轻、中、重度瓣膜反流55例(9.8%),左心室射血分数<50%18例(3.2%),局部室壁运动异常7例(1.2%),胸片提示肺纹理增粗紊乱61例(10.9%)。1.2 心肌梗死诊断标准
根据《2014年美国心脏病学会/美国心脏协会(ACC/AHA)非心脏手术围术期心血管评估与治疗指南》[2],心肌梗死定义为符合急性缺血性心脏病表现,且心肌标志物升高超过诊断标准的所有患者。参考世界卫生组织诊断标准,对于外科手术患者,围术期心肌梗死的诊断要求至少符合下列3个条件中的2项:(1)缺血性胸痛病史;(2)心电图一系列动态改变;(3)血清中心肌标志物升高。
1.3 研究方法
统计562例患者术前、术后临床资料,分析年龄、既往是否有心肌梗死病史、术前是否有不稳定型心绞痛或心功能不全、术前心电图是否显示有心肌缺血ST-T段改变、术前是否明确诊断有多支病变、是否按标准使用抗凝药物、非心脏手术的级别等因素是否与发生围术期心肌梗死相关。非心脏手术的分级:(1)高危手术,即较大急诊手术,较大头颈部或胸部、腹部手术,主动脉与其他大血管手术,外周血管手术,预计手术时间较长、体液丢失或失血多的手术。(2)中危手术,即小血管外科术(包括颈动脉内膜剥离术),腹膜内与胸内手术、头颈部手术、耳鼻咽喉科手术、整形外科手术与前列腺手术。(3)低危手术,包括内镜、眼外科手术、乳腺手术与浅表操作及皮肤整形术等。低危手术围术期心血管并发症的发生率<1%,未纳入本研究。
1.4 统计学分析

2 结果
2.1 患者临床资料情况(表1)
562例患者中有19例发生围术期心肌梗死,发生率为3.4%,发生时间为术后6~79(43.5±12.7)h。所有心肌梗死患者均急诊或择期行冠状动脉造影证实罪犯血管。11例非ST段抬高心肌梗死患者中,罪犯血管为左前降支5例,左回旋支3例,右冠状动脉3例。其中2例右冠状动脉梗死的患者行抗凝、抗血小板、扩张冠状动脉、改善心肌氧耗等药物保守治疗后好转,其余患者行急诊经皮冠状动脉介入治疗(PCI),并根据术中病情置入冠状动脉支架。8例ST段抬高心肌梗死患者中,罪犯血管为左前降支5例,左回旋支1例,右冠状动脉2例。1例左回旋支梗死患者行药物保守治疗,其余患者行急诊PCI并置入支架。给予上述处理后仍有2例患者存在不稳定型心绞痛。其中1例患者(编号5)为股骨头置换术后患者,术后45 h发生急性Q波左心室心肌梗死,PCI术中证实为双支病变,罪犯血管为左前降支,同时右冠状动脉近段管壁存在30%狭窄,罪犯血管内置入药物洗脱支架1枚;另1例患者(编号15)为胃大部分切除,术后47 h发生急性非ST段抬高心肌梗死,PCI术中证实为三支病变,罪犯血管为左前降支,同时左回旋支开口处30%狭窄,右冠状动脉中段管壁存在20%狭窄,罪犯血管内置入药物洗脱支架1枚,术后仍存在心绞痛,不排除与非犯罪血管痉挛有关。
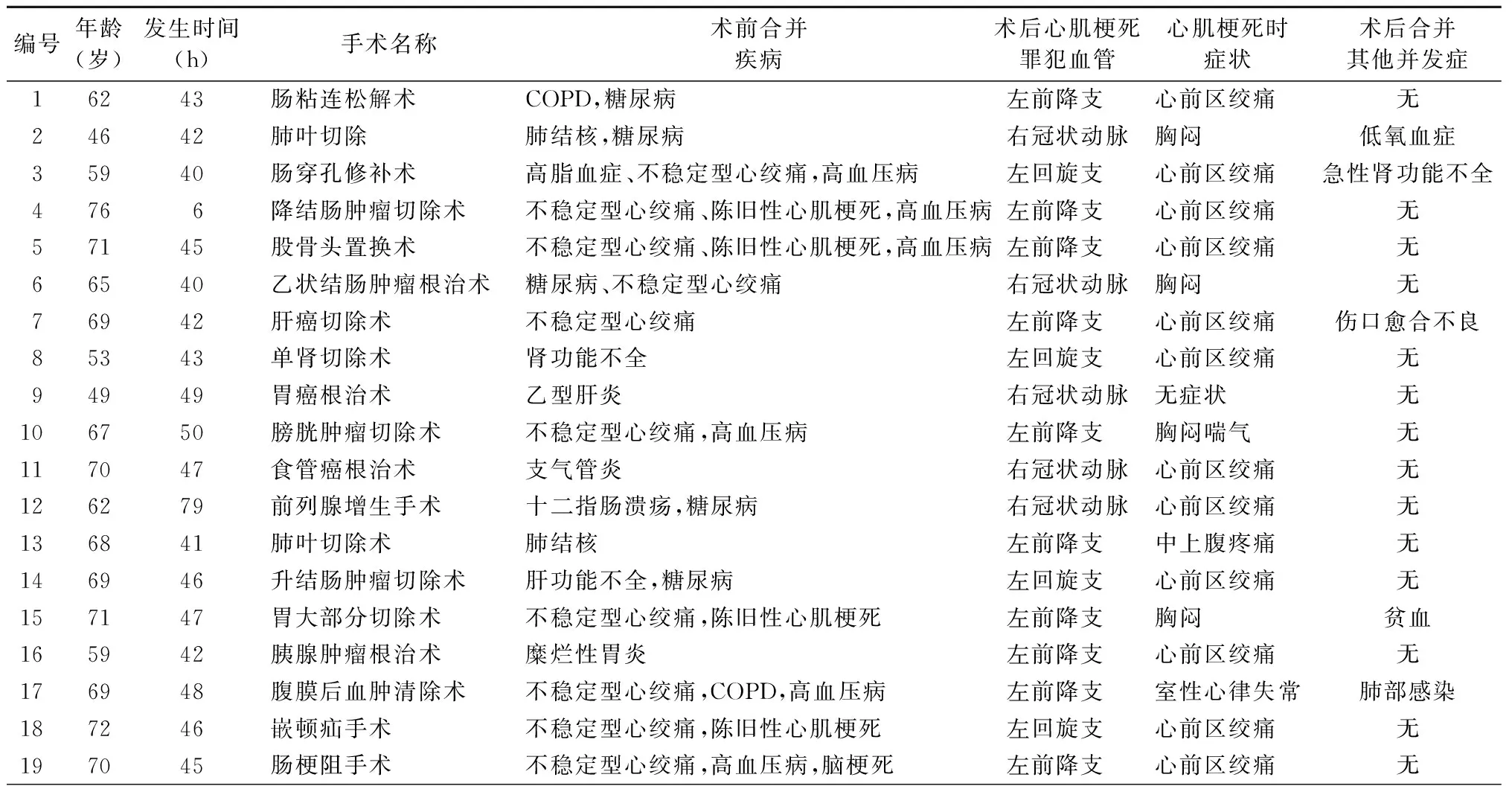
表1 19例围术期心肌梗死患者的临床情况
注:COPD,慢性阻塞性肺疾病
2.2 发生围术期心肌梗死的危险因素分析(表2、表3)
有33例患者术前有陈旧性心肌梗死,92例患者术前有不稳定型心绞痛病史,142例患者心功能异常,其中纽约心脏病协会(NYHA)心功能Ⅰ~Ⅱ级88例,Ⅲ~Ⅳ级54例。共有62例患者术前心电图检查有ST-T段改变。术前1年至术后1年共有128例患者冠状动脉造影提示阳性,其中多支病变78例,单支病变50例。有307例行高危手术,255例行中危手术。 年龄、既往有心肌梗死病史、术前有不稳定型心绞痛、术前心电图ST-T段改变、术前有冠状动脉病变、糖尿病、高血压病以及非心脏手术的级别均是围术期心肌梗死的高危因素。但NYHA心功能分级与心肌梗死的发生无显著相关。19例围术期心肌梗死的患者中,有16例行急诊PCI术,3例行药物保守治疗,处置后2例仍有不稳定型心绞痛。随访1年出现心功能下降1级及1级以上的患者有2例,心律失常1例,未再发心肌梗死,无死亡病例。相关危险因素与发生围术期心肌梗死的相关性分析显示:年龄、既往有心肌梗死病史、术前有不稳定型心绞痛、术前心电图ST-T段改变、术前冠状动脉病变、糖尿病、高血压病以及非心脏手术的级别均和围术期心肌梗死有显著相关性。
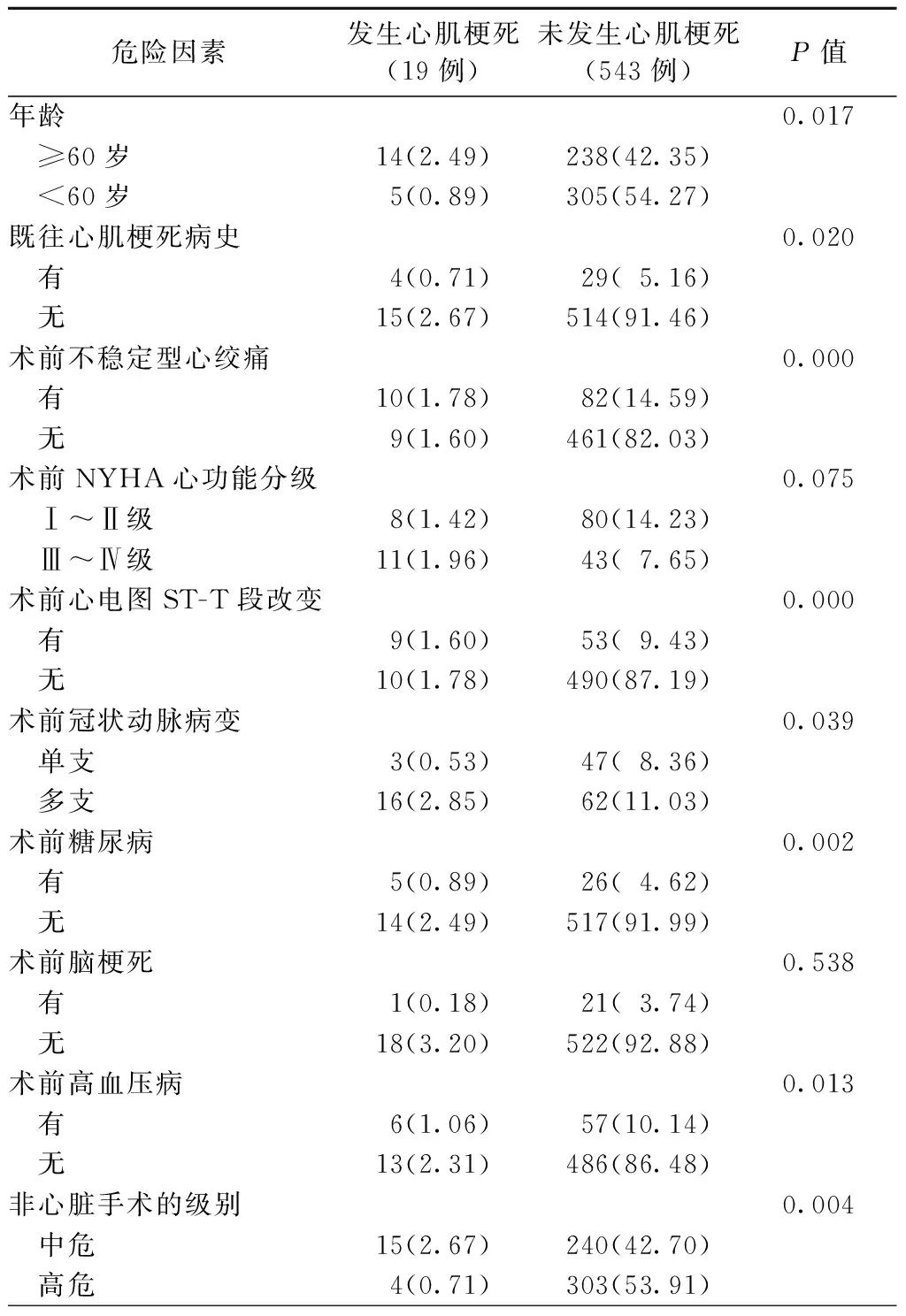
表2 发生围术期心肌梗死的危险因素分析[例(%)]

表3 危险因素与发生围术期心肌梗死的相关性分析
3 讨论
世界范围内,每年约2亿患者接受主要的非心脏手术,并且数量呈继续上升趋势[3]。非心脏手术围术期心血管事件风险明显增加。每年世界范围内大约有1千万成年患者在非心脏手术后30 d内发生心血管并发症[4]。2014年欧洲心脏病学会/欧洲麻醉学会(ESC/ESA)发布的《2014ESC/ESA非心脏手术指南:心血管评估与管理》[5]中指出,非心脏手术的并发症发生率为7%~11%,死亡率为0.8%~1.5%,其中约42%是心血管并发症。因此,认识非心脏手术围术期心血管并发症的发生机制,分析其高危因素,制定预防措施以及处理方式等极为重要。有研究表明,冠状动脉病变或其他相关的慢性疾病(如肾功能不全),均与围术期心血管不良事件相关[6]。围术期近期某些疾病史也证实和围术期心肌梗死独立相关,比如高危冠状动脉疾病、外科手术前6个月内有心肌梗死或加拿大心血管协会分级法(CCSC)Ⅲ级或Ⅳ心绞痛[7],外科手术前6个月行PCI术史[8],外科手术前3个月曾发生休克[9]。围术期心肌梗死的起因和病理生理机制尚不完全明确,但目前的主要观点认为,与三方面因素有关:(1)血流供需的不匹配,围术期血流动力学的波动可能会使狭窄的冠状动脉产生更严重的血流受限;(2)应激介导的急性冠状动脉综合征,外科手术作为应激因素,能导致机体交感神经活性增加,血压和心率急速上升,心肌氧耗量需求增加,应激也会导致血管炎性反应和血管舒张功能紊乱,这些因素都可能促进易损斑块的破裂[10-11];(3)术后凝血功能紊乱也会促进斑块破裂和冠状动脉内血栓形成,术中失血也会导致凝血因子的丢失,液体负荷失平衡。
围术期心肌梗死临床情况虽和未行手术患者的心肌梗死有共同之处,但也有一定的区别。围术期心肌梗死更加隐蔽,需要临床医师加强临床指标的检测。其主要原因包括:(1)外科手术患者胸痛发生率低,且胸痛症状经常会被镇静药物和麻醉药物的作用或残余效应所掩盖;(2)心电图对急性心肌梗死的诊断价值有限,尤其是非ST段抬高心肌梗死。且心电监护的导联通常为Ⅱ和V5导联,常见心肌缺血事件的导联改变出现在V2~V4导联;(3)心肌梗死标志物诊断心肌梗死在外科手术患者中敏感度和特异度均有所下降,围术期常见并发症如心力衰竭、微血栓形成、感染、肾功能不全均可能引起心肌梗死标志物的升高。因此,对接受外科手术的患者,围术期的监测需进一步加强。
目前,围术期心肌梗死的治疗方式基本分为3种。(1)药物治疗:包括抗血小板药物、β阻滞药、他汀类调脂药、血管紧张素转化酶抑制药(ACEI)、吗啡、硝酸甘油等。抗血小板药物又分为环氧化酶-1抑制药(COX-1)、腺苷二磷酸受体阻断药、血小板糖蛋白Ⅱb/Ⅲa受体拮抗药、磷酸二酯酶阻断药[12]。药物治疗的原则同非手术的心肌梗死,但是对外科手术患者来说,抗血小板药物导致的出血风险明显增加。(2)介入治疗:包括主动脉球囊反搏和PCI术。主动脉球囊反搏通过增加心脏舒张期冠状动脉血流改善心肌缺氧。介入治疗可及时开通阻塞的冠状动脉,出血风险小,是理想的手术方式。(3)冠状动脉旁路移植术(CABG):与PCI术相比,CABG创伤大,恢复慢。
本研究结果显示,在562例患者中共有19例发生围术心肌梗死,发生率为3.4%,马艳梅等[13]统计过412例老年冠心病非心脏手术患者的病例资料,共有10例患者发生围术期急性心肌梗死,发生率为2.4%。 年龄、既往有心肌梗死病史、术前有不稳定型心绞痛、术前心电图ST-T段改变、术前明确诊断有冠状动脉病变、糖尿病、高血压病以及非心脏手术的级别均是围术期心肌梗死的高危因素。但NNYHA心功能分级与心肌梗死的发生无显著相关,考虑与心功能不全的原因较多,不仅仅包括冠心病,还有其他疾病,如瓣膜病、高血压心脏病、心肌病等均有可能引起心功能不全。本中心经积极治疗,19例患者的预后均良好。
在心血管疾病发生率和外科手术量逐渐上升的情况下,围术期心肌梗死患者也逐年增加,在处理围术期心肌梗死患者时,医师需要比非围术期心肌梗死患者更加谨慎,既要处理心血管并发症,同时也要兼顾外科手术术后的潜在风险。及早识别危险因素,筛选出高危患者,并给予相应的预防措施是麻醉医师及外科医师的职责,对已发生的围术期心肌梗死,合理并正确的处理方式可将患者的损害降至最低。
[1] 王鹏,郑宏,叶建荣,等. 老年冠心病患者非心脏手术围术期心血管事件危险因素筛选与分析. 中华实用诊断与治疗杂志,2011,25(2):146-148.
[2] Fleisher LA, Fleischmann KE, Auerbach AD, et al. 2014 ACC/AHA guideline on perioperative cardiovascular evaluation and management of patients undergoing noncardiac surgery: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines. Circulation,2014,130(24):e278-333.
[3] Semel ME, Lipsitz SR, Funk LM,et al. Rates and patterns of death after surgery in the United States, 1996 and 2006. Surgery,2012,151(2):171-182.
[4] Botto F,Alonso-Coello P,Chan MT,et al. Myocardial injury after noncardiac surgery:a large, international,prospective cohort study establishing diagnostic criteria,characteristics, predictors,and 30-day outcomes. Anesthesiology,2014,120(3):564-578.
[5] Kristensen SD, Knuuti J, Saraste A, et al. 2014 ESC/ESA guidelines on noncardic surgery cardiovascular assessment and management. Kardiol Pol, 2014,72(11):857-918.
[6] 张菊红,黄至斌.非心脏手术围术期心血管事件风险评估与预防的研究进展. 心血管病学进展,2013,34(4):574-579.
[7] Kumar R,McKinney WP,Raj G,et al. Adverse cardiac events after surgery: assessing risk in a veteran population. J Gen Intern Med,2001,16(8):507-518
[8] Jørgensen ME,Torp-Pedersen C,Gislason GH, et al. Time elapsed after ischemic stroke and risk of adverse cardiovascular events and mortality following elective noncardiac surgery. JAMA, 2014,312(3):269-277.
[9] Hawn MT, Graham LA, Richman JS, et al. Risk of major adverse cardiac events following noncardiac surgery in patients with coronary stents. JAMA,2013,310(14):1462-1472.
[10] 王雅洁,于波.非心脏手术患者围手术期心肌梗死的处理.心血管病学进展,2009,30(4):638-642.
[11] 汤振,刘志忠,刘发军,等.冠状动脉慢性完全闭塞病变患者碎裂QRS波与血运重建术后左心室心功能改善的研究. 中国介入心脏病学杂志,2016,24(7):385-389.
[12] 郁正亚.非心脏手术患者围手术期抗血小板药物的使用. 中华临床医师杂志(电子版),2011,5(5):104-107.
[13] 马艳梅,王士雯,赵玉生. 老年冠心病非心脏手术患者围手术期心肌梗死的特点及危险因素. 中华老年多器官疾病杂志,2007,6(3):168-171.
Risk factors of perioperative myocardial infarction in the patients undergoing noncardiac surgery
CUIJun-kai,YUYang,ZHOUWen-jun,LIUMei.
DepartmentofGeneralSurgery,AffiliatedHospitalofJianghanUniversity,Wuhan430056,China
Correspondingauthor:YUYang,Email:yuyang7003@yahoo.com
Objective To investigate the risk factors and prognosis of perioperative myocardial infarction in the patients undergoing noncardiac surgery. Methods Clinical data of 562 patients who had accepted non-cardiac surgery was collected and retrospectively analyzed. The risk factors, treatments and outcomes of all these patients were recorded and analyzed. Results A total of 19 out of the 562 patients had perioperative myocardial infarction(PMI). The incidence was 3.4%. The mean occurrence time was (43.5±12.7)h after operation. Eleven PMI patients (11/19) were non-ST-segment elevation myocardial infarction and eight patients (8/19) were ST-segment elevation myocardial infarction. Thirteen PMI patients were left coronary artery occlusion and six patients were right coronary artery occlusion. Advanced age, history of myocardial infarction, unstable angina, change of ST-T segment on electrocardiography (ECG), multivessel diseases, diabetes,hypertension,and high risk non-cardiac surgery were the risk factors of PMI and positively correlated to PMI. Sixteen PMI (16/19) patients accepted PCI treatment and three patients (3/19) accepted drug conservative treatment. Two patients had unstable angina attack after treatment and one patient had arrhythmia. The heart function in two patients decreased by one or more than one class within the follow up of 1 year. No patient had recurrent acute myocardial infarction or deceased during follow-up. Conclusions Many factors could lead to PMI. Making preoperative assessment, recognizing patients of high risks and dealing with patients who had PMI in time was necessary.
Noncardiac surgery; Perioperative; Myocardial infarction
10.3969/j.issn.1004-8812.2017.02.006
430056 湖北武汉,江汉大学附属医院 武汉市第六医院普外科(崔军凯、余阳、周文君);武汉市第一医院重症医学科(柳梅)
余阳,Email:yuyang7003@yahoo.com
R542.22
2016-10-15)
