超声波处理对苦荞麦萌发、芽苗还原糖和总黄酮含量及抗氧化活性的影响
2017-03-14王顺民汪建飞
王顺民 汪建飞
(安徽工程大学生物与化学工程学院,安徽 芜湖 241000)
超声波处理对苦荞麦萌发、芽苗还原糖和总黄酮含量及抗氧化活性的影响
王顺民 汪建飞
(安徽工程大学生物与化学工程学院,安徽 芜湖 241000)
采用超声波预处理苦荞麦种子,研究超声波的功率、时间和温度对苦荞麦种子萌发率及麦苗还原糖、总黄酮含量和对DPPH自由基清除能力的影响。结果表明:超声波的功率、时间和温度对种子的初始萌发率影响显著。在超声波功率280 W、温度20℃、时间35 min处理条件下,苦荞麦种子的初始萌发率和最终萌发率分别达88.00%和100%。在超声波功率240 W、温度 15℃、时间35 min处理条件下,苦荞麦芽苗(4 d)中还原糖含量最高达11.24 g/100 g,分别比种子和对照增加303.99%和40.03%。而在超声波功率280 W、温度30℃、时间30 min处理条件下,苦荞麦芽苗(6 d)中总黄酮的含量达9.46 g/100 g,分别比种子和对照增加228.07%和69.71%,该条件下芽苗对DPPH自由基的清除率达86.47%。
苦荞麦;萌发;还原糖;总黄酮;DPPH
苦荞麦(Fagopyrumtataricum)是一种药食两用植物,富含黄酮类化合物[1]。苦荞麦萌发后芦丁含量成倍增加,营养价值和生物活性显著提高[2-5]。一些研究表明,磁场[6]、电场和超声波[7]等物理因素会对植物组织表现出一定的诱导效应[8-9],从而对萌发胚芽生长有调控作用[10-11],能有效激活荞麦种子萌发期的苯丙氨酸氨裂解酶(phenylalnine ammonialyase,PAL)和查尔酮异构酶 (chalconeisomerase,CHI),使黄酮类物质合成量增加[6]。植物在逆境胁迫下,通过调节基因的表达,细胞产生快速感应,进而使相关酶的活性发生变化,同时,黄酮类化合物和脯氨酸(Pro)等渗透调节物质含量增加,以此适应胁迫环境。超声波等逆境胁迫可诱导PAL和CHI基因的表达[12]。李妹娟等[13]研究表明,超声波处理可使在盐胁迫下水稻种子的萌发率均高于对照处理,使a-淀粉酶活性显著提高,MDA含量降低,SOD和POD活性增强。超声波(240 W,30 min,35℃)结合添加苯丙氨酸处理,可使发芽花生中白藜芦醇的含量比种子增加9.4倍[14]。超声波处理不仅可改善萌发后黄豆芽的品质[15],增加营养性,而且能有效增加发芽谷物中次生代谢产物的含量,增加其营养价值,提高发芽谷物品质[16]。目前采用超声波提取黄酮类物质报道较多[17-19],而关于超声波预处理植物种子后萌发富集活性成分的报道很少,仅报道[20]了超声波处理时间对甜荞的萌发及成分含量的影响。本研究将系统地研究超声波功率、处理时间,温度与苦荞种子的萌发及芽苗生物活性成分富集的关系。本试验拟采用超声波处理苦荞麦种子,研究超声波处理对萌发后的苦荞麦芽苗中还原糖、黄酮类物质的含量以及抗氧化性的影响。以期为促进苦荞麦种子萌发和提高其芽苗菜营养价值提供一种新的方法,为超声波技术的工业化应用提供理论参考。
1 材料与方法
1.1 材料与设备
苦荞麦:宁夏盐池县种子公司;
芦丁、3,5-二硝基水杨酸、1,1-二苯-2-苦基肼等:分析纯,国药集团化学试剂有限公司;
恒温培养箱:PYX-DHS·350-BS型,上海博泰实验设备有限公司;
电子天平:JY1002型,上海良平仪器仪表有限公司;
超声波清洗机:JK-400CDB型,合肥金尼克机械制造有限公司;
冷冻离心机:TGL-16A型,长沙平凡仪器仪表有限公司;
紫外可见分光光度计:UV-5800PC型,上海元析仪器有限公司;
大容量离心机:L-550型,湖南湘仪离心机仪器有限公司。
1.2 试验方法
1.2.1 原料预处理 选择粒大、饱满的苦荞麦种子,用清水冲洗干净,以1.0 g/L高锰酸钾溶液[7]浸泡消毒5~10 min,用清水洗涤至澄清。转入25℃纯净水中浸泡4 h,期间换水一次。后将种子置于50~60℃温水中催芽15 min。将种子(每组50~60粒)置于100 mL烧杯中,加入纯水浸没,进行超声波处理。
1.2.2 超声波处理对苦荞麦种子萌发的影响
(1) 超声波功率对种子萌发的影响:预处理后的苦荞麦种子置于烧杯,分别在功率为200,240,280,320,360,400 W,温度为20℃下,超声波处理30 min。后测定种子的萌发率,芽苗中总黄酮、还原糖含量及对DPPH自由基的清除能力。
(2) 超声波时间对种子萌发的影响:预处理后的苦荞麦种子置于烧杯,在功率为280 W,温度为20℃下,分别超声波处理10,15,20,25,30,35 min。后测定种子的萌发率,芽苗中总黄酮、还原糖含量及对DPPH自由基的清除能力。
(3) 超声波温度对种子萌发的影响:预处理后的种子置于烧杯,在功率为280 W,温度分别为15,20,25,30,35,40℃,超声波处理35 min。后测定种子的萌发率,芽苗中总黄酮、还原糖含量及对DPPH自由基的清除能力。
以上3种处理均做对照试验(除超声波未工作以外,其它条件相同下进行试验)。
1.2.3 苦荞麦种子萌发试验 将经超声波处理后的苦荞麦种子沥水,均匀平铺在内衬双层滤纸直径为10 cm的培养皿,后移至种子培养箱中,于25℃,RH 70%~80%下进行避光培养1~9 d,每天补充散失的水分2~4 mL。每12 h统计发芽种子数[8]。取生长期为2,4,6 d长势相同的苦荞麦芽苗称重,研磨,作为待测样品,进行各指标测定。
1.3 试验指标及测定方法
1.3.1 萌发率 自开始培养起,每隔12 h,依次测量其萌发率(胚轴突破种皮1 mm即为萌发),连续测定7 d,每组重复3次,直至个别处理组萌发率达到100%。萌发率及最终萌发率分别按式(1)、(2)计算:
(1)
(2)
式中:
Gt——萌发率,%;
Gf——最终萌发率,%;
m1——种子在1 d内的全部正常发芽粒数,粒;
梨花松开方竹沿河而行,她知道从此一别,就是永生。梨花走在河北岸,方竹走在河南岸;俩人依旧默默地隔河而行,边走边你看我一眼、我看你一眼。不知不觉,又回到他们相遇的地方,彼此都站住了。良久,梨花让方竹先走;但方竹不走,他让梨花先走。方竹说:“回去吧!回去……”梨花依旧没动。方竹又挥手道:“回去吧!回去……”梨花这才毅然转过身去,眼泪就哗地涌了出来。她小跑了几步,突然又站住了,转过身来,只见方竹依旧站在河边,呆呆地望着她,她就转身跑了。
m2——种子在7 d内的全部正常发芽粒数,粒;
m——供测种子的总粒数,粒。
1.3.2 总黄酮 采用亚硝酸钠—硝酸铝比色法[21]。将一定量的荞麦芽置于研钵中,加少量石英砂,以60%的乙醇进行研磨、提取,提取液用冷冻离心机在9 000 r/min下离心15 min,取上清液进行总黄酮测定。
1.3.3 干物质和还原糖含量
(1) 干物质含量:采用烘干恒重法[22]。
(2) 还原糖含量:采用3,5-二硝基水杨酸法[23]。
1.3.4 DPPH自由基清除能力 取苦荞麦芽苗乙醇提取物(60%乙醇,定容至50 mL) 液0.2 mL,加入7.8 mL浓度为0.025 mg/mL DPPH乙醇溶液,立即混匀,在一定时间间隔内(10 min) 测定其在517 nm处的吸光度。以VC做阳性对照。按式(3)计算苦荞麦芽苗对DPPH自由基的清除率[21]。
(3)
式中:
Q——对DPPH自由基的清除率,%;
A0——0时刻DPPH自由基反应液的吸光度;
At——t时刻DPPH自由基反应液基本稳定时的吸光度。
1.4 试验数据统计与方法
试验数据为3次重复,结果以平均值±标准差表示。采用SPSS 16.0统计分析软件对其进行One-way方差分析(ANOVA);并用Duncan's复相关试验法进行均值差异性的相关分析,显著性水平P≤0.05。
2 结果与分析
2.1 超声波处理对萌发苦荞麦种子萌发率的影响
苦荞麦种子吸水膨胀后,在24 h 时开始发芽,但在超声波的影响下部分种子发芽迟缓,甚至不发芽;而84 h时,不同超声波处理种子的萌发率达90%以上。之后继续培养,各处理种子的萌发率接近100%。故选择24,84 h的发芽率评价超声波处理对苦荞麦种子发芽率的影响。由表1可知,培养24 h时,苦荞麦种子的萌发率,随超声波功率的增加先增加后降低,随超声波处理时间的增加而升高(P<0.05),随超声波处理温度的升高而降低(P<0.05),且分别在功率为240 W、时间为 35 min和温度为20℃时萌发率最高。而培养84 h,萌发率差异不显著。说明低功率下促进萌发,而高功率则抑制萌发。在低功率下,延长超声时间和升高温度均有助于种子萌发。但温度过高则会抑制其萌发。因为超声波处理温度升高,会导致种子中酶的活性降低[24],抑制生长。不同超声波功率、时间和温度对种子初始萌发速率有影响,可能是少量的超声波能刺激细胞分裂,中等量的超声波会抑制细胞分裂,大量的能引起细胞死亡,长时间、大剂量的超声波处理则会造成负面的不可逆的影响[20]。有研究[20]证实,经10~20 min超声波处理(480 W)的荞麦种子萌发率比未经处理的增加90%,而超过30 min处理的萌发率反而降低。超声波处理可提高活力、显著促进荞麦萌发及幼苗的生长。但时间过久则会导致种子中酶活性降低。Yaldagard等[21]证实,在功率460 W,温度30℃下,超声波处理时间由5 min 延长至15 min时,可使大麦芽中а-淀粉酶的活性降低67.63%。超声波作为一种非生物逆境胁迫,对植物会造成一定的损伤。即适宜超声波功率、时间和温度均影响种子的萌发速率,但不会使种子失去萌发能力。
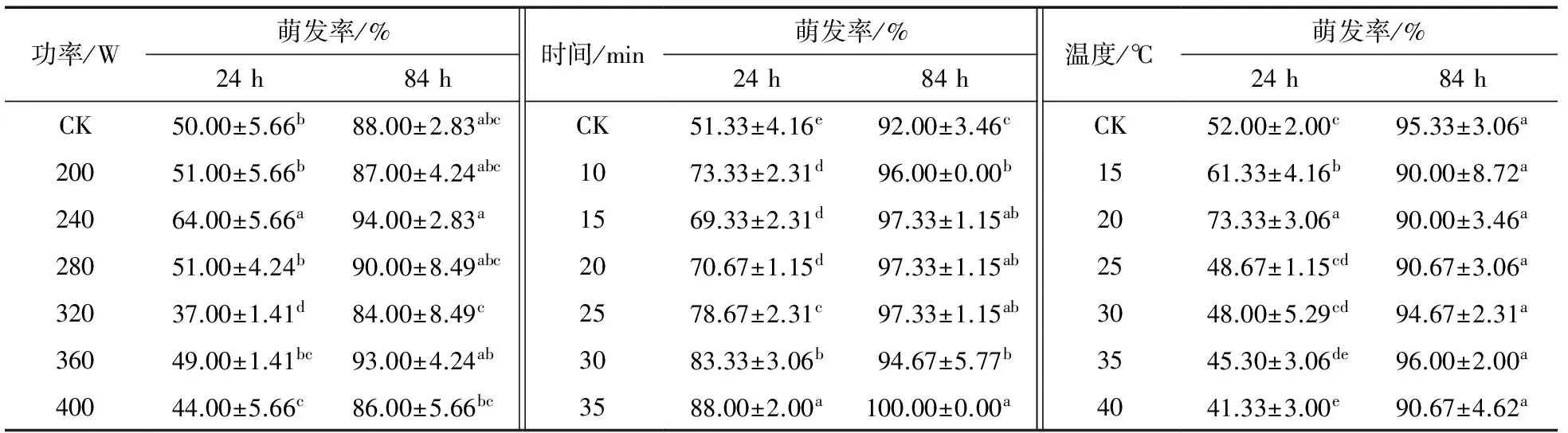
表1 不同超声波处理对苦荞麦种子萌发率的影响†Table 1 Effects of ultrasound treatment on the germination rate of seeds
2.2 超声波处理对苦荞麦芽苗中还原糖含量的影响
由图1可知,超声波处理后的苦荞麦芽苗的还原糖含量随着超声波功率的增加先增加后降低。培养2 d时,不同功率处理下的芽苗中还原糖含量显著高于种子而低于对照,而培养4~6 d 时,则显著高于种子和对照。培养6 d时,功率240 W下芽苗中还原糖含量比种子和对照组分别增加了3.36和0.21倍。说明超声波功率对芽苗中还原糖含量的影响显著(P<0.05)。
由图2可知,培养2 d时,不同处理时间下,苦荞麦芽苗中还原糖含量显著高于种子。其中10~15 min处理下的芽苗中还原糖含量高于对照,而30~35 min处理低于对照。培养4~6 d时,不同时间处理下的苦荞麦芽苗中还原糖含量显著高于种子和对照,且随超声波处理时间的增加先升高后降低,其中培养4 d时,超声10 min处理的种子,苦荞麦芽苗中还原糖含量达11.07 g/100 g。但6 d时,苦荞麦芽苗中还原糖含量要低于培养4 d的。萌发初期,种子中淀粉酶活力的逐渐增强,淀粉不断水解,还原糖含量增加。由于超声波处理加速了相关酶的活性,促进了芽苗生长,加速对还原糖的消耗,另外由于避光条件下无光合作用且呼吸作用会消耗还原糖等物质。
由图3可知,随着超声波处理温度的增加,培养2~4 d时,苦荞麦芽苗还原糖的含量先升高后降低。培养4 d时,15℃处理的种子,苦荞麦芽苗中还原糖含量最高,达11.24 g/100 g,比种子和对照分别增加303.99%和40.03%。作为一种非生物逆境胁迫,超声波对植物会造成一定的损伤。在逆境胁迫下,植物通过调节基因的表达,细胞产生快速感应,进而使相关酶的活性发生变化,同时,并增加黄酮类化合物和脯氨酸(Pro)等渗透调节物质含量,以此适应胁迫环境。培养6 d时,除15℃处理外,不同温度处理的还原糖含量均高于培养4 d的。因为适当的处理温度能够激活种子的淀粉酶,促进还原糖含量的增加。说明超声波处理有利于糖代谢进行,对苦荞麦种子萌发具有积极作用,但其处理温度不能过高,此结果与表1的结果相一致。
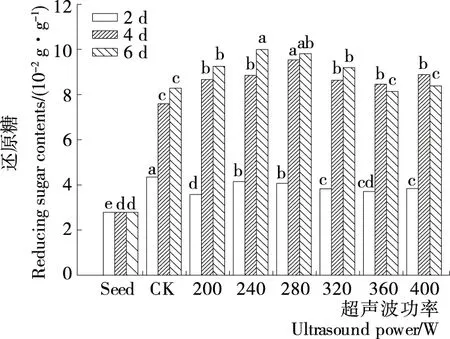
小写字母表示每列中不同处理功率间显著性差异(P<0.05)
2.3 超声波处理对苦荞麦芽苗中总黄酮含量的影响
由图4可知,培养2 d时,苦荞麦芽苗中的总黄酮含量显著低于种子而略高于对照,且随着功率的增加先增加后降低,功率小于360 W时,差异不显著。培养4~6 d时,总黄酮含量显著高于种子和对照(P<0.05),且随超声波功率的增加先升高后降低,功率280 W处理的芽苗中总黄酮含量最高。当培养6 d时,功率280 W处理的芽苗中,总黄酮含量达8.75 g/100 g,比种子和对照组分别增加了2.03和0.57倍。超声波功率对芽苗中总黄酮含量有显著影响(P<0.05)。
由图5可知,超声波处理后,培养2 d 时的芽苗中总黄酮含量均显著低于种子,但20~35 min处理下的含量高于对照。培养4 d时,总黄酮含量随超声波处理时间的增加而升高。30 min处理下,芽苗中总黄酮含量达4.77 g/100 g,比种子和对照分别增加65.36%和57.23%。培养6 d时,25,30 min 超声处理下芽苗中总黄酮含量可达9.16 g/100 g,其比种子和对照分别增加2.18和0.64倍。超声波处理时间的延长,显著增加苦荞麦芽苗中总黄酮含量。超声处理有助于芽苗中总黄酮含量的增加,但时间超过30 min 后,总黄酮含量开始有所降低。
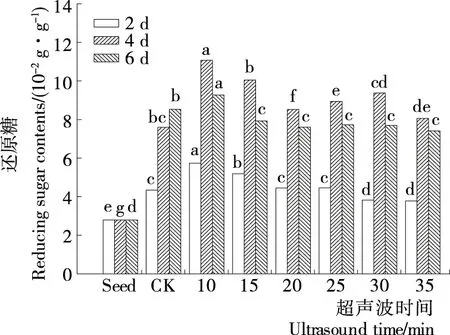
小写字母表示每列中不同处理功率间显著性差异(P<0.05)
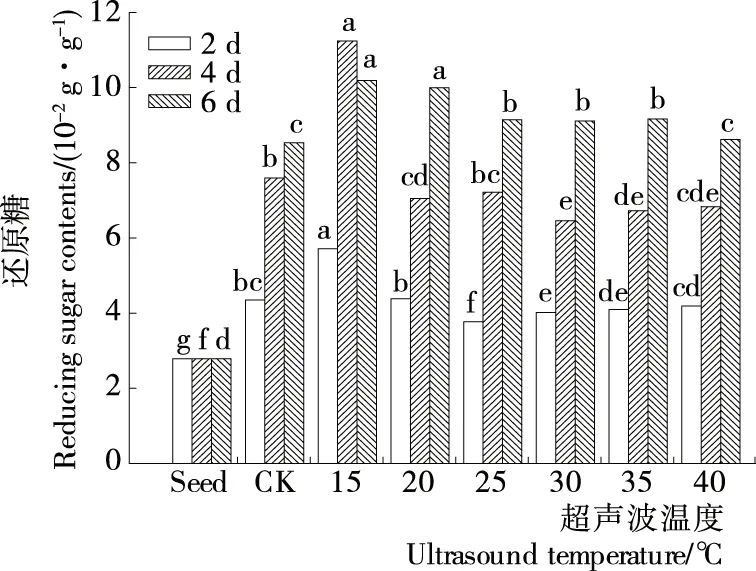
小写字母表示每列中不同处理功率间显著性差异(P<0.05)
由图6可知,培养2 d 时,随着超声波处理温度的升高,苦荞麦芽苗中总黄酮含量先增加后降低,30℃后含量高于对照。培养4 d时,芽苗中总黄酮含量在超声波处理温度低于15℃时低于种子和对照,而超声波处理温度为20~40℃时显著高于种子和对照。培养6 d下,苦荞麦芽苗中总黄酮含量随着超声波处理温度的升高先升高后降低,30℃最高,其苦荞麦芽苗中总黄酮的含量达9.46 g/100 g,分别比种子和对照增加228.07%和69.71%。培养6 d的芽苗中总黄酮含量的变化趋势与生长4 d的相似,但在相同处理温度下,含量要高于4 d处理。可能因为种子为了适应这种形成的超声波高温胁迫环境,通过调节基因的表达,细胞快速感应,进而改变相关酶的活性后合成了较高量的黄酮类化合物以调节渗透物适应新的胁迫环境。
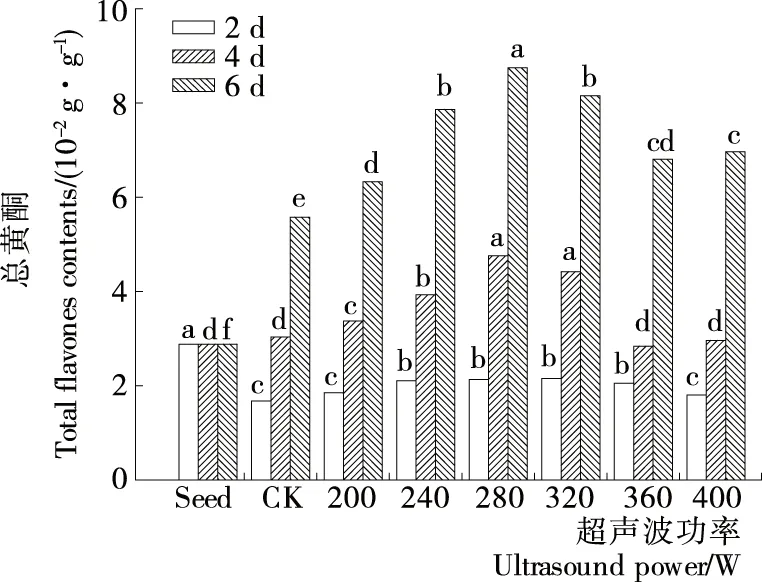
小写字母表示每列中不同处理功率间显著性差异(P<0.05)
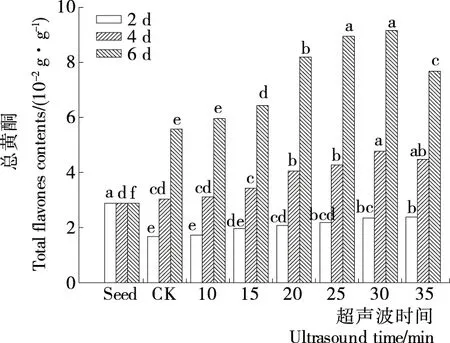
小写字母表示每列中不同处理功率间显著性差异(P<0.05)
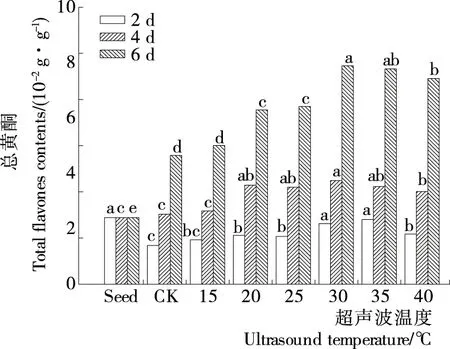
小写字母表示每列中不同处理功率间显著性差异(P<0.05)
2.4 超声波处理对苦荞麦芽苗清除DPPH自由基能力的影响
由图7可知,培养2 d,苦荞麦芽苗对DPPH自由基的清除率随超声波处理功率的增加先升高后降低,功率240~280 W 处理的芽苗,其对DPPH自由基清除率显著高于对照。培养4~6 d,240~280 W的功率处理下,超声波处理后的芽苗对DPPH自由基的清除率显著高于对照。其中培养6 d时,280 W功率的超声波处理下,苦荞麦芽苗对DPPH自由基的清除率为最高(85.64%),比对照增加13.70%,高于VC对DPPH自由基的清除率。
由图8可知,芽苗培养2 d 时,其对DPPH自由基的清除率随超声波处理时间的延长先升高后降低,15~35 min的超声处理下芽苗对DPPH自由基的清除率高于对照,而10 min 处理低于对照。培养4 d时,超声处理15~35 min下,苦荞麦芽苗对DPPH自由基的清除率比对照增加了2.32%~6.86%。培养6 d时,不同超声处理下的芽苗对DPPH自由基的清除率均显著高于对照。其中30 min超声处理的芽苗,其对DPPH自由基的清除率最高(83.81%),比对照增加10.57%,与 VC相比差异不显著。
由图9可知,芽苗培养2 d时,芽苗对DPPH自由基的清除率随超声波处理温度的升高先升高后降低。30℃ 处理下,芽苗对DPPH自由基的清除率最高,比对照增加8.72%。培养4 d时,15~40℃的超声处理下,芽苗对DPPH自由基的清除率比对照增加了5.66%~11.66%。培养6 d时,不同超声温度下的芽苗对DPPH自由基的清除率比对照增加了4.71%~14.13%,其中温度为30℃的超声波处理下,芽苗对DPPH自由基的清除能力最高(清除率达86.47%),高于 VC对DPPH自由基的清除率。本研究中,超声处理(280 W,30 min,30℃)可使苦荞麦芽苗中总黄酮的含量分别比种子和对照增加228.07%和69.71%,芽苗对DPPH的清除率为86.47%。荞麦经超声波处理(480 W,20 min),荞麦中总酚含量达到180.8 μg GAE/mL,总黄酮含量为156.701 mg芦丁/g样品,DPPH自由基清除活力达到最大值(0.197 mg Trolox eq/g冻干样)[20]。超声波预处理能有效提高苦荞麦种子的萌发率,增加总黄酮含量,增强对DPPH自由基的清除能力,以适应不良环境。但是超声波处理时,其功率、时间和温度均对种子有交互影响,故超声波处理的最佳工艺条件需要进一步优化。
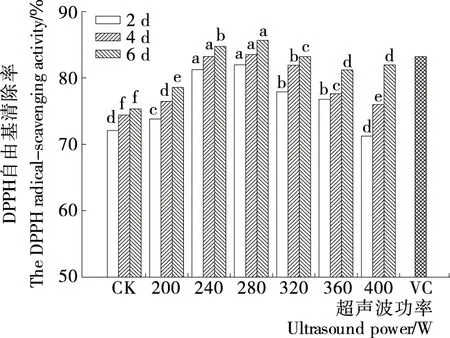
小写字母表示每列中不同处理功率间显著性差异(P<0.05)
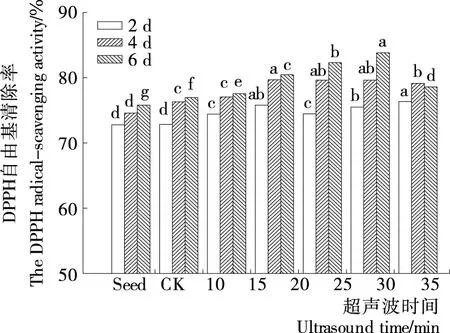
小写字母表示每列中不同处理功率间显著性差异(P<0.05)
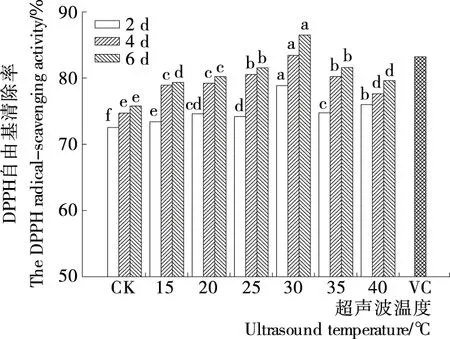
小写字母表示每列中不同处理功率间显著性差异(P<0.05)
3 结论
苦荞麦种子经适宜的超声波处理后,其萌发率显著提高。苦荞麦种子经超声波处理后,超声波的功率、时间和温度对其萌发生长过程有着显著影响,超声波显著增加荞麦芽苗中还原糖、总黄酮的含量,并且增强其对DPPH自由基的清除能力。适宜功率的长时间超声波处理,可以使苦荞麦芽苗中总黄酮含量高于对照和种子。在不同超声波功率、时间和温度处理下,培养2,4,6 d的苦荞麦芽苗中,总黄酮含量的高低与DPPH自由基清除能力大小的变化趋势一致。即苦荞麦芽苗中总黄酮的含量与DPPH自由基清除能力有一定的相关性。超声波处理对种子中生物活性成分的富集机理有待更深入的探究。
[1] ZHU Fan. Chemical composition and health effects of Tartary buckwheat [J]. Food Chemistry, 2016, 203(6): 231-245.
[2] 王学辉, 薛风照. 苦荞麦萌发过程中营养物质的变化及分布研究 [J]. 农业机械, 2013, 4(11): 63-66.
[3] BARTELME M Z. Germinated buckwheat more nutritious [J]. Food Technology, 2015, 69(7): 14-16.
[4] NAM T G, LEE S M, PARK J H, et al. Flavonoid analysis of buckwheat sprouts [J]. Food Chemistry, 2015, 170: 97-101.
[5] JIA Cai-feng, HU Wan-hong, CHANG Zhong-yi, et al. Acid alpha-galactosidase is involved in D-chiro-inositol accumulation during tartary buckwheat germination [J]. Acta Societatis Botanicorum Poloniae, 2015, 84(1): 53-58.
[6] ZHOU Xiao-li, FANG Xiang-zhou, YI Ming-ou, et al. Effect of magnetic field stimulation on flavonoid synthesis in tartary buckwheat (FagopyrumtataricumGaertn.) sprouts [J]. Food Science, 2012, 33(21): 20-23.
[7] IOAN O, SINGUREANU V, MOLDOVAN G, et al. High frequency pulsatile electromagnetic fields and ultrasound pulsatile fields impact on germination dynamic at ocimum basilicum L. and O. basilicum var. purpurascens benth., observed with open source software [J]. Notulae Botanicae Horti Agrobotanici Cluj-Napoca, 2016, 44(1): 41-47.
[8] CARBONELL M V, MARTINEZ E, AMAYA J M. Stimulation of germination in rice (Oryzasatival.) by astatic magnetic field [J]. Electromagnetic Biology and Medicine, 2000, 19(1): 121-128.
[9] 易翠平, 李艳, 黄寿恩, 等. 高浓度臭氧水对高粱种子发芽及其活性成分的影响[J]. 食品与机械, 2014, 30(6): 27-30.
[10] KADLEC P, RUBECOVA A, HINKOVA A, et al. Processing of yellow pea by germination, microwave treatment and drying [J]. Innovative Food Science & Emerging Technologies, 2001, 2(2): 133-137.
[11] ALADJADJIYAN A. Physical factors for plant growth stimulation improve food quality [J]. Food Production-Approaches, Challenges and Tasks, Publisher InTech, 2012, 1(20): 145-168.
[12] DHAWI F, AL KHAYRI J M. Magnetic field induced biochemical and growth changes in date palm seedlings [M]. [S. l.]: Date Palm Biotechnology, Springer Netherlands, 2011: 287-309.
[13] 李妹娟, 唐湘如, 聂俊, 等. 在盐胁迫下超声波处理对籼稻种子萌发的影响[J]. 西南农业学报, 2014, 27(6): 2 440-2 443.
[14] YU Miao, LIU Hong-zhi, YANG Ying, et al. Optimisation for resveratrol accumulation during peanut germination with phenylalanine feeding & ultrasound-treatment using response surface methodology [J]. International Journal of Food Science and Technology, 2016, 51(4): 938-945.
[15] 赵萌萌, 崔向军, 汪斌, 等. 超声波处理对黄豆种子萌发过程的影响[J]. 湖南农业科学, 2013, 35(7): 39-42.
[16] UPPAL V, BAINS K. Effect of germination periods and hydrothermal treatments on in vitro protein and starch digestibility of germinated legumes [J]. Journal of Food Science and Technology-Mysore, 2012, 49(2): 184-191.
[17] 杜若源, 谢晶, 王婷, 等. 超声波辅助提取银杏叶中总黄酮的工艺优化[J]. 食品与机械, 2015, 31(1): 167-170.
[18] 周燕芳, 丁利君. 超声波辅助提取艾叶黄酮的工艺研究[J]. 食品与机械, 2006, 22(4): 39-41.
[19] 陈洪彬, 郑金水, 蔡英卿, 等. 紫苏叶中总黄酮的超声波辅助提取工艺优化[J]. 食品与机械, 2014, 30(5): 232-236.
[20] 张冬晨, 刘海杰, 刘瑞, 等. 超声波处理对荞麦种子营养物质累积以及抗氧化活性的影响[J]. 食品工业科技, 2015, 36(7): 69-73, 78.
[21] JI Hong-bin, TANG Wen, ZHOU Xiao-li, et al. Combined effects of blue and ultraviolet lights on the accumulation of flavonoids in tartary buckwheat sprouts [J]. Polish Journal of Food and Nutrition Sciences, 2016, 66(2): 93-98.
[22] 李元, 牛文全, 吕望, 等. 加气灌溉改善大棚番茄光合特性及干物质积累[J]. 农业工程学报, 2016, 32(18): 125-132.
[23] 李合生. 植物生理生化实验原理和技术[M]. 北京: 高等教育出版社, 2000: 197-199.
[24] YALDAGARD M, MORTAZAVI S A, TABATABAIE F. The effect of ultrasound in combination with thermal treatment on the germinated barley’s alpha-amylase activity [J]. Korean J Chem Eng, 2008, 25(3): 517-523.
Ultrasonic enhancement of Tartary buckwheat germination and the production of nutrients in sprouts
WANG Shun-minWANGJian-fei
(CollegeofBiologicalandChemicalEngineering,AnhuiPolytechnicUniversity,Wuhu,Anhui241000,China)
Tartary buckwheat (Fagopyrumtataricum) seeds were treated using ultrasonic at different power and time and temperature. The exposed grains were germinated, then harvested after incubation on the 2rd, 4th, and 6th days. The effects of ultrasonic on the germination rate of the tartary buckwheat seeds and some nutrient compounds in the sprouts were detected, and the DPPH radical-scavenging activities of the seedlings were investigated. The results showed that with treatment of 280 W ultrasonic, at 20℃ for 35 min, the highest rates of initial (88.0%) and final (100.0%) germination were obtained after incubation. With the treatment of 240 W ultrasonic, at 15℃ for 35 min, the seedlings produced the highest contents of the reduced sugar (11.24 g/100 g) after 4 day of incubation, and this was 303.99% and 40.03% more than those in the seeds and the control, respectively. A treatment of seedlings of 280 W, at 30℃ for 30 min got the highest the total flavones contents, i.e., 9.46 g/100 g after 6 day of incubation, which was significantly increased by 228.07% and 69.71% compared to those in the seeds and the control, respectively. Moreover, the DPPH radical-scavenging activities of the seedlings was found to be 86.47%.
buckwheat; germination; flavonoids; reduced the sugar; DPPH - radical scavenging capacity
安徽省教育厅高校自然科学研究重点项目(编号:KJ2016A061);安徽工程大学国家科学基金预研项目(编号:2016yyzr08);安徽省大学生创新创业训练计划项目(编号:20161036300221)
王顺民(1975—),男,安徽工程大学副教授,博士。 E-mail:wangshunmin@126.com
2016-11-29
10.13652/j.issn.1003-5788.2017.01.037
