氧化锌催化尿素与乙二醇合成碳酸乙烯酯
2017-01-20陈艳梅王健沛朱志庆沈卫华方云进
陈艳梅,王健沛,朱志庆,沈卫华,方云进
(华东理工大学 化学工程联合国家重点实验室,上海 200237)
氧化锌催化尿素与乙二醇合成碳酸乙烯酯
陈艳梅,王健沛,朱志庆,沈卫华,方云进
(华东理工大学 化学工程联合国家重点实验室,上海 200237)
分别以商用氧化锌(ZnO-1)、碱式碳酸锌焙烧制备的氧化锌(ZnO-2)和尿素均匀沉淀法制备的氧化锌(ZnO-3)为催化剂催化尿素与乙二醇合成碳酸乙烯酯(EC),采用XRD、SEM和粒度分析仪对催化剂进行了表征,考察了不同制备方法对催化剂活性的影响,并优化了ZnO-3催化剂的制备条件。表征结果显示,ZnO-3催化剂属于六方晶系纤锌矿结构氧化锌,晶相完整,其XRD谱图中峰形尖锐,无其他杂质的衍射峰,其形貌主要由球状结构组成,粒径基本呈正态分布。实验结果表明,ZnO-3催化剂具有较高的催化活性,当ZnO-3催化剂的制备条件为n(尿素):n(Zn(NO3)2·6H2O)=4.0,溶于100 ℃水中加热回流4 h,500 ℃下焙烧2 h时,在n(乙二醇):n(尿素)=1.35、w(ZnO-3)=2%、170 ℃、0.07 MPa、2 h条件下催化尿素与乙二醇反应,EC收率可达93.6%。
氧化锌催化剂;尿素;乙二醇;碳酸乙烯酯
碳酸乙烯酯(EC)可作为性能优良的溶剂广泛应用于纺织、印染、高分子和电化学等方面[1-5],被称为21世纪的绿色化工原料[6-8],因此,研究EC的合成具有很好的工业应用价值。工业上通常采用CO2和环氧乙烷直接加压法合成EC[9],该方法工艺流程简单、收率高,但由于催化剂不易分离,原料易爆,副产物较多等问题[10-12],生产工艺还需进一步改进。尿素与乙二醇合成EC是近年来提出的新型工艺路线,与其他工艺相比,原料尿素廉价易得,反应条件温和,产物收率高[13-15];同时,EC可与甲醇酯交换生成绿色化工原料碳酸二甲酯并联产乙二醇,乙二醇可与尿素进一步反应生成EC,实现乙二醇的循环利用,降低了生产成本。因此,尿素法合成EC具有高效、绿色、环保等优点,且具有较高的经济效益和社会效益。以氧化锌及相关化合物为活性组分催化丙二醇与尿素合成碳酸丙烯酯的研究已有较多[16-21],而氧化锌作为催化剂用于催化乙二醇与尿素的反应,则鲜有文献报道。
本工作以不同制备方法得到的氧化锌为催化剂催化尿素和乙二醇合成EC的反应,采用XRD、SEM和粒度分析仪对制备的催化剂进行了表征,考察了不同制备方法对催化剂活性的影响,优化了催化剂制备条件。
1 实验部分
1.1 原料及试剂
氧化锌、碱式碳酸锌、苯乙酮:AR,国药集团化学试剂有限公司;Zn(NO3)2·6H2O、尿素、乙二醇:AR,上海凌峰化学试剂有限公司。
1.2 催化剂的制备
采用3种不同来源的氧化锌为催化剂:1)商品氧化锌,于100 ℃下干燥8 h,标记为ZnO-1;2)将商品碱式碳酸锌焙烧制备氧化锌,标记为ZnO-2,分别于240 ℃和500 ℃下焙烧2 h,焙烧后的氧化锌依次标记为ZnO-2.1和ZnO-2.2;3)尿素均匀沉淀法制备氧化锌,按一定配比将Zn(NO3)2·6H2O与尿素混合,溶于去离子水中,搅拌加热回流一定时间,过滤洗涤,于100 ℃干燥8 h,经高温焙烧制得氧化锌,标记为ZnO-3。
1.3 催化剂的表征
采用Bruker公司D8 Focus型X射线粉末衍射仪进行XRD表征,CuKα射线,管电压40 kV,管电流100 mA,扫描范围2θ=10°~80°,扫描速率8(°)/ min;采用Hitachi公司S-3400N型真空扫描电子显微镜进行SEM表征;采用Malvern公司MS-2000型激光粒度分析仪分析催化剂的粒径。
1.4 催化剂的评价
以EC的收率为评价指标考察催化剂的活性。在250 mL的三口烧瓶中分别加入60.06 g的尿素、83.7 g的乙二醇和2.9 g催化剂,搅拌加热至170 ℃,在减压(0.07 MPa)条件下恒温反应2 h。反应结束后冷却至室温,过滤分离脱除固体催化剂。采用上海科创有限公司GC9800型气相色谱仪分析产物组成,VO-1701毛细管色谱柱,FID检测,以苯乙酮为内标进行定量分析。采用脲酶法分析反应液中的尿素含量。
2 结果与讨论
2.1 催化剂的活性评价结果
不同氧化锌催化尿素与乙二醇反应的活性评价结果见表1(2组平行实验)。从表1可看出,尿素与乙二醇在无催化剂条件下也会发生反应,但EC的收率仅为10.4%。ZnO-2.1比ZnO-2.2的催化活性好,而ZnO-3催化剂的活性最高,EC收率可达93.6%,说明氧化锌的制备方法对其催化活性有显著的影响。

表1 不同氧化锌催化剂的催化活性Table 1 Reaction results over diferent ZnO catalysts
2.2 催化剂的表征结果
2.2.1 XRD表征结果
不同方法制备的氧化锌催化剂的XRD谱图见图1。

图1 不同方法制备的氧化锌催化剂的XRD谱图Fig.1 XRD spectra of ZnO catalysts prepared by diferent methods.
从图1可知, ZnO-3的XRD谱图与标准谱图(JCPDS80-0075)的衍射峰完全一致,即属于六方晶系纤锌矿结构氧化锌(晶胞参数为a=0.324 3 nm,c=0.519 5 nm),且晶相完整,峰形尖锐,无其他杂质的衍射峰。在ZnO-2.1的XRD谱图中,缺失(004)晶面的衍射峰,且存在杂质峰;而在ZnO-1的XRD谱图中,尽管衍射峰完整,但同样存在杂质峰,表明氧化锌纯度可能是影响其催化活性的因素之一。
2.2.2 SEM表征结果
不同方法制备的氧化锌催化剂的SEM照片见图2。从图2可看出,ZnO-1催化剂的晶体主要以棒状、粒状和片状结构存在,晶体形貌明显,但种类多且杂乱,尺寸不均一;ZnO-2.1催化剂的晶体呈棉絮状,晶体结构边缘模糊,形貌明显,与XRD表征结果中所分析的缺少(004)晶面而导致晶型不完整相吻合;ZnO-3催化剂的形貌主要由球状结构组成,尺寸均一且分布均匀。

图2 氧化锌催化剂的SEM照片Fig.2 SEM images of the ZnO catalysts.
2.2.3 粒径分析结果
不同方法制备的氧化锌催化剂的粒径分析结果见图3。由图3可知,ZnO-1催化剂的粒径主要分布在0.543 μm和2.598 μm 2个区域;ZnO-2.1催化剂的粒径分布较为分散,从0.399 μm到63.247 μm分布较宽;ZnO-3催化剂的粒径基本呈现正态分布,主要集中在2.418 μm处,与ZnO-3的SEM形貌相一致。

图3 不同ZnO催化剂的粒径分析Fig.3 Particle size analysis of the ZnO catalysts.
综上分析可知,由不同方法制备的氧化锌催化剂,虽具有相同的晶型,但形貌和粒径分布不同,且晶体纯度存在差异,这可能是影响催化活性的主要原因。为了提高催化剂的活性,增加EC的收率,有必要进一步优化催化剂的制备条件。
2.3 制备条件对ZnO-3催化剂活性的影响
将尿素与Zn(NO3)2·6H2O混合,加热溶解于水中,发生式(1)~(4)反应[22]。


图4是催化剂前体及焙烧后所得ZnO-3催化剂的XRD谱图。由图4可知,催化剂前体的衍射峰与标准碱式碳酸锌ZnCO3·3Zn(OH)2·H2O(03-0787)XRD谱图的特征峰一致,因此,尿素和Zn(NO3)2·6H2O在水溶液中加热反应生成的白色固体沉淀是碱式碳酸锌。将该固体置于马弗炉中高温焙烧,得到晶型完整、峰形尖锐、纯度较高的氧化锌晶体。而商品碱式碳酸锌结构为2ZnCO3· 3Zn(OH)2(54-0047),与尿素沉淀法制得的碱式碳酸锌结构不同,两者的热分解温度也不同,这可能是导致焙烧后的氧化锌活性不同的原因。
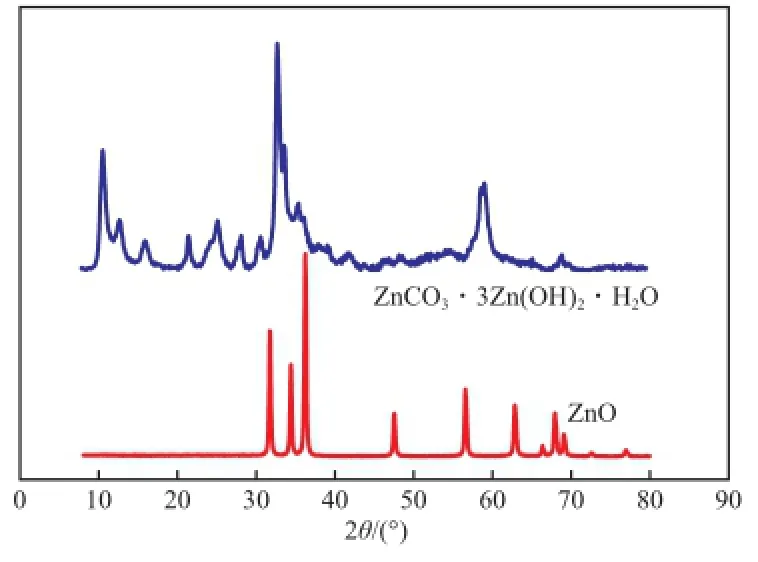
图4 催化剂前体及焙烧后所得ZnO-3催化剂的XRD谱图Fig.4 XRD spectra of basic zinc carbonate and ZnO-3.
2.3.1 原料配比的影响
在搅拌加热4 h,500 ℃焙烧2 h的条件下,改变尿素与Zn(NO3)2·6H2O的配比制得ZnO-3催化剂。尿素与Zn(NO3)2·6H2O的配比对催化剂活性的影响见图5。从图5 可看出,随尿素含量的增加,制得的ZnO-3催化剂催化尿素与乙二醇反应的EC收率也逐渐上升,在n(尿素):n(Zn(NO3)2· 6H2O)=4.0时,EC的收率达最大值93.6%。制备催化剂过程中发现,当尿素用量较小时,催化剂浆料的pH=6左右,陈化过程处于弱酸性环境,结晶效果较差;当尿素用量过大时,在加热过程中尿素的分解量增多,使水溶液碱性过大,部分生成的碱式碳酸锌沉淀重新溶解在溶液中,破坏原有的陈化结晶。因此,适宜的物料配比为n(尿素):n(Zn(NO3)2·6H2O)=4.0。

图 5n(尿素):n(Zn(NO3)2·6H2O)对反应收率的影响Fig.5 Efect ofn(urea):n(Zn(NO3)2·6H2O) on the catalyst activity.Reaction conditions referred to Table 1.Catalyst preparation conditions:heating and refuxing for 4 h,calcination at 500 ℃ for 2 h.
2.3.2 加热时间的影响
将尿素与Zn(NO3)2·6H2O混合后,置入水中进行加热,在这一过程中,尿素分解与Zn2+反应生成碱式碳酸锌沉淀。由于100 ℃下尿素在水溶液中分解缓慢,当加热时间过短时,产生的氨不足以与Zn2+反应,溶液处于弱酸性状态,所制得催化剂活性不高;加热时间延长时,有利于生成碱式碳酸锌沉淀,提高催化剂的活性。但加热时间过长,大量尿素分解产生的氨与Zn(OH)2发生式(5)的反应,生成锌氨络离子,破坏了原有晶型,导致催化剂活性下降。

加热时间对催化剂活性的影响见图6。从图6可看出,加热时间为4 h时所制得的催化剂催化尿素与乙二醇反应的EC收率达最高值93.6%,表明该条件下制备的催化剂活性最高。因此,适宜的加热时间为4 h。
2.3.3 焙烧温度的影响
高温焙烧是碱式碳酸锌分解成氧化锌的过程,因此,焙烧温度会直接影响碱式碳酸锌的分解和氧化锌的生成。在n(尿素):n(Zn(NO3)2· 6H2O)=4.0、搅拌加热4 h、焙烧时间2 h的条件下,改变焙烧温度制备ZnO-3催化剂,焙烧温度对催化剂活性的影响见图7。由图7可知,随焙烧温度的升高,EC的收率增加,当焙烧温度为500 ℃时,EC的收率达到最高为93.6%,继续升高焙烧温度,EC的收率下降。这是因为随焙烧温度的升高,碱式碳酸锌分解趋于完全,催化剂活性提高。当焙烧温度高于500 ℃时,导致催化剂在高温下发生烧结,造成颗粒增大,催化剂活性下降。因此,适宜的催化剂焙烧温度为500 ℃。

图6 加热时间对ZnO-3催化剂活性的影响Fig.6 Efect of heating time on the catalyst activity.Reaction conditions referred to Table 1.Catalyst preparation conditions:calcination at 500 ℃ for 2 h,n(Urea):n(Zn(NO3)2)=4.0.

图7 焙烧温度对ZnO-3催化剂活性的影响Fig.7 Efect of calcination temperature on the catalyst activity. Reaction conditions referred to Table 1.Catalyst preparationconditions:n(Urea):n(Zn(NO3)2)=4.0,heating and refuxing for 4 h,calcination time 2 h.
2.3.4 焙烧时间的影响
焙烧时间也是影响碱式碳酸锌分解的重要因素。在n(尿素):n(Zn(NO3)2·6H2O)=4.0、加热时间4 h、焙烧温度500 ℃条件下,改变焙烧时间制备ZnO-3催化剂。焙烧时间对催化剂活性的影响见图8。由图8 可知,EC的收率随焙烧时间的延长先增加后减小,焙烧2 h时达最高值93.6%。在温度为500 ℃时焙烧2 h,碱式碳酸锌已完全分解,继续延长焙烧时间,可能使生成的氧化锌晶粒融合长大,导致催化活性下降。因此,适宜的焙烧时间为2 h。

图8 焙烧时间对ZnO-3催化剂活性的影响Fig.8 Efect of calcination time on the catalyst activity.Reaction conditions referred to Table 1.Catalyst preparation conditions:heating and refuxing for 4 h,n(Urea):n(Zn(NO3)2)=4.0,calcination at 500 ℃.
3 结论
1)尿素均匀沉淀法制备的ZnO-3催化剂,属于六方晶系纤锌矿结构氧化锌,晶相完整,XRD谱图中峰形尖锐,无其他杂质的衍射峰,其形貌主要由球状结构组成,尺寸均一且分布均匀,粒径基本呈现正态分布。
2)采用尿素均匀沉淀法制备的ZnO-3催化剂具有良好的催化反应活性,适宜的制备条件为:n(尿素):n(Zn(NO3)2·6H2O)=4.0,溶于100 ℃水中加热回流4 h,500 ℃焙烧2 h,在此条件下制备的ZnO-3催化剂,在n(乙二醇):n(尿素)= 1.35、w(ZnO-3)=2%、170 ℃、0.07 MPa、2 h的条件下催化尿素与乙二醇反应,EC收率可达93.6%。
[1]Rokicki G. Aliphatic cyclic carbonates and spiroorthocarbonates as monomers[J]. Prog Polym Sci,2000,25(2):259 - 342.
[2]Macneil D D,Dahn J R. The reactions of Li0.5CoO2with nonaqueous solvents at elevated temperatures[J]. J Electrochem Soc,2002,149(7):A912 - A919.
[3]Aurbach D,Cofer Y,Ben Z M,et al. The behavior of lithium electrodes in propylene and ethylene carbonate:The major factors that influence Li cycling efficiency[J]. J Electroanal Chem,1992,339(1/2):451 - 471.
[4]程玲,周建成,吴东方,等. 碳酸乙烯酯的合成及应用进展[J]. 精细石油化工进展,2008,9(12):44 - 52.
[5]鲁荆林,刘绍岩,韩小平,等. 合成碳酸乙烯酯催化剂的研究进展[J]. 精细与专用化学品,2003,11(15):21 - 22.
[6]中国科学院山西煤炭化学研究所. 一种合成碳酸丙烯酯或碳酸乙烯酯的方法:1421431[P]. 2003-06-04.
[7]程能林. 溶剂手册[M]. 北京:化学工业出版社,1994:623.
[8]张玉宝. 碳酸乙烯酯的性质与应用[J]. 沈阳师范学院学报:自然科学版,1997,15(4):46 - 48.
[9]赵艳敏,刘绍英,王公应. 碳酸丙烯酯/碳酸乙烯酯的制备技术研究进展[J]. 现代化工,2005,25(zl):19 - 22.
[10]沈玺,刘定华,刘晓勤. 环氧乙烷水溶液和CO2合成碳酸乙烯酯[J]. 石油化工,2007,36(9):887 - 890.
[11]刘定华,赵贤广,王海善,等. 加压一步法合成碳酸乙烯酯[J]. 化学工业与工程技术,1998,19(1):1 - 3.
[12]黄焕升,杨波,黄科林,等. 碳酸乙烯酯合成的研究进展[J]. 化工技术与开发,2007,36(11):15 - 19.
[13]张瑾. 尿素合成碳酸乙烯酯的研究[D].天津:天津大学,2010.
[14]河北工业大学. 以脂肪族二元醇为循环剂的尿素醇解法合成碳酸甲酯的方法:1569810[P]. 2004-05-08.
[15]张建荣,王晓梅. 尿素醇解法合成碳酸乙烯酯及精制工艺研究[J]. 河北化工,2012,35(10):50 - 55.
[16]于桂玲,陈晓蓉,陈长林. ZnO/NaY催化尿素与1,2-丙二醇合成碳酸丙烯酯[J]. 南京工业大学学报:自然科学版,2008,30(3):11 - 14.
[17]李奇飚,彭伟才,郭启文,等. ZnO催化尿素和丙二醇合成碳酸丙烯酯的反应研究[J]. 燃料化学学报,2007,35(4):447 - 451.
[18]贾志光,赵新强,王延吉,等. 锌铁氧化物催化剂的制备及在尿素与1,2-丙二醇合成碳酸丙烯酯反应中的催化性能[J]. 石油学报:石油加工,2006,22(1):77 - 83.
[19]Zhao Xinqiang,Zhang Yan,Wang Yanji. Synthesis of propylene carbonate from urea and 1,2-propylene glycol over a zinc acetate catalyst[J]. Ind Eng Chem Res,2004,43:4038 -4042.
[20]Gao Zhiwen,Wang Shoufeng,Xia Chungu. Synthesis of propylene carbonate from urea and 1,2-propanediol[J]. Chin Chem Lett,2009,20:131 - 135.
[21]Li Qibiao,Zhao Ning,Wei Wei,et al. Catalytic performance of metal oxides for the synthesis of propylene carbonate from urea and 1,2-propanediol[J]. J Mol Catal A:Chem,2007,270:44 - 49.
[22]邸琬茗,宁文生,金杨福,等. 均匀沉淀法制备碱式碳酸锌的过程研究[J]. 材料导报,2015,29(18):60 - 64.
(编辑 平春霞)
Synthesis of ethylene carbonate from urea and ethylene glycol over zinc oxide catalyst
Chen Yanmei,Wang Jianpei,Zhu Zhiqing,Shen Weihua,Fang Yunjin
(State Key Laboratory of Chemical Engineering,East China University of Science and Technology,Shanghai 200237,China)
Zinc oxide catalysts,including commercial zinc oxide(ZnO-1),calcinated basic zinc carbonate(ZnO-2) and zinc oxide prepared by urea homogeneous precipitation(ZnO-3),were used for the catalytic synthesis of ethylene carbonate(EC) from urea and ethylene glycol(EG). The infuences of preparation methods on their catalytic properties were investigated by means of XRD,SEM and laser particle size analysis. The preparation conditions of ZnO-3 were optimized. The XRD result indicated the hexagonal wurtzite structure of ZnO-3 without difraction peak of any impurity,spherical morphology and uniform particle size distribution,which belonged to Gaussian distribution. The experimental results showed that the ZnO-3 catalyst had the highest catalytic activity and the optimization preparation conditions were:n(urea):n(Zn(NO3)2·6H2O) 4.0,heating and refuxing for 4 h at 100 ℃ and then calcining at 500 ℃ for 2 h. Under the conditions ofn(EG):n(urea) 1.35,ZnO-3 dosage 2%,170 ℃,0.07 MPa and 2 h,the EC yield reached 93.6%.
zinc oxide catalyst;urea;ethylene glycol;ethylene carbonate
1000 - 8144(2016)08 - 0920 - 05
TQ 203.2
A
10.3969/j.issn.1000-8144.2016.08.005
2016 - 01 - 25;[修改稿日期]2016 - 04 - 16。
陈艳梅(1991—),女,浙江省湖州市人,硕士生,电话 021 - 64252829, 电邮 cym864@163.com。联系人:方云进,电话021 - 64252829, 电邮 yjfang@ecust.edu.cn。
