纳米氢氧化镁的制备及其原位改性
2017-01-19申红艳刘有智
申红艳,刘有智
纳米氢氧化镁的制备及其原位改性
申红艳,刘有智
(中北大学超重力化工过程山西省重点实验室,山西太原030051)
以六水氯化镁为原料,氢氧化钠为沉淀剂,采用双向沉淀法,在制备过程中引入表面活性剂制备表面有机化的纳米氢氧化镁,同时提高氢氧化镁浆料的沉降性能。以吸油值、接触角衡量氢氧化镁的改性效果,考察了表面活性剂对氢氧化镁改性效果及氢氧化镁浆料沉降性能的影响。利用纳米粒度仪和红外光谱仪对产物的粒径和结构进行表征。结果表明,不同的表面活性剂对氢氧化镁的改性作用存在一定的差别。在制备过程中,油酸的引入对氢氧化镁的改性效果最好,改性后氢氧化镁的接触角和吸油值明显提高,同时改善了氢氧化镁浆料的沉降性能。FTIR分析证明油酸成功地吸附在氢氧化镁表面。
表面活性剂;改性;沉降;氢氧化镁;制备
氢氧化镁作为一种绿色环保型阻燃剂,因其具有热稳定性好、无毒、无腐蚀等优点,在高分子材料阻燃领域中得到广泛的应用[1-5]。但氢氧化镁颗粒表面能高,易团聚,同时由于氢氧化镁表面含有大量的羟基,使其呈亲水性,导致其难以在高分子材料中分散,当用量过大时,会使高分子材料的力学性能急剧下降,甚至使制品无法使用。因此,为了提高氢氧化镁与高分子材料的相容性和分散性,必须对氢氧化镁进行表面改性[6-8]。
李艳玲等[9]采用硅烷偶联剂对超细氢氧化镁进行湿法表面改性,改性后的氢氧化镁表面呈憎水性。ZHANG等[6]以硬脂酸钠为改性剂,采用超声法对氢氧化镁进行湿法改性,提高了氢氧化镁在有机相中的分散性。YAN等[10]采用油酸(OA)对氢氧化镁进行湿法改性,然后通过聚合反应,在油酸改性后的氢氧化镁表面生成聚甲基丙烯酸甲酯(PMMA)而将氢氧化镁微胶囊化,所获得的纳米氢氧化镁表面呈疏水性,分散性好,且在有机相中的分散稳定性和相容性得到了很大的提高。尽管这些改性方法均在一定程度上改善了氢氧化镁与高分子材料的相容性和亲和性,但绝大多数都是采用先制备氢氧化镁然后再进行改性的工艺,其工艺复杂,生产周期长,操作强度大,不易进行大规模生产。
针对目前改性方法存在的问题,本研究提出一步完成氢氧化镁的制备和改性,即在制备氢氧化镁的同时进行原位改性,研究了表面活性剂对氢氧化镁改性效果的影响。通过吸油值、接触角等测试氢氧化镁的改性效果,采用纳米粒度仪、红外光谱仪对产物进行表征,并且通过沉降实验考察氢氧化镁浆料的沉降性能。
1 实验部分
1.1 实验试剂
六水氯化镁,分析纯,天津市光复精细化工研究所;氢氧化钠,分析纯,天津市大陆化学试剂厂;聚乙二醇6000,分析纯,天津市光复精细化工研究所;脂肪醇聚氧乙烯醚,分析纯,天津市东丽区天大化学试剂厂;吐温80,分析纯,天津市风船化学试剂科技有限公司;硬脂酸钠,天津市大茂化学试剂厂;油酸,分析纯,天津市光复精细化工研究所;磺酸水杨酸,邻苯二甲酸二辛脂(DOP),分析纯,天津市东丽区天大化学试剂厂。
1.2 实验仪器
精密增力电动搅拌器(JJ-1型);数显恒温水浴锅(HH-S型);电子天平(AUY-120型);真空干燥箱(DZF-6030型);透射电子显微镜(JEM-1011型);纳米粒度仪(BT-90型);雷磁pH计(PHS-3C型);高速离心机(GT10-1);真空干燥箱(DZF-6030);傅里叶变换红外光谱仪(Spectrum Two型);接触角测量仪(JC2000D1型)。
1.3 实验方法与步骤
在室温下,按氢氧化镁的理论量取一定比例的表面活性剂,加入到200mL 0.75mol/L的氯化镁溶液中,超声至表面活性剂完全溶解并均匀分散于溶液中后,将其置于恒压滴液漏斗2中;取200mL 1.5mol/L的氢氧化钠溶液置于恒压滴液漏斗3中;水浴恒温至60℃,在强烈搅拌下,以3.3mL/min的滴加速度将上述的氯化镁溶液和氢氧化钠溶液同时滴加到50mL的衬底溶液中(0.75mol/L氯化钠)。滴加完毕后搅拌反应1h。将所得的氢氧化镁浆料经离心分离和洗涤数次至无氯离子检出后,在60℃下真空干燥6h,干燥后白色粉末样品封袋保存。
1.4 实验装置和工艺流程
(1)实验装置 采用双向沉淀法制备表面有机化的纳米氢氧化镁的实验装置如图1所示。
(2)工艺流程 采用双向沉淀法制备表面有机化的纳米氢氧化镁的工艺流程如图2所示。
1—精密增力电动搅拌器;2—恒压滴液漏斗;3—恒压滴液漏斗;4—恒温水浴锅;5—三口烧瓶
1.5 样品测试及表征
1.5.1 粒径测定
准确称量一定质量的氢氧化镁粉末置于100mL 烧杯中,加入一定量的2%的六偏磷酸钠溶液(质量分数),然后加蒸馏水至体积40mL,搅拌均匀后,用超声波细胞粉碎机超声分散3min,取上层液体加入样品池中,采用纳米粒度仪测定样品的的中位径50。
1.5.2 吸油值
称取1.000g样品放入蒸发皿中,将邻苯二甲酸二丁酯(DOP)置于微量滴定管中,滴入试样内,采用调墨刀将样品进行研压,使其以松散的小粒黏成一个密实的大团且不会破碎,又能黏附在蒸发皿上为终点,记录所用DOP的量[11]。
吸油值计算公式为式(1)。
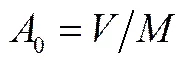
式中,0为吸油值,mL/g;为所用邻苯二甲酸二丁酯的体积,mL;为氢氧化镁的质量,g。
1.5.3 接触角
在10MPa的压力下,将样品制成一个平整的片,采用接触角测量仪测定氢氧化镁粉体的接触角。
1.5.4 沉降速度的测定
量取20mL氢氧化镁浆料置于量筒中,上清液高度每增加一定高度,读取一次沉降时间,以沉降速度曲线来表征沉降速度的快慢,上清液高度增长越快,表明氢氧化镁浆料沉降速度越快,从而表明其沉降性能越好。沉降速度计算如式(2)。
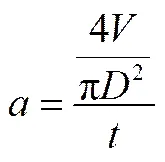
式中,为沉降速度,m/s;为氢氧化镁浆料上清液体积,m3;为量筒直径,m;为沉降时间,s。
1.5.5 红外光谱分析
采用KBr压片法,用傅里叶红外光谱仪,在450~4000cm–1进行红外光谱扫描,测试样品的结构。
2 实验结果与讨论
2.1 中位径分析
在反应温度为60℃,表面活性剂用量为1g/100gMg(OH)2时,考察了不同表面活性剂对氢氧化镁中位径的影响,结果如图3所示。
由图3可知,聚乙二醇6000、脂肪醇聚氧乙烯醚的加入,使氢氧化镁的中位径增大;吐温80、磺酸水杨酸、硬质酸钠和油酸的加入,使氢氧化镁的中位径减小,尤其是油酸和吐温 80的加入,使氢氧化镁的中位径明显减小,其中位径为139nm。
聚乙二醇6000和脂肪醇聚氧乙烯醚的分子式分别为HO(CH2CH2O)nH和RO(CH2CH2O)3H,从其分子式可以看出,聚乙二醇6000含有醚键与羟基两种亲水基,脂肪醇聚氧乙烯醚只含有醚键,两者均无疏水基。聚乙二醇6000、脂肪醇聚氧乙烯醚分子链上的大量醚键(—O—)与氢氧化镁表面的羟基以化学氢键的形式结合于氢氧化镁表面,即在氢氧化镁表面形成一层包覆层,当其用量为1.0g/100gMg(OH)2时,聚乙二醇6000、脂肪醇聚氧乙烯醚不足以完全包覆在氢氧化镁粒子表面,致使未完全包覆的氢氧化镁粒子间产生团聚,因此,采用聚乙二醇6000、脂肪醇聚氧乙烯醚改性后的氢氧化镁中位径增大。
吐温80属于非离子型表面活性剂,其分子链中的极性基团由聚氧乙烯基—(C2H4O)—构成,非极性基团为六元环结构。吐温80分子自发聚集呈疏水基朝外的反胶团,其中的醚键与氢氧化镁表面羟基以氢键的形式吸附在氢氧化镁表面形成保护层,增加了颗粒间的空间位阻。当其用量为1.0g/100gMg(OH)2时,吐温80分子在氢氧化镁表面形成单分子层定向排列,抑制了镁离子在已生成晶核表面的生长,从而使氢氧化镁的中位径有所减小。
油酸是含有一个双键的不饱和脂肪酸,分子式为CH3(CH2)7CH==CH(CH2)7COOH,其分子链中一端为非极性的十八碳直链状烃链,另一端为极性基团—COOH。由于油酸分子较大,且为不对称结构,其极性基团—COOH与氢氧化镁表面的—OH发生酯化反应,从而牢固地接枝到氢氧化镁表面。当其用量为1.0g/100g Mg(OH)2时,油酸分子在氢氧化镁表面形成单分子层定向排列,产生的空间位阻效应有效阻止了颗粒间的团聚,使氢氧化镁的中位径有所减小。
硬质酸钠分子式为C17H35COONa,其分子链中的极性基团为—COONa,非极性基团为直链烷烃结构,在氢氧化镁的表面改性过程中,氢氧化镁表面的—OH与硬质酸钠分子的极性基团—COONa以化学氢键的形式结合,当其用量为1.0g/100gMg(OH)2时,硬质酸钠分子在氢氧化镁表面形成单分子层定向排列,抑制了晶体的继续长大,从而使氢氧化镁的中位径有所减小。
磺酸水杨酸中的羧基、酚羟基与氢氧化镁表面的羟基发生类似醇和酸之间的酯化反应,形成稳定性较强的六元环结构。当其用量为1.0g/100gMg(OH)2时,磺酸水杨酸分子在氢氧化镁粉末表面产生的空间位阻效应抑制了晶体的继续长大,从而使氢氧化镁的中位径有所减小。
2.2 接触角分析
接触角是指液体在固体表面上达到热力学平衡时所形成的角。接触角<90°时,表明固体的表面能高和可润湿度高,亲水性强,亲油性弱;接触角>90°时,表明固体的表面能低和可润湿度低,亲水性弱,亲油性强。
氢氧化镁的接触角越大,在一定程度上表明氢氧化镁与高分子材料的相容性越好。图4为不同表面活性剂对氢氧化镁粉体接触角的影响。由图4可以看出,改性前氢氧化镁粉体接触角小于10°,其亲水性很强,而采用不同表面活性剂改性后的氢氧化镁粉体的接触角均有一定程度的增大,这表明改性后的氢氧化镁粉体表面被表面活性剂分子包覆,使表面活性剂的极性基团朝向氢氧化镁粉体的表面,而表面活性剂的非极性基团朝向气相,从而使氢氧化镁粉体的表面憎水性增加,极性减弱,由亲水性向亲油性转变,从而其接触角有所增大。当表面活性剂用量为1.0g/100gMg(OH)2时,油酸改性的氢氧化镁的接触角比其他表面活性剂改性的氢氧化镁的接触角大,说明油酸的改性效果最好。因此,确定油酸为最佳的表面改性剂。
2.3 吸油值分析
吸油值可用来直接判断改性剂在氢氧化镁颗粒表面所形成吸附层的稳定性以及改性后颗粒的润湿性和分散性,也可间接判断颗粒与有机相的相容性。因此,可用吸油值来评价改性效果。
图5为不同表面活性剂对氢氧化镁吸油值的影响。由图5可以看出,改性前氢氧化镁粉体的吸油值较高,对有机物邻苯二甲酸二丁酯(DOP)的无效吸收较严重,经表面活性剂改性后,其吸油值降低。原因在于表面活性剂在氢氧化镁表面定向排列吸附,其空间位阻效应抑制了颗粒间的团聚,提高了分散性,使颗粒间的空隙减少,同时使其表面由极性变为非极性,颗粒间的润滑性能变得较好。其中,油酸对氢氧化镁的改性效果最好。
2.4 沉降性能分析
在反应温度为60℃,表面活性剂用量为1g/100gMg(OH)2条件下对氢氧化镁进行在线改性,考察了不同表面活性剂对氢氧化镁浆料沉降性能的影响,如图6所示。由图6可以看出,无论加入何种表面活性剂,氢氧化镁浆料的沉降速度均呈上升趋势,即添加表面活性剂可以改善氢氧化镁浆料的沉降性能。原因在于表面活性剂通过“架桥”的方式同时吸附较多的氢氧化镁微粒,生成较大的絮状物,从而加速了氢氧化镁浆料的沉降速度。其中,油酸的加入使氢氧化镁浆料的沉降速度明显加快。因此,选择油酸作为最佳的表面改性剂。
2.5 FTIR分析
图7为油酸改性前后氢氧化镁的红外光谱图。从图7中可以看出,经油酸改性后的氢氧化镁,3699cm–1处的尖锐而高强度的吸收峰为氢氧化镁晶体结构中的O—H键的伸缩振动,在1601cm–1和1458cm–1处的吸收峰分别为Mg—OH和—OH的弯曲振动峰,除此外,在2925cm–1、2855cm–1和1705cm–1处出现了3个新的吸收峰,其分别对应于脂肪族—CH2—和—CH3的不对称、对称振动和油酸 中—COOH的特征吸收峰,并且改性后氢氧化镁表面羟基的强度减弱,这表明油酸分子与氢氧化镁表面的羟基发生化学键合,替代了氢氧化镁表面的部分羟基,从而使氢氧化镁由亲水性变为亲油性。
3 结论
采用双向沉淀法,以氯化镁为原料,氢氧化钠为沉淀剂,选用非离子表面活性剂(聚乙二醇6000、脂肪醇聚氧乙烯醚、吐温80)和阴离子表面活性剂(硬质酸钠、油酸、磺酸水杨酸)对氢氧化镁进行原位改性,研究了表面活性剂对氢氧化镁浆料的沉降性能、氢氧化镁粉体的粒径和表面性质的影响。
(1)6种表面活性剂对氢氧化镁的改性效果差别较大。在表面活性剂用量为1.0g/100g Mg(OH)2时,油酸对氢氧化镁的改性效果最好,氢氧化镁浆料的沉降速度提高2倍,所得氢氧化镁的中位径为139nm,氢氧化镁的接触角和吸油值有一定的提高。
(2)在一步合成表面有机化氢氧化镁的过程中,油酸替代了氢氧化镁表面的部分羟基,成功地结合在氢氧化镁表面,使氢氧化镁表面羟基的强度减弱,疏水性增强。
[1] MA X,MA H W,JIANG X Q,et al. Preparation of magnesium hydroxide nano owers from boron mudanti-drop precipitation method[J]. Materials Research Bulletin,2014,56(56):113-118.
[2] LI X,MA C,ZHAO J Y,et al. Preparation of magnesium hydroxide nanoplates using a bubbling setup[J]. Powder Technology,2010,198(2):292-297.
[3] HENRIST C,MATHIEU J P,VOGELS C,et al. Morphological study of magnesium hydroxide nanoparticles precipitated in dilute aqueous solution[J]. Journal of Crystal Growth,2003,249(1-2):321-330.
[4] YU J C,XU A W,ZHANG L Zi,et al. Synthesis and characterization of porous magnesium hydroxide and oxide nanoplates[J]. Journal of Physical Chemistry B,2003,108(1):64-70.
[5] SIERRA-FERNANDEZ A,GOMEZ-VILLALBA L S,MILOSEVIC O,et al. Synthesis and morpho-structural characterization of nanostructured magnesium hydroxide obtained by a hydrothermal method[J]. Ceramics International,2014,40(8):12285-12292.
[6] ZHANG F Z,ZHANG H,SU Z X. Surface treatment of magnesium hydroxide to improve its dispersion in organic phase by the ultrasonic technique[J]. Applied Surface Science,2007,253(18):7393-7397.
[7] GUO X J,ZHAO L H,ZHANG L,et al. Surface modification of magnesium aluminum hydroxide nanoparticles with poly(methyl methacrylate)one-potpolymerization[J]. Applied Surface Science,2012,258(7):2404-2409.
[8] LIU J H,FENG N,CHANG S Q,et al. Preparation and characterization of poly(glycidyl methacrylate)grafted from magnesium hydroxide particlesSI-ATRP[J]. Applied Surface Science,2012,258(16):6127–6135.
[9] 李艳玲,毛如增,吴立军,等. 超细氢氧化镁阻粉体表面改性研究[J]. 中国粉体技术,2007,13(1):29-32.
Li Y L,MAO R Z,WU L J,et al. Surface modification of ultrafine magnesium hydrozide powder[J]. China Powder Science and Technology,2007,13(1):29-32.
[10] YAN H,ZHANG X H,WEI L Q,et al. Hydrophobic magnesium hydroxide nanoparticlesoleic acid and poly(methyl methacrylate)-grafting surface modification[J]. Powder Technology,2009,193(2):125-129.
[11] 郑永林,王彩丽. 粉体表面改性[M]. 北京:中国建材工业出版社,2011.
ZHENG Y L,WANG C L. Surface modification of powder[M]. Beijing:China Building Materials Industry Press,2011.
Preparation andmodification of magnesium hydroxide nanoparticles
SHEN Hongyan,LIU Youzhi
(Shanxi Province Key Laboratory of High Gravity Chemical Engineering,North University of China,Taiyuan 030051,Shanxi,China)
Surface organic magnesium hydroxide nanoparticles were prepared by one-step double precipitation method with surfactant and using magnesium chloride hexahydrate as raw material and sodium hydroxide as precipitant. Moreover,the settlement property of the magnesium hydroxide slurry were improved. The oil absorption and contact angle were selected as parameters to characterize the effect of surfactant on the modified magnesium hydroxide and its slurry’s settlement property. The particle size and molecular structure were characterized by laser particle size analyzer(LPSA)and Fourier transform infrared spectrometer(FTIR),respectively. Experimental results indicated that the magnesium hydroxides modified by different surfactant were different. Among the surfactants,OA was the best for the modification of magnesium hydroxide,because the oil absorption and contact angle were significantly increased,and the settlement property was improved after OA modification. FTIR results indicated that OA had indeed been bonded on the surface of magnesium hydroxide.
surfactants;modification;sedimentation;magnesium hydroxide;preparation
TQ03.39
A
1000–6613(2017)01–0294–06
10.16085/j.issn.1000-6613.2017.01.037
2016-04-12;修改稿日期:2016-05-30。
国家自然科学基金(21376229)及山西省科技攻关项目(2015031019-5)。
申红艳(1982—),女,讲师,博士,主要从事纳米氢氧化镁阻燃剂的研究。E-mail:shy_shenhongyan@163.com。
