CHOP方案治疗血管免疫母T细胞淋巴瘤临床研究
2017-01-17陈宁斌何鸿鸣陈道光林剑扬郑艳彬邹思平王杰松陈秀容
陈宁斌,吴 晖,陈 英,杨 瑜,何鸿鸣,陈道光,林剑扬,郑艳彬,邹思平,王杰松,陈秀容
(福建省肿瘤医院、福建省肿瘤转化重点实验室、福建省医科大学教学医院,福建 福州 350014)
CHOP方案治疗血管免疫母T细胞淋巴瘤临床研究
陈宁斌,吴 晖,陈 英,杨 瑜,何鸿鸣,陈道光,林剑扬,郑艳彬,邹思平,王杰松,陈秀容
(福建省肿瘤医院、福建省肿瘤转化重点实验室、福建省医科大学教学医院,福建 福州 350014)
目的 探讨CHOP方案治疗血管免疫母T细胞淋巴瘤的临床疗效和不良反应。方法 入组18例经病理确诊的血管免疫母T细胞淋巴瘤患者,均接受CHOP方案化疗。结果 全部18例患者中,10例CR(55.6%),1例PR(5.6%),7例PD(38.9%)。治疗期间大部分患者出现Ⅲ、Ⅳ度骨髓抑制,经对症处理恢复正常,未影响下一步治疗。中位随访时间48个月,全组2 a无进展生存率38.9%,其中IPI≤1分者71.4%,IPI≥2分者18.1%。结论 CHOP方案治疗血管免疫母T细胞淋巴瘤有一定疗效,特别是对IPI≤1分者疗效显著,但对IPI≥2分者效果不理想,需进一步探讨有效治疗方案。
CHOP方案;血管免疫母T细胞淋巴瘤;疗效;不良反应
血管免疫母T细胞淋巴瘤是非霍奇金T细胞淋巴瘤中少见的一种亚型。2012年李小秋等[1]对全国10 002例恶性淋巴瘤病理类型分析中,血管免疫母T细胞淋巴瘤约占全部恶性淋巴瘤的3%。而在欧美国家,血管免疫母T细胞淋巴瘤占T细胞淋巴瘤18%。由于血管免疫母T细胞淋巴瘤发病率低,临床对其认识有限,治疗无统一规范。目前美国国家癌症综合网指南将其放入外周T细胞淋巴瘤治疗指南中,建议予含蒽环类治疗方案如CHOEP、CHOP、DA-EPOCH方案治疗。我科自2006年11月至2014年6月采用CHOP方案治疗20例血管免疫母T细胞淋巴瘤患者,现报道如下。
1 资料与方法
1.1 临床资料 入组18例经病理确诊的血管免疫母T细胞淋巴瘤患者,年龄45~72岁,中位年龄54岁;男12例,女6例;所有患者均行详细影像学检查(包括胸腹盆及病灶部位CT或MR检查)及骨髓穿刺检查;临床分期(Ann-arbor):Ⅰ期0例(0.0%),Ⅱ期1例(5.6%),Ⅲ期13例(72.2%),Ⅳ期4例(22.2%),其中Ⅲ~Ⅳ期患者占94.4%。国际预后指数(IPI):≤1分7例,≥2分11例。肿瘤主要侵犯:淋巴结、骨、韦氏环、肺、脾等部位。
1.2 治疗方法 所有患者采用CHOP方案化疗:环磷酰胺750 mg·m-2,静脉滴注,d1;长春瑞滨1.4 mg,静脉滴注,d1;表阿霉素70 mg·m-2,静脉滴注,d1;强的松 60 mg·m-2,口服,d1~5;每21 d为1周期,化疗6~8周期;每2周期评价疗效。
1.3 疗效评价 疗效评价按照国际淋巴瘤工作组制定非霍奇金淋巴瘤治疗反应标准,分为完全缓解(CR)、不确定的完全缓解(CRu)、部分缓解(PR)、稳定(SD)和进展(PD),以CR+CRu计算CR率,以CR+CRu+PR计算总有效率。
1.4 不良反应评价 按照WHO抗肿瘤药物不良反应分度标准分为Ⅰ~Ⅱ度。
1.5 随访 随访截止至2016年4月。失访患者生存期计算至末次随访时间。
1.6 统计学处理 采用SPSS 19.0进行统计分析,采用Kaplan-Meier方法对生存资料进行分析,采用log rank方法对生存资料进行检验,检验水准α=0.05。
2 结果
2.1 疗效 18例患者中,10例CR(55.6%),1例PR(5.6%),7例PD(38.8%)。中位随访时间48(22~108)个月,全组2 a无进展生存率38.9%。IPI≤1分者2 a无进展生存率71.4%,IPI≥2分者2 a无进展生存率18.1%。见图1~3。
2.2 不良反应 主要不良反应为血液学毒性,其中Ⅲ、Ⅳ度粒细胞减少占38.9%,22.2%出现粒缺伴发热;非血液学毒性发生率低,且较轻微;经过治疗所有不良反应均能恢复正常或减轻,不影响下周期化疗,未发生治疗相关死亡。
3 讨论
血管免疫母T细胞淋巴瘤是以T细胞异常增生伴内皮血管增生及滤泡树突细胞增生为主要特征的外周T细胞淋巴瘤,约占恶性淋巴瘤3%[1]。临床表现为侵袭性淋巴瘤,晚期常见,复发率高,预后差。

图1 全组患者2 a无进展生存曲线
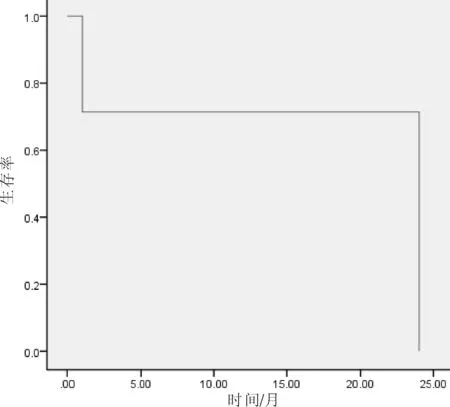
图2 IPI≤1分者2 a无进展生存曲线
目前,血管免疫母T细胞淋巴瘤的治疗尚无标准治疗方案,CHOP方案是最常选择治疗方案,但缓解期短,复发率高;一项Mata分析提示CHOP或CHOP样方案在血管免疫母T细胞淋巴瘤患者中CR率约为42.1%,5 a生存率为32.1%[2]。Mourad等[3]分析了GELA各项研究中的157例血管免疫母T细胞淋巴瘤患者,不同研究中依据患者年龄和年龄纠正后的IPI分组,分别接受ACVBP、m-BACOD、VIM、或CHOP、CHOP样方案,其中约50%患者接受大剂量化疗,分析发现CR率为46%,与常规化疗比较,强化方案未能带来更好生存预后。Federico等[4]分析了国际T细胞计划中243例血管免疫母T细胞淋巴瘤患者,82%接受蒽环类药物的联合化疗,5 a无失败生存率18%,总生存率为32%。Schmitz等[5]总结343例外周T细胞淋巴瘤,其中血管免疫母T细胞淋巴瘤28例,结果在CHOP方案基础上加用依托泊苷仅提高年轻、乳酸脱氢酶正常患者的无事件生存率,对其他亚组和总生存期无明显影响,是否加用依托泊苷更有利于血管免疫母T细胞淋巴瘤患者的预后尚无定论。

图3 IPI≥2分者2 a无进展生存曲线
本文结果显示,18例患者中10例CR(55.6%),1例PR(5.6%),7例PD(38.8%)。中位随访时间48(22~108)个月,全组2 a无进展生存率38.9%。IPI≤1分者2 a无进展生存率71.4%;IPI≥2分者2 a无进展生存率18.1%。既往研究[4]显示,IPI≥2分是重要预后因素,在大多数病例分析中,IPI≥2分患者5 a生存率仅为22%,而IPI≤1分患者能达到44%。结合我们的结果发现,IPI评分在血管免疫母T细胞淋巴瘤中同样重要;对IPI≤1分患者CHOP方案疗效较好,并有较长生存期;对IPI≥2分患者预后差。
本研究中主要不良反应为血液学毒性,其中Ⅲ、Ⅳ度粒细胞减少38.9%,22.2%出现粒缺伴发热;非血液学毒性发生率低,且较轻微;经过治疗所有不良反应均能恢复正常或减轻,不影响下周期化疗,未发生治疗相关死亡。
血管免疫母T细胞淋巴瘤预后差,目前已进行一些新的药物在该瘤治疗中的临床研究;Gallamini等[6]评价阿仑单抗联合CHOP方案作为一线治疗外周T细胞淋巴瘤的疗效(包含血管免疫母T细胞淋巴瘤),研究入组24患者,接受8周期CHOP方案化疗,其中4例患者第1~4周期加入阿仑单抗30 mg每天1次治疗,治疗结束评价疗效,24例患者中17例(71%)达CR,1例PR,6例SD或PD。中位随访时间16个月,14例患者生存,9例死于疾病进展,1例持续CR期间死于肺炎。PROPEL研究[7]是一项前瞻性研究,111例外周T细胞淋巴瘤患者(血管免疫母T细胞淋巴瘤13例)接受普拉曲沙治疗,治疗剂量为135 mg·m-2,隔周疗法,治疗有效率29%,中位缓解期为10.1个月,总生存期为14.5个月,治疗耐受性尚可。在血管免疫母T细胞淋巴瘤患者中B细胞活化很常见的,利妥昔单抗是CD20单克隆抗体,因此人们探索在血管免疫母T细胞淋巴瘤患者中加用利妥昔单抗能否取得效果。有研究[8]在25例初治的血管免疫母T细胞淋巴瘤患者中给予8周期利妥昔单抗联合CHOP方案治疗,结果提示44%的患者达CR,中位随访24个月,2 a无进展生存率42%,2 a总生存率62%。
CHOP方案治疗血管免疫母T细胞淋巴瘤有一定疗效,特别是对IPI≤1分的患者,疗效显著;但对IPI≥2分效果不理想,新的药物目前尚无对血管免疫母T细胞淋巴瘤患者有更多获益,更好一线治疗方案还需探索。
[1] 李小秋,李甘地,高子芬,等. 中国淋巴瘤亚型分布:国内多中心性病例10002例分析[J]. 诊断学理论与实践,2012,11(2):111-115.
[2] Abouyabis AN, Shenoy PJ, Sinha R,et al. A Systematic Review and Meta-Analysis of Front-line Anthracycline-Based Chemotherapy Regimens for Peripheral T-Cell Lymphoma[J].ISRN Hematol,2011,2011:623924.
[3] Mourad N, Mounier N, Brière J, Raffoux E,et al. Clinical, biologic, and pathologic features in 157 patients with angioimmunoblastic T-cell lymphoma treated within the Groupe d'Etude des Lymphomes de l'Adulte (GELA) trials[J].Blood,2008 ,111(9):4463-4470.
[4] Federico M, Rudiger T, Bellei M,et al.Clinicopathologic characteristics of angioimmunoblastic T-cell lymphoma: analysis of the international peripheral T-cell lymphoma project[J]. J Clin Oncol,2013,31(2):240-246.
[5] Schmitz N, Trümper L, Ziepert M,et al. Treatment and prognosis of mature T-cell and NK-cell lymphoma: an analysis of patients with T-cell lymphoma treated in studies of the German High-Grade Non-Hodgkin Lymphoma Study Group[J].Blood,2010,116(18):3418-3425.
[6] Gallamini A, Zaja F, Patti C,et al. Alemtuzumab (Campath-1H) and CHOP chemotherapy as first-line treatment of peripheral T-cell lymphoma: results of a GITIL (Gruppo Italiano Terapie Innovative nei Linfomi) prospective multicenter trial[J].Blood,2007,110(7):2316-2323.
[7] O'Connor OA, Pro B, Pinter-Brown L,et al. Pralatrexate in patients with relapsed or refractory peripheral T-cell lymphoma: results from the pivotal PROPEL study[J].J Clin Oncol, 2011,29(9):1182-1189.
[8] Delfau-Larue MH, de Leval L, Joly B,et al. Targeting intratumoral B cells with rituximab in addition to CHOP in angioimmunoblastic T-cell lymphoma. A clinicobiological study of the GELA[J].Haematologica,2012,97(10):1594-1602.
Clinical Research of Angioimmunoblastic T-cell Lymphoma Treated with CHOP Regimen
Chen Ningbin, Wu Hui, Chen Ying, Yan Yu, He Hongmin,Chen Daoguang, Lin Jianyang, Zheng Yanbing, Zhou Shipin, Wang Jiesong, Chen Xiurong
(FujianProvincialTumorHospital,Fuzhou350014,China)
Objective To evaluate the efficacy and toxicities of CHOP regimen on angioimmunoblastic T-cell lymphoma.Methods Eighteen patients with angioimmunoblastic T-cell lymphoma received the CHOP regimen chemotherapy.Results Of the 18 patients, CR was observed in the 10 patients (55.6%), PR in the 1 patient (5.6%), PD in the 7 patients (38.9%). Grade Ⅲ and Ⅳ myelosuppression occurred in most patients, and were recovered by active support care, and did not affect the next course of chemotherapy. At a median follow-up of 48 months, the 2- year progression-free survival rate was 38.9%, 71.4% in the patients with IPI≤1, 18.1% in the patients with IPI≥2.Conclusion CHOP regimen is effective for angioimmunoblastic T-cell lymphoma, especially for patients with IPI≤1, but the effect is not ideal for patients with IPI≥2.
CHOP regimen;angioimmunoblastic T-cell lymphoma;efficacy;toxicities
国家临床重点专科建设项目
陈宁斌(1977-),男,主治医师,主要从事淋巴瘤化疗工作。E-mail:chen_nb227@hotmail.com
吴晖(1964-),女,主任医师,主要从事淋巴瘤化疗工作。E-mail:kkwff123@163.com
10.3969/j.issn.1673-5412.2016.06.009
R733.1;R730.53
A
1673-5412(2016)06-0486-04
2016-04-20)
