牛膝多糖对软骨细胞Ⅱ型胶原及蛋白聚糖表达的影响
2017-01-14马玉环郑文伟陈后煌邵翔陈达叶蕻
马玉环+郑文伟+陈后煌+邵翔+陈达+叶蕻芝+李西海
【摘 要】目的:探讨牛膝多糖(ABPS)对大鼠膝关节软骨细胞Ⅱ型胶原及蛋白聚糖表达的影响。方法:取4周龄健康SD大鼠10只,分离膝关节,刮下双侧膝关节表面软骨组织,采用机械-Ⅱ型胶原酶消化法获取膝关节软骨细胞。建立软骨细胞体外培养体系,倒置相差显微镜观察细胞形态,采用
Ⅱ型胶原免疫组化法鉴定软骨细胞。体外培养到第2代软骨细胞,分别用0,50,100,200 μg·mL-1的ABPS对软骨细胞进行干预。干预后,Western blot检测各组Ⅱ型胶原、蛋白聚糖的表达变化,免疫荧光观察空白组与加药组Ⅱ型胶原的表达变化。结果:第2代软骨细胞的形态学表明软骨细胞的典型特征:软骨细胞含有丰富的Ⅱ型胶原。Western blot检测结果显示,ABPS促进软骨细胞Ⅱ型胶原表达,并且在
100 μg·mL-1时表达最高,差异有统计学意义(P < 0.05)。同时100 μg·mL-1的ABPS干预软骨细胞后,软骨细胞中的蛋白聚糖表达增加,但差异无统计学意义(P > 0.05)。与空白组的Ⅱ型胶原荧光表达相比,ABPS干预后软骨细胞的Ⅱ型胶原荧光表达更强。结论:ABPS促进了软骨细胞Ⅱ型胶原及蛋白聚糖的表达。
【关键词】 骨关节炎;牛膝多糖;Ⅱ型胶原;蛋白聚糖;软骨细胞;大鼠
Effect of ABPS on the Expressions of TypeⅡCollagen and Proteoglycan of Cartilage Cells
MA Yu-huan,ZHENG Wen-wei,CHEN Hou-huang,SHAO Xiang,CHEN Da,YE Hong-zhi,LI Xi-hai
【ABSTRACT】 Objective:To investigate the effect of Achyranthes bidentata polysaccharides(ABPS) on the expressions of typeⅡcollagen and proteoglycan in cartilage cells.Methods:Ten 4-week-old healthy SD rats were used to isolate the knee joints,scrape cartilaginous tissue off the surface of the knee joint,and get knee joint cartilage cells with the mechanical typeⅡcollagenase digestion method.An in vitro culture system was established and the cell morphology was observed with an inverted phase contrast microscope.TypeⅡ immunohistochemistry method was used to identify the chondrocytes.By the second generation of in-vitro-cultured chondrocytes,ABPS(0,50,100,200 μg·mL-1 respectively)was used to interfere in the cartilage cells.After intervention,Western blot was used to detect the expression changes of typeⅡcollagen and proteoglycan of each group,and immunofluorescence was used to observe the expression changes of typeⅡcollagen respectively in the blank control group and the dosing group.Results:The morphology of the second generation chondrocytes showed that cartilage cells contained rich typeⅡcollagen.Western blot showed that ABPS promoted chondrocyte typeⅡcollagen and the expression of typeⅡcollagen was the highest when there was 100 μg·mL-1 ABPS,the difference being statistically significant(P < 0.05).After intervention with 100 μg·mL-1 ABPS,the expression of proteoglycan in cartilage cells increased,but the difference was not statistically significant(P > 0.05).Compared with the blank control group,the expression of intervened collagen typeⅡcollagen was stronger.Conclusion:ABPS promotes the expression of typeⅡcollagen and proteoglycan.
【Keywords】 osteoarthritis;achyranthes
bidentata polysaccharide;typeⅡcollagen;pr-oteoglycan;cartilage cell;rats
牛膝多糖(ABPS)是从苋科类植物牛膝的干燥根中提取出来的有效成分。牛膝具有补肝肾、强筋骨、逐瘀通经、引血下行之功效[1-2],被广泛应用于治疗骨关节炎(osteoarthritis,OA)。OA是一种常见于中老年人的慢性、进展性关节疾病,其最典型的病理特征是软骨退变,以Ⅱ型胶原与蛋白聚糖破坏丢失、软骨胶原表型改变为主要病理变化[3-4]。关节软骨主要由软骨细胞和细胞外基质(ECM)组成[5-6],构成ECM的主要成分是Ⅱ型胶原和蛋白聚糖。课题组前期研究表明,ABPS促进了软骨细胞的增殖,因此,本文将探讨ABPS对软骨细胞Ⅱ型胶原及蛋白聚糖表达变化的
影响。
1 实验材料
1.1 实验动物 健康SD大鼠10只,雄性,4周龄,体质量200~300 g,由上海吴氏实验动物公司提供。实验动物合格证号:0001319。许可证号:SCXK(闽)2012-0001。大鼠分笼饲养,自由饮水,颗粒饲料喂养。
1.2 药 物 按照参考文献[7]研究方法提取。提取的ABPS溶解在培养液中。
1.3 主要试剂 RIPA裂解液(强)、BCA蛋白浓度测定试剂盒(碧云天生物技术研究所);PVDF膜(美国Millipore公司);TBST、转膜液、电泳液(北京普利莱基因技术有限公司);一抗Ⅱ型胶原、一抗蛋白聚糖(Abcam);二抗羊抗兔(北京中杉金桥生物技术有限公司);DAB检测试剂盒(北京博士德公司);DyLight 488 AffiniPure Goat Anti-Rabbit IgG(H+L)(艾美捷科技有限公司)。
1.4 实验仪器 超纯水装置(美国MILIPORE公司);LX-800酶标仪(美国Bio-tek公司);化学发光成像系统(美国Bio-RAD公司);64R型低温高速离心机(美国BECKMAN公司);激光共聚焦显微镜(德国ZEISS公司)。
2 方 法
2.1 关节软骨细胞的分离和培养 将10只SD大鼠脱颈法处死,无菌条件下刮下双侧膝关节表面软骨组织,1×PBS缓冲液漂洗3次,用眼科剪剪碎至1 mm3大小;移至培养皿中,加入质量分数为
0.2%的Ⅱ型胶原酶5 mL,置于37 ℃培养箱中消化2 h;接着用200目尼龙网筛过滤;然后放入1000 r·min-1离心机离心5 min,弃上清液,将沉淀的细胞团块用培养液制成细胞悬液;再将未消化完全的组织如此操作2次。将3次所得的细胞悬液质量分数为1×105·mL-1,接种于培养瓶中,放入体积分数为5%的CO2培养箱中培养。每2~
3天更换1次培养基,倒置相差显微镜观察细胞生长情况,待80%的细胞融合后进行传代培养。细胞生长单层铺满培养瓶后,用质量分数为0.25%的胰蛋白酶消化2~3 min,待镜下细胞圆缩时,用尖吸管吹打细胞使其悬于液体中,加质量分数为10%的FBS培养液终止消化,分瓶,加质量分数为10%的FBS培养。第2代(P2)软骨细胞分为空白组和ABPS组,空白组不加ABPS干预,ABPS组分别加入50,100,200 μg·mL-1的ABPS干预48 h[8]。
2.2 软骨细胞鉴定 P2软骨细胞接种于细胞爬片上,培养48 h,PBS冲洗,丙酮固定10 min,浸入质量分数为0.75%的H2O2-PBS 37 ℃处理30 min,PBS振洗2次,每次3 min;加入封闭血清,37 ℃
封闭30 min,弃去血清,加入Ⅱ型胶原一抗,37 ℃孵育2 h,PBS振洗3次,每次3 min,生物素化山羊抗兔IgG 37 ℃作用20 min,PBS冲洗
2 min,3次;链霉亲和素-过氧化物酶复合物置于室温30 min,PBS冲洗5 min,4次;DAB显色,水洗
5 min,浸入苏木素染液2 min,水洗,脱水,透明,
封片。阴性对照组不加入Ⅱ型胶原一抗孵育。
2.3 Western blot 参照试剂说明书,分组提取总蛋白,采用BCA法测定蛋白浓度。①质量分数为12%的SDS-PAGE胶每孔加20 μg变性后蛋白,60 V恒压至电泳超过浓缩胶后,90 V恒压至电泳结束。②PVDF膜无水甲醇活化10 min,PVDF膜、胶、滤纸,转膜液平衡10 min。③由下到上:滤纸-胶-PVDF膜-滤纸顺序,制作“三明治”夹,100 V恒压条件转膜。④转膜完成的PVDF膜,TBST荡洗后质量分数为5%的脱脂奶粉室温封闭2 h,相应一抗孵育,4 ℃摇床摇动过夜。⑤TBST洗3次,每次10 min,加入相应二抗,室温摇床孵育1 h,TBST洗3次,每次10 min。⑥PVDF膜蛋白面朝上放置,加入适量ECL显色液,反应2 min,
分析得出结果。
2.4 免疫荧光染色 将软骨细胞分为空白组及ABPS组,ABPS组中加入含ABPS 100 μg·mL-1的完全培养基。干预48 h后,去除培养基,PBS洗3次;多聚甲醛室温固定10 min,PBS洗3次;质量分数为1%的Triton X-100室温通透10 min,PBS洗3次;质量分数为5%的羊血清室温封闭1 h,Ⅱ型胶原抗体4 ℃孵育过夜;PBS洗3次,羊抗兔荧光二抗37 ℃孵育1 h,DAPI染色5 min,PBS洗5~6次。
2.5 统计学方法 采用SPSS 20.0软件进行统计分析。计量资料以表示,采用单因素方差分析(One-Way ANOVA)或Student's t-test。以P < 0.05为差异有统计学意义。
3 结 果
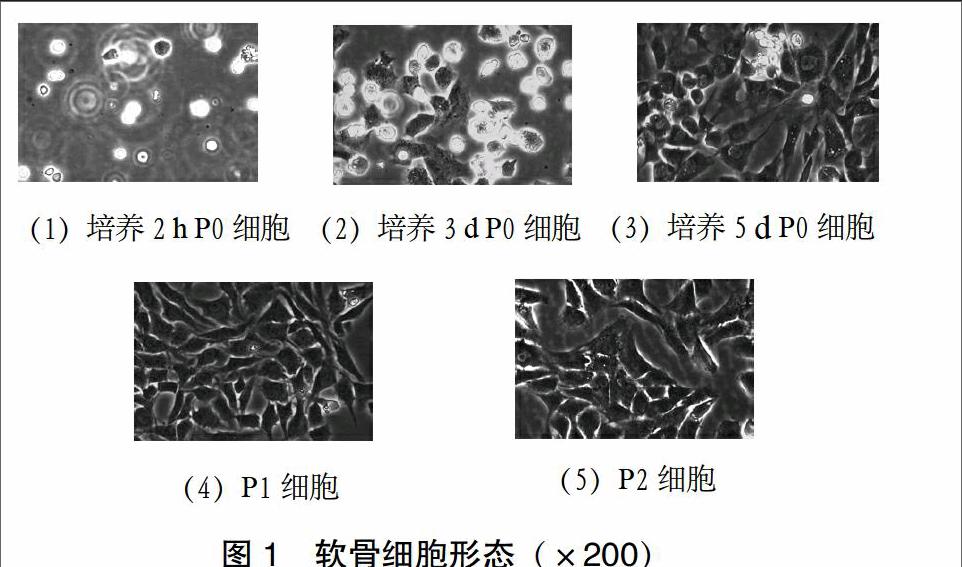
3.1 体外培养的软骨细胞形态 从大鼠膝关节经多次酶消化分离所得成骨细胞在倒置相差显微镜下观察,原代(P0)的软骨细胞具有小而圆的特征,经过2 d的培养,细胞的体积变大,少量的细胞开始拉长;3 d后,细胞具有梭型或者椭圆形的特征;到第5天细胞簇开始生长。第1代(P1)及P2细胞生长更为迅速。见图1。
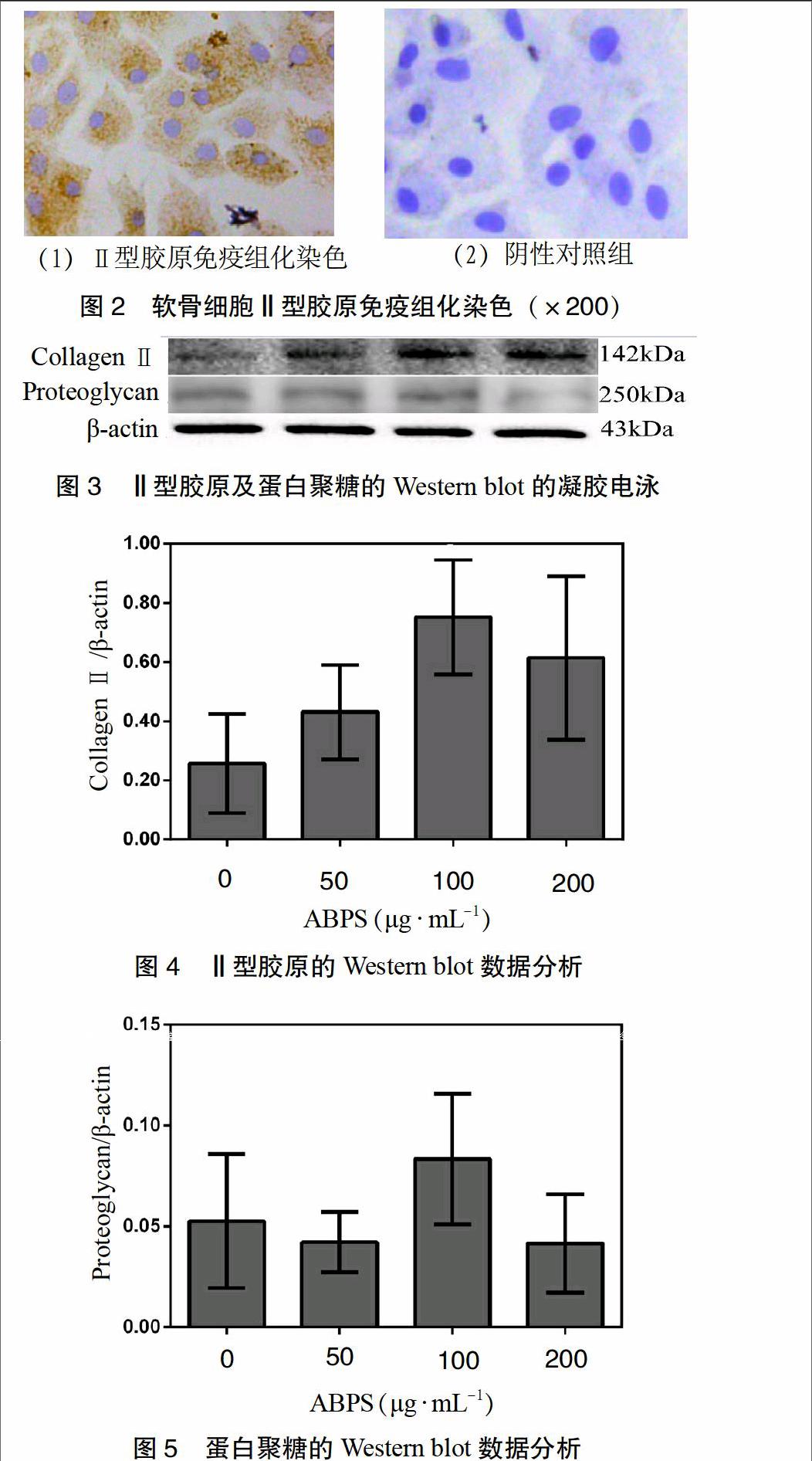
3.2 体外培养的软骨细胞的鉴定 P2软骨细胞的形态学表明软骨细胞的典型特征:软骨细胞含有丰富的Ⅱ型胶原。与阴性对照组比较,干预后的软骨细胞中细胞质染色棕色,这表明软骨细胞具有丰富的Ⅱ型胶原蛋白表达。见
图2。
3.3 Western blot检测结果 与空白组比较,ABPS组中的Ⅱ型胶原表达量增加,其中以
100 μg·mL-1ABPS对软骨细胞干预时Ⅱ型胶原的表达最高,差异有统计学意义(P < 0.05)(图3、
意义(P > 0.05)。
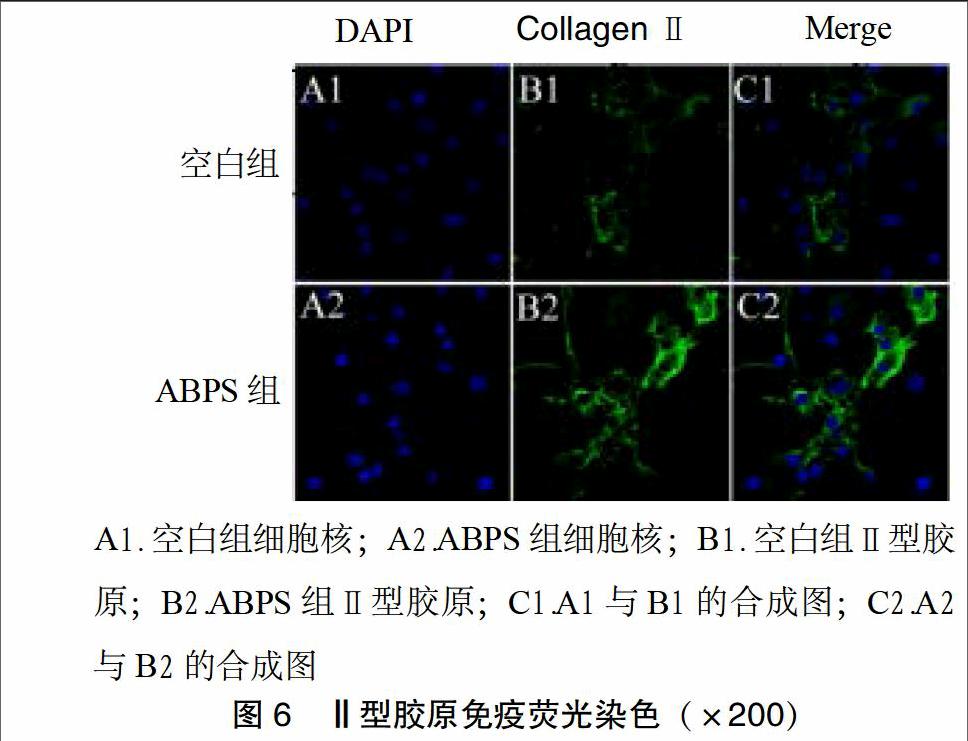
3.4 免疫荧光结果 2组软骨细胞核DAPI染色明显,呈蓝色(图6A1-A2),软骨细胞Ⅱ型胶原染色明显,呈绿色(图6B1-B2),细胞核与Ⅱ型胶原的合成图,结构清晰(图6C1-C2)。与空白组比较,ABPS组的细胞核染色明显,Ⅱ型胶原的荧光表达更强。可以说明100 μg·mL-1 ABPS干预的软骨细胞的活性、Ⅱ型胶原的表达都得到了增强。
4 讨 论
氨基葡萄糖是治疗OA的常用药物,具有一定的疗效。研究发现,氨基葡萄糖可以促进蛋白多糖的合成,抑制蛋白多糖及胶原的降解,延缓OA的进程[9]。然而近年来发现,长时间使用氨基葡萄糖会造成长链脂肪酸及过氧化物的积聚,对OA的治疗产生相反的作用[10]。而ABPS是一种具有广泛生物活性的高分子多糖,因在治疗疾病中具有重要作用而引起广泛的关注。课题组前期的结果表明,ABPS可以促进软骨细胞的增殖[8,11]。因此,ABPS可能是一种潜在新型的治疗OA的药物。
关节软骨的胶原蛋白主要以Ⅱ型胶原为主,占软骨胶原总量的90%~95%。Ⅱ型胶原经过多次聚集,在软骨内形成三维网状结构,同时与蛋白多糖链接、缠绕,形成了使软骨具有伸缩力的纤维网,起到固定蛋白多糖以及维持组织结构和张力恒定的作用。Ⅱ型胶原蛋白形成的网状结构遭到破坏被认为是OA的重要环节,软骨的这种结构框架遭到破坏从而引发软骨生物力学、生物化学等一系列变
化[12-14]。因此促进Ⅱ型胶原表达,在一定程度上可以缓解OA进程。本实验Western blot的结果表明,ABPS促进了软骨细胞Ⅱ型胶原的表达,并且
100 μg·mL-1时表达最高。免疫荧光结果表明,ABPS可以明显增加软骨细胞中Ⅱ型胶原的
表达。
蛋白聚糖是关节软骨ECM的主要大分子成分,在维持软骨正常功能及ECM的结构上具有重要作用[15]。在OA中,蛋白聚糖的过度降解和丢失是软骨代谢失衡中最早发生的代谢变化。随着OA病理改变出现,蛋白聚糖的降解持续存在,则会进一步引起关节软骨胶原的过度降解及细胞表型的改变。而软骨细胞的表型改变,又能导致蛋白聚糖代谢的异常增加,随着细胞功能的丧失,蛋白聚糖的分解加快,并且多于合成,最终导致蛋白聚糖的大量丢失。因此,促进蛋白聚糖的表达对治疗OA具有重要作用[16]。本实验研究结果发现,ABPS在100 μg·mL-1时可以促进蛋白聚糖的合成,表明ABPS可通过促进蛋白聚糖的表达抑制软骨退变。
本实验通过对大鼠软骨细胞进行ABPS干预发现,ABPS具有促进大鼠软骨细胞Ⅱ型胶原与蛋白聚糖表达的作用,提示ABPS可以通过促进软骨细胞ECM分泌来抑制软骨退变。
5 参考文献
[1] 黄丽婵,杨世奎,刘发元,等.川牛膝、怀牛膝治疗骨关节炎的药效物质基础探讨[J].风湿病与关节炎,2014,3(11):52-54.
[2] 林平冬,翁霞萍,刘发元,等.牛膝有效成分防治骨关节炎的作用机制探讨[J].风湿病与关节炎,2015,4(2):56-59.
[3] Lahm A,Mrosek E,Spank H,et al.Changes in content and synthesis of collagen types and proteoglycans in osteoarthritis of the knee joint and comparison of quantitative analysis with Photoshop-based image analysis[J].
Arch Orthop Trauma Surg,2010,130(4):557-564.
[4] 中华中医药学会.骨性关节炎[J].风湿病与关节炎,2013,2(2):71-72.
[5] Temenoff JS,Mikos AG.Review:tissue engineering for regeneration of articular cartilage[J].Biomaterials,2000,21(5):431-440.
[6] Sophia Fox AJ,Bedi A,Rodeo SA.The basic science of articular cartilage:structure,composition,and function[J].
Sports Health,2009,1(6):461-468.
[7] Yu F,Li X,Cai L,et al.Achyranthesbidentata polysac
charides induce chondrocyte proliferation via the promotion of the G1/S cell cycle transition[J].Mol Med Rep,2013,7(3):935-940.
[8] Tiku ML,Narla H,Jain M,et al.Glucosamine prevents in
vitro collagen degradation in chondrocytes by inhibiting advanced lipoxidation reactions and protein oxidation[J].
Arthritis Res Ther,2007,9(4):R76.
[9] Kang YH,Park S,Ahn C,et al.Beneficial reward-to-risk action of glucosamine during pathogenesis of osteoarthritis[J].Eur J Med Res,2015,20:89.
[10] Weng X,Lin P,Liu F,et al.Achyranthesbidentata polysaccharides activate the Wnt/beta-catenin signaling pathway to promote chondrocyte proliferation[J].Int J Mol Med,2014,34(4):1045-1050.
[11] 张猛,周嘉俊,罗宗平.软骨损伤后Ⅰ、Ⅱ型胶原蛋白的表达[J].中国组织工程研究,2014,18(51):8305-8309.
[12] Lee JW,Qi WN,Scully SP.The involvement of beta1 integrin in the modulation by collagen of chondrocyte-response to transforming growth factor-beta1[J].J Orthop Res,2002,20(1):66-75.
[13] 姚如愚,张晓.基质金属蛋白酶与骨关节炎[J].国外医学(内科学分册),2001,28(4):159-162.
[14] 管剑龙,施桂英.基质金属蛋白酶与骨关节炎[J].中华风湿病学杂志,2000,4(1):54-56.
[15] Chandran PL,Horkay F.Aggrecan,an unusual polyelectrolyte:review of solution behavior and physiological implications[J].ActaBiomater,2012,8(1):3-12.
[16] Reginster JY,Bruyere O,Fraikin G,et al.Current concepts in the therapeutic management of osteoarthritis with glucosamine[J].Bull Hosp Jt Dis,2005,63(1-2):31-36.
收稿日期:2016-07-13;修回日期:2016-08-29
