反相-高效液相色谱法测定人血清中万古霉素浓度
2017-01-10盛长城谢娟熊世娟王清忱张玲敏李龙宽沈祥春
盛长城 谢娟 熊世娟 王清忱 张玲敏 李龙宽 沈祥春
(1.贵州医科大学天然药物资源优效利用重点实验室,贵州 贵阳 550004;2.贵州省人民医院药剂科,贵州 贵阳 550002; 3.贵州医科大学药理教研室,贵州 贵阳 550004)
反相-高效液相色谱法测定人血清中万古霉素浓度
盛长城1,2谢娟2熊世娟2王清忱2张玲敏3李龙宽3沈祥春1△
(1.贵州医科大学天然药物资源优效利用重点实验室,贵州 贵阳 550004;2.贵州省人民医院药剂科,贵州 贵阳 550002; 3.贵州医科大学药理教研室,贵州 贵阳 550004)
万古霉素; 治疗药物监测; 反相-高效液相色谱法
万古霉素是三环糖肽类抗生素,对革兰氏阳性菌有强大杀菌作用,是治疗耐药革兰阳性菌特别是耐甲氧西林金黄色葡萄球菌(MRSA)所致重症感染的首选药物。万古霉素治疗窗窄,谷浓度<10 mg/L时易增加诱导耐药风险,导致治疗失败[1-2],而谷浓度>20 mg/L时肾损害发生率显著增加[3]。国内外文献[4-5]均推荐维持万古霉素稳态血清谷浓度>10 mg/L,针对MRSA所引起的血流感染、心内膜炎及脑膜炎等,应维持稳态血清谷浓度在15~20 mg/L。因此,结合患者病理生理情况进行血药浓度监测,指导剂量调整,实施个体化治疗就尤为重要。目前临床上用于万古霉素血药浓度监测的方法主要有荧光偏振免疫(FPIA)法、微生物法和高效液相色谱(HPLC)法。FPIA法所需仪器成本和试剂盒价格较昂贵,需集中标本后进行检测,不能完全满足临床即时检测的需求,且其检测结果偏高[6],在慢性肾功能不全和血透患者中偏高尤为明显[7],而微生物法则易受合并使用抗生素的影响,其临床应用受到一定限制。笔者查阅文献[8-12],结合实验室自身条件,建立了一种简单、快捷的反相-高效液相色谱(RP-HPLC)法,现报告如下。
1 仪器与试剂
1260高效液相色谱仪(美国Aglient公司);TG16-W高速离心机(湖南湘仪实验室仪器开发有限公司);AL204电子分析天平(梅特勒-托利多仪器有限公司);XH-B旋涡混合器(江苏康健医疗用品有限公司);PHS-3C pH计(上海理达仪器厂);DW-86L338超低温冰箱(Haier)。万古霉素对照品(中国食品药品检定研究院,批号130360-201302);替硝唑对照品(中国食品药品检定研究院,批号100336-200703);甲醇、乙腈为色谱纯,Mreda Technology Inc生产;磷酸二氢钾、高氯酸、磷酸均为分析纯;水为双蒸水。
2 方法与结果
2.1 色谱条件
色谱柱:ZORBAX SB-C18(4.6 mm×150 mm,5 μm);流动相:甲醇-乙腈-磷酸二氢钾缓冲液=10∶3∶87;流速:1 mL/min;柱温:30 ℃;检测波长:210 nm;进样量:20 μL。在该色谱条件下,万古霉素与内标替硝唑分离完全,血中内源性物质对测定结果无干扰,见图1。

(a) 空白血清

(b) 空白血清+万古霉素对照品+内标

(c) 血清样品+内标图1 万古霉素色谱图(1:内标,2:万古霉素)
2.2 溶液配制
2.2.1 流动相 称取磷酸二氢钾3.402 5 g,加入双蒸水至1 000 mL使溶解,用磷酸调节pH值至3.1,用0.22 μm微孔滤膜过滤,即得0.025 mol/L磷酸二氢钾缓冲液。
2.2.2 沉淀剂 将乙腈和6% 高氯酸以1∶6的比例混合即得。
2.2.3 内标溶液 精密称取75.0 mg替硝唑于50 mL容量瓶中,用双蒸水溶解并稀释至刻度,即得1.5 mg/mL的内标溶液,密封,4 ℃避光保存。
2.2.4 标准工作液 精密称取64.0 mg万古霉素对照品于50 mL容量瓶中,用0.025 mol/L磷酸二氢钾缓冲液溶解并稀释至刻度,摇匀,即得1 280 mg/L的标准储备液。精密量取该贮备液适量,逐级稀释成浓度为640、320、160、80、40、20、10 mg/L的系列标准工作液,密封,4 ℃避光保存。
2.3 血清样品预处理
取血清样品300 μL于1.5 mL EP管中,加入1.5 mg/mL替硝唑30 μL,涡旋混匀1 min,再加入沉淀剂300 μL,涡旋混匀3 min,16 000r/min离心10 min,取上清液用0.22 μm微孔滤膜过滤,自动进样20 μL。
2.4 标准曲线制备
取空白血清270 μL于1.5 mL EP管中,加入不同浓度的标准工作液30 μL,配制成浓度为64、32、16、8、4、2、1 mg/L标准血样。按“2.3”项处理后进样测定,以样品与内标峰面积比(Y)对浓度(X)进行线性回归,得回归方程:Y=0.092 6X+0.004 6(r=0.999 8,n=7),表明万古霉素血清浓度在1.0~64.0 mg/L内线性良好。以S/N≥3计算,万古霉素的最低检测浓度为0.4 mg/L。
2.5 回收率试验
配制含万古霉素64、8、1 mg/L的血清样品各6份,按“2.3”项处理后进样测定,记录万古霉素峰面积(AX),计算实测浓度与理论浓度的比值即得相对回收率;另在同样条件下进行相应浓度的万古霉素标准溶液,记录峰面积(AS),计算相应的峰面积比(AX/AS)即得提取回收率。结果见表1。


理论浓度/(mg/L)实测浓度/(mg/L)相对回收率/%RSD/%提取回收率/%RSD/%6468.157±1.213106.496±1.8961.78090.216±2.4762.74488.053±0.370100.663±4.6294.59893.223±4.4204.74211.045±0.094104.520±9.4189.01194.578±6.1966.551
2.6 精密度试验
配制含万古霉素64、8、1 mg/L的血清样品,按“2.3”项处理后进样测定,每日平行操作6次,连续3 d,计算日内与日间精密度。结果见表2。


理论浓度/(mg/L)实测浓度/(mg/L)日内RSD/%日间RSD/%6467.178±2.4783.2885.87888.130±0.3143.6964.90311.023±0.0656.5734.646
2.7 稳定性试验
2.7.1 标准工作液稳定性 以磷酸二氢钾缓冲液代替空白血清和沉淀剂,配制含万古霉素64、8、1 mg/L的样品各5份,按“2.3”项处理,4 ℃避光保存。分别于0时、7 d、15 d进样测定,记录万古霉素与内标峰面积比(AVan/AIS)。结果见表3。


时间64mg/LAVan/AISRSD/%8mg/LAVan/AISRSD/%1mg/LAVan/AIS RSD/%0时8.662±0.5836.7260.933±0.0091.0120.114±0.0054.7947d8.280±0.6357.6710.898±0.0202.2280.109±0.0032.67515d8.880±0.4424.9750.906±0.0414.5210.110±0.0087.009
2.7.2 含药血清样品稳定性 配制含万古霉素64、8、1 mg/L的血清样品,分别于0时、室温24 h、4 ℃冷藏7 d、4 ℃冷藏15 d、-20 ℃冷冻1个月、-20 ℃冻融3次、-80 ℃冻融3次,按“2.3”项处理后进样测定。结果见表4。
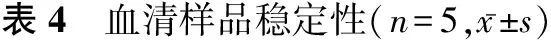

时间64mg/L实测浓度/(mg/L)RSD/%8mg/L实测浓度/(mg/L)RSD/%1mg/L实测浓度/(mg/L) RSD/%0时67.377±1.1271.6728.368±0.1842.2001.093±0.0575.193室温24h66.518±1.0221.5378.171±0.2533.0911.045±0.0706.6704℃冷藏7d66.335±0.3640.5488.199±0.5857.1291.089±0.0615.6014℃冷藏15d65.292±0.5140.7878.373±0.1421.6911.085±0.1029.439-20℃冷冻1个月66.504±1.1601.7458.233±0.2102.5511.054±0.0423.978-20℃冻融3次65.623±0.9751.4858.173±0.2893.5331.072±0.0847.795-80℃冻融3次67.108±0.6560.9788.149±0.5206.3861.100±0.1089.793
3 讨 论
经多种流动相实验,本法最终选择了甲醇-乙腈-磷酸二氢钾,乙腈有助于改善二者的分离,而甲醇可改善峰形。且三者比例对万古霉素保留时间影响很大,将其比例调整为10∶3∶87时,内源性杂质、内标与万古霉素分离完全,峰形较好。如增加水相比例,万古霉素出峰时间明显延长,峰形变差;如增加有机相比例,虽然万古霉素出峰时间大幅提前,但内源性杂质的干扰也加大。
在内标选择上,文献报道较多的是去甲万古霉素,但万古霉素与去甲万古霉素均由发酵法制备,在万古霉素中含有少量去甲万古霉素,去甲万古霉素中亦含有少量万古霉素,因此在低浓度时测量误差较大。笔者亦曾尝试以红霉素、维生素B12、头孢呋辛、2-甲基-5-硝基咪唑为内标,分离效果均不甚理想。经反复实验,最终选择以替硝唑为内标,回收稳定,色谱峰峰形好,与万古霉素及内源性杂质分离完全。
在血清样品处理方法上,文献报道有蛋白沉淀后液-液提取法[12]、蛋白沉淀后直接进样法[7]和固相萃取法[11],以蛋白沉淀后直接进样法最为简单、快捷。笔者考察了5%硫酸锌、10%硫酸锌、20%硫酸锌、30%硫酸锌、甲醇、20%高氯酸、乙腈-6%高氯酸(1∶6)等常用沉淀剂,单从外观上看,均可达到理想的净化效果。与文献[13]报道不同的是,各种比例硫酸锌的提取回收率均在40%~60%,甲醇的提取回收率仅为30%,未达到相关分析要求;20%高氯酸的提取回收率在65%左右,但基线不平,考虑与万古霉素被高氯酸降解破坏所致;乙腈-6%高氯酸(1∶6)的提取回收率可达90%,基线平坦。
综上所述,本实验所建立的分析方法快速、简捷、灵敏度高,经考察准确度和精密度良好,可用于人血清中万古霉素浓度测定,满足临床开展治疗药物监测和进行群体药动学研究的需要。
[1] Howden BP, Ward PB, Charles PGP, et al. Treatment outcomes for serious infections caused by methicillin-resistant Staphylococcus aureus with reduced vancomycin susceptibility[J]. Clin Infect Dis, 2004,38(4):521-528.
[2] Sakoulas G, Gold HS, Cohen RA, et al. Effects of prolonged vancomycin administration on methicillin-resistant Staphylococcus aureus (MRSA) in a patient with recurrent bacteraemia[J]. J Antimicrob Chemother, 2006,57(4):699-704.
[3] Vanhal SJ, Paterson DL, Lodise TP. Systematic review and meta-analysis of vancomycin-induced nephrotoxicity associated with dosing schedules that maintain troughs between 15 and 20 milligrams per liter[J]. Antimicrob Agents Chemother, 2013,57(2):734-744.
[4] Rybak MJ, Lomaestro BM, Rotschafer JC, et al. Vancomycin therapeutic guidelines: a summary of consensus recommendations from the infectious diseases Society of America, the American Society of Health-System Pharmacists, and the Society of Infectious Diseases Pharmacists[J]. Clin Infect Dis, 2009,49(3):325-327.
[5] 万古霉素临床应用剂量专家组. 万古霉素临床应用剂量中国专家共识[J]. 中华传染病杂志, 2012,30(11):641-646.
[6] 邹国芳, 钱文璟, 李巍, 等. 高效液相色谱法和荧光偏振免疫法测定万古霉素血清浓度的比较[J]. 中国医院药学杂志, 2015,35(1):68-71.
[7] 崔艳丽, 武峰. HPLC法同时快速测定万古霉素和去甲万古霉素的血药浓度[J]. 中国医院用药评价与分析, 2011,11(10):920-922.
[8] 祝文兵, 阳利龙, 何周康. 高效液相色谱法测定血浆中万古霉素的浓度[J]. 药物分析杂志, 2006,26(8):1106-1108.
[9] 宋新文, 许琼, 汪洋, 等. HPLC法测定人血清中万古霉素的浓度[J]. 中国药房, 2010,21(18):1663-1665.
[10] 罗奕, 刘文, 邓楠, 等. 万古霉素血药浓度监测方法的建立及稳定性考察[J]. 中国实验方剂学杂志, 2011,17(20):133-135.
[11] 郭志磊, 范捷. 固相萃取和蛋白沉淀法在高效液相色谱法测定万古霉素血药浓度中的比较[J]. 中国医院药学杂志, 2013,33(9):745-747.
[12] 万丽丽, 余奇, 李颜, 等. 高效液相色谱法测定血浆中去甲万古霉素和万古霉素浓度[J]. 中国药师, 2008,11(8):998-1000.
[13] 黄晓会, 刘艳, 张健. HPLC法测定人血清中万古霉素及去甲万古霉素浓度及临床应用[J]. 中国药物应用与监测, 2014,11(2):92-94.
R965
B
1000-744X(2016)04-0372-03
2015-12-03)
△通信作者,E-mail:shenxiangchun@126.com
