黄钾铁矾固溶物的制备及拉曼光谱分析
2017-01-05张云霞王蒙郭兆清冯敏王斌曹学伟徐晓轩王玉芳
张云霞,王蒙,郭兆清,冯敏,王斌,曹学伟,徐晓轩,王玉芳
(南开大学物理科学学院,天津 300071)
黄钾铁矾固溶物的制备及拉曼光谱分析
张云霞,王蒙,郭兆清,冯敏,王斌,曹学伟,徐晓轩,王玉芳*
(南开大学物理科学学院,天津 300071)
利用水热法实验制备黄钾铁矾固溶系列样品AFe3(SO4)2(OH)6,其中A位置可以被K+、Na+和H3O+占据。此外,还制备近全钾占据的黄钾铁矾作为对比样品。对制备的黄钾铁矾群样品进行了拉曼光谱测试,黄钾铁矾的拉曼光谱分为羟基区(3000~4000 cm-1)、硫酸根内部模式、点阵振动模三个主要部分,并对有异议的振动模的归属重新做了分析。利用拉曼光谱峰的数目以及频移,离子半径的大小、键长、键角的变化等信息,采用胡克定律分析了黄钾铁矾固溶系列A位置的离子替换作用。A位置离子的替换作用主要影响黄钾铁矾结构中OH基周围的环境,使得与羟基相关的振动模发生变化。
黄钾铁矾群;拉曼光谱;水热法
1 引言

常见的黄钾铁矾群矿物,端元水合氢黄钾铁矾很罕见。在地球上,黄钾铁矾是在富含硫和氧化的环境中发现的,属于硫酸盐矿物,其形成常与酸性矿山排水和硫酸盐土壤有关[1-3]。黄钾铁群矿物质在金属处理工业中有重要作用,常用在锌、铜、铅产业中除去溶液里面的铁[1-4],可以通过冶炼来回收银、铟等[5]。这些表明黄钾铁矾群矿物在矿物资源探索、环境保护方面意义重大[1-2,6-7]。2004年在火星上发现黄钾铁矾,表明火星上曾经存在过液体,再次掀起研究黄钾铁矾的热潮。黄钾铁矾实验制备方法主要有水热法和生物氧化法[2-3,8-12]。其中水热法操作简单、耗时较短。近期有研究利用加入金刚石、针铁矿和赤铁矿等种子材料来研究黄钾铁矾成核和晶体生长[13]。不论是自然矿物还是合成样品,黄钾铁矾结晶差,目前只有极少量的单晶分析研究,并且A位置经常存在H3O+,研究发现在高浓度氯的环境下,能够减弱H3O+的替换作用[1]。由于A、B、X位置可以被多种离子占据,故存在多种系列固溶体[2]。拉曼光谱能够用来鉴别分子的种类,并且与XRD相比,拉曼光谱不受结晶差的影响,因而有许多文献利用拉曼散射光谱研究和辨别黄钾铁矾群矿物种类,并且能够在分子层面上分析因离子替换引起的结构变化[1,6,9-10,14]。黄钾铁矾拉曼光谱振动模的归属仍有模糊和异议,目前关于黄钾铁矾固溶物的拉曼光谱的研究极少,尤其是利用拉曼光谱研究固溶物中A位置K+、Na+、H3O+的离子的替换作用。
本文中采用水热法制备了A位置为K+、Na+、H3O+的黄钾铁矾固溶系列AFe3(SO4)2(OH)6以及A位置几乎全钾占据样品,对样品进行拉曼散射测试,并从拉曼光谱的变化讨论了晶体结构方面的不同。
2 实验
2.1 主要实验用品及仪器
实验用品:硫酸钾、硫酸钠、硫酸铁、无水三氯化铁、氯化钾、氯化钠,除无水三氯化铁为化学纯外,其他药品均为分析纯,使用前未经过任何处理。
实验仪器:聚四氟乙烯内衬水热反应釜、FA1204B电子天平、DZF6020真空干燥箱、RENISHAW100共焦显微拉曼光谱仪。
2.2 样品制备
采用类似Basciano的实验制备方法,水热法制备K-H3O黄钾铁矾、Na-H3O黄钾铁矾和Na-K黄钾铁矾三种固溶系列样品,以及A位置几乎全钾占据的黄钾铁矾样品[2-3]。K-H3O黄钾铁矾和Na-H3O黄钾铁矾的制备将一定量的Fe2(SO4)3分别与不同量的K2SO4或 Na2SO4在常温下混合,加入去离子水搅拌溶解,配成50 mL或40 mL溶液,160 ℃加热48小时,样品分别标记为S#A1、S#A2、S#B1和S#B2。A位置全钾占据样品的实验方法如下:配制12 mL高浓度的LiCl溶液,分别将0.5 g KCl与5 mL的1.23 M FeCl3溶液加入LiCl溶液中,称取4.9 g Fe2(SO4)3溶解于25 mL去离子水,将Fe2(SO4)3溶液缓慢加入上述含氯的溶液中,最终溶液160 ℃加热48小时,样品标记为S#D[2]。采用类似的方法制备Na-K黄钾铁矾,将上述的0.5 g KCl更换为0.5 g的NaCl和KCl混合物,样品标记为S#C1、S#C2、S#C3、S#C4、S#C5。参与反应的溶液中K+、Na+、Fe3+摩尔浓度与Basciano的实验相同。以上所有反应结束后,将上层清液移出,刮取沉淀,用去离子水冲洗沉淀多次,而后将沉淀自然晾干,得到样品。具体实验条件见表1。

Tab.1 Synthesis conditions of jarosite samples
带*表示在含氯的环境中合成样品
2.3 测试
在室温条件下利用RENISHAW100共焦显微拉曼光谱仪进行拉曼散射测试,本文工作选取785 nm波长,实际测试时功率选择50%,积分时间为10 s,累积扫描次数设为1,扫描光谱范围为100~4000 cm-1。
3 结果与讨论
3.1 拉曼光谱分析
黄钾铁矾群固溶系列样品的拉曼光谱如图1、2所示,所有样品的拉曼光谱峰频率可分为100~700 cm-1、900~1300 cm-1、3000~4000 cm-1三个区间。表2给出了不同样品主要振动模的频率。

Fig.1 Raman spectra of synthetic natrojarosite-potassium jarosite (Na-K jarosite) solid-solution series (a) 100~1300 cm-1region ; (b) 3000~4000 cm-1region

Fig.2 Raman spectra of synthetic potassium jarosite-hydronium jarosite (K-H3O jarosite) solid-solution series,natrojarosite-hydronium jarosite (Na-H3O jarsite) solid-solution series and jarosite of fully occupied with K solid-solution series.left:100~1300 cm-1region;right:3000~4000 cm-1region
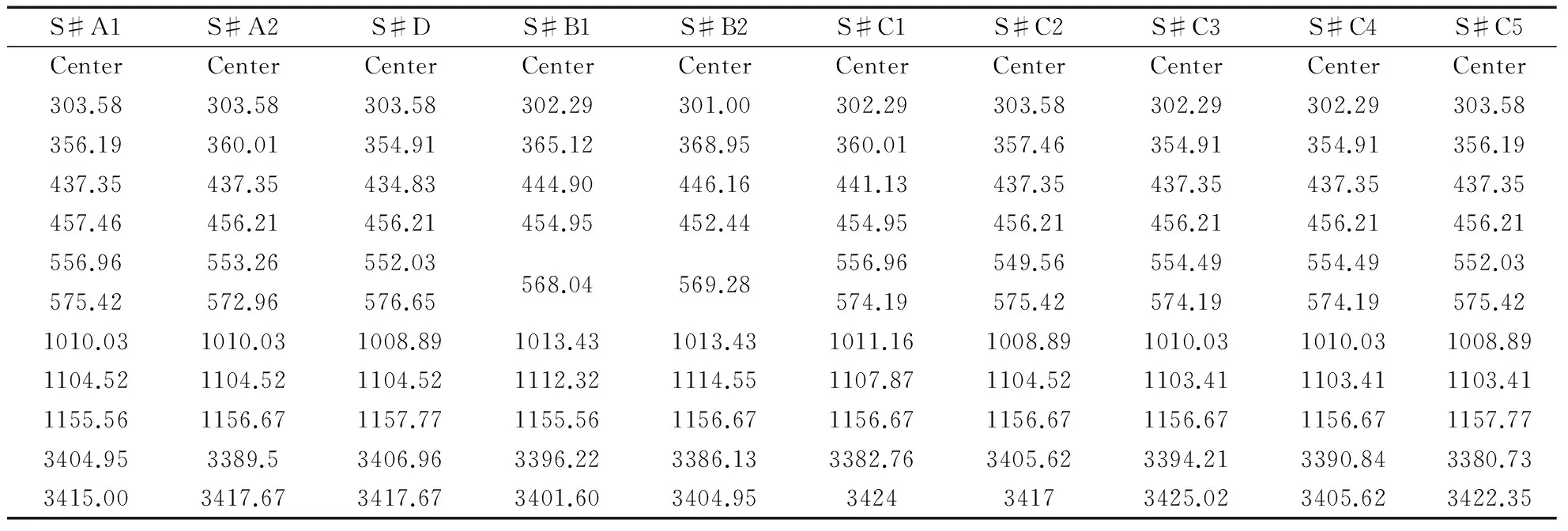
Tab.2 Some peaks of the Raman spectral analysis of jarosite samples(unit:cm-1)
在100~700 cm-1区间出现点阵振动模、羟基弯曲模、A-O键和v2(SO4)多种振动模,导致拉曼峰的归属振动模存在疑问和异议。225 cm-1附近拉曼峰归属模糊,文献[10]将其归属Fe-O伸缩振动模,而文献[6]认为此峰还可能是结构弯曲振动模引起的。文献[10]将301 cm-1、354 cm-1附近拉曼峰归属Fe-O伸缩振动模。然而文献[6]中明矾石拉曼光谱345 cm-1、395 cm-1处的两个峰,A位置离子的变化导致后一个峰频移,因此它们分别归属Al-O伸缩振动模和Al-OH伸缩振动模。434 cm-1附近有峰,文献[10]将其归属Fe-OH伸缩振动模,但是文献[6,9,14]认为应将其归属v2(SO4)弯曲振动模,并将626 cm-1及其肩峰646 cm-1归属v4(SO4)弯曲振动模。454 cm-1处有一个较弱的肩峰,文献[10]认为其归属于Fe-O伸缩振动模,而文献[9,15]将其归属于v2(SO4)弯曲振动模。文献[6]根据Breitiger等人利用重氢研究的结果,将454 cm-1、573 cm-1及556 cm-1都归属Fe-O伸缩振动模和OH弯曲振动模的叠加。1000~1300 cm-1区间的出现3个较强的拉曼峰。Frost 和Sasaki 将1102 cm-1归属v3(SO4),Maubec将其归属v3(SO4)与δOH振动模的叠加[6,9-10,14]。群论预测在3000~4000 cm-1区间内存在两个OH伸缩振动模,Frost利用公式ν1=(3592-304)×109-d(O-O)/0.1321cm-1得出明矾石中存在两个强度略有不同的氢键,Maubec认为两个O1-H有不同的键长导致了OH 伸缩振动模不同[6,17]。研究发现天然的和实验合成样品的拉曼光谱在该区间都出现了两个主峰,都归属于v(OH)。
在我们合成样品的拉曼光谱中也出现上述拉曼峰,且峰位基本一致,详见表3。下面利用胡克定律和群论方法对上述拉曼峰的归属振动模进行分析。
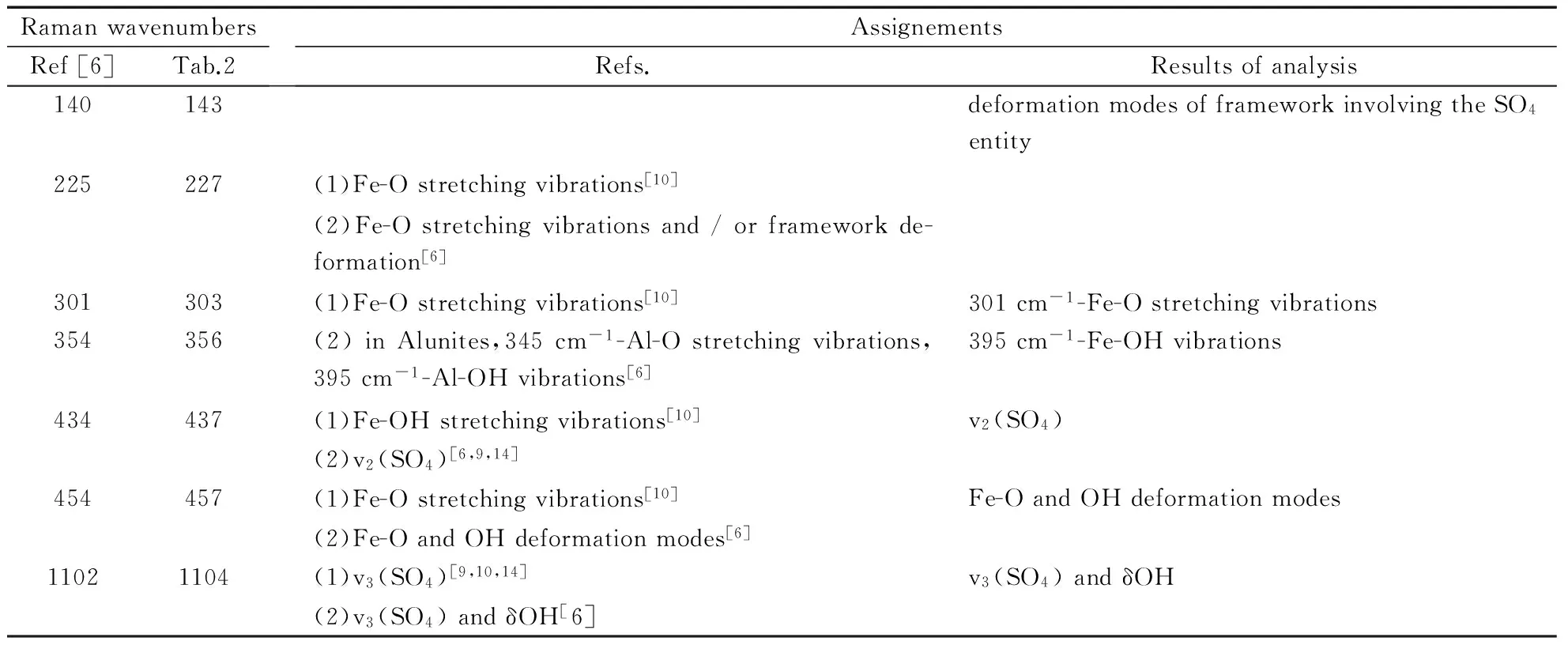
Tab.3 Assignements of Raman wavenumbers of jarosites(unit:cm-1)
溶液中自由硫酸根离子的对称性为Td,振动模的对称性分类为A1+E+2T2,其中A1模是对称伸缩振动模v1,二重简并E模是弯曲振动模v2,T2是三重简并的反对称伸缩振动模v3和弯曲振动模v4,这些模对应的峰位一般为415 cm-1(v2)、613 cm-1(v4)、981 cm-1(v1)和1104 cm-1(v3)[1]。在黄钾铁矾晶体中,硫酸根离子对称性降低,导致了振动模的劈裂,利用因子群分析,可知存在6个硫酸基本振动模:3个伸缩振动模(1个v1(SO4)和2个v3(SO4))和3个弯曲振动模(1个v2(SO4)和2个v4(SO4))[6,16]。出现在437 cm-1、628 cm-1、1010 cm-1、1104 cm-1、1156 cm-1附近的拉曼峰分别归属于v2(SO4)、v4(SO4)、v1(SO4)、v3(SO4)、v3(SO4),此外将628 cm-1的肩峰645 cm-1归属v4(SO4),这与因子群分析的结果一致。文献[6]中发现明矾石拉曼光谱中归属v3(SO4)的1077 cm-1与归属δOH的1151 cm-1发生费米共振,Bishop研究黄钾铁矾合成样品的透射谱中将997 cm-1、1010 cm-1分别归属于v1(SO4)和δOH,1094 cm-1和1187 cm-1都归属于v3(SO4)。归属δOH的拉曼峰应该出现此区间内,因此将1104 cm-1归属v3(SO4)与δOH振动模的叠加更加合理。若457 cm-1处的肩峰将也归属于v2(SO4)弯曲振动模,这意味着硫酸根基团对称性降低为C2v甚至Cs,根据因子群分析,在100~700 cm-1处将多于10种振动模式,且导致黄钾铁矾比明矾石中的拉曼峰个数多一倍,而在本文和前人研究中并未出现这种情况[6,9-10,14]。群论预测BO2(OH)4八面体有5个拉曼峰,前面提到的303 cm-1、356 cm-1处的2个峰,许多文献中将573 cm-1及其肩峰551 cm-1归属Fe-O伸缩振动模[6,9,14]。则457 cm-1很有可能也归属Fe-O伸缩振动模,根据Breitiger等人利用重氢研究的结果,文献[6]的结论更为合理。
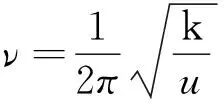
本文实验制备的黄钾铁矾群样品,与前人研究的结果基本一致,说明本文制备黄钾铁矾固溶系列样品是成功的[6,9-10,14]。
3.2 A位置离子替换作用的分析
3.2.1 A位置离子的替换在拉曼谱上的表现及对黄钾铁矾结构的影响
图1中从S#C1到S#C5样品的拉曼谱发现:Fe-OH伸缩振动模频率微有下降;vOH振动模频率增加;Fe-O和OH弯曲叠加振动模的频率基本不变;v2(SO4)、v4(SO4)弯曲振动模的频率不变,v1(SO4)伸缩振动模的频率略微变小、1108 cm-1附近拉曼峰的频率变小。这与Maubec研究明矾石拉曼光谱K+替换Na+对OH相关振动模的影响一致,Maubec认为由于K离子半径(1.33 Å)大于Na离子半径(0.95 Å)引起分子结构变化,导致振动模频率变化。Basciano等人[3]在他们的研究中曾经合成不同投料比的系列样品,并进行了的ICP-OES测试研究,发现在Na-K黄钾铁矾固溶系列中,随着投料中K+含量的增加,产物样品中K+的占比增加;根据结构分析的结果获得键长、键角等数据,发现A-O3H键变长,Fe-O2键稍微变短,O3-H键的键长呈现略减再增又再减的变化。根据胡克定律,这些键长的变化会导致OH相关振动摸频率发生变化。由图1中不同投料比拉曼散射峰的变化规律,与文献[3]给出的规律一致,预示着从S#C1到S#C5样品中,A位置K+含量有逐渐增加的趋势。Frost等人认为随着A 离子半径的增大,硫酸伸缩振动模的频率减少,而硫酸弯曲振动模的频率只有轻微的变化,但Maubec认为硫酸振动模基本不受A位置离子替换的影响,峰位的变化源于δOH[1,6]。本文的发现与Maubec的分析基本一致。由此得出结论,当A位置出现K+替换Na+时,随着K+含量的变化,A-O3H键、Fe-O键和O3-H键长变化,导致OH周围环境变化,引起Fe-OH伸缩振动模频率变小而vOH振动模频率变大,但对于硫酸基周围的环境影响不大,在拉曼谱上表现为与OH振动模相关的拉曼峰频移,而与硫酸基相关的拉曼峰位置基本不变。
观察图2,S#D与S#A1、S#A2对比发现,Fe-OH伸缩振动模的频率微增,Fe-O和OH弯曲叠加振动模的频率微减,vOH振动模频率变大,v3(SO4)和δOH叠加振动模略增;S#B1与S#B2对比发现,Fe-OH伸缩振动模的频率微增,Fe-O和OH弯曲叠加振动模的频率变化很小,vOH振动模频率变小,v3(SO4)和δOH频率变大。这说明,当A位置发生H3O+替换时,与OH相关的振动模的受较大影响,硫酸振动模基本不受影响。Na-H3O黄钾铁矾固溶系列在568cm-1附近只有一个峰,Basciano在其短波红外光谱有类似发现,随着H3O+浓度的增加,有些肩峰强度减弱或消失[2]。从离子半径上分析,H3O+的离子半径是1.355 Å,比K+、Na+的半径大。本文发现在K,Na-H3O黄钾铁矾固溶样品中,v3(SO4)和δOH叠加振动模向高频率处移动,与Frost等人的发现不同,Maubec提出引起这些峰位变化的是源于δOH的观点可能是对的[1,6]。分析K+替换Na+时,发现当A位置离子半径大的K+含量比增加时,Fe-OH伸缩振动模频率变小,vOH伸缩振动模频率微增。但是H3O+的替换导致的振动模频率的变化不完全符合此规律。可能与H3O+位置的不确定性有关。在键长和键角方面,分析Basciano研究黄钾铁矾固溶物所得的数据,利用胡克定律推出:当H3O+替换K+时,随着A位置H3O+含量比变大,O3-H键变短,则v(OH)振动模频率变大,A-O2键变长,A-O3不变,Fe-O2键变短,Fe-O3变长,则Fe-OH振动模频率可能变大;当H3O+替换Na+时,随着A位置H3O+含量比变大,O3-H键略变长,vOH振动模频率变小,A-O键都变长、Fe-O键都变短,则Fe-OH振动模频率可能变大。Basciano发现在这三种固溶系列中,S-O键长、角度基本不变,则硫酸振动模基本不受A位置离子种类的影响。人工合成的所有黄钾铁矾固溶系列样品的拉曼光谱峰位的变化与Basciano的数据吻合。由此看来Maubec将1108 cm-1归属于v3(SO4)和δOH叠加振动模,并将其频率的变化归于δOH的变化是正确的。根据目前已有的拉曼光谱研究结果看出,借助拉曼光谱暂时还无法准确给出A位置离子的占位比情形,还有待进一步探究。
3.2.2 A位置离子替换作用分析
140 ℃时,能够合成K-H3O黄钾铁矾和Na-K黄钾铁矾,但无法合成Na-H3O黄钾铁矾,160℃时才有少量Na-H3O黄钾铁矾沉淀生成。这表明温度高易形成含Na的黄钾铁矾,有研究发现温度较高有利于自然明矾石中钠对钾的替换[18]。
不同的离子占据A位主要影响与OH基相关的振动。当K+替换Na+时,随着A位置K+含量比的增大,v(OH)伸缩振动模频率增加,Fe-OH伸缩振动模频率变减小;当发生H3O+替换时,对与OH相关的振动模有较大的影响,但变化规律不明显,可能是由H3O+在结构中位置的不确定性引起的。Na-K黄钾铁矾固溶系列的大部分拉曼峰的频率比其他样品的要大,这可能与A位置平均离子半径有关。相关拉曼峰的偏移程度小,且频率不是简单的线性变化,这与前人的研究发现不同,可能是因为A位置发生复杂的离子含量比的变化,引起黄钾铁矾结构的变化复杂。
关于A位置离子的替换对于黄钾铁矾晶体中硫酸基的影响,曾经存在分歧[1,6,14]。由表2发现,S#B1、S#B2的v1(SO4)振动模频率大于其他样品,即A位置共存Na+、H3O+时,v1(SO4)频率大于Na+、K+共存或者K+、H3O+共存的情况。这与文献[6]中v1(SO4)振动模的频率在水合氢钾铁矾、黄钠铁矾和黄钾铁矾中,由大变小的现象一致。在各系列样品中v2(SO4)、v4(SO4)弯曲振动模的频率基本不变,v3(SO4)和δOH叠加振动模的频率变化较明显,这种变化源于δOH。所以,由A位置离子替换作用引起的结构修正对于硫酸基的影响不大,硫酸伸缩振动模频率轻微变化,硫酸弯曲振动模频率基本不变。
4 结论
利用水热法成功制备了黄钾铁矾固溶系列样品及A位置近全钾占据样品,发现Na-H3O黄钾铁矾需要的实验温度较高,对样品的拉曼光谱进行分析,将356 cm-1、437 cm-1、457 cm-1、1104 cm-1等存在异议的拉曼峰的归属进行了分析。通过观察拉曼光谱峰位频率的变化,结合前人研究的离子半径和键长等数据,利用胡克定律对A位置离子替换作用做了分析,由于固溶物中A位置发生离子含量比的变化,使黄钾铁矾的结构变化复杂,特别是对于具有位置不确定性的H3O+,总体看来A位置的离子替换主要影响OH周围的环境,使得与羟基相关的振动模发生变化。
[1] Spratt H J,Rintoul L,Avdeev M,etal.The crystal structure and vibrational spectroscopy of jarosite and alunite minerals[J].American Mineralogist,2013,98(10):1633-1643.
[2] Basciano L C.Crystal chemistry of the jarosite group of minerals soild-solution and atomic structures[D].Kingston Ontario,Canada,Queen's University,2008:1-106.
[3] Basciano L C,Peterson R C.Jarosite hydronium jarosite solid-solution series with full iron site occupancy:Mineralogy and crystal chemistry[J].American Mineralogist,2007,92(8-9):1464-1473.
[4] 王长秋,马生凤,鲁安怀,等.黄钾铁矾形成条件研究及其环境意义[J].岩石矿物学杂质,2005,24(6):607-611.(Wang Changqiu,Ma Shengfeng,Lu Anhuai,etal.The formation conditions of jarosite and its environmental significance[J].Acta Petrologica Et Mineralogica,2005,24(6):607-611.
[5] 宁顺明,陈志飞.从黄钾铁矾渣中回收锌铟[J].中国有色金属学报,1997,7(3):56-58.(Ning Shunming,Chen Zhifei.Recovery of zinc and indium from jarosite residues [J].Transactions of nonferrous minerals society of China,1997,7(3):56-58)
[6] Maubec N,Lahfid A,Lerouge C,etal.Characterization of alunite supergroup minerals by Raman spectroscopy[J].Spectrochim Acta Part A,012,96:925-939.
[7] Savage K S,Bird D K,O'Day P A.Arsenic speciation in synthetic jarosite[J].Chemical Geology,2005,215(1-4):473-498.
[8] Driscoll R L,Leinz R W.Methods for synthesis of some jarosites.Techniques and Methods:No.5-D1.U.S.Geological Survey,Reston,Virginia:2005:1-5.
[9] Frost R L,Wills R A,Weier M L,etal.Comparison of the Raman spectra of natural and sythetic K- and Na-jarosites at 298 and 77 K[J].Journal of Raman spectroscopy,2005,36(5):435-444.
[10] Sasaki K,Tanaike O,Konno H.Distinction of jarosite-group compounds by Raman spectroscopy[J].Canadian Mineralogist,1998,36:1225-1235.
[11] 朱长见,陆建军,陆现彩,等.氧化亚铁硫杆菌作用下形成的黄钾铁矾的SEM研究[J].高校地质学报,2005,11(2):234-238.(Zhu Changjian,Lu Jianjun,Lu Xiancai,etal.SEM study on jarosite mediated by thiobacillus ferrooxidans[J].Geological Journal of China Universities,2005,11(2):234-238)
[12] 时启立,朱艳彬,杨钱华,等.细菌氧化法制取黄钾铁矾的研究[J].环境科学与技术,2010,33(9):39-43.(Shi Qili,Zhu Yanbin,Yang Qianhua,etal. Synthesis of jarosite by bacteria oxidation[J].Environmental Science & Technology,2010,33(9):39-43)
[13] Brang H E A,Scarlett N V Y,Grey I E.Formation of jarosite minerals in the presence of seed material[C].Lunar and Planetary Science Conference.2015,46:1825.
[14] Frost R L,Wills R A,Weier M L,etal.A Raman spectroscopic study of selected natural jarosites[J].Spectrochim Acta Part A,2006,63(1):1-8.
[15] Spratt H J,Avdeev M,Pfrunder M C,etal.Location of hydrogen atoms in hydronium jarosite[J].Phys Chem Miner,2014,41(7):505-517.
[16] Bishop J L,Murad E.The visible and infrared spectral properties of jarosite and alunite[J].American Mineralogist,2005,90(7):1100-1107.
[17] Frost R L,Wills R A,Weier M L,etal.A Raman spectroscopic study of alunites[J].J Molr Struc,2006,785(1-3):123-132.
[18] 王翠芝,熊欣.紫金山金铜矿明矾石的拉曼光谱特征[J].光谱学与光谱分析:2014,34(2):415-420.(Wang Cuizhi,Xiong Xin.Raman spectra characteristics of alunite in the Zijinshan gold-copper deposit[J].Spectrosc Spect Anal,2014,34(2):415-420)
Synthesis and Raman Spectral Analysis of Solid-Solution Series of Jarosite Group
ZHANG Yun-xia,WANG Meng,GUO Zhao-qing,Feng Min,Wang Bin,CAO Xue-wei,Xu Xiao-xuan,WANG Yu-fang*
(SchoolofPhysics,NankaiUniversity,Tianjin,300071,China)
In this paper,the solid-solution series of the jarosite group AFe3(SO4)2(OH)6have been synthesized,where the site of A can be occupied by K+,Na+and H3O+.In addition,nearly fully occupied potassium jarosite is prepared for comparison.Raman spectra of the jarosite group are measured and analysized.The jarosite group minerals can be characterized by Raman spectra and the bonds can be due to the hydroxyl groups,internal modes of sulfate and lattice modes.Some bonds assignment which are open to question are analysized.According to the number of the scattered peaks and frequencies,the size of the ionic radius,bonds length and bonds angle,the effect of the substitutions of ions in A-site of jarosite solid solution series is analysized by hooke's law.The substitution effect of A position ion mainly affect the OH in the jarosite and the hydroxyl vibration mode.
jarosite;Raman spectra;hydro-thermal method
2015-07-18; 修改稿日期:2015-12-02
张云霞(1989-),硕士,主要研究方向为固体光谱。E-mail:yxzhangnku@163.com
王玉芳.E-mail:yfwang@nankai.edu.cn
1004-5929(2016)04-0317-07
O482
A
10.13883/j.issn1004-5929.201604008
