慢性炎症痛过程脊髓背角Caveoline-1蛋白表达变化
2016-12-23王丹萍
韩 坤,王丹萍
1.漯河医学高等专科学校 生理教研室(河南 漯河 462000) 2.漯河市中心医院(漯河医学高等专科学校第一附属医院) 内分泌科(河南 漯河 462000)
慢性炎症痛过程脊髓背角Caveoline-1蛋白表达变化
韩 坤1,王丹萍2
1.漯河医学高等专科学校 生理教研室(河南 漯河 462000) 2.漯河市中心医院(漯河医学高等专科学校第一附属医院) 内分泌科(河南 漯河 462000)
目的 观察慢性炎症痛过程脊髓背角Caveoline-1蛋白表达。方法 实验动物分组和动物模型制作:空白组4只:不作任何处理同期条件分笼饲养。炎性痛(足底注射CFA)模型组24只,炎性痛假手术组24只。炎性痛模型组和炎性痛假手术组大鼠按处理时间不同又分为1、3、5、7、10、14 d每组4只,分别于1、3、5、7、10、14 d制备动物模型。痛行为学检测:术后1、3、5、7、14 d,测定各组机械撤足阈值和热撤足潜伏期,手术组和空白组、假手术组对比,确定疼痛模型制作成功。组织标本制备和组织中总蛋白的提取及检测:炎性痛模型和炎性痛假手术组大鼠分别在术后第15 d处死取L5脊髓,按同侧和对侧分别提取L5脊髓组织总蛋白,利用蛋白质印迹法(western-blot)检测Caveolin-1在各实验分组脊髓背角同侧和对侧的表达量。结果 在同侧脊髓背角,注射CFA后的第5、7、10、14 d,Caveolin-1表达量比假手术组分别升高了(78.8±3.31)%,(115.3±3.56)%,(69.2±5.21)%,(61.5±5.06)%,其中第5、7、10 d有统计学差异(P<0.05),第14 d差异有显著性(P<0.01)。在CFA后各个时间点与假手术组相比,对侧脊髓背角Caveolin-1的表达无明显变化。结论 炎症引起的慢性痛可诱导SD大鼠Caveolin-1在同侧脊髓背角表达的增加。
炎性痛;谷氨酸代谢型受体;脊髓背角;Caveoline-1
疼痛是机体与组织损伤有关的复杂情感体验[1],分为生理性疼痛和病理性疼痛。炎症性疼痛是病理性疼痛中的一个重要分类,是指受损的组织受到化学或物理因素刺激痛觉感受器而诱导机体发生血管的舒缩变化、躯体的感受获得改变以及外周感受器的敏化等一系列改变,进而诱发持续性疼痛[2],该过程中多种潜在机制可能发挥作用,包括神经递质、异位冲动、受体和离子通道的表达以及功能改变等。其中,脊髓背角谷氨酸代谢型受体(metabotropicglutmate receptors,mGluRs)广泛参与痛觉过敏、自发痛和触诱发痛等病理性疼痛,在疼痛中发挥重要作用[3]。Caveolin是一种整合膜蛋白,其功能是在调节细胞信号转导过程中发挥信号通路的枢纽作用,该作用需与多种蛋白相互作用才能发挥。研究表明[4]Caveolin-1和mGluR1/5定位共存,Caveolin-1调控mGluR1/5转运和信号传导,进一步研究还发现Caveolin-1可以调控依赖mGluR5的ERK-MAPK途径的激活[5]。Caveolin-1和mGluR在神经元信号传导中的共同作用已被多项研究所证实,而mGluR通过磷酸肌醇水解途径、胞外信号调节激酶(ERK)途径等多种途径在炎性痛、神经损伤疼痛及脊髓损伤慢性中枢痛中均发挥重要作用,但炎症引起的慢性痛过程是否伴有Caveolin-1在背根神经节和相关脊髓背角的表达变化至今未见报道。本实验旨在信号转导途径水平观察炎症痛模型中大鼠脊髓后角Caveolin-1的表达水平,进一步明确疼痛体内信号转导的分子机制。
1 材料与方法
1.1 动物 60只成年SD大鼠(2月龄,180~250 g)雄性,SPF级,由河南省实验动物中心提供(许可证号:SCXK豫2010-0002,合格证号:0008142)。于该实验室动物房分笼饲养,室温18~25℃,湿度40%~60%,白/夜12 h,自由饮食水。
1.2 主要仪器及试剂 完全弗氏试剂(CFA)(美国Sigma公司),机械痛敏检测仪(美国Stoeling公司),热痛刺激仪(中国医学科学院生物工程研究所),兔Caveolin-1受体-抗购自美国Cell Signaling公司;小鼠Beta-actin单克隆抗体购自美国SIGMA公司,Blottinggradegoat Anti-Rabbit IgG(H+L)购自美国Bio-Rad公司,Blottinggrade Affinity Purifiedgoat Anti-Mouse IgG(H+L) 购自美国Bio-Rad公司,vonFrey纤维丝购自中国医学科学院生物工程研究所。
1.3 实验方法
1.3.1 实验动物分组和动物模型制作 空白组4只:不作任何处理同期条件分笼饲养。炎性痛(足底注射CFA)模型组24只,炎性痛假手术组24只。炎性痛模型组和炎性痛假手术组大鼠按处理时间不同又分为1、3、5、7、10、14 d每组4只,分别于1、3、5、7、10、14 d制备动物模型。
1.3.2 痛行为学检测 术后1、3、5、7、14 d,测定各组机械撤足阈值和热撤足潜伏期,手术组和空白组、假手术组对比,确定疼痛模型制作成功。
1.3.3 组织标本制备和组织中总蛋白的提取及检测 炎性痛模型和炎性痛假手术组大鼠分别在术后第15 d处死取L5脊髓,按同侧和对侧分别提取L5 脊髓组织总蛋白,利用蛋白质印迹法(western-blot)检测Caveolin-1在各实验分组脊髓背角和背根神经节同侧和对侧的表达量。

2 结果
2.1 炎性痛模型机械缩足阈值和热撤足潜伏期检测结果 与假手术组和空白对照组相比,炎性痛模型组在术后1、3、5、7、14d均出现机械撤足阈值和热撤足潜伏期降低(P<0.05),而假手术组和空白对照组在各时间点变化无统计学差异。以上结果表明炎性痛模型组术后大鼠手术侧足部均出现明显痛觉过敏现象,模型建立成功(见图1、图2)。
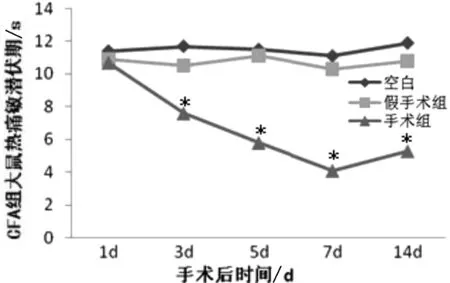
VS假手术组and空白对照组,*:P<0.05,n=4图1 CFA组大鼠热撤足潜伏期测试结果
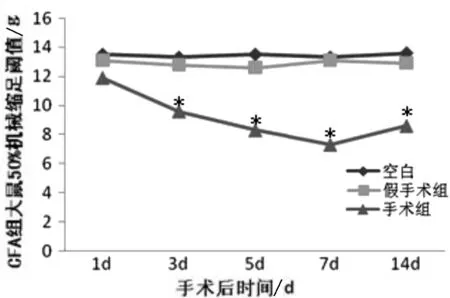
VS假手术组and空白对照组,*:P<0.05,n=4图2 CFA组大鼠50%机械撤足阈值测试结果
2.2 炎性痛模型不同作用时间脊髓背角Caveolin-1表达量变化SD大鼠足底注射CFA可引起Caveolin-1在同侧脊髓背角表达的升高。在同侧脊髓背角,注射CFA后的第5、7、10、14d,Caveolin-1表达量比假手术组分别升高了(78.8±3.31)%,(115.3±3.56)%,(69.2±5.21)%,(61.5±5.06)%,其中第5、7、10d有统计学差异(P<0.05),第14d差异有显著性(P<0.01)。在CFA后各个时间点与假手术组相比,对侧脊髓背角Caveolin-1的表达无明显变化(见图3)。
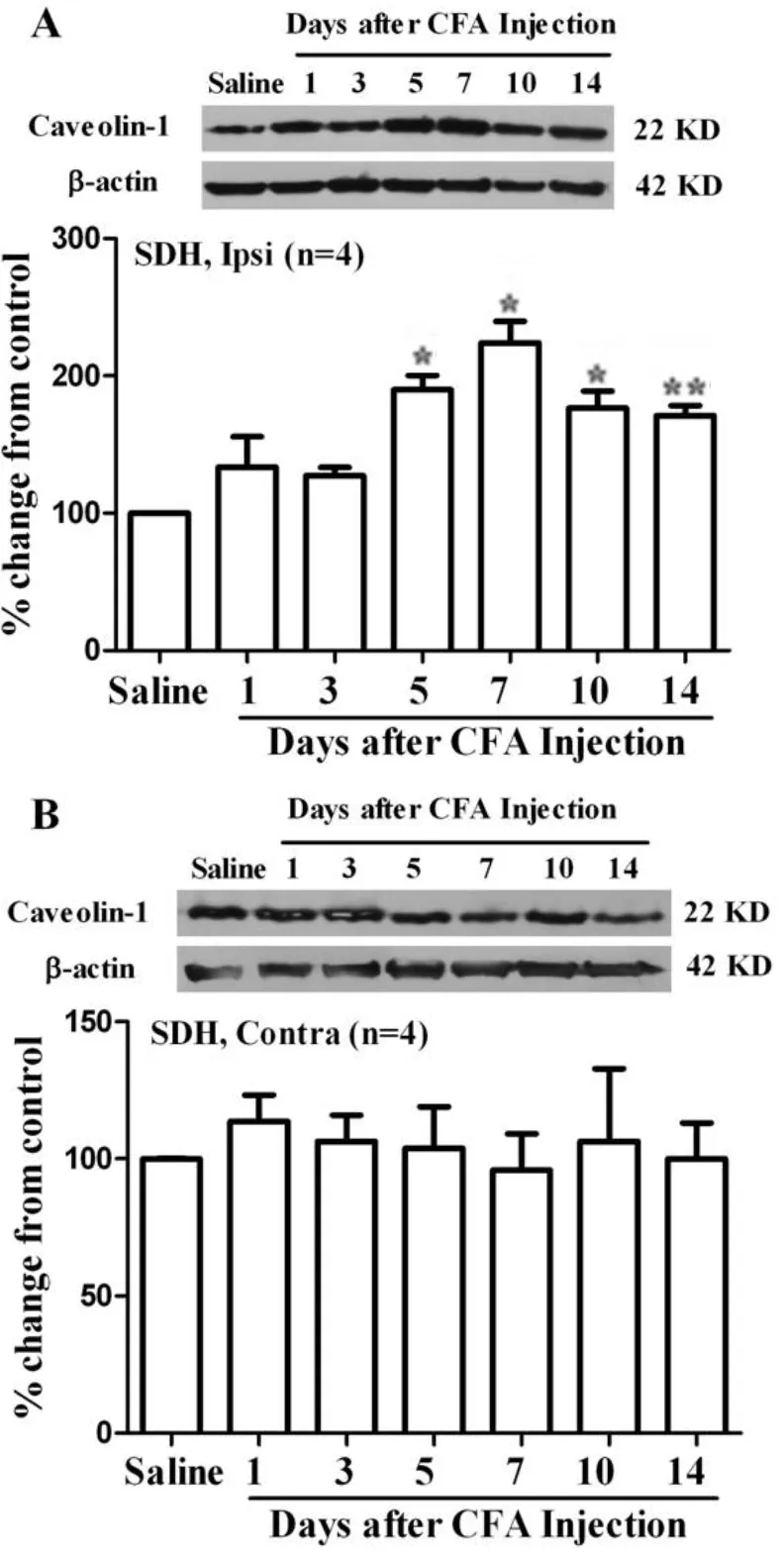
VS假手术组,*:P<0.05,**:P<0.01,n=4图3 炎性痛模型组不同作用时间脊髓背角Caveolin-1表达量变化
3 讨论
本研究采用大鼠足底注射CFA诱导大鼠产生炎症性慢性痛模型,结合western-bolt检测了大鼠注射CFA后1、3、5、7、10、14d,Caveolin-1在同侧和对侧L5脊髓背角的表达。结果发现:在脊髓背角注射CFA后的第5、7、10、14d,Caveolin-1表达量比假手术组分别升高了(78.8±3.31)%,(115.3±3.56)%,(69.2±5.21)%,(61.5±5.06)%,其中第5、7、10d有统计学差异(P<0.05),第14d差异有显著性(P<0.01)。在CFA后各个时间点与假手术组相比,对侧脊髓背角Caveolin-1的表达均无明显变化,表明在慢性炎症痛模型中可诱导Caveolin-1在脊髓背角表达显著升高,提示脊髓背角Caveolin-1的表达与炎性疼痛大鼠痛觉变化和信号的传导中可能发挥重要作用。
疼痛传导通路中痛觉传入纤维进入脊髓后,在后角更换神经元并发出纤维交叉到双侧,再经脊髓丘脑侧束上行抵达丘脑的体感觉核,转而向皮层体表感觉区投射,在本实验中同侧Caveolin-1在DRG和脊髓背角表达显著增加,对侧DRG和脊髓背角Caveolin-1的表达各个时间点与对照组相比,均无明显变化,更进一步证实了慢性痛中Caveolin-1介导信号传导的作用的存在。
但在本实验中,炎症引起的慢性痛可诱导Caveolin-1在同侧DRG和脊髓背角表达的升高与与以往的研究中Caveolin-1发挥的负性调控作用的结论不一致[6]。考虑Caveolin-1的负性调控作用并非适用于所有的信号转导途径,同时研究证实也只有部分mGluR5和Caveolin-1相关而非全部[7]。所以,在慢性疼痛的信号传导通路中更多的信号传导途径及其更详细的分子机制都有待进一步证实。
综上,Caveolin-1在慢性痛过程痛觉信号的传递中可能发挥重要作用,慢性炎症性痛可诱导Caveolin-1在同侧DRG和脊髓背角表达的增加,进一步明确了体内疼痛信号转导的分子机制,并为临床上疼痛的治疗提供理论基础。
[1] 赵志奇.疼痛及其脊髓机理[M].上海:上海科技教育出版社,2000:1-2.
[2]FalkS,DickensonAH.Painandnociception:mechanismsofcancer-inducedbonepain[J].JClinOncol,2014,32(16):1 647-1 654.
[3]NeugebauerV,LuckeT,SctmibleHg.Requirementofmetabotropicglutamatereceptorsforthegenerationofinflammationevokedhyperexcitabilityinratspinalcordneurons[J].EurJNeurosci,1994,6(7):1 179-1 186.
[4]AnnaFrancesconi,RanjuKumari,andR.SuzanneZukin.RegulationofgroupIMetabotropicglutamateReceptorTraffickingandSignalingbytheCaveolar/LipidRaftPathway[J].TheJournalofNeuroscience,2009,29(11):3 590-3 602.
[5]BhatnagarA,ShefflerDJ,KroezeWK.Caveolin-1interactswith5-HT2Aserotoninreceptorsandprofoundlymodulatesthesignalingofselectedgalphaq-coupledproteinreceptors[J].BiolChem,2004(279):34 614-34 623.
[6]FrancesconiA,KumariR,ZukinRS.RegulationofgroupIetabotropicglutamatereceptortraffickingandsignalingbytheCaveolar/lipidraftpathway[J].Neurosci,2009,29(11):3 590-3 602.
[7]ShenJ,MaS,ChanP.Nitricoxidedown-regulatesCaveolin-1expressioninratbrainsduringfocalcerebralischemiaandreperfusioninjury[J].Neurochem,2006,81(96):1 078-1 089.
责任编辑:牟冬生
The Caveoline-1 Protein Expression of Spinal Cord Dorsal Horn in Inflammatory Pain Model
Han Kun1,Wang Danping2
[1.DepartmentofPhysiology,LuoheMedicalColloge,Luohe462000,China; 2.LuoheCentralHospital(DepartmentofEndocrinology,The1stAffiliatedHospitalofLuoheMedicalCollege),Luohe462000,China]
Objective To observe the Caveoline-1 protein expression of spinal cord dorsal horn in inflammatory pain model.Methods 4 rats in the blank group were raised in the same condition.24 rats (plantar injection CFA) were in the inflammatory pain model group and 24 rats were in the inflammatory pain sham operation group.According to the different processing time,the rats in the two groups were prepared respectively on 1,3,5,7,10 d and 14 d.4 rats in each group were made into animal model on 1,3,5,7,10 d and 14 d.The mechanical shrinkage foot threshold and hot shrinkage foot incubation period were detected 1,3,5,7,10 d and 14 d after operation.The surgery group,blank group and sham operation group were compared to be successful in the pain model.The rats in the inflammatory pain model group and inflammatory pain sham operation group were put to death 15 days after operation and extracted L5 spinal cord.The total protein was extracted from L5 spinal cord according to the same side and the contralateral side. The Caveolin-1 expression of spinal cord dorsal horn was detected by the Western-blot method.Results on 5,7,10,14 d after the CFA injection in the same side of the spinal cord dorsal horn,the Caveolin-1 expressions were increased by(78.8±3.31)%, (115.3±3.56)%,(69.2±5.21)% and (61.5±5.06)%. It had statistic difference on 5,7,10 d (P<0.05) and the difference was significant on 14 d (P<0.01).Compared with the sham operation group at every times after CFA,the Caveolin-1 expressions on the contralateral side of spinal cord dorsal horn had no significant change.Conclusion the chronic pain caused by the inflammation can increase the Caveolin-1 expressions on the same side of spinal cord dorsal horn for SD rats.
inflammatory pain;metabolicglutamate receptor;spinal cord dorsal horn;caveolin-1
韩坤(1982- ),男,河南漯河人,研究生,讲师,研究方向:神经生理和内分泌。
R741;R966
A
1008-8164(2016)04-0004-03
2016-11-09
