三水杨醛三乙基四胺合锑(III)金属配合物的合成及其表征
2016-12-20周成勇史家丽
周成勇,史家丽
(长治学院化学系,山西长治046011)
三水杨醛三乙基四胺合锑(III)金属配合物的合成及其表征
周成勇,史家丽
(长治学院化学系,山西长治046011)
利用水杨醛,三乙基四胺和SbCl3首次合成了三水杨醛三乙基四胺合锑(III)金属配合物,并通过熔点的测定、电导率法、红外光谱法以及X-衍射等方法对所合成的有机配体及其金属配合物进行了初步的结构表征,结果表明所合成的金属配合物为离子型金属配合物。合成该金属配合物的意义在于进一步考察该金属配合物与生物大分子(如DNA、蛋白质等)的相互作用后,可为其在分子生物学、化学生物学、药物化学方面的应用和研究以及新型药物的研发等方面提供有价值的信息。
三水杨醛;三乙基四胺;锑金属配合物
1 引言
随着人们对金属配合物药理作用的深入研究,新的高效低毒、具有抗癌活性的金属配合物不断被合成,其中包括一些铂配合物、茂钛衍生物、多酸化合物等。丰富多样的金属配合物以其卓越的放射化学性质、光化学性质、生物化学性质吸引了众多化学家的研究兴趣[1,2]。
目前有机配体与过渡金属以及稀土金属形成配合物的研究非常活跃,而对主族金属与有机配体形成配合物的研究却鲜有报道。医学研究发现,一些主族非金属和金属元素都有相当重要的抗肿瘤以及抗癌抑菌活性,如砷族的砷、锑、铋元素,虽然在地壳中的含量很低,但由于其化合物活性很强,所以在临床上具有非常广泛的应用[3]。
在治疗肿瘤和其他疾病方面,许多有机配体与金属形成的配合物比单独的有机化合物更有优势,即配合物的活性一般要比底物好,这是因为配离子的引入可增大药物的活性。一方面,金属离子作为化合物中心,在抗癌药物中起到中心角色的作用,有机分子配位的化合物可能会改变生物体的正常新陈代谢方式或减慢有机分子运输过程中的释放机制;另一方面,有机配体与金属离子配位后,可对生物体内金属离子的生物活性和功能起到缓释作用,从而降低生物体重金属中毒的可能性[4]。
锑在人体内含量约为8 mg,可用来制作许多药物。锑剂应用于人类疾病的治疗,历史悠久,是治疗肺病、血吸虫病、黑热病的特效药,由于它具有毒性又可用于治疗疾病,因此对所用计量的控制非常重要。锑化合物在治疗各种寄生感染方面具有重要的医学价值,包括利什曼病、血吸虫病、锥虫病等。Sb2O3虽然有毒,但毒性比As2O3小,可有效治疗早幼粒细胞白血病(acute promyelocytic leukemia,APL)[5]。
随着细胞生物学的发展,人们对于天然多胺,如腐胺、亚睛胺、精胺在细胞生长和死亡过程中所起关键作用的了解不断深入。近年来,天然或人工合成的多胺在癌症化学防治及其潜在的抗HIV活性方面的研究已多见文献报道。而人工合成的多胺化学核酸还对新型抗肿瘤艾滋病化学药物的定向设计及其基因治疗,以及基因工程中研究基因分离、大片段基因序列分析,染色体图谱分析及DNA定位诱变,分子印记技术,DNA的构象识别等方面均有重要的意义和应用前景。多胺类化合物与DNA作用的意义和应用前景非常广泛,它不仅能在体外与DNA特异性地结合,而且还能透过细胞膜,穿过核膜,进入细胞内抑制基因表达。同时多胺类化合物能与许多金属离子配位,生成具有多种用途的配合物[6-8]。
文章首次设计合成了三水杨醛三乙基四胺合锑(III)金属配合物,并通过熔点测定、电导率测定以及红外光谱法对金属配合物做了初步的表征。目的在于进一步研究其与生物大分子如DNA、蛋白质等的作用,从而为其在药物开发和分子生物学中的应用提供有价值的信息。
2 实验部分
2.1实验试剂

表1 实验试剂
2.2实验仪器

表2 实验仪器
2.3配合物的合成
2.3.1配体的合成方法
搅拌下,将三乙基四胺(7.5 mL,0.05 mol)溶于50 mL的甲醇溶液滴加到水杨醛(26.5 mL,0.25 mol)溶于50 mL甲醇溶液中,室温下搅拌,溶液立即变为橙黄色,约30 min滴加完毕,继续搅拌3 h,在搅拌过程中溶液变为黄色浊液。停止反应,抽滤,用甲醇和乙醚混合液(1:1)洗涤3次,真空干燥,得16.4323 g的黄色固体。产率:71.28%,熔点:101.3℃。
2.3.2配合物的合成
搅拌下,将SbCl3(1.233 g,3.8 mmol)溶于5 mL无水乙醇的溶液滴加到三水杨醛三乙基四胺(2.5110 g,5.38 mmol)溶于20 mL苯的黄色溶液中,立即有黄色片状物生成,继续滴加则有乳黄色沉淀析出,约10 min滴加完毕,室温下继续搅拌3 h,停止反应,抽滤,用苯-无水乙醇溶液(1:1)洗涤3次,真空干燥,得到2.1803 g的乳黄色固体,产率为65.3%,熔点为:218.3℃。配合物合成路线见图1。

图1 配合物合成路线
2.4配体及配合物的表征
2.4.1配体的晶体结构测定
将合成的三水杨醛三乙基四胺的浅黄色固体溶于无水乙醇得其饱和液,静止数日,获得黄色单晶。在室温下将晶体置于D8QUEST单光源微焦斑单晶衍射仪中,MoKa(λ=0.071073 nm)射线作为辐射光源,用CMOS二维探测器PHOTON100收集衍射数据。晶体结构采用SHELXS-97程序由直接法解析,采用SHELXL-97程序,用全矩阵最小二乘法对所有非氢原子坐标和各向异性热参数进行精修。主要晶体学数据见表3。
2.4.2熔点的测定
三水杨醛三乙基四胺及其锑(III)金属配合物的熔点见表4。
2.4.3电导率的测定
分别称取配体、配合物及SbCl30.1113 g,0.2368 g,0.0113 g溶于DMSO-H2O(1:1)中,配制溶液,其物质的量浓度分别4.8×10-3mol/L、7.2×10-3mol/L、1.5×10-3mol/L,置于恒温水浴25℃下测其电导率(见表5)。

表3 配体的晶体学数据

表4 熔点的测定

表5 各物质的电导率
2.4.4配体及配合物的红外光谱
KBr做载体压片,测定配体三水杨醛三乙基四胺及其锑金属配合物的红外光谱,如图2、图3所示。
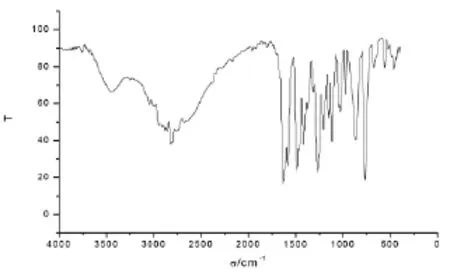
图2 配体的红外光谱图

图3 配合物的红外光谱图
3 结果与讨论
3.1配体晶体结构分析
配体的晶体结构见图4。为清晰起见,图中氢原子被略去。
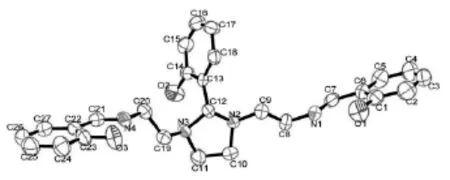
图4 配体的晶体结构图
3.2熔点分析
由表4可见,配体的熔程为100.8℃~101.8℃,配合物的熔程为216.2℃~220.4℃,熔程都较短,由此可初步判断这两种固体都比较纯净,且配合物的熔点明显高于配体的熔点,可初步证明配合物的生成。
3.3电导率分析
从表5中可以看出SbCl3的摩尔电导率为135.6S cm2mol-1,金属配合物的摩尔电导率为128.5 Scm2mol-1,二者的摩尔电导率相近,可以推断出所合成的金属配合物为离子型配合物[9],即配体在形成配合物时酚羟基没有电离,只是酚羟基氧原子的孤对电子与锑离子配位形成了离子型配合物,而金属配合物的摩尔电导率稍低是由于形成配离子后体积增大而导致移动速度变慢而致。
3.4红外光谱分析
对比图2、图3可以明显看出,在配合物的IR图中也出现明显的O-H大宽峰,说明形成配合物后酚羟基仍然存在,并未电离,进一步证明所合成的金属配合物为离子型配合物。
从图2、图3可得配体和配合物主要官能团的红外吸收峰变化如表6。
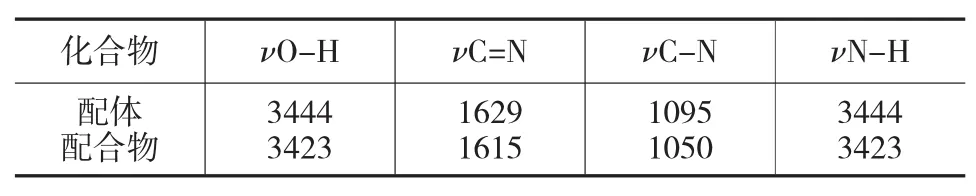
表6 配体及配合物红外光谱分析(cm-1)
从表6中可以看出,形成配合物后主要官能团吸收峰明显发生红移。配体和配合物中的O-H和N-H键IR吸收峰重合,且在配体中其伸缩振动吸收峰为3444 cm-1,而在配合物中为3423 cm-1,向低频方向移动了21 cm-1,这是由于氧原子、氮原子与金属离子配位后,其电子云密度降低,使得O-H和N-H键中的成键电子更偏向于配位原子,从而导致O-H和N-H共价键的键强度降低,因此向低频方向移动。同理,配体中C=N键的伸缩振动吸收峰为1629 cm-1,而配合物中C=N键的伸缩振动吸收峰为1615 cm-1,向低频方向移动了14 cm-1;配体中C-N键的伸缩振动吸收峰为1095 cm-1,而配合物中C-N键的伸缩振动吸收峰为1050 cm-1,也向低频方向移动了45 cm-1,因此可以确定配合物的形成。
4 结论
综上所述,文章利用水杨醛,三乙基四胺和SbCl3合成了三水杨醛三乙基四胺合锑(III)金属配合物,并通过熔点的测定、电导率法、红外光谱法以及X-衍射等方法对所合成的有机配体及其金属配合物进行了初步的结构表征,结果表明所合成的金属配合物为离子型金属配合物。在后续工作中,将进一步考察该金属配合物与生物大分子(如DNA、蛋白质等)的相互作用,以便为其在分子生物学、化学生物学、药物化学方面的应用和研究以及新型药物的研发等方面提供有价值的信息。
[1]Cheng-Yong Zhou,Yan-Bo Wu,and Pin Yang, Synthesis,Characterization,and Studies on DNA Binding of the Complex Fe(Sal2dienNO3·H2O), Biochemistry(Moscow),2010,75(4):505-512.
[2]Cheng-Yong Zhou,Jing Zhao,Yan-Bo Wu, Cai-XiaYin,PinYang.Synthesis,characterizationand studiesonDNA-bindingofanewCu(II)complexwith N1,N8-bis(l-methyl-4-nitropyrrole-2-carbonyl)triethylenetetramine[J].Journal of Inorganic Biochemistry,2007,101(01):10-18.
[3]张志朋,钟国清,蒋琪英等.砷、锑、铋配合物的生物活性[J].化学进展,2008,20(9):1315-1323.
[4]Reisner E.,Arion V.B.,Keppler B.K.,et al.Inorg. Chim.Acta,2007,361(6):1569-1583.
[5]Elliott B.M.,Mackay J.M.,Clay P.,et al.Mutat. Res,1998,415(1P2):109-117.
[6]Cheng-Yong Zhou,Yan-Bo Wu,and Pin Yang. Synthesis,Characterization,and Studies on DNA Binding of a New Mg Complex with N1,N8-bis (1-methyl-4-nitropyrrole-2-carbonyl) triethylenetetramine[J]Biochemistry(Moscow), 2008,73(3):245-251.
[7]Zhou Cheng-Yong,Xi Xiao-Li,and Yang Pin, Studies on DNA Binding to Metal Complexes of Sal2trien[J].Biochemistry(Moscow),2007,72(1), 37-43.
[8]张志刚,杨频.二茂钛二甘氨酸盐酸盐的体外抗肿瘤活性及其与DNA的作用研究[J].高等学校化学学报,1999,20(11):1682-1688.
[9]Rosenberg,V.,CampL.V.,KringasT. Inhibition of Cell Division in Escherichia coli by Electrolysis Products from a Platinum Electrode[J].Nature,1965,205(4972):698-699.
[10]李景宁,杨定桥,张前.有机化学(第5版)[M].北京:高等教育出版社,2011.
(责任编辑王璟琳)
O621.13
A
1673-2014(2016)05-0008-04
国家自然科学基金(21402012);国家级大学生创新创业项目(201510122003);山西省大学生创新创业项目(2015428)。
2016—03—27
周成勇(1963—),男,河南沁阳人,教授,博士,主要从事有机合成及化学生物学研究。
