基于碘酸钾基准试剂直接法配制碘标准溶液
2016-12-19戴兴德
晁 辉,戴兴德
(甘肃医学院, 甘肃 平凉 744000)
基于碘酸钾基准试剂直接法配制碘标准溶液
晁 辉,戴兴德
(甘肃医学院, 甘肃 平凉 744000)
本文基于碘酸钾基准试剂完成碘标准溶液直接配制,建立了一种快速配制碘标准溶液的新方法,操作简单,安全性高.基于此法测定了市售维生素C样品中抗坏血酸含量,RSD=0.18%,回收率在98.38%~100.8%之间,快速准确,稳定性好.
碘酸钾;碘标准溶液;抗坏血酸;滴定
当前,分析化学实验教材中碘标准溶液配制均采用间接法[1-3],即在碘化钾强制溶解后用三氧化二砷基准物质标定或标准硫代硫酸钠标准液比较标定.三氧化二砷剧毒,学生实验很少使用;硫代硫酸钠溶液稳定性差且配制麻烦,在配置过程中易造成误差累积;碘溶液易挥发,难保存,配制时所用试剂多,操作费时.采用碘酸钾基准试剂直接法配制碘标准溶液,完成抗坏血酸含量测定,实验结果符合滴定分析要求[4].
1 实验部分
1.1 实验用品
1mol/L盐酸,0.5%淀粉指示剂,抗坏血酸,碘化钾,维生素C片.
1.2 实验原理
5I-+IO3-+6H+=3I2+3H2O
CI2=3×CKIO3
C6H8O6+I2=C6H6O6+2HI
mC6H8O6=CI2VI2×176×10-3
1.3 配制方法
碘酸钾标准溶液(0.1675mol/L):精密称定3.5667g经105℃烘干2小时的碘酸钾(优级纯),溶解于水,移入100mL容量瓶中,再用水定容.
碘标准溶液(0.05000mol/L):称取碘化钾固体6.0g,加水溶解后,准确移入10.00mL碘酸钾标准溶液,加盐酸10mL,充分搅拌,转移至100mL容量瓶,加水定容,静置1分钟.
1.4 滴定方法
准确称取0.15~0.3g抗坏血酸标准物质(维生素C药剂),加新煮沸且已冷却的纯化水溶解,加入2mL淀粉指示剂.用新配制碘标准溶液滴定,当溶液变蓝且1分钟内颜色不消失,即达到终点.计算抗坏血酸质量,并进行方法学验证.
2 结果与讨论
2.1 酸性条件选择
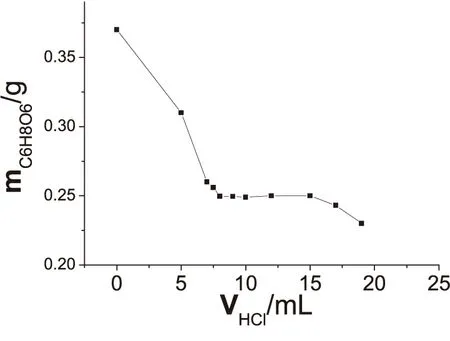
图1 盐酸加入量对测定结果影响
KIO3与I-的反应必须在酸性条件下进行,准确称取0.2500g抗坏血酸标准物质,改变混合液中的盐酸加入量,按1.4步骤操作,结果见图1.当
VHCl<8mL时,溶液酸度太低,KIO3氧化能力减弱,所得碘溶液浓度偏小,造成正误差;VHCl=9~15mL时,所测结果比较稳定,误差控制在0.2%以内;当VHCl>15mL时,高酸度导致部分碘离子被氧化,所得碘溶液浓度偏大,测定结果误差反向增大.故可选取盐酸溶液加入量为10mL.
2.2 KI用量选择
准确称取0.2500g抗坏血酸标准物质,改变KI用量,按1.4步骤操作,结果见图2.当KI用量超过4g时,滴定误差较小并趋于恒定,误差损失小于0.2%,满足容量分析的要求;当KI用量低于4g时,碘酸钾反应不彻底,碘溶解不均匀,标准溶液用量偏大,出现了明显正误差,显然,碘酸钾与抗坏血酸有反应,但反应计量关系复杂;KI用量增加基本无影响.因此,本实验确定KI用量为6g.
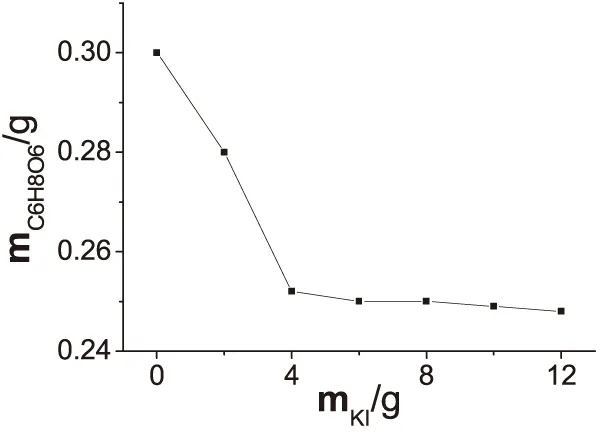
图2 碘化钾加入量对测定结果影响
2.3 静置时间选择
改变混合液静置时间,用新制碘标准溶液测定同质量抗坏血酸标准样品(m=0.2000g),所得结果表明,静置时间对测定结果影响不大,但若放置时间过长,测定结果略有偏小(图3),即碘浓度变大,故可将碘酸钾标准溶液(0.1675mol/L)作为储备液,碘标准溶液随用随配.
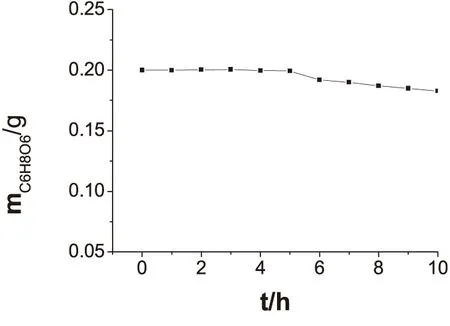
图3 新制碘标准溶液静置时间对测定结果影响
2.4 精密度考察
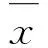
2.5 加样回收试验

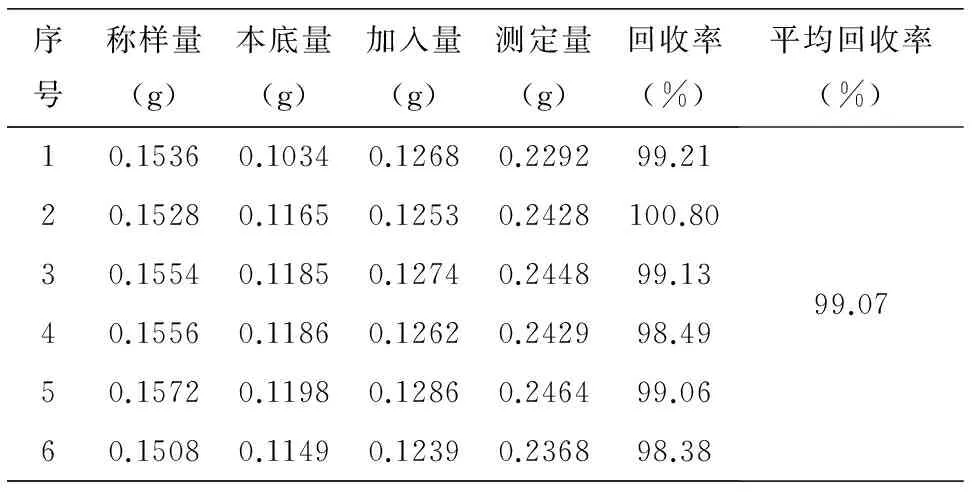
表1 加样回收率测定
3 结论
基于碘酸钾基准试剂完成碘标准溶液直接配制,避免使用强毒性物质三氧化二砷和稳定性较差的硫代硫酸钠溶液,克服存放过程中碘溶液挥发损失,随用随配,操作简化,安全性高,值得推广应用.
[1]刘燕娥.分析化学[M].西安:第四军医大学出版社,2012:97-98.
[2]王仁国.无机及分析化学实验[M].成都:四川科学技术出版社,2003:130-131.
[3]武汉大学.分析化学实验[M].武汉:武汉大学出版社,2003:131-132.
[4]武汉大学.分析化学[M].北京:高等教育出版社,2005:16-18.
(责任编辑:王海波)
10.13877/j.cnki.cn22-1284.2016.08.019
2016-05-10
晁辉,男,本科,实验师.
戴兴德,学士,副教授.
G808
A
1008-7974(2016)04-0058-02
